14/01/2024
En el vasto y fascinante mundo de la química, la comprensión de cómo las sustancias se disuelven y en qué medida lo hacen es fundamental. Desde la preparación de medicamentos hasta el tratamiento de aguas residuales o la formación de estalactitas en una cueva, el concepto de solubilidad juega un papel crucial. Cuando hablamos de compuestos iónicos poco solubles, es decir, aquellos que no se disuelven completamente en un solvente, introducimos dos términos esenciales: la solubilidad molar y el producto de solubilidad (Ksp). Ambos nos permiten cuantificar la cantidad de una sustancia que puede disolverse en una solución y las condiciones bajo las cuales esto ocurre. Este artículo te guiará a través de estos conceptos, te enseñará a realizar los cálculos pertinentes y te ayudará a entender los factores que influyen en la solubilidad de las sustancias.

La solubilidad no es solo una medida de cuánto soluto se disuelve, sino que también es una indicación de un estado de equilibrio dinámico. En una solución saturada, el sólido que no se ha disuelto está en constante intercambio con sus iones disueltos, disolviéndose y precipitando simultáneamente a la misma velocidad. Es este delicado balance el que define las propiedades de una solución saturada y nos permite utilizar el Ksp para hacer predicciones importantes.
- ¿Qué es la Solubilidad Molar y por qué es Importante?
- El Producto de Solubilidad (Ksp): La Constante del Equilibrio de Disolución
- Cálculo del Ksp a partir de Datos de Solubilidad Experimental
- Determinación de la Solubilidad Molar a partir del Ksp
- El Efecto del Ion Común en la Solubilidad
- Predicción de la Formación de un Precipitado: El Cociente de Reacción Qsp
- Factores Adicionales que Afectan la Solubilidad
- Preguntas Frecuentes sobre Solubilidad Molar y Ksp
¿Qué es la Solubilidad Molar y por qué es Importante?
La solubilidad molar es una medida de la máxima cantidad de un soluto que puede disolverse en un solvente dado, expresada en moles por litro (mol/L). Es una forma estandarizada de cuantificar la solubilidad, permitiendo comparaciones directas entre diferentes sustancias.
A diferencia de la solubilidad expresada en gramos por litro, la solubilidad molar tiene en cuenta la masa molar del compuesto, proporcionando una visión más precisa de la cantidad de partículas disueltas. Por ejemplo, si tenemos 10 gramos de sal disueltos en un litro de agua, la solubilidad en masa sería 10 g/L. Sin embargo, si convertimos esos 10 gramos a moles, obtenemos la solubilidad molar, que es lo que realmente nos interesa para entender la estequiometría de la disolución y el equilibrio.
La importancia de la solubilidad molar radica en su relación directa con las concentraciones de los iones en una solución saturada. Esta relación es clave para el cálculo del producto de solubilidad (Ksp) y para predecir si una sustancia precipitará o permanecerá disuelta en una solución.
El Producto de Solubilidad (Ksp): La Constante del Equilibrio de Disolución
El producto de solubilidad, denotado como Ksp, es una constante de equilibrio que se utiliza para describir soluciones saturadas de compuestos iónicos de baja solubilidad. Representa el producto de las concentraciones molares de los iones, cada una elevada a la potencia de su coeficiente estequiométrico en la ecuación de equilibrio, en una solución saturada a una temperatura dada.
Para un compuesto iónico genérico MxAy que se disuelve en agua, la ecuación de equilibrio es:
MxAy (s) → x My+(aq) + y Ax-(aq)
Y la expresión de la constante del producto de solubilidad (Ksp) es:
Ksp = [My+]x[Ax-]y
Es importante notar que, dado que MxAy es un sólido puro, su concentración es constante y, por convención, no se incluye en la expresión del Ksp. Esto simplifica la constante de equilibrio a solo las concentraciones de los iones en solución. El valor de Ksp indica cuán soluble es un compuesto iónico: un Ksp pequeño significa baja solubilidad, mientras que un Ksp grande indica una solubilidad relativamente alta.
Cálculo del Ksp a partir de Datos de Solubilidad Experimental
Para calcular el Ksp de un compuesto iónico, necesitamos conocer la ecuación de disolución y las concentraciones molares de cada ion en una solución saturada. A menudo, estas concentraciones se obtienen a partir de datos de solubilidad en masa (gramos disueltos por volumen).
Ejemplo: Cálculo del Ksp para el Cloruro de Plomo(II)
Supongamos que se encontró que 50.0 mL de una solución saturada de cloruro de plomo(II) (PbCl2) contenían 0.2207 g de PbCl2 disueltos.
Paso 1: Escribir la ecuación de disolución y la expresión del Ksp.

PbCl2 (s) → Pb2+(aq) + 2 Cl-(aq)
Ksp = [Pb2+][Cl-]2
Paso 2: Convertir la cantidad de PbCl2 disuelto a moles por litro (solubilidad molar).
Primero, calculamos la masa molar del PbCl2: Pb (207.2 g/mol) + 2 * Cl (35.45 g/mol) = 207.2 + 70.9 = 278.1 g/mol.
Concentración molar = (0.2207 g PbCl2) * (1 mol PbCl2 / 278.1 g PbCl2) * (1 / 50.0 mL solución) * (1000 mL / 1 L)
Concentración molar = 0.0159 mol/L PbCl2 (Esta es la solubilidad molar del PbCl2)
Paso 3: Determinar las concentraciones de los iones en el equilibrio.
Dado que 0.0159 moles de PbCl2 se disuelven por litro, y por cada mol de PbCl2 se produce 1 mol de Pb2+ y 2 moles de Cl-:
- [Pb2+] = 0.0159 M
- [Cl-] = 2 * 0.0159 M = 0.0318 M
Paso 4: Sustituir las concentraciones de equilibrio en la expresión del Ksp y resolver.
Ksp = [0.0159][0.0318]2
Ksp = 0.0159 * 0.00101124
Ksp = 1.61 x 10-5
Determinación de la Solubilidad Molar a partir del Ksp
A menudo, el problema es el inverso: se nos da el valor de Ksp y se nos pide estimar la solubilidad molar del compuesto en agua pura. Esto requiere establecer una relación algebraica entre la solubilidad molar (generalmente denotada como 'x' o 'S') y las concentraciones de los iones en equilibrio.
Ejemplo: Estimación de la Solubilidad de Ag2CrO4
Estimar la solubilidad de Ag2CrO4 en agua pura si su Ksp es 1.1 x 10-12.
Paso 1: Escribir la ecuación de disolución y la expresión del Ksp.
Ag2CrO4 (s) → 2 Ag+(aq) + CrO42-(aq)
Ksp = [Ag+]2[CrO42-]
Paso 2: Definir la solubilidad molar 'x' y expresar las concentraciones de iones en términos de 'x'.
Sea 'x' la solubilidad molar de Ag2CrO4 en mol/L. Esto significa que 'x' moles de Ag2CrO4 se disuelven por litro.
- [Ag+] = 2x (porque se producen 2 moles de Ag+ por cada mol de Ag2CrO4 disuelto)
- [CrO42-] = x (porque se produce 1 mol de CrO42- por cada mol de Ag2CrO4 disuelto)
Paso 3: Sustituir en la expresión del Ksp y resolver para 'x'.
1.1 x 10-12 = [2x]2[x]
1.1 x 10-12 = 4x2 * x
1.1 x 10-12 = 4x3
x3 = (1.1 x 10-12) / 4
x3 = 0.275 x 10-12
x = (0.275 x 10-12)1/3
x = 6.50 x 10-5 M
Por lo tanto, la solubilidad molar de Ag2CrO4 es 6.50 x 10-5 mol/L.
La Importancia de la Estequiometría en la Relación S-Ksp
Es crucial entender que la relación entre la solubilidad molar (S) y el Ksp depende directamente de la estequiometría de la reacción de disolución. Por ejemplo:
- Para una sal 1:1 (ej. AgCl → Ag+ + Cl-): Ksp = S * S = S2
- Para una sal 1:2 (ej. PbCl2 → Pb2+ + 2Cl-): Ksp = S * (2S)2 = 4S3
- Para una sal 1:3 (ej. La(IO3)3 → La3+ + 3IO3-): Ksp = S * (3S)3 = 27S4
Debido a esta dependencia estequiométrica, es imposible comparar directamente las solubilidades de dos sales basándose únicamente en sus valores de Ksp si tienen fórmulas diferentes. Un compuesto con un Ksp numéricamente menor podría ser más soluble que otro con un Ksp mayor si sus estequiometrías son distintas. Para comparar solubilidades, siempre se debe calcular la solubilidad molar (S) a partir de sus respectivos Ksp.
El Efecto del Ion Común en la Solubilidad
La solubilidad de un compuesto iónico poco soluble disminuye significativamente en presencia de un ion común. Un ion común es cualquier ion ya presente en la solución que también es producido por la disociación del compuesto que se está disolviendo. Este fenómeno se explica por el Principio de Le Chatelier: si se añade un producto (el ion común) a un sistema en equilibrio, el equilibrio se desplazará hacia los reactivos para aliviar el estrés, en este caso, reduciendo la disolución del sólido.
Ejemplo: Estimación de la Solubilidad de BaSO4 en una Solución de Na2SO4
Estimar la solubilidad del sulfato de bario (BaSO4) en una solución de sulfato de sodio (Na2SO4) 0.020 M. El Ksp para BaSO4 es 1.1 x 10-10.
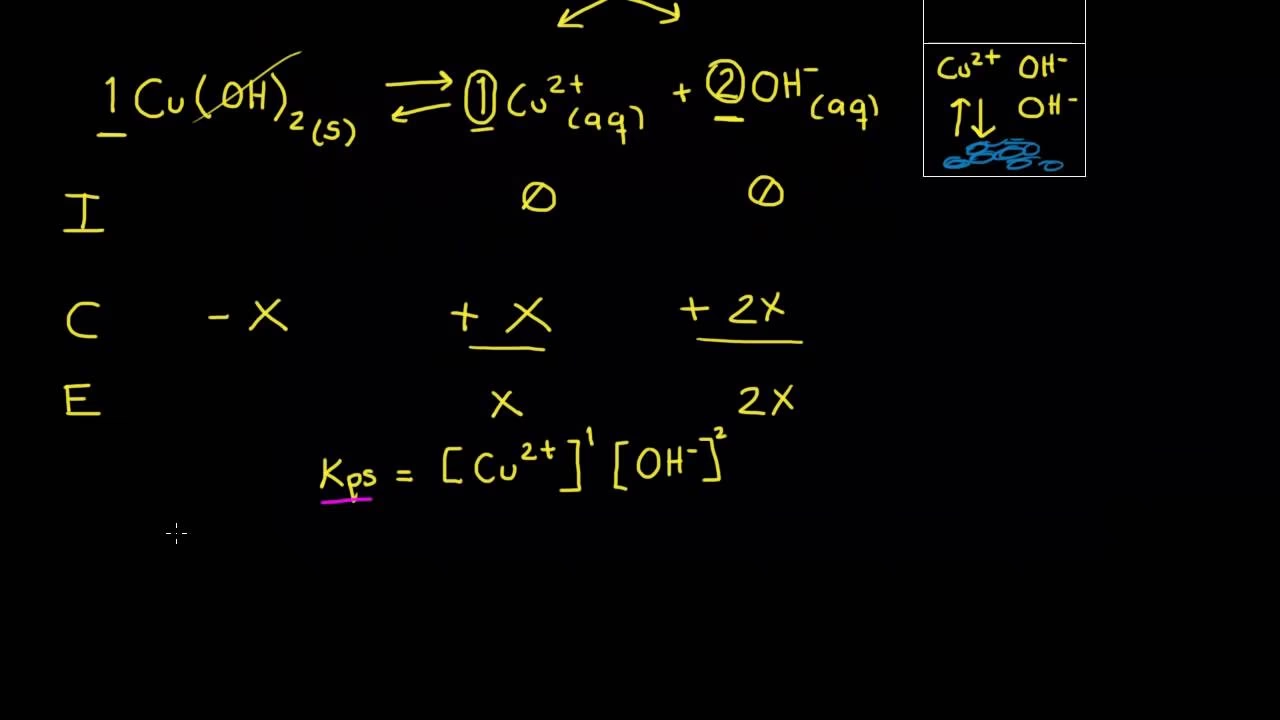
Paso 1: Escribir la ecuación de disolución y la expresión del Ksp.
BaSO4 (s) → Ba2+(aq) + SO42-(aq)
Ksp = [Ba2+][SO42-]
Paso 2: Definir la solubilidad molar 'x' y establecer las concentraciones iniciales y de equilibrio.
Sea 'x' la solubilidad molar de BaSO4 en mol/L. La solución ya contiene un ion común, SO42-, de la disociación completa de Na2SO4 (Na2SO4 → 2Na+ + SO42-). Por lo tanto, la concentración inicial de SO42- es 0.020 M.
| Especie | Concentración Inicial (M) | Cambio (M) | Concentración en Equilibrio (M) |
|---|---|---|---|
| Ba2+ | 0 | +x | x |
| SO42- | 0.020 | +x | 0.020 + x |
Paso 3: Sustituir en la expresión del Ksp y resolver para 'x'.
1.1 x 10-10 = [x][0.020 + x]
Dado que Ksp es muy pequeño, la solubilidad 'x' será muy pequeña. Podemos hacer la suposición de que 'x' es despreciable en comparación con 0.020 M. Es decir, 0.020 + x ≈ 0.020.
1.1 x 10-10 ≈ [x][0.020]
x = (1.1 x 10-10) / 0.020
x = 5.5 x 10-9 M
La solubilidad molar de BaSO4 en la solución de sulfato de sodio es 5.5 x 10-9 mol/L. Nótese que esta solubilidad es significativamente menor que la que tendría en agua pura (donde Ksp = x2, x = √(1.1 x 10-10) ≈ 1.05 x 10-5 M), lo que demuestra el efecto del ion común.
Predicción de la Formación de un Precipitado: El Cociente de Reacción Qsp
Cuando se mezclan dos soluciones electrolíticas, la formación de un precipitado (un sólido insoluble) es una pregunta común. Para determinar si se formará un precipitado, utilizamos el cociente de reacción de solubilidad, Qsp, y lo comparamos con el Ksp del compuesto potencialmente insoluble.
El Qsp tiene la misma forma matemática que el Ksp, pero utiliza las concentraciones iniciales (o instantáneas) de los iones en la solución, antes de que se establezca cualquier equilibrio.
- Si Qsp < Ksp: La solución está insaturada. No se formará precipitado, o si ya hay sólido, se disolverá.
- Si Qsp = Ksp: La solución está saturada. El sistema está en equilibrio; no se formará más precipitado ni se disolverá más sólido.
- Si Qsp > Ksp: La solución está sobresaturada. Se formará un precipitado hasta que las concentraciones de los iones disminuyan y Qsp sea igual a Ksp.
Un factor importante a considerar es la dilución de todas las especies al mezclar dos soluciones. Siempre se deben calcular las nuevas concentraciones de los iones después de la mezcla pero antes de que ocurra cualquier reacción de precipitación.
Ejemplo: ¿Se formará un precipitado de cromato de plomo(II)?
Se mezclan 25.0 mL de cromato de potasio 0.0020 M con 75.0 mL de nitrato de plomo(II) 0.000125 M. El Ksp del cromato de plomo(II) (PbCrO4) es 1.8 x 10-14. ¿Se formará un precipitado?
Paso 1: Escribir la ecuación iónica neta y la expresión del Ksp para el precipitado potencial.
K2CrO4(aq) + Pb(NO3)2(aq) → 2 KNO3(aq) + PbCrO4(s)
La ecuación iónica neta para la formación del precipitado es:
Pb2+(aq) + CrO42-(aq) → PbCrO4(s)
La disolución en términos de Ksp es:
PbCrO4(s) → Pb2+(aq) + CrO42-(aq)
Ksp = [Pb2+][CrO42-]
Paso 2: Calcular las concentraciones iniciales de los iones relevantes después de la mezcla (dilución).
Volumen total de la solución = 25.0 mL + 75.0 mL = 100.0 mL
Para CrO42- (proviene de K2CrO4):
C1V1 = C2V2
(0.0020 M)(25.0 mL) = (C2)(100.0 mL)
C2 = [CrO42-] = (0.0020 M * 25.0 mL) / 100.0 mL = 0.00050 M
Para Pb2+ (proviene de Pb(NO3)2):
C1V1 = C2V2
(0.000125 M)(75.0 mL) = (C2)(100.0 mL)
C2 = [Pb2+] = (0.000125 M * 75.0 mL) / 100.0 mL = 0.0000938 M
Paso 3: Calcular el Qsp y compararlo con el Ksp.
Qsp = [Pb2+][CrO42-]
Qsp = (0.0000938)(0.00050)
Qsp = 4.69 x 10-8
Ahora, comparamos Qsp con Ksp:
Qsp (4.69 x 10-8) > Ksp (1.8 x 10-14)
Dado que Qsp es mayor que Ksp, se formará un precipitado de cromato de plomo(II).
Factores Adicionales que Afectan la Solubilidad
Más allá del Ksp, que se aplica a compuestos iónicos poco solubles en condiciones de equilibrio, la solubilidad de las sustancias en general puede verse afectada por otros factores importantes:
Temperatura
La temperatura tiene un efecto variable en la solubilidad:
- Para la mayoría de los sólidos iónicos: La solubilidad suele aumentar con el aumento de la temperatura. Esto se debe a que la disolución de muchos sólidos es un proceso endotérmico (requiere energía), y el aumento de temperatura favorece la absorción de calor, desplazando el equilibrio hacia la disolución.
- Para los gases: La solubilidad de los gases en líquidos casi siempre disminuye a medida que aumenta la temperatura. Esto se debe a que las moléculas de gas disueltas tienen más energía cinética a temperaturas más altas y pueden escapar más fácilmente de la solución hacia la fase gaseosa. Este fenómeno es crucial en ecología acuática, donde el aumento de la temperatura del agua (contaminación térmica) reduce el oxígeno disuelto, afectando la vida marina.
Presión (Especialmente para Gases)
La presión tiene un efecto significativo en la solubilidad de los gases en líquidos, pero un efecto mínimo en la solubilidad de sólidos y líquidos.

- Ley de Henry: Esta ley establece que la cantidad de un gas ideal que se disuelve en un volumen definido de líquido es directamente proporcional a la presión parcial de ese gas sobre la solución. Matemáticamente, Cg = kPg, donde Cg es la concentración del gas disuelto, Pg es su presión parcial, y k es la constante de Henry, específica para cada gas y solvente a una temperatura dada.
Un ejemplo común es el de las bebidas carbonatadas. Se envasan bajo alta presión de dióxido de carbono, lo que aumenta su solubilidad. Al abrir el envase, la presión disminuye, y el CO2 disuelto escapa en forma de burbujas, haciendo que la bebida se “desinfle”. En medicina, la enfermedad por descompresión (el “mal de descompresión”) en buceadores es otro ejemplo: el nitrógeno se disuelve en la sangre bajo alta presión y burbujea si el ascenso es demasiado rápido.
Naturaleza del Soluto y del Solvente: "Lo Semejante Disuelve a lo Semejante"
La regla general para la solubilidad es que "lo semejante disuelve a lo semejante". Esto significa que las sustancias con polaridades similares tienden a disolverse entre sí debido a las fuerzas intermoleculares compatibles.
- Solventes Polares: Como el agua, disuelven mejor los solutos polares e iónicos (sales, azúcares). Las atracciones dipolo-dipolo o ion-dipolo son fuertes.
- Solventes No Polares: Como el hexano o el benceno, disuelven mejor los solutos no polares (aceites, grasas). Predominan las fuerzas de dispersión de London.
Cuando dos líquidos pueden mezclarse en cualquier proporción para formar una solución homogénea, se dice que son miscibles (ej. etanol y agua). Si apenas se mezclan y forman capas separadas, son inmiscibles (ej. aceite y agua). Algunos líquidos son parcialmente miscibles, lo que significa que tienen una solubilidad mutua moderada, formando dos capas saturadas entre sí.
Preguntas Frecuentes sobre Solubilidad Molar y Ksp
¿Qué es una solución saturada, insaturada y sobresaturada?
Una solución saturada es aquella que contiene la máxima cantidad de soluto que puede disolverse en un solvente a una temperatura y presión dadas, en equilibrio con el soluto no disuelto. Una solución insaturada contiene menos soluto que la cantidad máxima posible y puede disolver más. Una solución sobresaturada contiene más soluto del que normalmente podría disolver en condiciones de equilibrio; son inestables y el exceso de soluto puede precipitar con facilidad.
¿Por qué no se incluyen los sólidos en la expresión de Ksp?
Los sólidos puros tienen una concentración efectiva constante. En un equilibrio heterogéneo que involucra un sólido y sus iones en solución, la cantidad de sólido presente no afecta la posición del equilibrio, siempre y cuando haya algo de sólido presente. Por lo tanto, su concentración se absorbe dentro del valor de la constante de equilibrio, y no se incluye explícitamente en la expresión del Ksp.
¿Se puede comparar la solubilidad de dos sales solo por sus valores de Ksp?
No, solo se pueden comparar directamente los valores de Ksp de sales que tienen la misma estequiometría (por ejemplo, dos sales 1:1 o dos sales 1:2). Para sales con diferentes estequiometrías (ej. AgCl vs. Ag2CrO4), se debe calcular la solubilidad molar (S) de cada una para poder compararlas de manera significativa.
¿Qué es el efecto del ion común?
El efecto del ion común describe la disminución de la solubilidad de un compuesto iónico poco soluble cuando se añade a la solución una fuente externa de uno de sus iones constituyentes. Esto se explica por el Principio de Le Chatelier, que predice que el equilibrio de disolución se desplazará hacia la formación del sólido para compensar el aumento de la concentración del ion común.
¿Cómo sé si se formará un precipitado?
Para saber si se formará un precipitado al mezclar dos soluciones, se calcula el cociente de reacción de solubilidad (Qsp) utilizando las concentraciones de los iones después de la mezcla pero antes de que cualquier reacción ocurra. Si Qsp > Ksp del compuesto potencialmente insoluble, se formará un precipitado. Si Qsp < Ksp, no se formará. Si Qsp = Ksp, la solución está en equilibrio saturado.
Comprender la solubilidad molar y el Ksp es más que un ejercicio académico; es una herramienta práctica que nos permite predecir el comportamiento de las sustancias en solución, desde la química inorgánica hasta la bioquímica y la ciencia de materiales. Dominar estos conceptos te abrirá las puertas a una comprensión más profunda de cómo interactúan las moléculas y los iones en el mundo que nos rodea.
Si quieres conocer otros artículos parecidos a Solubilidad Molar y Ksp: Guía Completa de Cálculos y Conceptos puedes visitar la categoría Química.
