26/10/2023
La solubilidad es un concepto fundamental en la química, la biología y la ingeniería, que nos permite comprender cómo las sustancias interactúan entre sí para formar mezclas homogéneas, conocidas como disoluciones. Desde la preparación de un café por la mañana hasta complejos procesos industriales y biológicos dentro de nuestro cuerpo, la capacidad de una sustancia para disolverse en otra es crucial. Pero, ¿alguna vez te has preguntado por qué el azúcar se disuelve en el agua mientras que la arena no? O, ¿por qué los refrescos pierden su efervescencia al calentarse? La respuesta yace en la intrincada ciencia de la solubilidad.

Este artículo te guiará a través de los principios esenciales de la solubilidad, explorando su definición, los factores clave que la influencian, y las diversas metodologías utilizadas para cuantificarla. Comprender estos aspectos no solo enriquecerá tu conocimiento científico, sino que también te permitirá predecir y manipular el comportamiento de las sustancias en diferentes escenarios.
¿Qué es la Solubilidad? Un Vistazo Profundo
En su esencia, la solubilidad se define como la máxima cantidad de un soluto que puede disolverse en una cantidad dada de disolvente a una temperatura y presión específicas, formando una disolución saturada. Es un equilibrio dinámico entre las fuerzas de atracción intermoleculares que existen entre las moléculas del soluto y las del disolvente, y la variación de entropía que acompaña al proceso de solvatación. Es decir, las moléculas del disolvente deben ser capaces de rodear y separar eficazmente las partículas del soluto para que este se disuelva.
Es importante destacar que la solubilidad se define para fases específicas. Por ejemplo, aunque el aragonito y la calcita son ambos polimorfos de carbonato de calcio (CaCO₃) con la misma fórmula molecular, su solubilidad en agua puede diferir debido a sus distintas estructuras cristalinas. Esta distinción subraya que la organización atómica y molecular del soluto juega un papel tan importante como su composición química.
Factores Clave que Modifican la Solubilidad
La solubilidad de una sustancia no es una propiedad fija, sino que está influenciada por múltiples factores ambientales y químicos. Entender estos factores nos permite predecir y, en muchos casos, controlar el grado de disolución de un compuesto. A continuación, exploraremos los más relevantes:
El Impacto Crucial de la Temperatura
La temperatura es, quizás, el factor más conocido y con mayor influencia en la solubilidad, aunque su efecto puede variar significativamente según la naturaleza del soluto y el disolvente. Para la mayoría de los sólidos, la solubilidad en un líquido aumenta a medida que se incrementa la temperatura. Esto se debe a que el aumento de energía térmica permite que las moléculas del disolvente superen con mayor facilidad las fuerzas intermoleculares que mantienen unidas a las partículas del soluto en su estado sólido, facilitando su dispersión.
Un ejemplo claro de este comportamiento se observa con sales como el nitrato de bario (Ba(NO₃)₂) o el arseniato ácido disódico, que muestran un marcado aumento de solubilidad con la temperatura. Sin embargo, existen excepciones. El cloruro de sodio (NaCl), por ejemplo, exhibe una solubilidad relativamente independiente de la temperatura en agua. Otros compuestos, como el sulfato de cerio(III) o el carbonato de litio, presentan una "solubilidad inversa" o "retrógrada", volviéndose menos solubles en agua a medida que la temperatura aumenta. Un caso aún más complejo es el del sulfato de sodio (Na₂SO₄), que a 32 °C pierde su agua de cristalización (deca-hidratado) para formar una fase anhidra menos soluble, invirtiendo su patrón de solubilidad.

En el ámbito de la química orgánica, la solubilidad de los compuestos casi siempre aumenta con la temperatura. Esta propiedad es la base de la técnica de la recristalización, utilizada para purificar sólidos: el compuesto se disuelve en un disolvente caliente y luego, al enfriar la disolución, el soluto puro cristaliza, dejando las impurezas en la disolución.
Para los solutos gaseosos en disolventes líquidos, el comportamiento es generalmente inverso al de los sólidos. Al elevarse la temperatura, los gases suelen volverse menos solubles en agua. Esto se explica por el hecho de que las moléculas de gas tienen más energía cinética a temperaturas más altas y, por lo tanto, es más probable que escapen de la disolución y regresen a la fase gaseosa. Sin embargo, en disolventes orgánicos, los gases pueden volverse más solubles con el aumento de la temperatura. En cuanto a la solubilidad de líquidos en otros líquidos, la influencia de la temperatura es muy variada; algunos aumentan su miscibilidad, otros la disminuyen, e incluso pueden separarse en dos fases a ciertas temperaturas, como la mezcla de agua y nicotina, que se vuelve inmiscible por encima de los 60 °C.
La Influencia de la Presión en Gases
Mientras que la presión tiene un efecto despreciable en la solubilidad de sólidos y líquidos, es un factor crucial para los solutos gaseosos en disolventes líquidos. La solubilidad de un gas en un líquido aumenta directamente con la presión parcial de ese gas por encima de la disolución. Esta relación se describe mediante la Ley de Henry, que establece que la cantidad de gas disuelto en un líquido es directamente proporcional a la presión parcial del gas sobre el líquido a una temperatura constante.
Un ejemplo cotidiano de la Ley de Henry es el envasado de bebidas carbonatadas. El dióxido de carbono (CO₂) se disuelve en la bebida bajo una presión elevada (alrededor de 4 atmósferas). Al abrir la botella, la presión disminuye drásticamente, lo que reduce la solubilidad del CO₂ y provoca que el gas escape en forma de burbujas, dando lugar a la efervescencia característica.
Otros Factores Determinantes
- Presencia de otras Sustancias: La solubilidad de un compuesto puede verse afectada por la presencia de otras sustancias disueltas en el disolvente. Por ejemplo, la formación de complejos metálicos en líquidos puede aumentar la solubilidad de un ion metálico. Por otro lado, el "efecto del ion común" es un fenómeno donde la solubilidad de un compuesto iónico poco soluble disminuye si se añade a la disolución un ion que ya es parte de ese compuesto. Este efecto se cuantifica mediante la ecuación de equilibrio de solubilidad.
- Fuerza Iónica: Aunque en menor medida, la fuerza iónica de las disoluciones también puede influir en la solubilidad, afectando las actividades de los iones en la disolución.
- Potencial Redox: Para sólidos que se disuelven mediante una reacción redox, la solubilidad dependerá del potencial redox del sistema. Por ejemplo, la solubilidad del oro en agua a alta temperatura puede ser significativamente mayor bajo condiciones altamente oxidantes.
- Tamaño Físico y Defectos Cristalinos: La solubilidad (metaestable) también depende del tamaño físico del grano de cristal o, más estrictamente, de la superficie específica del soluto. Los cristales con mayor área superficial o con defectos significativos en su estructura pueden presentar una solubilidad aumentada. Ambos efectos se relacionan con la energía libre de Gibbs asociada al cristal, proporcionando la fuerza motriz para la precipitación y el crecimiento espontáneo de cristales con el tiempo.
Cuantificando la Solubilidad: Más Allá de lo Cualitativo
Para aplicaciones prácticas y científicas, no basta con saber si una sustancia es soluble o no; es esencial cuantificar su solubilidad. La solubilidad de un soluto específico en un disolvente se expresa generalmente como la concentración de una disolución saturada, utilizando diversas formas de expresar la concentración:
Formas de Expresar la Solubilidad
La solubilidad puede expresarse de varias maneras, dependiendo del contexto y de la fase del soluto y el disolvente. Las unidades más comunes se resumen en la siguiente tabla:
| Base de Cuantificación | Unidades Comunes | Descripción | Aplicación Típica |
|---|---|---|---|
| Por cantidad de Disolvente | g/100 mL, g/dL, g/L | Gramos de soluto por volumen de disolvente. | Laboratorio (cuando el volumen del disolvente es fácil de medir). |
| Por cantidad de Disolvente | g/100 g, g/kg (p/p) | Gramos de soluto por masa de disolvente (peso por peso). | Industria, estudios termodinámicos. |
| Por cantidad de Disolvente | Molalidad (mol/kg) | Moles de soluto por kilogramo de disolvente. | Propiedades coligativas, alta precisión en temperatura. |
| Por cantidad de Disolución | Molaridad (mol/L) | Moles de soluto por litro de disolución. | Volumetrías, reacciones químicas. |
| Por cantidad de Disolución | Fracción molar, Fracción másica (%) | Moles o masa de soluto por moles o masa totales de la disolución. | Estudios de fases, mezclas complejas. |
| Para Líquidos/Gases | v/v (volumen por volumen) | Volumen de soluto por volumen de disolvente o disolución. | Mezclas de líquidos, gases en líquidos. |
Es importante señalar que la conversión entre estas diferentes formas de expresar la solubilidad no siempre es sencilla, ya que a menudo requiere conocer la densidad de la disolución, que puede no ser constante y variar con la concentración. Además, muchos sólidos (como ácidos y sales) se disocian en iones al disolverse, y el disolvente puede formar complejos de coordinación. En estos casos, la suma de los moles de soluto y disolvente no representa el total de moles de partículas independientes en la disolución. Por ello, la solubilidad molar se suele calcular asumiendo que el soluto no se disocia.
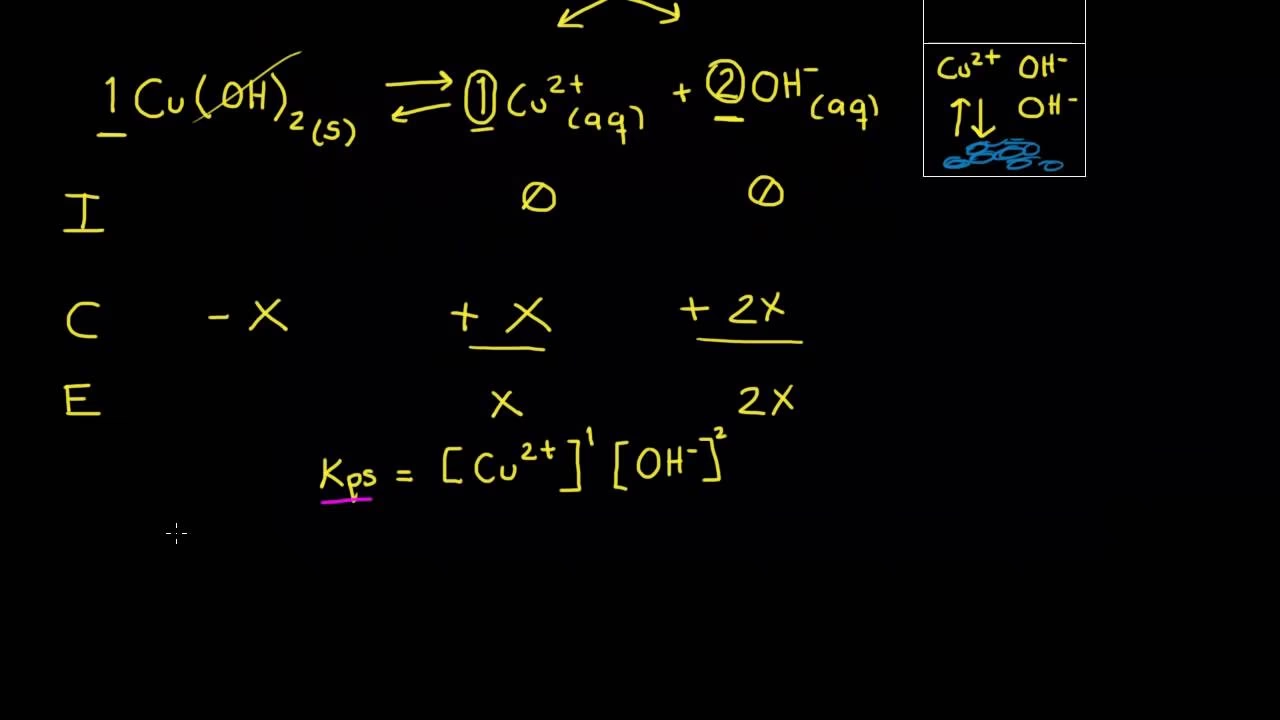
El Producto de Solubilidad (Kps) para Compuestos Iónicos
Para las sales iónicas que son solo ligeramente solubles en agua, su solubilidad se cuantifica a menudo mediante el estudio del equilibrio de solubilidad y la constante conocida como Kps (Producto de Solubilidad). Consideremos el equilibrio de una sal poco soluble, MX:
MX (s) ⇌ M⁺ (ac) + X⁻ (ac)
Cuando un sólido participa en un equilibrio, su concentración no se incluye en la expresión de la constante de equilibrio porque permanece constante. Así, la expresión del producto de solubilidad (Kps) para este ejemplo es:
Kps = [M⁺][X⁻]
El producto de solubilidad de un compuesto iónico es el producto de las concentraciones molares de sus iones constituyentes en una disolución saturada, cada una elevada a la potencia de su coeficiente estequiométrico en la ecuación de equilibrio. Un valor de Kps pequeño indica una baja solubilidad, mientras que un valor grande sugiere una mayor solubilidad. El Kps es crucial para predecir la formación de precipitados o la disolución de sales en diversas condiciones.
Disoluciones Sólidas: Un Mundo Diferente
El concepto de solubilidad no se limita únicamente a líquidos y gases. También existe el fenómeno de las disoluciones sólidas, especialmente relevante en campos como la metalurgia y la ciencia de los materiales. Una disolución sólida se refiere al grado en que un elemento aleado puede disolverse en un metal base sin formar una fase separada.
En un diagrama de fases, la "línea de solubilidad" o "curva de solubilidad" indica los límites de adición de un soluto, mostrando la cantidad máxima de un componente que se puede añadir a otro y aún permanecer como una disolución sólida. Dentro de la estructura cristalina del sólido, el elemento soluto puede ocupar el lugar de un átomo de la matriz (posición sustitucional, como el cromo en el hierro) o un espacio entre los puntos de la red (posición intersticial, como el carbono en el hierro).
En la fabricación microelectrónica, la solubilidad sólida se refiere a la concentración máxima de impurezas que se pueden incorporar en un sustrato semiconductor. En compuestos sólidos (a diferencia de los elementos puros), la solubilidad de un elemento soluto puede depender significativamente de las fases que se separan en equilibrio. Por ejemplo, la cantidad de estaño (Sn) soluble en la fase ZnSb puede variar si las fases en equilibrio son (Zn₄Sb₃ + Sn(L)) o (ZnSnSb₂ + Sn(L)).
Determinar experimentalmente la "solubilidad máxima" en compuestos sólidos puede ser un desafío, ya que requiere equilibrar muchas muestras y considerar el número de fases que se separan, lo cual puede ser complejo según la regla de las fases de Gibbs. Sin embargo, el conocimiento de los defectos cristalográficos dominantes y el uso de pautas termodinámicas sencillas pueden reducir considerablemente el número de experimentos necesarios.
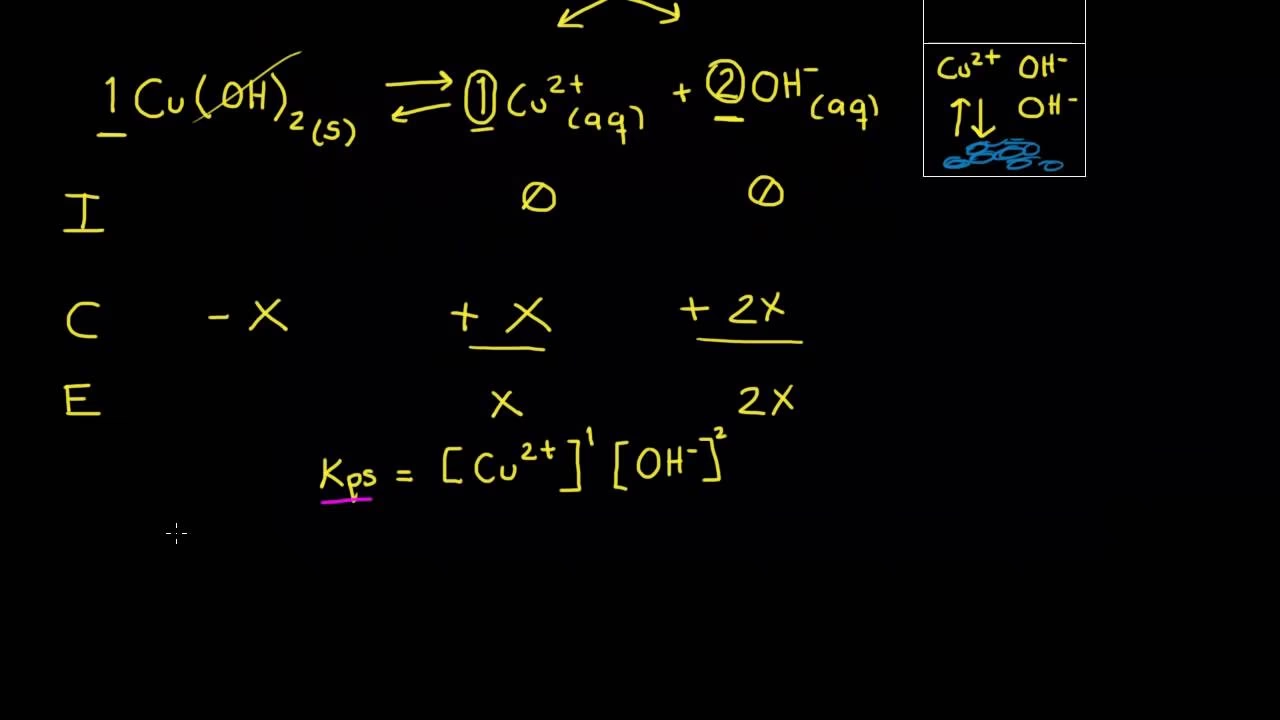
Preguntas Frecuentes (FAQ)
¿Cómo se calcula la solubilidad molar?
La solubilidad molar se calcula como la cantidad de moles de soluto disueltos en un litro de disolución saturada (mol/L). Si conoces la solubilidad en gramos por litro (g/L) y la masa molar del soluto, puedes convertirla dividiendo los gramos de soluto por su masa molar. Por ejemplo, si tienes 10 g/L de un compuesto con una masa molar de 50 g/mol, la solubilidad molar sería 10 g/L / 50 g/mol = 0.2 mol/L.
¿Qué significa una solubilidad en g/L?
Una solubilidad expresada en g/L (gramos por litro) indica la masa máxima de soluto (en gramos) que puede disolverse completamente en un litro de una disolución saturada a una temperatura y presión dadas. Es una forma común y práctica de cuantificar la solubilidad, especialmente en laboratorios y aplicaciones industriales donde la masa y el volumen son medidas convenientes.
¿Por qué la temperatura afecta la solubilidad de manera diferente para sólidos y gases?
La diferencia radica en las interacciones y la naturaleza de las fases. Para la mayoría de los sólidos, la disolución es un proceso endotérmico (requiere energía), por lo que un aumento de temperatura proporciona la energía necesaria para romper los enlaces del sólido y permitir su dispersión. Para los gases, la disolución en un líquido es un proceso exotérmico (libera energía), y las moléculas de gas tienen más energía cinética a temperaturas más altas, lo que las impulsa a escapar de la disolución y volver a la fase gaseosa. Es decir, el aumento de temperatura favorece la fase de mayor energía, que para un gas es la gaseosa, no la disuelta.
¿Qué es el efecto del ion común?
El efecto del ion común es la disminución de la solubilidad de una sal poco soluble cuando se añade a la disolución una fuente externa de uno de los iones de la sal. Según el principio de Le Châtelier, la adición de un ion común desplaza el equilibrio de disolución hacia la formación del sólido, reduciendo así la cantidad de sal que puede disolverse. Por ejemplo, la solubilidad del cloruro de plata (AgCl) disminuye si se añade cloruro de sodio (NaCl) a la disolución, ya que el ion cloruro (Cl⁻) es común a ambos.
Conclusión
La solubilidad es mucho más que la simple capacidad de una sustancia para disolverse. Es un concepto complejo y dinámico que depende de un delicado equilibrio de fuerzas intermoleculares, variaciones de energía y entropía, y una serie de factores externos como la temperatura, la presión y la composición de la disolución. Desde la purificación de compuestos orgánicos mediante recristalización hasta la formulación de bebidas carbonatadas bajo la Ley de Henry o la predicción de precipitados usando el Kps, la comprensión de la solubilidad es indispensable en innumerables aplicaciones científicas e industriales. Al dominar estos principios, obtenemos una poderosa herramienta para manipular y predecir el comportamiento de las sustancias en el vasto mundo de las disoluciones.
Si quieres conocer otros artículos parecidos a ¿Cómo Determinar y Entender la Solubilidad? puedes visitar la categoría Química.

