21/09/2022
El agua, la sustancia más abundante en la superficie terrestre y esencial para la vida, existe en tres estados: sólido, líquido y gaseoso. Este último, conocido como vapor de agua, es un componente invisible pero omnipresente que juega un papel fundamental en numerosos procesos naturales, desde el ciclo hidrológico hasta la regulación de la temperatura global. Comprender la presión de vapor del agua no es solo un ejercicio académico, sino una clave para entender fenómenos meteorológicos, procesos industriales y el mismo comportamiento de nuestro planeta.

En este artículo, exploraremos en profundidad qué es el vapor de agua, cómo se forma y cuáles son sus propiedades distintivas. Nos adentraremos en los métodos experimentales y las ecuaciones que nos permiten determinar su presión de vapor a diferentes temperaturas, un parámetro crítico en diversas aplicaciones científicas y de ingeniería. Finalmente, analizaremos su trascendental rol en la atmósfera terrestre y su influencia en el cambio climático.
- ¿Qué es el Vapor de Agua y Cómo se Forma?
- El Comportamiento de la Densidad del Agua con la Temperatura
- Midiento la Presión de Vapor del Agua: Un Experimento Detallado
- La Ecuación de Antoine: Un Modelo Predictivo
- El Vapor de Agua en la Atmósfera: Un Actor Climático Clave
- Formación de Nubes a Partir de Vapor de Agua
- Preguntas Frecuentes sobre el Vapor de Agua
- Conclusión
¿Qué es el Vapor de Agua y Cómo se Forma?
El vapor de agua es, en esencia, agua (H2O) en su estado gaseoso. Es un gas incoloro e inodoro, aunque a menudo lo asociamos con la niebla o las nubes, que son en realidad diminutas gotas de agua líquida suspendidas en el aire (vapor húmedo). La formación del vapor de agua ocurre principalmente a través de dos procesos físicos: la evaporación y la ebullición del agua líquida, o por sublimación directa del hielo.
A nivel molecular, la formación de vapor de agua implica que las moléculas de H2O obtengan suficiente energía para liberarse de las fuerzas de cohesión que las mantienen unidas en estado líquido o sólido. En el agua líquida, las moléculas están en constante movimiento, separándose y uniéndose. Al aplicar calor, la energía cinética de las moléculas aumenta, y más enlaces de hidrógeno se rompen de lo que se forman. Eventualmente, las moléculas más energéticas escapan a la fase gaseosa. Este proceso se acelera drásticamente al aumentar la temperatura, ya que se requiere más energía para romper los enlaces de hidrógeno.
La ebullición es un caso particular de evaporación acelerada que ocurre a una temperatura específica (100°C a presión atmosférica normal), donde el agua se transforma rápidamente en vapor. Sin embargo, la evaporación puede ocurrir a cualquier temperatura por encima del punto de congelación, aunque de forma más lenta. Una vez que el agua se convierte en vapor, puede permanecer en ese estado hasta que la temperatura descienda o la concentración de vapor en el aire exceda un límite, momento en el cual se produce la condensación, transformándose de nuevo en agua líquida.
El Comportamiento de la Densidad del Agua con la Temperatura
Antes de abordar la presión de vapor, es crucial entender cómo la densidad del agua varía con la temperatura, ya que esta propiedad es fundamental en los métodos de medición. A diferencia de la mayoría de los materiales que se dilatan y disminuyen su densidad al calentarse, el agua tiene un comportamiento anómalo y fascinante.
El hielo (fase sólida) es menos denso que el agua líquida, por lo que flota. La densidad del agua a 0°C es de 999.84 kg/m³. Sorprendentemente, su densidad alcanza un valor máximo alrededor de los 4°C (aproximadamente 999.96 kg/m³) y solo entonces comienza a disminuir con el aumento de la temperatura. Esto significa que el coeficiente de dilatación del agua es negativo entre 0°C y 4°C y positivo a partir de esa temperatura.
Para ilustrar esta característica, se han recopilado datos experimentales de la densidad del agua a diversas temperaturas:
| Temperatura (°C) | Densidad (kg/m³) | Temperatura (°C) | Densidad (kg/m³) |
|---|---|---|---|
| 0 | 999.84 | 45 | 990.22 |
| 5 | 999.96 | 50 | 988.05 |
| 10 | 999.70 | 55 | 985.70 |
| 15 | 999.10 | 60 | 983.21 |
| 20 | 998.20 | 65 | 980.57 |
| 25 | 997.05 | 70 | 977.78 |
| 30 | 995.65 | 75 | 974.86 |
| 35 | 994.03 | 80 | 971.80 |
| 40 | 992.21 | 85 | 968.62 |
La medición de la densidad del agua, como se simula en experimentos, generalmente implica un recipiente cilíndrico con un volumen conocido y un tubo de vidrio delgado que actúa como manómetro. Al calentar el agua, su volumen se expande (excepto entre 0°C y 4°C), haciendo que el nivel de agua ascienda por el tubo. Midiendo esta altura y conociendo las dimensiones del sistema, se puede calcular la densidad del agua a la temperatura deseada, usando la conservación de la masa del agua.
Midiento la Presión de Vapor del Agua: Un Experimento Detallado
La medición de la presión de vapor del agua a diferentes temperaturas es un proceso que se basa en principios termodinámicos y en la interacción entre el vapor y el aire en un sistema cerrado. A continuación, se detalla un método experimental simulado para su determinación.
Presión de Vapor a 0°C
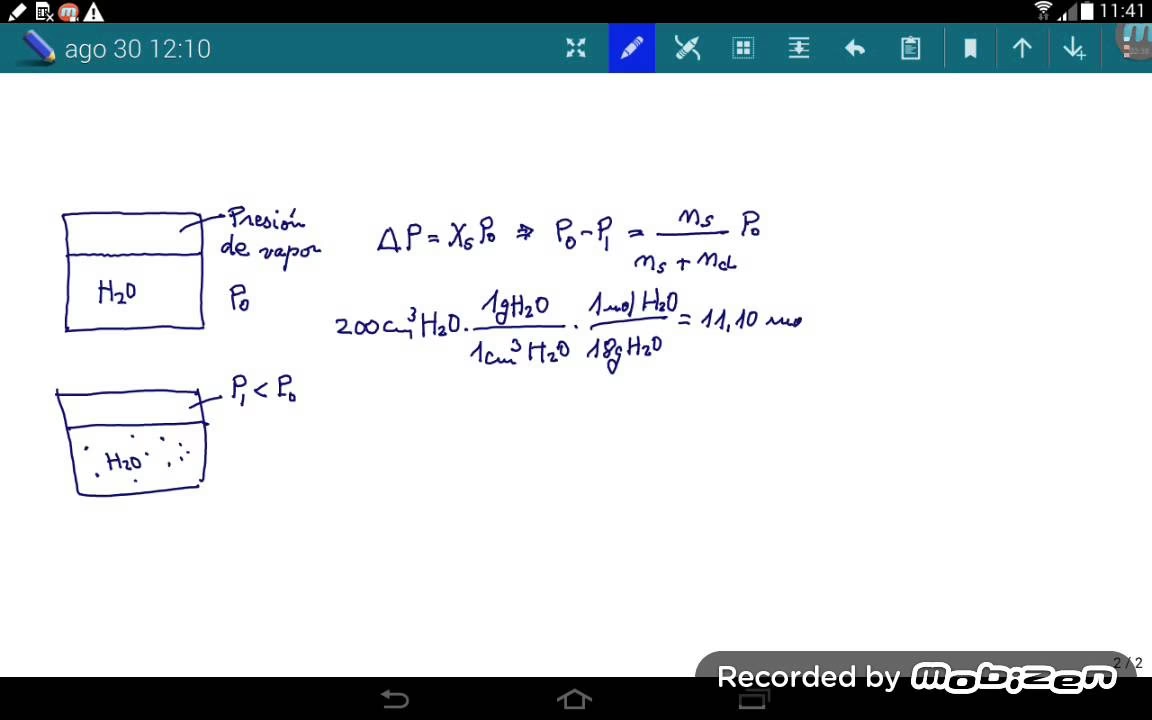
Imaginemos un recipiente cilíndrico sumergido en un baño térmico a 0°C (mezcla de agua y hielo). Se llena el recipiente con agua hasta una altura inicial H0 y se sella con un tapón que contiene un tubo de vidrio que actúa como manómetro. Inicialmente, el volumen S·H0 (donde S es el área de la sección del recipiente) contiene aire a presión atmosférica (Patm).
Una vez cerrado el recipiente, el aire se mezcla con el vapor de agua que se genera. Según la Ley de Dalton de las presiones parciales, la presión total (P) en el recipiente será la suma de la presión parcial del aire (Pa) y la presión de vapor del agua (Pv): P = Pa + Pv.

El aumento de presión hará que el nivel de líquido en el recipiente baje a una altura H, y simultáneamente el agua ascenderá por el tubo de vidrio a una altura h (que puede ser negativa si el nivel baja respecto al origen). Considerando que la cantidad de aire no cambia, su nueva presión parcial Pa se relaciona con el volumen que ocupa: Patm · S · H0 = Pa · S · H.
La conservación de la masa de agua en el sistema cerrado permite relacionar las alturas y densidades:
ρ0 · S · (L - H0) = ρ0 · S · (L - H) + ρ0 · s · H + ρ0 · s · h (para h < 0)
Donde L es la longitud del recipiente, s es el área de la sección del tubo de vidrio y ρ0 es la densidad del agua a 0°C. Al despejar H de esta ecuación y sustituir en la relación de presiones (Pa + Pv = Patm + ρ0 · g · (H + h)), se puede determinar Pv.
Ejemplo práctico a 0°C:
Considerando un recipiente con D=5.5 cm, d=0.59 cm, Patm=101324 Pa y ρ0=999.84 kg/m³. Si la altura inicial de agua en el recipiente es H0=3.0 cm, y se mide una altura h=-1.77 cm (el nivel de agua en el tubo está por debajo del origen), los cálculos arrojan H=3.01 cm y, finalmente, una presión de vapor Pv=602 Pa.
Presión de Vapor a una Temperatura T
El procedimiento para medir la presión de vapor a una temperatura T diferente de 0°C es similar, pero con una consideración adicional importante: la densidad del agua en el tubo de vidrio. Si el líquido asciende por el tubo (h > 0), el agua en esa sección está a temperatura ambiente (Ta = 20°C) y su densidad es ρa = 998.20 kg/m³. Si el líquido desciende (h < 0), la temperatura del líquido en el tubo es la misma que la del recipiente (T), y su densidad es ρ (la densidad del agua a esa temperatura T).
Las ecuaciones de conservación de masa y equilibrio de presiones se ajustan en consecuencia:
- Para h > 0: ρ0 · S · (L - H0) = ρ · S · (L - H) + ρ · s · H + ρa · s · h
- Para h < 0: ρ0 · S · (L - H0) = ρ · S · (L - H) + ρ · s · H + ρ · s · h
Y para la presión:
- Para h > 0: Pa + Pv = Patm + ρ · g · H + ρa · g · h
- Para h < 0: Pa + Pv = Patm + ρ · g · H + ρ · g · h
Ejemplo práctico a 25°C:
Con los datos D=5.5 cm, d=0.59 cm y L=5.514 cm. Sabiendo que Patm=101324 Pa, ρ0=999.84 kg/m³, ρa=998.20 kg/m³ y ρ=997.05 kg/m³ a T=25°C. Si H0=3.0 cm y se mide la altura h=3.99 cm, los cálculos resultan en H=3.07 cm y una presión de vapor Pv=3139 Pa.
La Ecuación de Antoine: Un Modelo Predictivo
Más allá de las mediciones experimentales, existen modelos matemáticos que permiten predecir la presión de vapor del agua en función de la temperatura. Una de las más conocidas y utilizadas es la Ecuación de Antoine. Esta ecuación empírica proporciona una buena aproximación para un rango de temperaturas determinado:
Pv = 1000 · exp(16.573 - 3988.842 / (273 + T - 39.47))
Donde Pv se mide en Pascales (Pa) y T en grados centígrados (°C). Esta fórmula es ampliamente utilizada en simulaciones y cálculos de ingeniería para determinar la presión de vapor saturado del agua a diferentes temperaturas sin necesidad de realizar un experimento físico.
El Vapor de Agua en la Atmósfera: Un Actor Climático Clave
El vapor de agua no es solo un objeto de estudio en el laboratorio; es un componente vital de nuestra atmósfera y un jugador principal en los sistemas climáticos de la Tierra. Aunque incoloro e inodoro, es el gas de efecto invernadero natural más importante, superando en impacto al dióxido de carbono debido a su abundancia y capacidad de absorción de radiación infrarroja.
Propiedades y Distribución Atmosférica
El vapor de agua se encuentra en la atmósfera en niveles traza, pero con concentraciones extremadamente variables que dependen del tiempo y el espacio. Más del 99% del agua atmosférica está en forma de vapor, principalmente en la troposfera (los primeros 2000 metros de altitud). Si todo el vapor de agua en la atmósfera se condensara y cayera, cubriría la Tierra con una capa de aproximadamente 25 mm de profundidad, aunque esta distribución no es homogénea: puede ser de 50 mm en el ecuador y tan solo 2.5 mm en los polos.
La cantidad de vapor de agua en el aire se conoce como humedad. Se distingue entre:
- Humedad absoluta: La cantidad de vapor de agua por unidad de volumen de aire, expresada en g/m³.
- Humedad relativa: La relación porcentual entre la cantidad actual de vapor de agua en el aire y la máxima cantidad que el aire puede contener a una temperatura dada. Cuando la humedad relativa es del 100%, el aire está saturado y el exceso de vapor condensa en forma de nubes, niebla o rocío.
La distribución del vapor de agua en la atmósfera no es uniforme. Las mayores concentraciones se encuentran sobre los océanos y en la zona intertropical debido a la mayor evaporación, mientras que las zonas desérticas presentan las menores cantidades. Esta distribución está estrechamente ligada a la circulación atmosférica y los patrones de temperatura, y varía en todas las escalas temporales, desde la turbulencia diaria hasta fenómenos de gran escala como El Niño.
Saturación y Presión de Vapor Saturante
El aire tiene una capacidad máxima para incorporar vapor de agua a una determinada presión y temperatura. Cuando esta capacidad se excede, el vapor de agua se condensa. A este límite se le llama saturación. Cuanto mayor sea la temperatura del aire, mayor será la cantidad de vapor de agua que puede contener antes de saturarse. La presión de vapor saturante, que es la presión parcial del vapor de agua en aire saturado, aumenta exponencialmente con la temperatura.
Rol en el Ciclo Hidrológico y el Clima
El vapor de agua es un motor fundamental del ciclo hidrológico. Se evapora de la superficie terrestre (océanos, lagos, ríos), es transportado por los vientos, se condensa formando nubes y precipita de nuevo a la superficie, cerrando el ciclo. Este proceso es vital para la distribución del agua dulce en el planeta y la renovación de los reservorios.
En cuanto al clima, el vapor de agua es el gas de efecto invernadero más potente. Absorbe la radiación infrarroja emitida por la superficie terrestre, devolviéndola y provocando un aumento de la temperatura. Sin el vapor de agua y otros gases de efecto invernadero, la temperatura media de la Tierra sería de aproximadamente -18°C en lugar de los 15°C actuales, lo que haría la vida tal como la conocemos imposible.
Sin embargo, en el contexto del cambio climático, el aumento de la temperatura global debido a otros gases de efecto invernadero (como el CO₂) provoca una mayor evaporación y, por ende, un incremento en la cantidad de vapor de agua atmosférico. Esto genera un fenómeno de retroalimentación positiva: más vapor atrapa más calor, lo que a su vez eleva más la temperatura, creando un ciclo que acelera el calentamiento global. Aunque las nubes (agua en estado líquido o sólido) pueden reflejar parte de la radiación solar, el efecto neto del aumento del vapor de agua es un mayor calentamiento.
Formación de Nubes a Partir de Vapor de Agua
Las nubes son la manifestación más visible del vapor de agua condensado en la atmósfera. Se forman cuando una masa de aire cálido y húmedo asciende y se enfría hasta alcanzar su punto de rocío, momento en el que el vapor de agua comienza a condensarse en diminutas gotitas líquidas o cristales de hielo. Para que esto ocurra, se necesitan pequeños "núcleos de condensación" (partículas de polvo, polen, sal, etc.) que sirvan como superficie para que el vapor se adhiera.
El ascenso de las masas de aire puede ser provocado por varios mecanismos:
- Convección: Calentamiento del aire superficial que lo hace menos denso y lo impulsa hacia arriba.
- Convergencia: Convergencia de vientos en superficie que fuerza el aire a ascender.
- Orografía: El aire es forzado a subir al encontrarse con una cadena montañosa.
- Frentes: El encuentro de dos masas de aire de diferente temperatura donde la masa de aire cálido es obligada a ascender sobre la fría.
Preguntas Frecuentes sobre el Vapor de Agua
¿Es el vapor de agua un contaminante?
Aunque el vapor de agua es el gas de efecto invernadero más importante, no se considera un contaminante en el mismo sentido que el CO2 o el metano. Su permanencia en la atmósfera es muy corta (unos 9 días en promedio), a diferencia de otros gases que pueden permanecer por décadas o siglos. Su aumento en la atmósfera es más una consecuencia del calentamiento global impulsado por otros gases que una causa directa.
¿Cómo se mide la humedad en el aire?
La humedad relativa del aire se mide con un instrumento llamado higrómetro. Este dispositivo capta la cantidad de vapor de agua presente en el aire y la compara con la cantidad máxima posible a esa temperatura, expresando el resultado en porcentaje.
¿Puede el agua hervir a menos de 100°C?
Sí, la temperatura de ebullición del agua depende de la presión atmosférica. A mayor altitud, donde la presión atmosférica es menor, el agua hierve a una temperatura inferior a los 100°C. Por ejemplo, en el monte Everest, el agua hierve a unos 71°C.
¿De dónde proviene la mayor parte del vapor de agua atmosférico?
La inmensa mayoría del vapor de agua en la atmósfera se origina por la evaporación de los mares y océanos, impulsada por la energía solar. Una porción menor proviene de la transpiración de las plantas y de la evaporación de cuerpos de agua dulce.
Conclusión
La presión de vapor del agua es una propiedad termodinámica fundamental que rige muchos de los procesos que observamos en la naturaleza y que son aprovechados en la tecnología. Desde su compleja variación de densidad con la temperatura hasta su rol como el principal gas de efecto invernadero, el vapor de agua es un componente dinámico y esencial de nuestro entorno. Comprender cómo medirla y cómo interactúa con otros factores nos permite no solo avanzar en la ciencia, sino también tomar decisiones más informadas sobre cómo gestionar nuestro medio ambiente y sus delicados equilibrios.
Si quieres conocer otros artículos parecidos a Descifrando la Presión de Vapor del Agua puedes visitar la categoría Cálculos.
