05/11/2024
El amoníaco, conocido por su fórmula química NH3, es un compuesto fundamental tanto en la naturaleza como en la industria. Su presencia se extiende desde la atmósfera y los océanos hasta el interior de nuestros cuerpos y los confines del sistema solar. Comprender cómo calcular su masa y la relación entre las masas de sus elementos constituyentes no solo es un ejercicio químico esencial, sino que también es clave para diversas aplicaciones prácticas, desde la formulación de fertilizantes hasta la gestión de su seguridad.
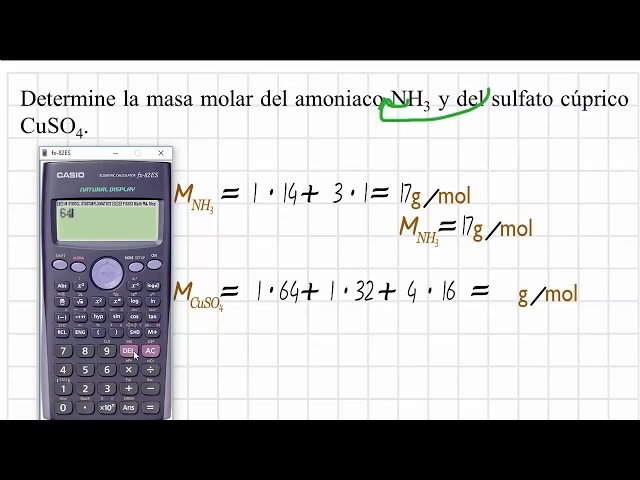
En este artículo, exploraremos en detalle los métodos para determinar la masa molar del amoníaco, cómo calcular la masa de una cantidad dada en gramos y, lo que es igualmente importante, cómo establecer la relación de masas de sus componentes. A través de ejemplos claros y explicaciones concisas, desentrañaremos la química detrás de esta molécula, proporcionando las herramientas necesarias para abordar cualquier cálculo relacionado con el NH3.
¿Qué es el Amoníaco (NH3)?
El amoníaco es un compuesto químico inorgánico de nitrógeno e hidrógeno. A temperatura y presión ambiente, es un gas incoloro con un olor característico y penetrante que muchas personas asocian con productos de limpieza. Su fórmula química, NH3, indica que cada molécula de amoníaco está compuesta por un átomo de nitrógeno (N) y tres átomos de hidrógeno (H).
Este compuesto se encuentra en pequeñas cantidades en la atmósfera, producto de la descomposición de materia orgánica nitrogenada. También está presente en el agua de lluvia, en zonas volcánicas e incluso en el guano. En el cuerpo humano, los riñones secretan amoníaco para neutralizar el exceso de ácido, lo que demuestra su papel vital en procesos biológicos. En el espacio, ha sido detectado en las atmósferas de planetas gigantes como Júpiter y Saturno, y es una molécula clave en las nubes moleculares interestelares, donde se forman nuevas estrellas.
Debido a sus propiedades únicas, el amoníaco es una materia prima indispensable en la industria. Su producción a gran escala se realiza principalmente a través del proceso Haber-Bosch, una reacción que combina nitrógeno atmosférico con hidrógeno bajo condiciones de alta presión y temperatura, y en presencia de un catalizador. Este proceso es fundamental para la fabricación de fertilizantes, lo que lo convierte en un pilar de la agricultura moderna.

Cálculo de la Masa Molar del Amoníaco (NH3)
La masa molar de un compuesto es la masa de un mol de esa sustancia, expresada en gramos por mol (g/mol). Para calcular la masa molar del amoníaco (NH3), necesitamos conocer las masas atómicas de sus elementos constituyentes: el nitrógeno (N) y el hidrógeno (H).
- Masa atómica del nitrógeno (N): Aproximadamente 14.01 g/mol.
- Masa atómica del hidrógeno (H): Aproximadamente 1.008 g/mol.
Dado que una molécula de NH3 contiene un átomo de nitrógeno y tres átomos de hidrógeno, el cálculo se realiza de la siguiente manera:
Masa molar de NH3 = (1 × Masa atómica de N) + (3 × Masa atómica de H)
Masa molar de NH3 = (1 × 14.01 g/mol) + (3 × 1.008 g/mol)
Masa molar de NH3 = 14.01 g/mol + 3.024 g/mol
Masa molar de NH3 = 17.034 g/mol
Este valor nos indica que un mol de amoníaco tiene una masa de 17.034 gramos. Este es un dato crucial para realizar cálculos estequiométricos, como determinar la masa de amoníaco producida en una reacción o la cantidad necesaria para una aplicación específica.
Cómo Calcular la Masa de Amoníaco en Gramos
Una vez que conocemos la masa molar del amoníaco, podemos calcular fácilmente la masa en gramos de cualquier cantidad de moles de NH3 utilizando la siguiente fórmula:
Masa (gramos) = Cantidad de moles (mol) × Masa molar (g/mol)
Ejemplo de Cálculo:
Si necesitamos saber cuál es la masa de 2.5 moles de amoníaco (NH3):
Masa = 2.5 mol × 17.034 g/mol
Masa = 42.585 g
Por lo tanto, 2.5 moles de amoníaco tienen una masa de 42.585 gramos. Este tipo de cálculo es fundamental en laboratorios y procesos industriales para medir y manipular cantidades precisas de amoníaco.
Cómo Calcular la Relación de Masas de NH3
La relación de masas entre los elementos en un compuesto nos indica la proporción en la que se combinan los átomos para formar la molécula. Para el amoníaco (NH3), podemos calcular la relación de masas de nitrógeno a hidrógeno.

Utilizando las masas atómicas:
- Masa de N en NH3 = 1 × 14.01 g/mol = 14.01 g
- Masa de H en NH3 = 3 × 1.008 g/mol = 3.024 g
La relación de masas de N a H es 14.01: 3.024. Para simplificar esta relación, podemos dividir ambos valores por el menor de ellos (3.024):
Relación de N = 14.01 / 3.024 ≈ 4.63
Relación de H = 3.024 / 3.024 = 1
Así, la relación de masas de nitrógeno a hidrógeno en el amoníaco es aproximadamente 4.63: 1. Esto significa que por cada 4.63 gramos de nitrógeno, hay 1 gramo de hidrógeno en el amoníaco.
Porcentaje en Masa de Cada Elemento en NH3
También es útil expresar esta relación como un porcentaje en masa para cada elemento. El porcentaje en masa de un elemento en un compuesto se calcula como:
Porcentaje en masa = (Masa total del elemento en el compuesto / Masa molar del compuesto) × 100%
Para el Nitrógeno (N):
Porcentaje de N = (14.01 g / 17.034 g) × 100% ≈ 82.25%
Para el Hidrógeno (H):
Porcentaje de H = (3.024 g / 17.034 g) × 100% ≈ 17.75%
La suma de los porcentajes (82.25% + 17.75%) es aproximadamente 100%, lo que confirma nuestros cálculos.
Aplicaciones y Consideraciones de Seguridad del Amoníaco
El conocimiento preciso de la masa y la composición del amoníaco es crucial en diversas aplicaciones:
- Fertilizantes: Gran parte del amoníaco producido industrialmente se convierte en fertilizantes. El cálculo de su masa es vital para formular mezclas con la concentración adecuada de nitrógeno, un nutriente esencial para las plantas.
- Limpiadores: Las soluciones de amoníaco (5-10% en peso) se usan comúnmente en limpiadores domésticos, especialmente para cristales. Conocer la concentración en masa es importante para la seguridad y efectividad del producto.
- Refrigeración: El amoníaco es un refrigerante eficiente en sistemas industriales, y su masa es un parámetro clave para el diseño y operación de estos sistemas.
- Seguridad: El amoníaco es un gas con un hedor agudo e irritante. Las concentraciones elevadas pueden causar irritación en la garganta, inflamación pulmonar y daños en las vías respiratorias y los ojos. Una exposición superior a 500 ppm puede ser letal. Es inflamable en un rango de 16-25% en volumen en el aire y tiene una temperatura de autoignición de 651 °C. El conocimiento de su masa, volumen y toxicidad es fundamental para implementar protocolos de seguridad, como el uso de equipos de protección y la instalación de detectores de gas. Es crucial nunca mezclar soluciones de amoníaco con blanqueadores, ya que puede producir gases peligrosos como la cloramina.
Aquí una tabla comparativa de las propiedades relevantes del amoníaco:
| Propiedad | Valor |
|---|---|
| Fórmula Química | NH3 |
| Masa Molar | 17.034 g/mol |
| Estado Físico (Condiciones Estándar) | Gas incoloro |
| Olor | Pungente, irritante |
| Límite Inferior de Inflamabilidad | 16% en volumen en aire |
| Límite Superior de Inflamabilidad | 25% en volumen en aire |
| Temperatura de Autoignición | 651 °C |
| Límite de Exposición Ocupacional (8 horas) | 25 ppm |
| Concentración Letal (aprox.) | >500 ppm |
| Solubilidad en Agua | Alta |
Preguntas Frecuentes (FAQ)
¿Cuál es la masa molar de NH3?
La masa molar del NH3 (amoníaco) es de aproximadamente 17.034 gramos por mol (g/mol). Este valor se obtiene sumando la masa atómica de un átomo de nitrógeno (14.01 g/mol) y la de tres átomos de hidrógeno (3 x 1.008 g/mol).
¿Cómo se calcula la masa de amoníaco en gramos si tengo los moles?
Para calcular la masa en gramos, simplemente multiplicas la cantidad de moles de amoníaco por su masa molar. La fórmula es: Masa (g) = Moles (mol) × Masa Molar (g/mol). Por ejemplo, 5 moles de NH3 serían 5 mol × 17.034 g/mol = 85.17 gramos.

¿Cuál es la relación de masas de nitrógeno e hidrógeno en el amoníaco?
La relación de masas de nitrógeno (N) a hidrógeno (H) en el amoníaco (NH3) es aproximadamente 4.63: 1. Esto significa que por cada 4.63 gramos de nitrógeno, hay 1 gramo de hidrógeno en la molécula de amoníaco.
¿Qué porcentaje en masa de nitrógeno contiene el amoníaco?
El amoníaco contiene aproximadamente un 82.25% de nitrógeno en masa. El resto, un 17.75%, corresponde al hidrógeno.
¿Es peligroso el amoníaco?
Sí, el amoníaco es un gas irritante y tóxico en altas concentraciones. Puede causar daños severos en las vías respiratorias, los ojos y la piel. También es inflamable en ciertas concentraciones en el aire. Es fundamental manejarlo con precaución y seguir las normas de seguridad.
Conclusión
El amoníaco es una molécula de inmensa importancia, y la capacidad de calcular su masa molar, su masa en gramos y la relación de masas de sus componentes es una habilidad química fundamental. Estos cálculos no solo nos permiten comprender la composición intrínseca del NH3, sino que también son herramientas indispensables para su manejo seguro y eficiente en aplicaciones industriales, agrícolas y domésticas. Dominar estos conceptos es un paso crucial para cualquier persona interesada en la química o en la manipulación de sustancias químicas en un entorno práctico.
Si quieres conocer otros artículos parecidos a Calculando la Masa del Amoníaco (NH3) puedes visitar la categoría Química.
