23/04/2023
En el fascinante mundo de la química y la ciencia de materiales, la comprensión de la estructura a nivel atómico es crucial para predecir y manipular las propiedades de los sólidos. La piedra angular de esta comprensión es la celda unitaria, el bloque de construcción fundamental que, al repetirse en las tres dimensiones, da origen a la estructura completa de un cristal. Calcular su masa y densidad no es solo un ejercicio teórico, sino una herramienta indispensable para ingenieros y científicos. Este artículo te guiará paso a paso a través de los conceptos y fórmulas necesarios para dominar estos cálculos esenciales, desvelando cómo la disposición de los átomos influye directamente en las características macroscópicas de un material.

- ¿Qué es una Celda Unitaria?
- Componentes Clave para los Cálculos
- Cálculo de la Masa de una Celda Unitaria
- Cálculo del Volumen de una Celda Unitaria
- Cálculo de la Densidad de una Celda Unitaria: La Fórmula Maestra
- Tipos Comunes de Celdas Unitarias y sus Densidades
- Eficiencia de Empaquetamiento: ¿Cuánto Espacio se Aprovecha?
- La Relación entre la Constante de Red y la Densidad
- Aplicaciones y Significado Práctico
- Preguntas Frecuentes (FAQ)
- ¿Qué es exactamente una celda unitaria y por qué es importante?
- ¿Cómo se determina el número de átomos (z) en una celda unitaria?
- ¿Qué es el Número de Avogadro y por qué se utiliza en estos cálculos?
- ¿Por qué la densidad de la celda unitaria es igual a la densidad del material a granel?
- ¿Qué es la eficiencia de empaquetamiento y cómo se relaciona con la densidad?
- ¿Qué unidades debo usar para asegurar un cálculo correcto de la densidad?
- Conclusión
¿Qué es una Celda Unitaria?
Imagina un patrón que se repite infinitamente, como el de un papel tapiz o los azulejos de un baño, pero extendido al espacio tridimensional. En los sólidos cristalinos, este patrón repetitivo está formado por átomos, iones o moléculas organizadas de manera regular. La unidad mínima de este patrón que conserva la simetría general del cristal y a partir de la cual se puede construir toda la red mediante repetición, es lo que conocemos como celda unitaria.
Los sólidos cristalinos exhiben una disposición regular y repetitiva de partículas constituyentes. La representación diagramática de la disposición tridimensional de estas partículas en un cristal, donde cada partícula se representa como un punto en el espacio, se conoce como red cristalina. Una red es un marco, que se asemeja a una matriz periódica de puntos tridimensionales, sobre la cual se construye un cristal.
En 1850, M. A. Bravais demostró que los puntos idénticos pueden organizarse espacialmente para producir 14 tipos de patrones regulares. Estas 14 redes espaciales se conocen como redes de Bravais. La red cristalina de un sólido puede describirse en términos de su celda unitaria. Una red cristalina está compuesta por un número muy grande de celdas unitarias, donde cada punto de la red está ocupado por una partícula constituyente. La celda unitaria puede verse como una estructura tridimensional que contiene uno o más átomos.
Componentes Clave para los Cálculos
Antes de sumergirnos en las fórmulas, es fundamental comprender los componentes que utilizaremos en nuestros cálculos. Estos son los pilares sobre los que se construyen la masa y la densidad de la celda unitaria:
- Número de átomos en la celda unitaria (z): Este valor representa la cantidad efectiva de átomos que residen dentro de una celda unitaria. No es simplemente contar los átomos visibles, sino considerar las fracciones de átomos que se encuentran en las esquinas, caras o el centro de la celda. Por ejemplo, un átomo en una esquina de una celda cúbica contribuye con 1/8 a esa celda, mientras que uno en una cara contribuye con 1/2 y uno en el centro con 1.
- Masa molar (M): Es la masa de un mol de la sustancia de la que está hecho el cristal, expresada en gramos por mol (g/mol). Este valor es específico para cada elemento o compuesto.
- Número de Avogadro (NA): Una constante fundamental en química, que representa el número de partículas (átomos, moléculas, iones) en un mol de cualquier sustancia. Su valor es aproximadamente 6.022 x 1023 partículas/mol.
- Longitud de la arista de la celda unitaria (a): Para celdas unitarias cúbicas, 'a' es la longitud de uno de sus lados, generalmente expresada en centímetros (cm) o picómetros (pm) y luego convertida.
Cálculo de la Masa de una Celda Unitaria
La masa de una celda unitaria se determina por la cantidad de átomos que contiene y la masa individual de cada uno de esos átomos. La lógica es sencilla: si sabes cuántos átomos hay efectivamente dentro de la celda y cuánto pesa cada uno, puedes calcular la masa total de la celda.
La masa de una celda unitaria se calcula mediante la siguiente relación:
Masa de la celda unitaria = (Número de átomos en la celda unitaria) × (Masa de cada átomo)
Masa de la celda unitaria = z × m
Donde:
- z = número de átomos en la celda unitaria
- m = masa de cada átomo
Pero, ¿cómo calculamos la masa de un solo átomo (m)? Aquí es donde entra en juego la masa molar (M) y el Número de Avogadro (NA). Sabemos que un mol de cualquier sustancia contiene NA átomos y tiene una masa de M gramos. Por lo tanto, la masa de un solo átomo se puede expresar como:
m = M / NA
Sustituyendo esta expresión para 'm' en la fórmula de la masa de la celda unitaria, obtenemos la fórmula completa para la masa de la celda unitaria:
Masa de la celda unitaria = z × (M / NA)
Esta fórmula nos permite calcular la masa de la celda unitaria en gramos, utilizando valores que son fácilmente accesibles o determinables.
Cálculo del Volumen de una Celda Unitaria
El volumen de una celda unitaria es un componente crucial para determinar su densidad. Aunque las celdas unitarias pueden tener diversas geometrías (cúbicas, hexagonales, romboédricas, etc.), el cálculo más común y directo se aplica a las celdas cúbicas debido a su simplicidad y prevalencia en muchos metales y aleaciones.
Para una celda unitaria cúbica, donde todos los lados tienen la misma longitud (a) y los ángulos entre ellos son de 90 grados, el volumen (V) se calcula simplemente elevando al cubo la longitud de su arista:
V = a³
Donde 'a' es la longitud de la arista de la celda unitaria. Es vital asegurarse de que la longitud de la arista se exprese en unidades coherentes con las demás variables de la densidad, típicamente centímetros (cm) para obtener una densidad en g/cm³.
En el caso de celdas unitarias no cúbicas, el cálculo del volumen puede ser más complejo e involucrar ángulos y diferentes longitudes de arista, pero el principio sigue siendo el mismo: determinar el espacio tridimensional que ocupa la celda unitaria.
Cálculo de la Densidad de una Celda Unitaria: La Fórmula Maestra
La densidad (ρ) de cualquier objeto se define como su masa dividida por su volumen. Aplicando esta definición a una celda unitaria, obtenemos la fórmula central para calcular la densidad de un material cristalino a nivel atómico.
La densidad de una celda unitaria se expresa como:
Densidad (ρ) = Masa de la celda unitaria / Volumen de la celda unitaria
ρ = m / V
Ahora, sustituyendo las expresiones que derivamos anteriormente para la masa de la celda unitaria (z × M / NA) y el volumen de una celda unitaria cúbica (a³), obtenemos la fórmula general y más utilizada para la densidad de una celda unitaria:
ρ = (z × M) / (a³ × NA)
Donde:
- ρ = Densidad de la celda unitaria (comúnmente en g/cm³)
- z = Número de átomos en la celda unitaria
- M = Masa molar del elemento o compuesto (en g/mol)
- a = Longitud de la arista de la celda unitaria (en cm)
- NA = Número de Avogadro (6.022 x 1023 mol-1)
Esta fórmula es increíblemente poderosa. Conociendo el tipo de celda unitaria (que nos da 'z'), la masa molar del material, y la longitud de su arista, podemos determinar con precisión la densidad teórica del material cristalino. Esta densidad calculada es fundamental para verificar la pureza de los materiales, diseñar aleaciones con propiedades específicas y comprender el empaquetamiento atómico.
Tipos Comunes de Celdas Unitarias y sus Densidades
El valor de 'z', el número efectivo de átomos por celda unitaria, varía según el tipo de celda unitaria. Comprender estos valores es clave para aplicar correctamente la fórmula de la densidad. A continuación, exploraremos los tipos más comunes de celdas unitarias cúbicas y su valor 'z' asociado, así como la eficiencia de empaquetamiento.

Celda Unitaria Cúbica Simple (SC)
En una celda unitaria cúbica simple, los átomos se encuentran solo en las esquinas de la celda. Como cada esquina es compartida por ocho celdas unitarias adyacentes, cada átomo de esquina contribuye con 1/8 a la celda. Por lo tanto, el número efectivo de átomos en una celda cúbica simple es:
z = 8 esquinas × (1/8 átomo/esquina) = 1 átomo
La fórmula de la densidad para una celda cúbica simple es:
ρ = M / (a³ × NA)
El empaquetamiento en esta estructura no es muy eficiente, con un porcentaje de llenado de solo el 52%. Debido a esta baja eficiencia, es una estructura cristalina muy rara para los metales.
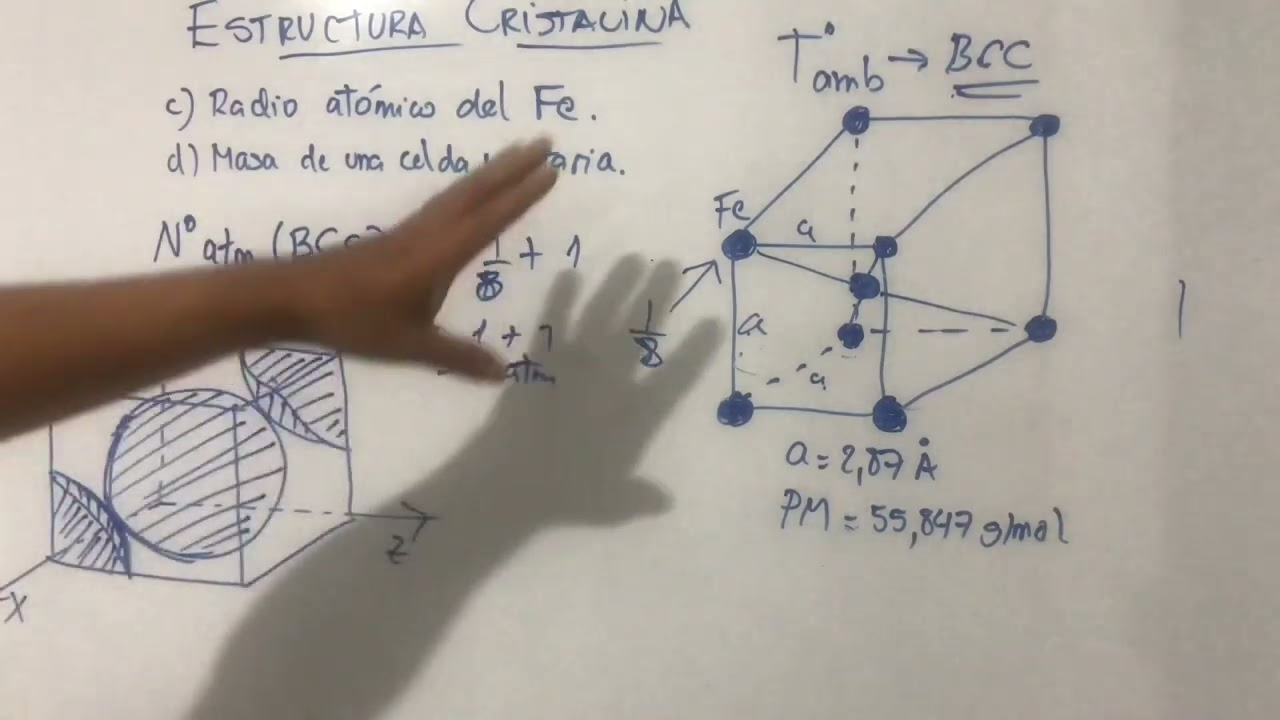
Celda Unitaria Cúbica Centrada en el Cuerpo (BCC)
Una celda unitaria cúbica centrada en el cuerpo tiene átomos en cada esquina (contribuyendo 1/8 cada uno) y un átomo adicional en el centro exacto de la celda, que contribuye con 1 átomo completo. Por lo tanto, el número efectivo de átomos en una celda BCC es:
z = (8 esquinas × 1/8 átomo/esquina) + (1 átomo central × 1 átomo/central) = 1 + 1 = 2 átomos
La fórmula de la densidad para una celda BCC es:
ρ = 2M / (a³ × NA)
El empaquetamiento en las estructuras BCC es más eficiente que en las SC, alcanzando un 68%. Esta estructura es común en muchos metales alcalinos y metales de transición temprana, así como en algunas aleaciones como el latón (CuZn).
Celda Unitaria Cúbica Centrada en la Cara (FCC o CCP)
En una celda unitaria cúbica centrada en la cara, además de los átomos en las esquinas, hay un átomo en el centro de cada una de las seis caras de la celda. Cada átomo de cara es compartido por dos celdas unitarias, contribuyendo con 1/2 a la celda. El número efectivo de átomos en una celda FCC es:
z = (8 esquinas × 1/8 átomo/esquina) + (6 caras × 1/2 átomo/cara) = 1 + 3 = 4 átomos
La fórmula de la densidad para una celda FCC es:
ρ = 4M / (a³ × NA)
Las estructuras FCC, junto con la hexagonal compacta (HCP), tienen la eficiencia de empaquetamiento más alta posible para esferas idénticas, con un 74%. Muchos metales comunes como el cobre, el oro, el aluminio y la plata adoptan esta estructura.
Celda Unitaria Hexagonal Compacta (HCP)
Aunque no es cúbica, la estructura hexagonal compacta es muy común en metales (como el magnesio, el zinc y el titanio) y comparte la misma eficiencia de empaquetamiento del 74% que la FCC. El número efectivo de átomos por celda unitaria en una estructura HCP es 2 (considerando una celda unitaria primitiva que es una sección del cristal hexagonal). Su volumen se calcula de manera diferente a las celdas cúbicas, involucrando su altura y el lado de la base hexagonal.
La siguiente tabla resume las características clave de estos tipos de celdas unitarias:
| Tipo de Celda Unitaria | Átomos efectivos por celda (z) | Fórmula de Densidad (ρ) | Eficiencia de Empaquetamiento |
|---|---|---|---|
| Cúbica Simple (SC) | 1 | M / (a³ × NA) | 52% |
| Cúbica Centrada en el Cuerpo (BCC) | 2 | 2M / (a³ × NA) | 68% |
| Cúbica Centrada en la Cara (FCC) | 4 | 4M / (a³ × NA) | 74% |
| Hexagonal Compacta (HCP) | 2 (en la celda primitiva) | Varía según la geometría específica | 74% |
Eficiencia de Empaquetamiento: ¿Cuánto Espacio se Aprovecha?
La eficiencia de empaquetamiento es una medida de cuán densamente se empaquetan los átomos en una estructura cristalina. Se define como la fracción del volumen de la celda unitaria que está ocupada por los átomos. Dado que los átomos se aproximan a esferas, siempre habrá algún espacio vacío entre ellos, similar a cómo una pila de balas de cañón no llena completamente el espacio.
El cálculo de la eficiencia de empaquetamiento se realiza dividiendo el volumen total de los átomos dentro de la celda unitaria por el volumen total de la celda unitaria en sí:
Eficiencia de Empaquetamiento = (Volumen de los átomos en la celda) / (Volumen de la celda unitaria)
El volumen de los átomos en la celda se obtiene multiplicando el número efectivo de átomos por celda (z) por el volumen de una esfera, que es (4/3)πr³, donde 'r' es el radio atómico.
Como ejemplo, calculemos la eficiencia de empaquetamiento de una celda unitaria cúbica simple. Como vimos, contiene un átomo (z=1). En una celda cúbica simple, los átomos en las esquinas se tocan a lo largo de las aristas, lo que significa que la longitud de la arista 'a' es igual a 2r (dos radios atómicos).
Volumen de los átomos = 1 × (4/3)πr³
Volumen de la celda unitaria = a³ = (2r)³ = 8r³
Eficiencia de Empaquetamiento (SC) = [(4/3)πr³] / [8r³] = (4/3)π / 8 = π / 6 ≈ 0.523 = 52.3%
Este mismo método se puede aplicar a estructuras BCC y FCC, aunque la relación entre 'a' y 'r' es diferente para cada una debido a cómo los átomos se tocan y empaquetan dentro de la celda.
- Para BCC: Los átomos se tocan a lo largo de la diagonal del cuerpo de la celda. La longitud de esta diagonal es 4r. Por el teorema de Pitágoras, la diagonal del cuerpo de un cubo es a√3. Así, 4r = a√3, o a = 4r/√3. La eficiencia de empaquetamiento es aproximadamente 68%.
- Para FCC: Los átomos se tocan a lo largo de la diagonal de la cara de la celda. La longitud de esta diagonal es 4r. Por el teorema de Pitágoras, la diagonal de la cara de un cubo es a√2. Así, 4r = a√2, o a = 4r/√2 = 2r√2. La eficiencia de empaquetamiento es aproximadamente 74%.
La eficiencia de empaquetamiento es un indicador directo de la compacidad de una estructura cristalina, influyendo en propiedades como la densidad y la conductividad.
La Relación entre la Constante de Red y la Densidad
La longitud de la arista de la celda unitaria, a menudo denominada constante de red 'a' (especialmente para celdas cúbicas), es un parámetro fundamental que se mide experimentalmente, por ejemplo, mediante difracción de rayos X. Esta constante es un reflejo directo del tamaño de los átomos y de cómo están empaquetados en el cristal.
La relación entre la constante de red y la densidad es inversamente proporcional a la tercera potencia de la constante de red. Esto significa que un pequeño cambio en la longitud de la arista puede tener un impacto significativo en la densidad del material. Una celda unitaria más grande (mayor 'a') para el mismo número de átomos y masa molar resultará en una menor densidad, ya que el mismo número de átomos ocupa un volumen mayor.

La fórmula de la densidad, ρ = (z × M) / (a³ × NA), encapsula esta relación. Nos permite ver cómo la geometría del empaquetamiento atómico (a través de 'a' y 'z') y la naturaleza de los átomos (a través de 'M') se combinan para determinar la densidad macroscópica de un material. Es esta interconexión lo que permite a los científicos de materiales diseñar aleaciones con densidades específicas para aplicaciones desde la aeronáutica hasta la medicina.
Aplicaciones y Significado Práctico
Los cálculos de la masa y la densidad de la celda unitaria son mucho más que simples ejercicios académicos; tienen una profunda relevancia práctica en la ciencia y la ingeniería de materiales:
- Caracterización de Materiales: La densidad calculada teóricamente puede compararse con la densidad medida experimentalmente para verificar la pureza de un material. Discrepancias pueden indicar la presencia de defectos cristalinos (vacantes, intersticios) o impurezas.
- Diseño de Aleaciones: Al comprender cómo la adición de diferentes elementos afecta el tamaño de la celda unitaria y el número efectivo de átomos, los ingenieros pueden diseñar aleaciones con densidades específicas para aplicaciones donde el peso es crítico, como en la industria aeroespacial o automotriz.
- Predicción de Propiedades: La densidad es una propiedad física fundamental que influye en otras características del material, como la dureza, la conductividad térmica y eléctrica. Un conocimiento preciso de la densidad atómica ayuda a predecir y optimizar estas propiedades.
- Investigación y Desarrollo: En la investigación de nuevos materiales, el cálculo de la densidad de la celda unitaria es un paso inicial para comprender la estructura fundamental y las posibles aplicaciones de un compuesto.
- Ingeniería de Cristalografía: Para los cristalógrafos, estos cálculos son esenciales para la determinación y refinamiento de estructuras cristalinas a partir de datos de difracción.
En esencia, la capacidad de calcular la masa y la densidad de la celda unitaria proporciona una ventana al mundo submicroscópico de los materiales, permitiéndonos comprender y manipular sus propiedades desde la base atómica.
Preguntas Frecuentes (FAQ)
¿Qué es exactamente una celda unitaria y por qué es importante?
Una celda unitaria es la unidad estructural más pequeña y repetitiva que, al replicarse en tres dimensiones, construye toda la red cristalina de un sólido. Es importante porque encapsula toda la información estructural del cristal, permitiendo a los científicos predecir y comprender las propiedades macroscópicas de los materiales a partir de su organización atómica fundamental.
¿Cómo se determina el número de átomos (z) en una celda unitaria?
El valor de 'z' se determina contando la contribución efectiva de cada átomo dentro de la celda unitaria. Los átomos en las esquinas de una celda cúbica contribuyen 1/8 a la celda. Los átomos en las caras contribuyen 1/2. Los átomos en las aristas contribuyen 1/4. Y los átomos en el centro de la celda contribuyen 1. Sumando estas contribuciones se obtiene el valor de 'z' para cada tipo de celda.
¿Qué es el Número de Avogadro y por qué se utiliza en estos cálculos?
El Número de Avogadro (NA = 6.022 x 1023 mol-1) es una constante que representa el número de unidades elementales (átomos, moléculas, etc.) en un mol de cualquier sustancia. Se utiliza en estos cálculos para convertir la masa molar (que es la masa por mol de átomos) a la masa de un solo átomo, lo cual es necesario para calcular la masa de la celda unitaria que contiene un número discreto de átomos.
¿Por qué la densidad de la celda unitaria es igual a la densidad del material a granel?
La densidad de la celda unitaria es igual a la densidad del material a granel (macroscópico) porque la celda unitaria es la unidad repetitiva fundamental del cristal. Si el material es perfectamente cristalino y no tiene defectos significativos (como porosidad o vacantes a gran escala), la densidad promedio de un volumen grande del material será la misma que la densidad de su unidad de repetición más pequeña.
¿Qué es la eficiencia de empaquetamiento y cómo se relaciona con la densidad?
La eficiencia de empaquetamiento es el porcentaje del volumen total de una celda unitaria que está realmente ocupado por los átomos. Se relaciona directamente con la densidad: una mayor eficiencia de empaquetamiento significa que los átomos están más juntos en el espacio, lo que generalmente resulta en una mayor densidad para un material dado, asumiendo que el tamaño y la masa de los átomos son constantes.
¿Qué unidades debo usar para asegurar un cálculo correcto de la densidad?
Para obtener la densidad en unidades comunes como gramos por centímetro cúbico (g/cm³), la masa molar (M) debe estar en g/mol, la longitud de la arista (a) en centímetros (cm) y el Número de Avogadro (NA) en mol-1. Si la longitud de la arista se da en picómetros (pm), debe convertirse a centímetros (1 pm = 10-10 cm).
Conclusión
El cálculo de la masa y la densidad de una celda unitaria es una habilidad fundamental para cualquier persona interesada en la ciencia de materiales, la química del estado sólido o la física de la materia condensada. Hemos explorado cómo la definición de la celda unitaria como la unidad repetitiva de un cristal, junto con el conocimiento de la masa molar del elemento, el Número de Avogadro y las dimensiones de la celda, nos permite desentrañar las propiedades más íntimas de los materiales.
Desde la simple aritmética de contar átomos efectivos hasta la aplicación de la fórmula maestra de la densidad, cada paso es crucial para comprender cómo los átomos se empaquetan y cómo esta organización microscópica se traduce en las propiedades que experimentamos a diario. Dominar estos cálculos no solo amplía nuestra comprensión teórica, sino que también nos equipa con herramientas prácticas para el diseño y la caracterización de materiales en un sinfín de aplicaciones tecnológicas.
Si quieres conocer otros artículos parecidos a Calculando Masa y Densidad de una Celda Unitaria puedes visitar la categoría Química.