18/04/2026
En el fascinante mundo de la bioquímica, las enzimas actúan como los motores de la vida, acelerando las reacciones químicas esenciales para el funcionamiento de todos los organismos. Para comprender cómo estas proteínas catalíticas llevan a cabo su trabajo de manera eficiente, es fundamental analizar su comportamiento cinético. Uno de los parámetros más importantes en este análisis es la constante de Michaelis, conocida como Km. Este valor nos ofrece una visión crucial sobre la interacción entre una enzima y su sustrato, revelando aspectos clave de su afinidad y eficiencia.
Calcular la Km no es solo un ejercicio académico; es una herramienta vital para investigadores y profesionales que buscan entender la regulación metabólica, diseñar fármacos o incluso optimizar procesos biotecnológicos. Aunque existen diversas metodologías para su determinación, una de las más fundamentales y conceptualmente claras es la derivación algebraica a partir de la icónica ecuación de Michaelis-Menten. A lo largo de este artículo, exploraremos en detalle cómo se calcula la Km, su significado biológico y por qué es un pilar en la cinética enzimática.
- ¿Qué es la Constante de Michaelis (Km)?
- La Ecuación de Michaelis-Menten: El Punto de Partida
- Derivación Algebraica de la Km a Partir de la Ecuación de Michaelis-Menten
- Significado Biológico y Práctico de la Km
- Otros Métodos para la Determinación de Km
- Preguntas Frecuentes sobre la Constante de Michaelis (Km)
- Conclusión
¿Qué es la Constante de Michaelis (Km)?
La constante de Michaelis (Km) es un parámetro fundamental en la cinética enzimática que se define como la concentración de sustrato a la cual la velocidad de reacción es la mitad de la velocidad máxima (Vmax). En términos más sencillos, es una medida de la afinidad de una enzima por su sustrato. Un valor de Km bajo indica que la enzima tiene una alta afinidad por su sustrato, lo que significa que puede alcanzar la mitad de su velocidad máxima con una concentración baja de sustrato. Por el contrario, un valor de Km alto sugiere una baja afinidad, requiriendo una mayor concentración de sustrato para alcanzar la misma proporción de velocidad.
Es importante destacar que la Km es una constante característica de cada enzima para un sustrato específico y en condiciones ambientales dadas (pH, temperatura, fuerza iónica). No es una constante universal, sino un valor intrínseco que refleja la eficiencia con la que una enzima puede unirse y procesar su sustrato en un contexto particular. Comprender este valor nos permite predecir cómo se comportará una enzima en diferentes concentraciones de sustrato dentro de un sistema biológico.
La Ecuación de Michaelis-Menten: El Punto de Partida
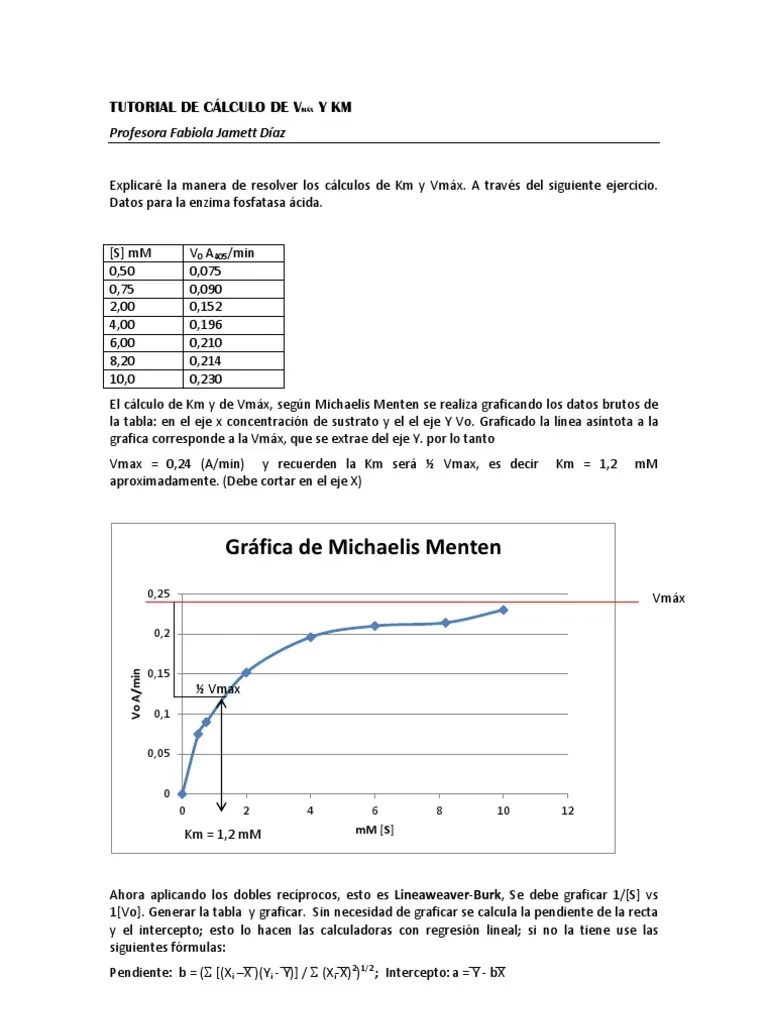
La base para el cálculo de la Km es la ecuación de Michaelis-Menten, desarrollada por Leonor Michaelis y Maud Menten en 1913. Esta ecuación describe la relación entre la velocidad de reacción inicial (V) de una reacción catalizada por una enzima, la concentración de sustrato ([S]), la velocidad máxima (Vmax) y la constante de Michaelis (Km). La ecuación se expresa de la siguiente forma:
V = (Vmax · [S]) / (Km + [S])
Donde:
- V es la velocidad de reacción inicial observada a una concentración de sustrato dada.
- Vmax es la velocidad máxima de reacción que la enzima puede alcanzar cuando está completamente saturada con sustrato. En este punto, todos los sitios activos de la enzima están ocupados.
- [S] es la concentración de sustrato en el medio de reacción.
- Km es la constante de Michaelis, la concentración de sustrato a la cual V = Vmax/2.
Esta ecuación es un modelo simplificado que asume ciertas condiciones, como que la concentración de la enzima es mucho menor que la del sustrato y que la reacción se mide al principio, cuando la concentración de producto es despreciable. A pesar de estas simplificaciones, ha demostrado ser increíblemente útil para describir la cinética de muchas enzimas y es un pilar de la enzimología.
Derivación Algebraica de la Km a Partir de la Ecuación de Michaelis-Menten
Para calcular la Km, podemos reorganizar algebraicamente la ecuación de Michaelis-Menten. El objetivo es aislar Km para poder determinar su valor conociendo las otras variables. Siga los pasos a continuación:
Paso 1: Eliminar el Denominador
Comenzamos con la ecuación original:
V = (Vmax · [S]) / (Km + [S])
Para eliminar el denominador y facilitar el manejo de la ecuación, multiplicamos ambos lados de la ecuación por (Km + [S]):
V · (Km + [S]) = Vmax · [S]
Paso 2: Distribuir V
Ahora, distribuimos la velocidad V en el lado izquierdo de la ecuación:
V · Km + V · [S] = Vmax · [S]
Paso 3: Agrupar Términos con [S]
Nuestro objetivo es aislar Km. Para ello, movemos todos los términos que contienen [S] a un lado de la ecuación. Restamos V · [S] de ambos lados:
V · Km = Vmax · [S] - V · [S]
Paso 4: Factorizar [S]
En el lado derecho de la ecuación, podemos observar que [S] es un factor común. Lo factorizamos:
V · Km = [S] · (Vmax - V)
Paso 5: Aislar Km
Finalmente, para aislar Km, dividimos ambos lados de la ecuación por V:
Km = ([S] · (Vmax - V)) / V
Esta es una forma general de la ecuación para calcular Km si se conocen V, Vmax y [S].
Paso 6: La Condición Clave: V = Vmax/2
La definición de Km establece que es la concentración de sustrato a la cual la velocidad de reacción (V) es exactamente la mitad de la velocidad máxima (Vmax). Sustituyamos V = Vmax/2 en la ecuación derivada en el Paso 5:
Km = ([S] · (Vmax - (Vmax/2))) / (Vmax/2)
Simplificamos el término dentro del paréntesis en el numerador:
Vmax - (Vmax/2) = Vmax/2
Ahora, sustituimos esto de nuevo en la ecuación:
Km = ([S] · (Vmax/2)) / (Vmax/2)
Observamos que el término (Vmax/2) aparece tanto en el numerador como en el denominador, por lo que se cancelan:
Km = [S]
Esta simplificación final es crucial y confirma la definición de la constante de Michaelis: Km es igual a la concentración de sustrato ([S]) cuando la velocidad de reacción (V) es la mitad de la velocidad máxima (Vmax). Esta es la forma más directa y conceptualmente importante de entender el valor de Km.
Significado Biológico y Práctico de la Km
La Km no es simplemente un número; es una ventana al comportamiento de una enzima en un entorno biológico. Su valor tiene implicaciones profundas para entender cómo operan las vías metabólicas y cómo las enzimas responden a los cambios en la disponibilidad de sustrato:
- Afinidad Enzimática: Como se mencionó, una Km baja indica una alta afinidad de la enzima por su sustrato. Esto significa que la enzima puede unirse y catalizar la reacción eficientemente incluso cuando la concentración de sustrato es baja. Esto es vital para enzimas que operan en entornos donde el sustrato es escaso, asegurando que la reacción proceda a una velocidad razonable.
- Regulación Metabólica: En las células, la concentración de muchos sustratos fluctúa. Las enzimas con una Km cercana a la concentración fisiológica de su sustrato son particularmente sensibles a los cambios en esa concentración. Esto les permite ajustar la velocidad de la vía metabólica en respuesta a las necesidades de la célula, actuando como puntos de control.
- Diseño de Fármacos: El conocimiento de la Km es invaluable en farmacología. Los inhibidores enzimáticos, que son la base de muchos medicamentos, a menudo se diseñan para unirse a la enzima con una afinidad mucho mayor que el sustrato natural (es decir, con una Km aparente muy baja para el inhibidor). Comprender la Km de la enzima objetivo y del sustrato natural es crucial para desarrollar fármacos efectivos y específicos.
- Comparación de Enzimas: La Km permite comparar la eficiencia de diferentes enzimas que catalizan la misma reacción, o la eficiencia de una enzima con diferentes sustratos. Esto es útil para comprender la especificidad enzimática y su rol en diversas vías.
Otros Métodos para la Determinación de Km
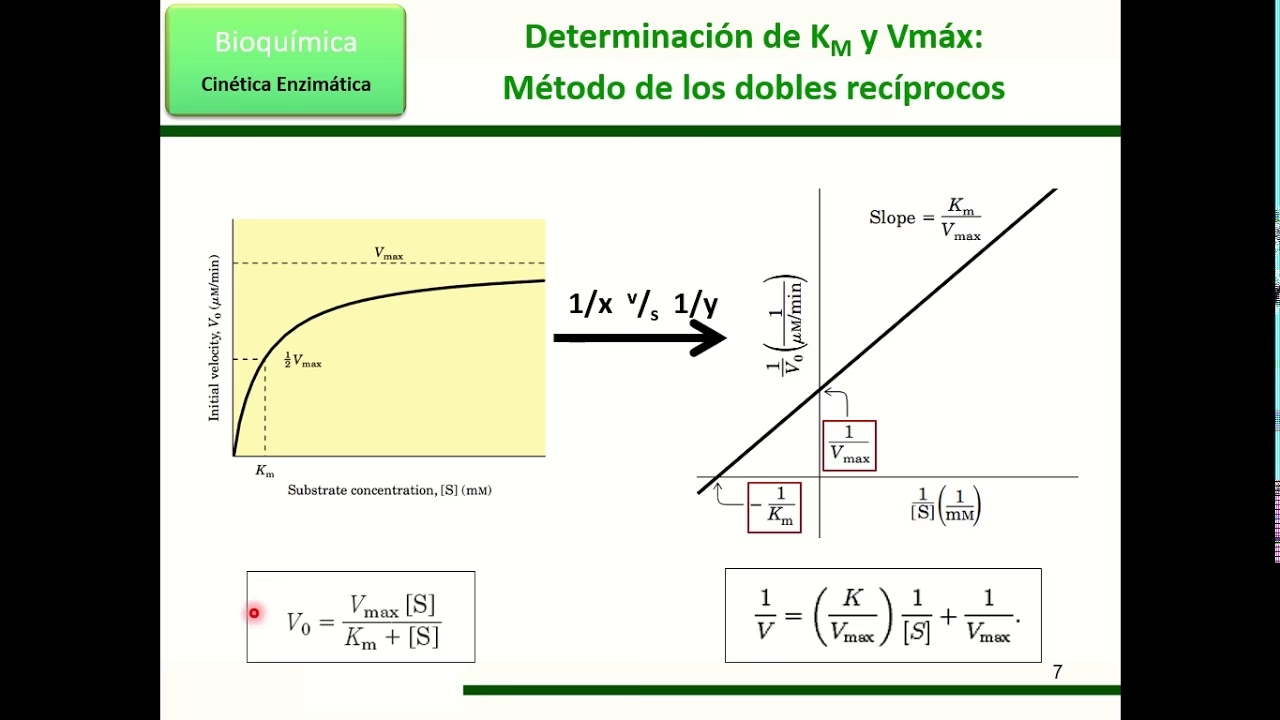
Aunque la derivación algebraica es fundamental para comprender el concepto de Km, en la práctica experimental, la determinación de Km a menudo se realiza utilizando métodos gráficos que transforman la ecuación de Michaelis-Menten en una forma lineal. Estas representaciones permiten una determinación más precisa de Km y Vmax a partir de datos experimentales, así como la identificación de tipos de inhibición enzimática.

- Gráfico de Lineweaver-Burk (Doble Recíproco): Es uno de los métodos más comunes. Implica graficar 1/V contra 1/[S]. La intersección con el eje y es 1/Vmax, y la intersección con el eje x es -1/Km.
- Gráfico de Eadie-Hofstee: Grafica V contra V/[S]. Ofrece una línea recta con pendiente -Km y una intersección con el eje y de Vmax.
- Gráfico de Hanes-Woolf: Grafica [S]/V contra [S]. La pendiente es 1/Vmax, la intersección con el eje y es Km/Vmax, y la intersección con el eje x es -Km.
Si bien estos métodos gráficos son poderosos, la base conceptual para todos ellos sigue siendo la ecuación de Michaelis-Menten y la definición fundamental de Km como la concentración de sustrato a la mitad de la velocidad máxima.
Preguntas Frecuentes sobre la Constante de Michaelis (Km)
¿Qué significa un valor de Km bajo?
Un valor de Km bajo significa que la enzima tiene una alta afinidad por su sustrato. Esto implica que la enzima puede alcanzar la mitad de su velocidad máxima de reacción (Vmax/2) incluso a concentraciones muy bajas del sustrato. En términos biológicos, esto indica que la enzima es muy eficiente en la unión y catálisis de su sustrato, incluso cuando este es escaso.
¿Cómo se relaciona Km con la velocidad máxima (Vmax)?
Km y Vmax son dos parámetros cinéticos independientes pero complementarios. Vmax representa la velocidad máxima de una reacción cuando la enzima está saturada con sustrato, es decir, cuando todos los sitios activos están ocupados. Km, por otro lado, es la concentración de sustrato necesaria para alcanzar la mitad de esa Vmax. Mientras Vmax nos dice cuán rápido puede ir la enzima en su mejor momento, Km nos dice cuán fácilmente (o con qué afinidad) la enzima se une a su sustrato para alcanzar esa velocidad. Ambos son cruciales para describir completamente la eficiencia catalítica de una enzima.
¿Es la Km una constante universal para todas las enzimas?
No, la Km no es una constante universal. Es un valor específico para cada enzima y para cada sustrato con el que interactúa. Además, el valor de Km puede variar ligeramente dependiendo de las condiciones ambientales, como el pH, la temperatura y la fuerza iónica, ya que estas condiciones pueden afectar la estructura y la actividad de la enzima y, por lo tanto, su afinidad por el sustrato.
¿Por qué es importante calcular la Km en la investigación bioquímica?
Calcular la Km es fundamental en la investigación bioquímica por varias razones: permite comparar la eficiencia y la afinidad de diferentes enzimas o de la misma enzima con diferentes sustratos; ayuda a comprender cómo las enzimas operan dentro de las vías metabólicas y cómo responden a los cambios en la concentración de sustrato; es esencial para el diseño y cribado de fármacos, especialmente inhibidores enzimáticos; y proporciona información sobre la regulación y el control de los procesos biológicos a nivel molecular.
¿Qué es la Vmax y cómo se determina?
Vmax, o velocidad máxima, es la velocidad más alta a la que una reacción catalizada por una enzima puede proceder. Se alcanza cuando la concentración de sustrato es tan alta que todos los sitios activos de la enzima están constantemente ocupados. En la práctica, Vmax se determina midiendo la velocidad de reacción a varias concentraciones de sustrato y observando el punto en el que la velocidad ya no aumenta significativamente con el incremento de sustrato. Gráficamente, en un modelo de Michaelis-Menten, Vmax es la asíntota horizontal a la que se aproxima la curva de velocidad vs. concentración de sustrato.
Conclusión
La constante de Michaelis (Km) es mucho más que un simple número en un cálculo; es una medida esencial que desvela la afinidad entre una enzima y su sustrato, proporcionando información invaluable sobre la eficiencia y el comportamiento de las reacciones biológicas. La habilidad para calcular y entender la Km, ya sea mediante la elegante derivación algebraica de la ecuación de Michaelis-Menten o a través de métodos gráficos, es una competencia fundamental para cualquiera que busque comprender a fondo el complejo y dinámico mundo de la bioquímica. Al dominar este concepto, no solo se desentrañan los secretos de la catálisis enzimática, sino que también se abren puertas a aplicaciones prácticas en campos tan diversos como la medicina, la biotecnología y la ingeniería metabólica.
Si quieres conocer otros artículos parecidos a Desvelando la Constante de Michaelis (Km) puedes visitar la categoría Cálculos.