17/10/2023
En el vasto y fascinante universo de la química, los átomos no son entidades aisladas; interactúan constantemente para formar moléculas, la base de toda la materia que nos rodea. Pero, ¿qué impulsa estas interacciones? ¿Por qué algunos átomos se unen fuertemente mientras que otros apenas lo hacen? La respuesta a estas preguntas reside en una propiedad fundamental de los elementos: la electronegatividad. Comprender este concepto no solo nos permite desentrañar cómo se forman los enlaces químicos, sino también predecir las propiedades de las sustancias resultantes. Desde el agua que bebemos hasta los materiales más complejos, la electronegatividad es una fuerza invisible que dicta el comportamiento de la materia.

- ¿Qué es la Electronegatividad?
- ¿Cómo se Determina la Electronegatividad de un Elemento?
- Determinando el Tipo de Enlace por Diferencia de Electronegatividad
- Factores que Influyen en la Electronegatividad
- Importancia y Aplicaciones de la Electronegatividad
- Preguntas Frecuentes (FAQ) sobre la Electronegatividad
- Conclusión
¿Qué es la Electronegatividad?
La electronegatividad es una medida de la tendencia relativa de un átomo a atraer electrones hacia sí mismo cuando forma un enlace químico con otro átomo. Es crucial entender que no se trata de una propiedad de un átomo aislado, sino de su capacidad de atracción de electrones dentro del contexto de un enlace. Cuanto mayor sea la electronegatividad de un elemento, mayor será su poder de atracción sobre los electrones compartidos en una unión. Es una propiedad periódica, lo que significa que sigue patrones predecibles a lo largo de la tabla periódica.
- Tendencia en la Tabla Periódica: La electronegatividad generalmente aumenta a medida que nos movemos de izquierda a derecha en un período (debido a un aumento en la carga nuclear efectiva y una disminución en el radio atómico), y disminuye a medida que bajamos en un grupo (debido a un aumento en el radio atómico y el efecto de apantallamiento de los electrones internos).
- Ejemplo: Consideremos el flúor (F) y el cesio (Cs). El flúor, situado en la esquina superior derecha de la tabla periódica, es el elemento más electronegativo, con un valor de 3.98 en la escala de Pauling. Esto significa que tiene una gran tendencia a atraer electrones. Por otro lado, el cesio, en la esquina inferior izquierda, es uno de los menos electronegativos (0.79 en la escala de Pauling), lo que indica una baja tendencia a atraer electrones y, de hecho, una alta tendencia a cederlos. Cuando un átomo de flúor se une a un átomo de cesio, el flúor atraerá fuertemente los electrones del cesio, resultando en un enlace iónico.
Es importante destacar que la electronegatividad no tiene unidades específicas, ya que es una medida relativa y no una cantidad física absoluta que se pueda medir directamente.
¿Cómo se Determina la Electronegatividad de un Elemento?
A diferencia de otras propiedades como la masa atómica o el punto de ebullición, la electronegatividad no se "calcula" directamente en el sentido de una simple fórmula aritmética a partir de datos fundamentales. En cambio, se deriva o se estima a partir de otras propiedades atómicas y energéticas, y existen varias escalas que intentan cuantificarla. Las más conocidas son la escala de Pauling, la escala de Mulliken y la escala de Allred-Rochow.
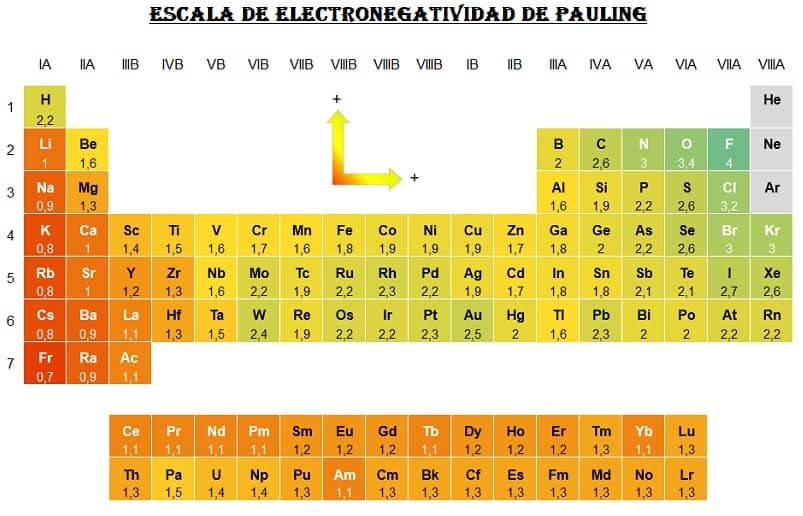
La Escala de Pauling: La Más Utilizada
Desarrollada por el químico Linus Pauling en 1932, esta escala es la más difundida y reconocida. Se basa en la energía de disociación de los enlaces químicos. Pauling observó que la energía de un enlace entre dos átomos diferentes (A-B) es a menudo mayor que la media geométrica de las energías de los enlaces entre átomos idénticos (A-A y B-B). Esta energía extra, o "energía iónica de resonancia", se atribuye a la contribución de la forma iónica del enlace, y se correlaciona con la diferencia de electronegatividad entre los dos átomos.
La fórmula original de Pauling para la diferencia de electronegatividad (ΔEN) entre dos elementos A y B es:
ΔEN = |ENA - ENB| = 0.102 * sqrt(ΔE)
Donde:
ENAyENBson las electronegatividades de los átomos A y B, respectivamente.ΔEes la energía de resonancia iónica, calculada como:ΔE = EAB - sqrt(EAA * EBB)EABes la energía de disociación del enlace A-B.EAAes la energía de disociación del enlace A-A.EBBes la energía de disociación del enlace B-B.
Todas las energías de disociación se expresan en kilocalorías por mol (kcal/mol). Pauling asignó arbitrariamente un valor de 2.1 al hidrógeno para establecer la escala, y luego calculó los valores para los demás elementos de forma relativa. Los valores en la escala de Pauling varían desde aproximadamente 0.7 para el francio (Fr) hasta 4.0 para el flúor (F).
Esta escala es empírica y muy práctica, ya que se basa en propiedades medibles de los enlaces. Sin embargo, no siempre es posible obtener todas las energías de enlace necesarias, lo que puede limitar su aplicación a ciertos pares de elementos.
La Escala de Mulliken: Un Enfoque Teórico
Robert S. Mulliken propuso su escala en 1934, basándose en propiedades atómicas fundamentales: la energía de ionización (IE) y la afinidad electrónica (EA). La energía de ionización es la energía necesaria para remover un electrón de un átomo, mientras que la afinidad electrónica es la energía liberada o absorbida cuando un átomo neutro gana un electrón. Mulliken argumentó que la electronegatividad de un átomo es el promedio de su capacidad para retener electrones (IE) y su capacidad para aceptar electrones (EA).
La fórmula de Mulliken es:
EN = (IE + EA) / 2
Donde IE y EA se expresan en electronvoltios (eV) o kilojulios por mol (kJ/mol). Los valores obtenidos con la escala de Mulliken son típicamente más altos que los de Pauling, pero se pueden convertir a la escala de Pauling mediante una relación lineal (ENPauling ≈ 0.336 * ENMulliken - 0.156). La ventaja de la escala de Mulliken es que se basa en propiedades de átomos aislados, lo que la hace más fundamental y teórica. Sin embargo, la afinidad electrónica no se conoce para todos los elementos, lo que limita su aplicabilidad.
La Escala de Allred-Rochow: Basada en la Fuerza Electroestática
En 1958, A. L. Allred-Rochow desarrollaron una escala que define la electronegatividad como la fuerza electrostática que el núcleo de un átomo ejerce sobre sus electrones de valencia. Esta fuerza se calcula utilizando la ley de Coulomb, teniendo en cuenta la carga nuclear efectiva (Zeff) y el radio covalente (r) del átomo.
La fórmula es:
EN = 0.359 * (Zeff / r²) + 0.744
Donde Zeff es la carga nuclear efectiva experimentada por los electrones de valencia, y r es el radio covalente en angstroms (Å). El término 0.744 es una constante de ajuste para hacer que los valores se aproximen a la escala de Pauling. Esta escala es particularmente útil porque se basa en propiedades atómicas que son relativamente fáciles de calcular o estimar, proporcionando una comprensión más física de la electronegatividad.
En resumen, aunque no hay un "cálculo" directo en el sentido estricto, la electronegatividad se determina mediante el análisis de la energía de los enlaces o de las propiedades fundamentales de los átomos. La escala de Pauling sigue siendo la referencia estándar debido a su utilidad práctica para predecir el comportamiento químico.
Determinando el Tipo de Enlace por Diferencia de Electronegatividad
Una de las aplicaciones más poderosas y prácticas de la electronegatividad es su capacidad para predecir el tipo de enlace químico que se formará entre dos átomos. La diferencia en los valores de electronegatividad (ΔEN) entre los dos átomos enlazados es el factor clave. Cuanto mayor sea esta diferencia, más pronunciada será la polaridad del enlace, y más se acercará a ser un enlace iónico. Por el contrario, una diferencia pequeña o nula indica un enlace covalente.
Tipos de Enlace y sus Rangos de ΔEN
Generalmente, los enlaces se clasifican en tres tipos principales basándose en la diferencia de electronegatividad. Es importante recordar que estos rangos son guías y que la transición entre un tipo de enlace y otro es un continuo, no un corte brusco.
| Rango de Diferencia de Electronegatividad (ΔEN) | Tipo de Enlace Predominante | Descripción | Ejemplo |
|---|---|---|---|
| ΔEN < 0.4 | Covalente No Polar (o Puro) | Los electrones se comparten de manera equitativa entre los dos átomos. Ambos átomos tienen una capacidad de atracción similar. | Cl2 (ΔEN = 0), O2 (ΔEN = 0), H-H (ΔEN = 0) |
| 0.4 ≤ ΔEN < 1.7 (o 1.9) | Covalente Polar | Los electrones se comparten de manera desigual; el átomo más electronegativo atrae los electrones con más fuerza, creando cargas parciales (δ+ y δ-) y un momento dipolar. | H-Cl (ΔEN ≈ 0.9), H2O (O-H ΔEN ≈ 1.4), C-O (ΔEN ≈ 0.9) |
| ΔEN ≥ 1.7 (o 1.9) | Iónico | Ocurre una transferencia completa de uno o más electrones desde el átomo menos electronegativo al más electronegativo, formando iones con cargas opuestas que se atraen electrostáticamente. | Na-Cl (ΔEN ≈ 2.2), K-F (ΔEN ≈ 3.2) |
Es importante notar que el punto de corte para los enlaces iónicos puede variar ligeramente entre 1.7 y 1.9 dependiendo de la fuente o el contexto, ya que, como se mencionó, es un continuo. Un ΔEN de 1.7 se considera el punto donde el carácter iónico es aproximadamente del 50%.
Ejemplos Detallados
- Enlace Covalente No Polar: En una molécula de cloro (Cl2), ambos átomos de cloro tienen la misma electronegatividad (3.16). Por lo tanto, la diferencia es 0. Los electrones compartidos se encuentran exactamente a medio camino entre los dos núcleos, resultando en un enlace no polar.
- Enlace Covalente Polar: En una molécula de cloruro de hidrógeno (HCl), la electronegatividad del cloro es 3.16 y la del hidrógeno es 2.20. La diferencia es 0.96. Esto significa que el cloro atrae los electrones compartidos con más fuerza que el hidrógeno, creando una carga parcial negativa (δ-) en el cloro y una carga parcial positiva (δ+) en el hidrógeno. Aunque los electrones se comparten, el reparto es desigual.
- Enlace Iónico: En el cloruro de sodio (NaCl), la electronegatividad del sodio es 0.93 y la del cloro es 3.16. La diferencia es 2.23. Esta gran diferencia indica que el cloro tiene una atracción tan fuerte por los electrones que "arranca" un electrón del sodio, formando un ion sodio positivo (Na+) y un ion cloruro negativo (Cl-). Estos iones se mantienen unidos por fuertes fuerzas electrostáticas.
La capacidad de predecir el tipo de enlace es fundamental para comprender las propiedades de las sustancias. Por ejemplo, los compuestos iónicos suelen ser sólidos cristalinos con altos puntos de fusión y ebullición, mientras que los compuestos covalentes pueden ser gases, líquidos o sólidos con puntos de fusión y ebullición más bajos, y sus propiedades dependen en gran medida de su polaridad.

Factores que Influyen en la Electronegatividad
Varios factores atómicos influyen en el valor de la electronegatividad de un elemento:
- Carga Nuclear Efectiva (Zeff): Cuanto mayor sea la carga positiva neta experimentada por los electrones de valencia (debido a la carga nuclear real menos el apantallamiento de los electrones internos), mayor será la atracción del núcleo por los electrones y, por lo tanto, mayor la electronegatividad. Esto explica el aumento de la electronegatividad a lo largo de un período.
- Radio Atómico: Cuanto menor sea el radio atómico, más cerca estarán los electrones de valencia del núcleo. Una menor distancia significa una mayor fuerza de atracción, lo que resulta en una mayor electronegatividad. Esto explica la disminución de la electronegatividad al descender en un grupo.
- Apantallamiento Electrónico: Los electrones internos "apantallan" o escudan a los electrones de valencia de la carga completa del núcleo. Un mayor apantallamiento reduce la carga nuclear efectiva y, por ende, la electronegatividad.
Importancia y Aplicaciones de la Electronegatividad
La electronegatividad es una herramienta conceptual indispensable en química por varias razones:
- Predicción de la Reactividad: Permite predecir cómo reaccionarán los elementos entre sí y qué tipo de compuestos formarán.
- Polaridad Molecular: Las diferencias de electronegatividad en los enlaces determinan la polaridad de las moléculas, lo cual es crucial para comprender propiedades físicas como los puntos de ebullición, la solubilidad y las fuerzas intermoleculares. Por ejemplo, la polaridad del agua (debido a los enlaces O-H polares) es responsable de su capacidad como solvente universal y de su alto punto de ebullición.
- Propiedades de los Materiales: Comprender la naturaleza de los enlaces (iónicos, covalentes, metálicos) es fundamental para el diseño y la síntesis de nuevos materiales con propiedades específicas, desde semiconductores hasta polímeros.
Preguntas Frecuentes (FAQ) sobre la Electronegatividad
¿Cuál es el elemento más electronegativo?
El flúor (F) es el elemento más electronegativo, con un valor de 3.98 en la escala de Pauling. Su pequeño tamaño atómico y su alta carga nuclear efectiva le permiten atraer electrones con gran fuerza.
¿Cuál es el elemento menos electronegativo?
El francio (Fr) y el cesio (Cs) son los elementos menos electronegativos. El francio tiene un valor de 0.7 en la escala de Pauling, mientras que el cesio tiene 0.79. Su gran tamaño atómico y el fuerte apantallamiento de sus electrones internos hacen que el electrón de valencia esté muy lejos del núcleo y sea fácilmente cedido.
¿La electronegatividad tiene unidades?
No, la electronegatividad es una cantidad adimensional. Es un valor relativo que se utiliza para comparar la tendencia de los átomos a atraer electrones en un enlace. Las escalas se construyen de manera que los valores sean números puros.
¿Es lo mismo electronegatividad que afinidad electrónica?
No, aunque están relacionadas, son conceptos distintos. La afinidad electrónica es la energía liberada o absorbida cuando un átomo neutro en estado gaseoso gana un electrón para formar un ion negativo. Es una propiedad de un átomo aislado. La electronegatividad, en cambio, es la capacidad de un átomo para atraer electrones compartidos *dentro de un enlace químico* con otro átomo. La afinidad electrónica es una medida absoluta (se mide en energía por mol, como kJ/mol o eV), mientras que la electronegatividad es una medida relativa y sin unidades.
¿Cómo afecta el tamaño del átomo a la electronegatividad?
Generalmente, cuanto más grande es un átomo, menor es su electronegatividad. Esto se debe a que los electrones de valencia están más lejos del núcleo y son menos atraídos por él. Además, hay más electrones internos que "apantallan" la carga nuclear efectiva, reduciendo aún más la atracción sobre los electrones de valencia.
¿Puede un átomo tener una electronegatividad negativa?
No, los valores de electronegatividad son siempre positivos. La escala de Pauling, por ejemplo, asigna valores que van de aproximadamente 0.7 a 4.0. Un valor más alto indica una mayor tendencia a atraer electrones, mientras que un valor más bajo indica una menor tendencia.
Conclusión
La electronegatividad es mucho más que un simple número en la tabla periódica; es una propiedad fundamental que rige las interacciones atómicas y define la naturaleza de los enlaces químicos. Desde las variaciones sutiles en la polaridad de las moléculas hasta la formación de los compuestos iónicos más estables, la diferencia de electronegatividad entre los átomos es la clave para entender por qué las sustancias se comportan de la manera en que lo hacen. Al dominar este concepto, no solo se obtiene una visión más profunda de la estructura de la materia, sino que también se adquiere una herramienta invaluable para predecir y manipular el mundo químico que nos rodea. Es un pilar esencial en el estudio de la química, revelando los secretos de las uniones que dan forma a todo lo existente.
Si quieres conocer otros artículos parecidos a Electronegatividad: La Clave de los Enlaces Químicos puedes visitar la categoría Química.

