05/02/2025
El agua, esa sustancia omnipresente y vital para la vida tal como la conocemos, es mucho más que una simple combinación de hidrógeno y oxígeno. Sus propiedades únicas la convierten en el solvente universal por excelencia y en un pilar fundamental de innumerables procesos químicos y biológicos. Comprender a fondo sus características es clave para desentrañar los misterios de la naturaleza y avanzar en la ciencia. Entre sus propiedades más intrigantes y fundamentales se encuentra su molaridad, un concepto que, aunque a menudo asociado con soluciones, tiene una aplicación peculiar y significativa cuando hablamos del agua en su estado puro. ¿Alguna vez te has preguntado cuántas "partículas" de agua hay en un litro, o cómo se cuantifica su concentración intrínseca? La respuesta reside en la molaridad del agua pura, un valor constante que refleja su composición y densidad inherentes.

Para adentrarnos en la molaridad del agua, primero debemos comprender qué es la molaridad en un sentido más amplio y cómo se aplica a las sustancias químicas. La molaridad es una medida de la concentración de una solución, que nos indica la cantidad de soluto disuelto en un volumen determinado de disolvente. Es una de las formas más comunes y útiles de expresar la concentración en química, permitiendo a los científicos realizar cálculos estequiométricos precisos y predecir el comportamiento de las reacciones. Su importancia radica en que nos proporciona una relación directa entre la cantidad de sustancia (en moles) y el volumen de la solución, facilitando el trabajo en laboratorio y la comprensión de los fenómenos químicos.
- ¿Qué es la Molaridad?
- La Molaridad del Agua Pura
- ¿Por qué es importante la Molaridad del Agua Pura?
- Preguntas Frecuentes (FAQ)
- ¿Qué es el Mol?
- ¿Por qué el agua pura tiene molaridad si no es una solución?
- ¿Es la molaridad del agua siempre 55.56 M?
- ¿Cómo se relaciona la molaridad con la densidad?
- ¿Qué otras unidades de concentración existen además de la molaridad?
- ¿Existe alguna relación entre la molaridad del agua y el resultado del examen UPSC CSE 2023?
- Conclusión
¿Qué es la Molaridad?
La molaridad (M) es una unidad de concentración que se define como el número de moles de soluto por litro de solución. Su unidad de medida en el Sistema Internacional (SI) es moles por litro (mol/L), o simplemente se representa con la letra "M". Esta medida es crucial porque el mol es la unidad que nos permite cuantificar las entidades microscópicas (como átomos, moléculas o iones) en cantidades macroscópicas, sirviendo de puente entre el mundo atómico y el que podemos observar y manipular.
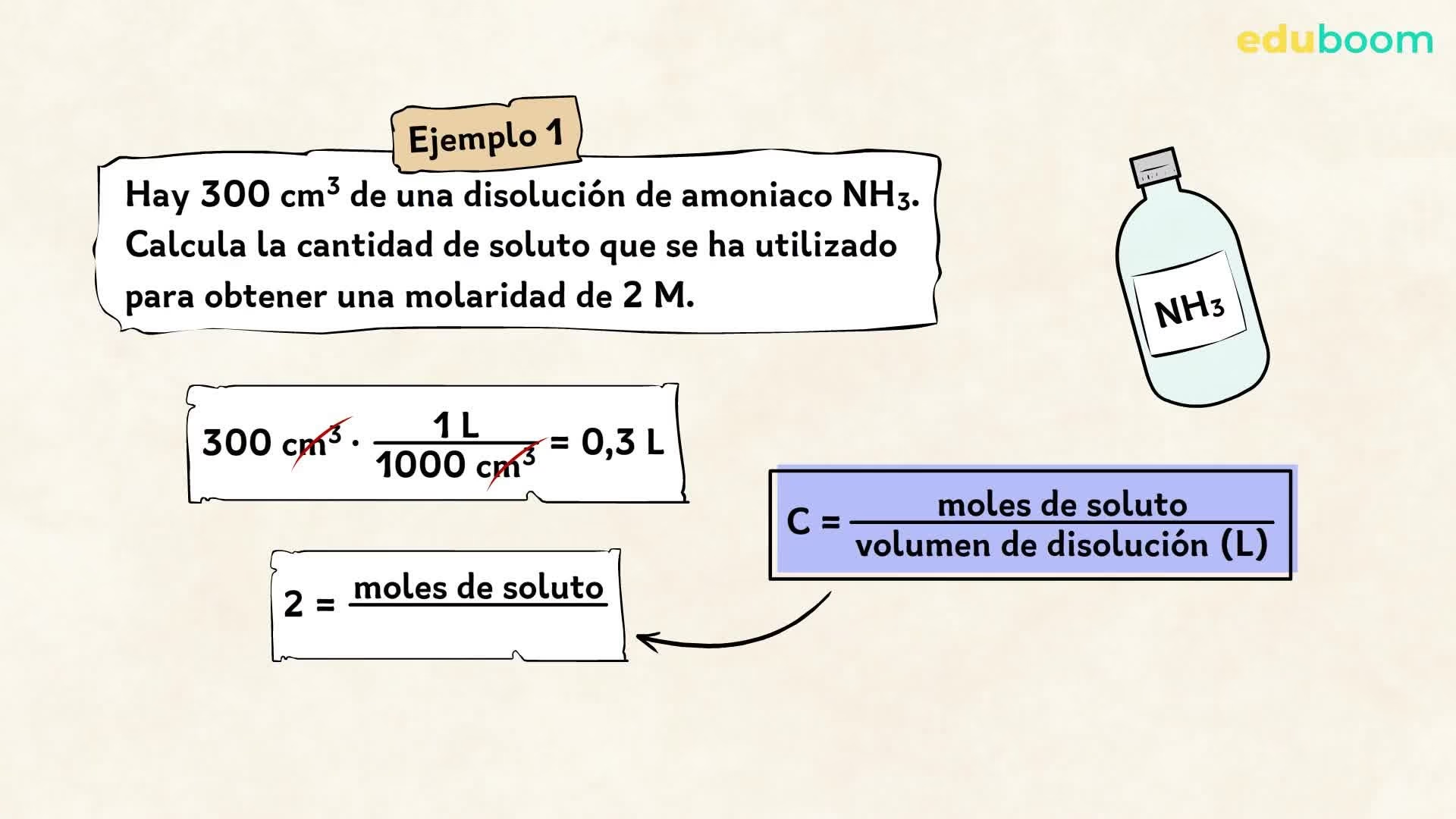
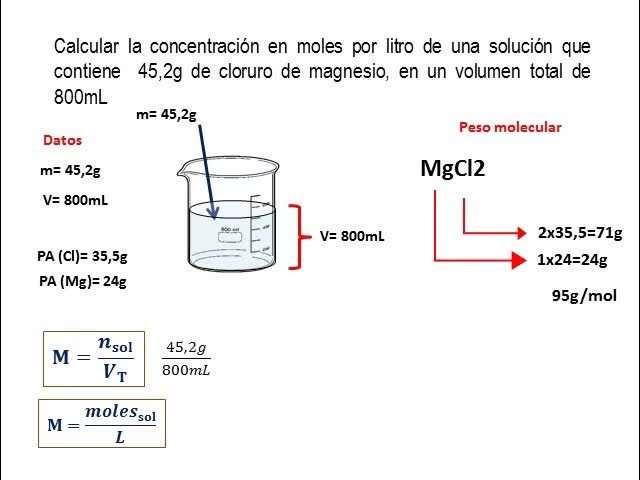
La fórmula fundamental para calcular la molaridad es la siguiente:
Molaridad = Moles de soluto / Litros de solución
Para aplicar esta fórmula, primero necesitamos determinar la cantidad de moles de la sustancia en cuestión. Los moles se calculan dividiendo la masa dada de la sustancia por su masa molecular (o peso molecular). La masa molecular se obtiene sumando las masas atómicas individuales de todos los átomos presentes en una molécula. Por ejemplo, para calcular la masa molecular del dióxido de carbono (CO2):
- Masa atómica del carbono (C) = 12 g/mol
- Masa atómica del oxígeno (O) = 16 g/mol
Así, la masa molecular del CO2 es: (1 * 12) + (2 * 16) = 12 + 32 = 44 gramos/mol.
Una vez que tenemos la masa molecular, podemos calcular los moles dividiendo la masa de la sustancia por esta masa molecular. Esta metodología es aplicable a cualquier sustancia, incluyendo el agua.
La Molaridad del Agua Pura
Cuando hablamos de la molaridad del agua pura, el concepto adquiere una connotación ligeramente diferente a la de una solución típica. En una solución, el agua suele ser el disolvente, y la molaridad se refiere a la concentración del soluto. Sin embargo, para el agua pura, estamos calculando su propia "concentración intrínseca", es decir, cuántos moles de moléculas de H2O hay en un litro de agua sin otras sustancias disueltas.
El agua pura se refiere al agua destilada o desionizada, libre de impurezas, sales disueltas y otros contaminantes. En la naturaleza, el agua de lluvia recién formada por condensación es el ejemplo más cercano al agua pura, aunque incluso esta puede contener pequeñas cantidades de gases disueltos del aire. Para calcular la molaridad del agua pura, partimos de su densidad y su masa molecular.
Cálculo Paso a Paso de la Molaridad del Agua Pura
Para determinar la molaridad del agua pura, seguimos los siguientes pasos:
- Densidad del agua pura: La densidad del agua pura a 4°C es aproximadamente 1 gramo por mililitro (1 g/mL). Esta es una propiedad fundamental que nos permite relacionar la masa con el volumen.
- Conversión de volumen a litros: Dado que la molaridad se define en moles por litro, necesitamos convertir la densidad a gramos por litro.
- 1 g/mL = 1 g / (1/1000 L) = 1000 g/L
Esto significa que 1 litro de agua pura tiene una masa de 1000 gramos (o 1 kilogramo). Este valor se convierte en la "masa de soluto" en nuestro cálculo, aunque en este caso, el "soluto" es el propio agua.
- Masa molecular del agua (H2O): Necesitamos calcular la masa de un mol de moléculas de agua.
- Masa atómica del hidrógeno (H) = 1 g/mol
- Masa atómica del oxígeno (O) = 16 g/mol
La masa molecular del H2O es: (2 * 1) + (1 * 16) = 2 + 16 = 18 gramos/mol.
- Cálculo del número de moles: Ahora que tenemos la masa de un litro de agua pura y su masa molecular, podemos calcular cuántos moles de agua hay en ese litro.
- Moles = Masa de agua pura / Masa molecular del agua
- Moles = 1000 gramos / 18 gramos/mol = 55.555... moles
- Redondeando, obtenemos aproximadamente 55.56 moles.
- Cálculo de la Molaridad: Finalmente, aplicamos la fórmula de molaridad.
- Molaridad = Moles de agua / Volumen de la solución (en litros)
- Molaridad = 55.56 moles / 1 litro = 55.56 M o 55.56 mol/L
Por lo tanto, la concentración molar del agua pura es de aproximadamente 55.56 M.
¿Por qué es importante la Molaridad del Agua Pura?
Aunque a primera vista pueda parecer un cálculo trivial, la molaridad del agua pura tiene implicaciones significativas en diversos campos de la química y la biología:
- Estequiometría de reacciones acuosas: Al conocer la concentración intrínseca del agua, los químicos pueden entender mejor la proporción de reactivos y productos en reacciones que ocurren en soluciones acuosas, especialmente cuando el agua participa directamente como reactivo o producto.
- Termodinámica y propiedades coligativas: La molaridad del agua influye en propiedades como la presión de vapor, el punto de ebullición y el punto de congelación de las soluciones, así como en la presión osmótica. Es un valor de referencia para comprender cómo la adición de solutos altera estas propiedades.
- Disociación iónica y pH: La autoionización del agua (H2O ⇌ H+ + OH-) es un equilibrio fundamental que define el pH y pOH. La concentración de agua es un factor clave en la constante de equilibrio de esta reacción.
- Composición de sistemas biológicos: El agua es el principal componente de los seres vivos. Comprender su molaridad nos ayuda a modelar y entender mejor los entornos celulares y las reacciones bioquímicas que tienen lugar en un medio acuoso.
- Educación y comprensión fundamental: Es un excelente ejemplo para ilustrar el concepto de molaridad en sustancias puras y para solidificar la comprensión de la relación entre masa, moles y volumen.
La molaridad del agua pura es un valor de referencia que subraya su papel no solo como disolvente, sino como una sustancia con su propia "concentración" definida, esencial para la comprensión de sus propiedades y su participación en incontables procesos químicos.
Preguntas Frecuentes (FAQ)
¿Qué es el Mol?
El mol es la unidad de medida del Sistema Internacional (SI) para la cantidad de sustancia. Desde el 20 de mayo de 2019, la definición de mol establece que un mol es la cantidad de una sustancia química que contiene exactamente 6.02214076 × 1023 partículas, ya sean átomos, moléculas, iones u otras entidades elementales. Este número se conoce como la Constante de Avogadro (NA o L). La constante de Avogadro proporciona una forma conveniente de relacionar el peso de una sustancia con el número de partículas que contiene, lo que es fundamental para cálculos en estequiometría.
¿Por qué el agua pura tiene molaridad si no es una solución?
Aunque la molaridad se usa comúnmente para soluciones, donde hay un soluto disuelto en un disolvente, el concepto de molaridad del agua pura se refiere a la concentración de las propias moléculas de agua en un volumen dado. Es una forma de expresar cuántos moles de H2O hay por cada litro de agua, tratándola como si fuera el "soluto" de sí misma. Esto es útil para comparar la "densidad de moles" entre diferentes líquidos puros o para cálculos donde el agua es un reactivo o producto.
¿Es la molaridad del agua siempre 55.56 M?
Sí, la molaridad del agua pura es un valor constante de aproximadamente 55.56 M, siempre y cuando se asuma su densidad estándar de 1 g/mL (o 1000 g/L) a una temperatura cercana a los 4°C. Pequeñas variaciones de temperatura pueden causar ligeros cambios en la densidad del agua, lo que a su vez alteraría mínimamente este valor, pero para la mayoría de los propósitos químicos, 55.56 M se considera la molaridad estándar del agua pura.
¿Cómo se relaciona la molaridad con la densidad?
La densidad es una medida de la masa por unidad de volumen (masa/volumen), mientras que la molaridad es moles por unidad de volumen (moles/volumen). La densidad es crucial para calcular la molaridad de una sustancia pura porque nos permite determinar la masa de esa sustancia presente en un volumen específico (por ejemplo, 1 litro). Una vez que conocemos la masa, podemos convertirla a moles utilizando la masa molecular, y así obtener la molaridad. Por lo tanto, la densidad actúa como un puente entre la masa y el volumen, esenciales para el cálculo de la molaridad.
¿Qué otras unidades de concentración existen además de la molaridad?
Además de la molaridad, existen otras unidades importantes para expresar la concentración de soluciones, como la molalidad (moles de soluto por kilogramo de disolvente), el porcentaje en masa (% m/m), el porcentaje en volumen (% v/v), el porcentaje masa/volumen (% m/v), la fracción molar, y la normalidad (equivalentes gramo de soluto por litro de solución). Cada una de estas unidades tiene aplicaciones específicas y ventajas según el contexto químico o físico en el que se utilice.
| Característica | Molaridad de una Solución | Molaridad del Agua Pura |
|---|---|---|
| Definición Principal | Moles de soluto por litro de solución. | Moles de moléculas de agua por litro de agua (tratada como sustancia "pura"). |
| ¿Qué se disuelve? | Un soluto (ej. NaCl, glucosa) en un disolvente (ej. agua). | No hay soluto disuelto; se calcula la "concentración" de las propias moléculas de H2O. |
| Valor Típico | Varía ampliamente (ej. 0.1 M, 2.5 M, etc.). | Constante, aproximadamente 55.56 M. |
| Dependencia | Depende de la cantidad de soluto y el volumen total de la solución. | Depende de la densidad y la masa molecular del agua. |
| Aplicación | Cálculos de reacciones, preparación de soluciones, propiedades coligativas. | Comprender la densidad molar del agua, su papel como reactivo, punto de referencia. |
¿Existe alguna relación entre la molaridad del agua y el resultado del examen UPSC CSE 2023?
No, la concentración molar del agua pura es un concepto fundamental de la química y no tiene ninguna relación directa con los resultados de exámenes como el UPSC CSE 2023. La mención de dicho examen en la información proporcionada es irrelevante para el tema central del artículo, que se enfoca exclusivamente en la ciencia de las calculadoras y los cálculos químicos.
Conclusión
La molaridad del agua pura, un valor de aproximadamente 55.56 M, es más que un simple número; es una ventana hacia la comprensión profunda de las propiedades fundamentales del H2O. Este cálculo nos permite cuantificar la abundancia de moléculas de agua en un volumen dado, revelando su concentración inherente y su papel como un componente activo en innumerables procesos químicos y biológicos. Desde la estequiometría de las reacciones hasta las propiedades coligativas de las soluciones, la molaridad del agua pura es un pilar conceptual que refuerza nuestro conocimiento sobre esta sustancia vital. Al desentrañar cómo se calcula y por qué es importante, no solo enriquecemos nuestra comprensión de la química, sino que también apreciamos la precisión y la consistencia que rigen el mundo molecular que nos rodea.
Esperamos que este recorrido por la molaridad del agua pura haya sido tan esclarecedor como el propio H2O. Comprender estos conceptos básicos es el primer paso para desentrañar los secretos más complejos de la química y la vida misma.
Si quieres conocer otros artículos parecidos a La Molaridad del Agua Pura: Un Cálculo Esencial puedes visitar la categoría Química.