05/09/2023
En el vasto mundo de la química, la biología y numerosas disciplinas científicas, la preparación de soluciones y el ajuste de sus concentraciones son tareas cotidianas. Sin embargo, un concepto que a menudo genera confusión es el de la dilución y, más específicamente, cómo calcular la concentración de una muestra después de haber sido diluida. Comprender este proceso es fundamental no solo para el éxito en el laboratorio, sino también para aplicaciones prácticas en la industria, la medicina y la vida diaria. Este artículo te guiará paso a paso a través de los principios de la dilución, te enseñará las fórmulas esenciales y te proporcionará ejemplos claros para que puedas calcular la concentración con total confianza.
La dilución es un proceso mediante el cual se reduce la concentración de un soluto en una solución, añadiendo más solvente sin modificar la cantidad de soluto. Es una técnica crucial para preparar soluciones de una concentración específica a partir de una solución madre más concentrada, o para llevar una muestra a un rango de medición adecuado para un instrumento analítico. A menudo, nos encontramos con expresiones como 'dilución 1:4' o 'dilución 1/10', que pueden parecer crípticas al principio. Nuestro objetivo es desmitificar estos términos y equiparte con el conocimiento necesario para realizar cálculos precisos.
Entendiendo los Conceptos Fundamentales de las Soluciones
Antes de sumergirnos en los cálculos, es vital tener claros algunos términos básicos que son la piedra angular de cualquier discusión sobre soluciones y concentraciones.
Soluto, Solvente y Solución
- Soluto: Es la sustancia que se disuelve en otra. Generalmente, es el componente que se encuentra en menor proporción en una solución. Por ejemplo, la sal en agua salada.
- Solvente: Es la sustancia en la que se disuelve el soluto. Es el componente que se encuentra en mayor proporción. El solvente más común es el agua, que se conoce como el 'solvente universal' debido a su capacidad para disolver una gran variedad de sustancias.
- Solución: Es una mezcla homogénea de una o más sustancias (solutos) disueltas en otra sustancia (solvente). Las soluciones son mezclas donde las partículas del soluto están distribuidas uniformemente a nivel molecular o iónico, de modo que la mezcla tiene una composición y propiedades uniformes en toda su extensión.
¿Qué es la Concentración?
La concentración de una solución es una medida de la cantidad de soluto disuelto en una cantidad dada de solvente o de solución. Existen diversas formas de expresar la concentración, como la molaridad (moles de soluto por litro de solución), el porcentaje en masa/volumen, partes por millón (ppm), etc. Para los propósitos de la dilución, lo importante es que la concentración nos dice 'cuánto soluto hay en cuanta solución'.
El Factor de Dilución: Clave para el Cálculo
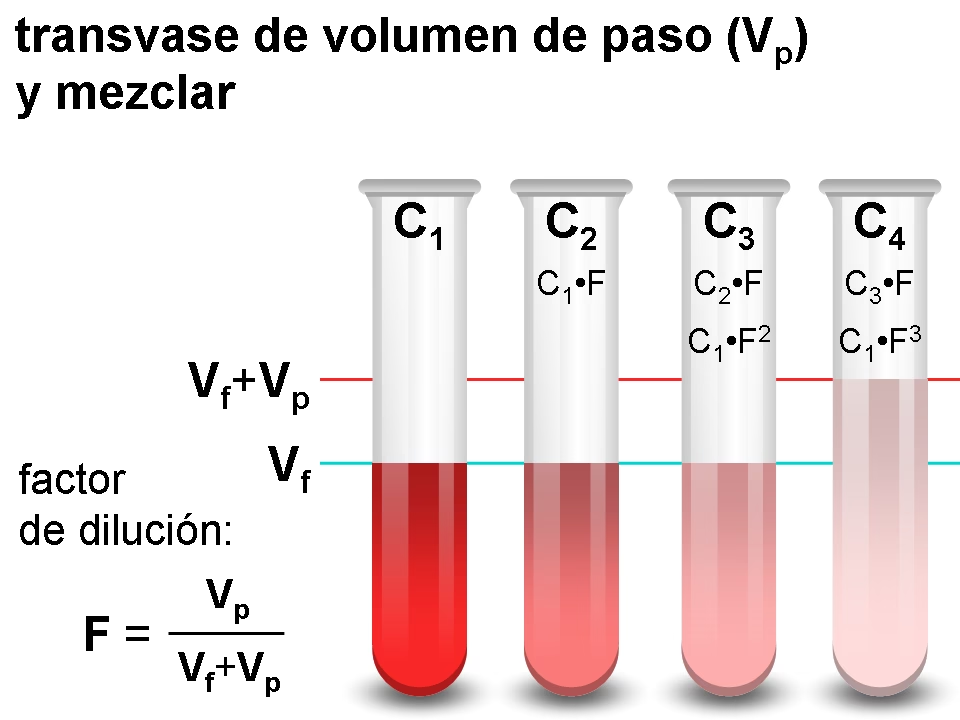
El factor de dilución es un número que representa la relación entre el volumen final de la solución diluida y el volumen inicial de la solución concentrada (o la muestra original). También puede entenderse como el número de veces que la concentración original ha sido reducida. Es crucial no confundir el factor de dilución con la relación de dilución (o ratio de dilución).
Consideremos el ejemplo proporcionado: "hay una parte de volumen de muestra y cuatro partes de volumen del líquido utilizado para diluir la muestra, lo que da un total de cinco partes de volumen."
- Volumen de la muestra (soluto): 1 parte
- Volumen del diluyente (solvente): 4 partes
- Volumen total de la solución diluida: 1 parte (muestra) + 4 partes (diluyente) = 5 partes
En este caso, la relación de dilución se expresa a menudo como 1:4 (muestra:diluyente) o 1:5 (muestra:volumen total final). Es fundamental entender la diferencia.
El factor de dilución (FD) se calcula como:
FD = Volumen Final de la Solución / Volumen Inicial de la Muestra
Para nuestro ejemplo de '1 parte de muestra y 4 partes de diluyente', el volumen inicial de la muestra es 1 y el volumen final es 5. Por lo tanto:
FD = 5 / 1 = 5
Esto significa que la solución original ha sido diluida 5 veces. En otras palabras, la concentración de la solución original es 5 veces mayor que la concentración de la solución diluida.
Tabla Comparativa de Expresiones de Dilución
| Expresión de Dilución | Significado | Ejemplo para FD = 5 (1 parte de muestra + 4 partes de diluyente) |
|---|---|---|
| Ratio (Muestra:Diluyente) | Partes de muestra por partes de diluyente. No incluye el volumen total. | 1:4 (Se mezcla 1 parte de muestra con 4 partes de diluyente) |
| Ratio (Muestra:Volumen Total) | Partes de muestra en el volumen total final. | 1:5 (1 parte de muestra en un volumen total final de 5 partes) |
| Fracción de Dilución | Volumen de muestra sobre el volumen total final. Es el inverso del factor de dilución. | 1/5 (La concentración final es 1/5 de la original) |
| Factor de Dilución (X-fold) | Cuántas veces se ha diluido la muestra. Es el volumen total final dividido por el volumen de la muestra. | 5 (La muestra original es 5 veces más concentrada que la diluida) |
La Fórmula Fundamental para la Dilución: C1V1 = C2V2
La relación entre la concentración y el volumen de una solución antes y después de la dilución se describe mediante una fórmula simple pero poderosa: C1V1 = C2V2.
- C1: Concentración inicial de la solución (antes de la dilución).
- V1: Volumen inicial de la solución (antes de la dilución).
- C2: Concentración final de la solución (después de la dilución).
- V2: Volumen final de la solución (después de la dilución).
Esta fórmula se basa en el principio de que la cantidad de soluto permanece constante durante el proceso de dilución. Es decir, aunque se añade más solvente, la cantidad de soluto (moles, gramos, etc.) no cambia. Por lo tanto, (Concentración inicial * Volumen inicial) debe ser igual a (Concentración final * Volumen final).
Cálculo de la Concentración a Partir de la Dilución
Ahora que conocemos los conceptos y la fórmula, podemos abordar el cálculo de la concentración de una muestra diluida.
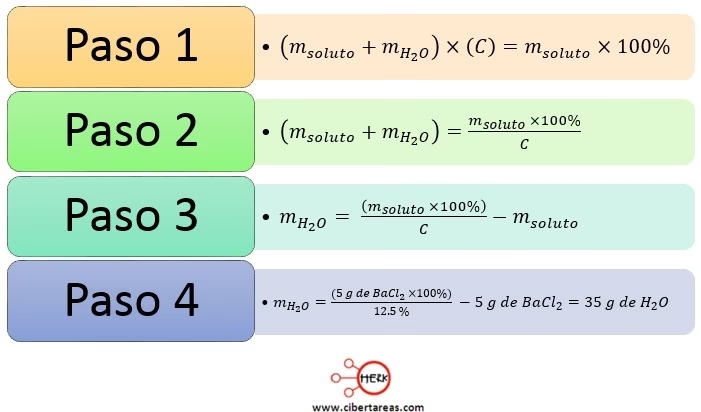
Paso a Paso para Calcular C2
- Identifica tus valores conocidos: Generalmente, conocerás C1 (concentración de la solución madre), V1 (volumen de la solución madre que tomaste) y V2 (volumen final de la solución diluida).
- Asegúrate de que las unidades sean consistentes: Si C1 está en g/L, C2 también estará en g/L. Si V1 está en mL, V2 también debe estar en mL.
- Despeja C2 de la fórmula C1V1 = C2V2:
- Calcula el factor de dilución (FD): Recuerda que FD = V2 / V1.
- Relaciona C2 con C1 y el Factor de Dilución:
C2 = (C1 * V1) / V2
C2 = C1 / FD
Esta última relación es la que el fragmento de texto original se refiere al decir: "Para calcular la concentración de la muestra diluida, multiplicamos por el inverso del factor de dilución." El inverso del factor de dilución (FD) es 1/FD. Entonces, C2 = C1 * (1/FD).

Ejemplo Práctico 1: Dilución Estándar
Tienes una solución madre de glucosa con una concentración de 100 mg/mL (C1). Tomas 5 mL de esta solución (V1) y la diluyes con agua hasta un volumen final de 50 mL (V2). ¿Cuál es la concentración de la solución diluida (C2)?
- C1 = 100 mg/mL
- V1 = 5 mL
- V2 = 50 mL
Usando la fórmula C2 = (C1 * V1) / V2:
C2 = (100 mg/mL * 5 mL) / 50 mL
C2 = 500 mg / 50 mL
C2 = 10 mg/mL
Alternativamente, podemos calcular el factor de dilución:
FD = V2 / V1 = 50 mL / 5 mL = 10
Entonces, C2 = C1 / FD = 100 mg/mL / 10 = 10 mg/mL. Ambos métodos dan el mismo resultado.
Ejemplo Práctico 2: Interpretando la Dilución 1:4 del Prompt
Retomemos el escenario inicial: "hay una parte de volumen de muestra y cuatro partes de volumen del líquido utilizado para diluir la muestra, lo que da un total de cinco partes de volumen. Para calcular la concentración de la muestra diluida, multiplicamos por el inverso del factor de dilución."
Supongamos que la concentración original de la muestra (C1) es de 200 µg/mL.
- Volumen de la muestra (V1): Asumimos 1 unidad de volumen (por ejemplo, 1 mL)
- Volumen del diluyente: 4 unidades de volumen (por ejemplo, 4 mL)
- Volumen total final (V2): 1 mL + 4 mL = 5 mL
- Concentración inicial (C1): 200 µg/mL
Primero, calculamos el factor de dilución (FD):
FD = V2 / V1 = 5 mL / 1 mL = 5
Ahora, para calcular la concentración de la muestra diluida (C2), aplicamos la regla: "multiplicamos por el inverso del factor de dilución". El inverso del factor de dilución (5) es 1/5.
C2 = C1 * (1/FD)
C2 = 200 µg/mL * (1/5)
C2 = 40 µg/mL
Este ejemplo ilustra perfectamente cómo la frase en el prompt se aplica para encontrar la concentración de la muestra diluida cuando se conoce la concentración original y la relación de dilución. La concentración de la muestra diluida es un quinto de la original.
Importancia y Aplicaciones de la Dilución
La capacidad de diluir soluciones y calcular su concentración resultante es una habilidad indispensable en muchos campos. Su importancia radica en:
- Ajuste de Concentraciones: Permite preparar soluciones con la concentración exacta requerida para experimentos, tratamientos o procesos industriales, a partir de soluciones madre más concentradas, que son más fáciles de almacenar.
- Análisis Cuantitativo: Muchas técnicas analíticas tienen un rango de detección limitado. Las muestras muy concentradas deben diluirse para que su concentración caiga dentro del rango detectable del instrumento, permitiendo una medición precisa.
- Seguridad: Ciertas sustancias son peligrosas en altas concentraciones. La dilución las hace más seguras para la manipulación.
- Economía: Es más económico y práctico almacenar y transportar soluciones concentradas, diluyéndolas solo cuando sea necesario.
Áreas Clave de Aplicación
- Laboratorio Clínico: En análisis de sangre y orina, las muestras a menudo se diluyen para que los componentes como glucosa, proteínas o enzimas puedan medirse con precisión.
- Farmacia y Medicina: Preparación de medicamentos con la concentración adecuada para el paciente, así como dilución de vacunas o soluciones intravenosas.
- Química Analítica: Preparación de estándares de calibración para cromatografía, espectrofotometría y otras técnicas.
- Industria Alimentaria: Control de calidad de bebidas y alimentos, donde las concentraciones de azúcares, ácidos o aditivos deben ser exactas.
- Agricultura: Preparación de soluciones de fertilizantes o pesticidas a la concentración óptima para las plantas sin dañarlas.
- Biología Molecular: Dilución de ADN, proteínas o reactivos para reacciones enzimáticas o PCR.
Errores Comunes al Realizar Diluciones
A pesar de la aparente simplicidad, es fácil cometer errores durante el proceso de dilución que pueden llevar a resultados inexactos. Algunos de los más comunes incluyen:
- Medición Imprecisa de Volúmenes: Utilizar material volumétrico inadecuado (por ejemplo, vasos de precipitados en lugar de probetas o pipetas volumétricas) o no leer correctamente el menisco.
- Confusión entre Diluyente y Volumen Final: No diferenciar entre el volumen de diluyente añadido y el volumen total de la solución final. Siempre es el volumen final el que se usa en C1V1=C2V2.
- Mezcla Inadecuada: No asegurar una mezcla homogénea después de añadir el diluyente, lo que resulta en una concentración no uniforme.
- Unidades Inconsistentes: No convertir todas las unidades a un sistema común antes de realizar los cálculos (por ejemplo, mezclar mL con L).
- Error al Interpretar el Factor de Dilución: Confundir una relación de dilución (ej., 1:4) con el factor de dilución (ej., 5) o su inverso.
Preguntas Frecuentes (FAQ)
¿Cuál es la diferencia entre dilución y disolución?
La disolución es el proceso de formar una solución, donde un soluto se disuelve en un solvente. Por ejemplo, disolver azúcar en agua. La dilución, por otro lado, es el proceso de reducir la concentración de una solución ya existente añadiendo más solvente.
¿Qué es una dilución seriada?
Una dilución seriada es una serie de diluciones consecutivas, donde la solución de cada paso se diluye a una concentración inferior. Se utiliza para obtener una gama de concentraciones muy bajas a partir de una solución madre, o para determinar la concentración de una muestra desconocida mediante la titulación o el recuento de unidades formadoras de colonias (UFC) en microbiología.
¿Cómo se expresa el factor de dilución?
El factor de dilución (FD) se expresa generalmente como un número entero (por ejemplo, 5x, 10x, 100x), indicando cuántas veces se ha diluido la solución original. También se puede expresar como una fracción (por ejemplo, 1/5, 1/10, 1/100) que representa la proporción de la concentración final respecto a la inicial. Es importante ser claro con la notación para evitar confusiones.
¿Cuándo se utiliza la concentración en porcentaje (p/v, v/v, p/p)?
Las concentraciones en porcentaje son muy comunes en aplicaciones prácticas. Porcentaje peso/volumen (% p/v) se refiere a gramos de soluto por 100 mL de solución. Porcentaje volumen/volumen (% v/v) se refiere a mL de soluto por 100 mL de solución (común para líquidos). Porcentaje peso/peso (% p/p) se refiere a gramos de soluto por 100 gramos de solución. La fórmula C1V1=C2V2 funciona perfectamente con estas unidades, siempre y cuando C1 y C2 estén en el mismo tipo de porcentaje y V1 y V2 en las mismas unidades de volumen.
¿Se puede usar C1V1=C2V2 si las concentraciones están en molaridad?
¡Absolutamente! La fórmula C1V1=C2V2 es universal y funciona con cualquier unidad de concentración (molaridad, normalidad, g/L, ppm, porcentaje) siempre que las unidades de C1 y C2 sean las mismas, y las unidades de V1 y V2 también sean las mismas.
Conclusión
Calcular la concentración a partir de la dilución es una habilidad fundamental en el ámbito científico y práctico. Al comprender los conceptos de soluto, solvente, solución, factor de dilución y dominar la fórmula C1V1 = C2V2, podrás realizar diluciones con precisión y confianza. Recuerda siempre ser meticuloso con tus mediciones, mantener la consistencia en las unidades y verificar tus cálculos. Con la práctica y la atención a los detalles, la dilución se convertirá en una de tus herramientas más poderosas en el laboratorio o en cualquier aplicación que la requiera.
Si quieres conocer otros artículos parecidos a Dominando la Dilución: Calcular Concentración Fácil puedes visitar la categoría Química.