09/08/2023
La capacidad calorífica molar es un concepto fundamental en la termodinámica y la química física que nos permite entender cómo los diferentes materiales absorben o liberan energía térmica. Es una propiedad intensiva de la materia, lo que significa que no depende de la cantidad de sustancia, sino de su naturaleza intrínseca. Comprender este concepto es crucial para predecir el comportamiento térmico de sustancias en diversas aplicaciones, desde el diseño de motores hasta la formulación de reacciones químicas. En este artículo, exploraremos en profundidad qué es la capacidad calorífica molar, cómo se calcula, sus variantes como la capacidad calorífica a presión constante (Cp) y a volumen constante (Cv), y su relevancia en el mundo real.
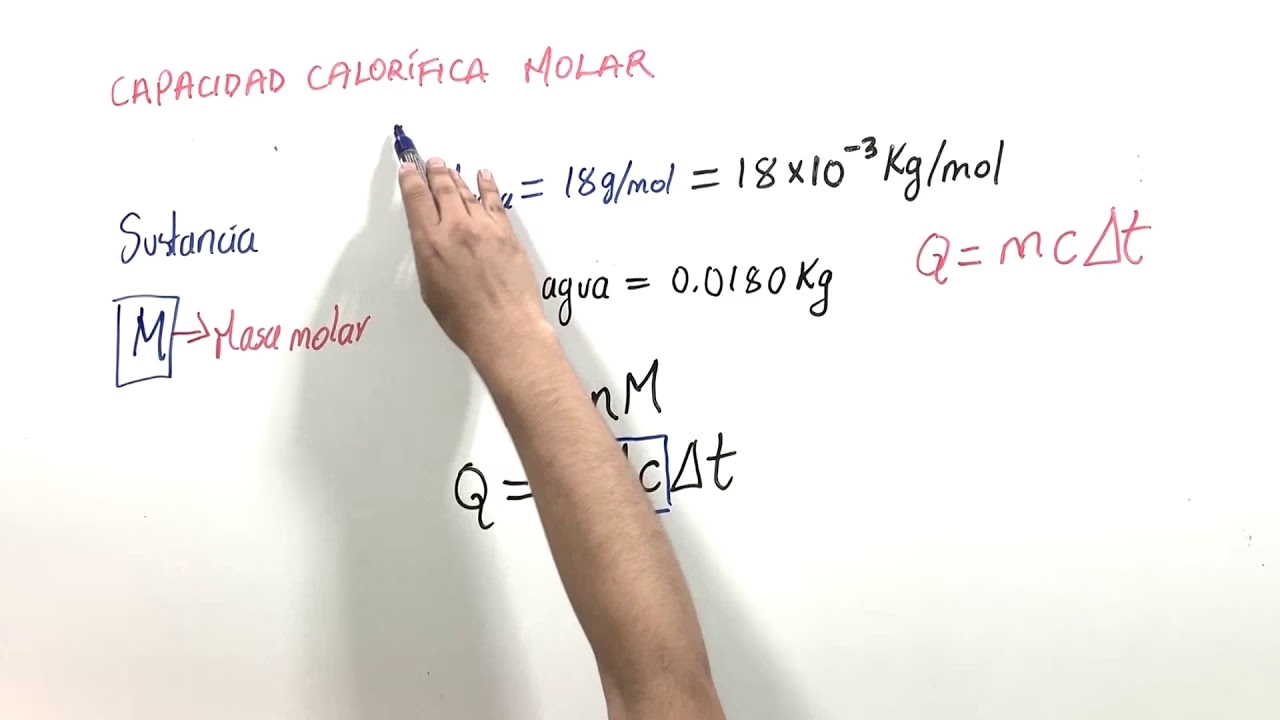
Antes de sumergirnos en la capacidad calorífica molar, es esencial comprender el concepto más amplio de capacidad calorífica. La capacidad calorífica (C) de una sustancia es la cantidad de energía térmica requerida para elevar su temperatura en un grado Celsius (o Kelvin). Se expresa comúnmente en Joules por grado Celsius (J/°C) o Joules por Kelvin (J/K). Esta propiedad es extensiva, lo que significa que depende de la cantidad de sustancia presente: cuanta más masa tenga un objeto, más energía requerirá para cambiar su temperatura. Por ejemplo, se necesita mucha más energía para calentar una piscina de agua que una taza pequeña de café.
Sin embargo, para comparar la capacidad de diferentes materiales para almacenar calor, los científicos y los ingenieros utilizan la capacidad calorífica específica (c), que es la cantidad de calor necesaria para elevar la temperatura de un gramo de una sustancia en un grado Celsius. Sus unidades son J/(g·°C) o J/(g·K). Esta es una propiedad intensiva, ya que es independiente de la cantidad de masa.
- La Capacidad Calorífica Molar: Una Perspectiva Molecular
- ¿Cómo se Calcula la Capacidad Calorífica Molar?
- Calor Molar de Solución (ΔH_sol)
- Capacidades Caloríficas Molares a Presión Constante (Cp) y Volumen Constante (Cv)
- Factores que Afectan la Capacidad Calorífica Molar
- Aplicaciones Prácticas de la Capacidad Calorífica Molar
- Tabla Comparativa de Capacidades Caloríficas Molares (Valores Típicos a 25°C y 1 atm)
- Preguntas Frecuentes (FAQs)
La Capacidad Calorífica Molar: Una Perspectiva Molecular
Mientras que la capacidad calorífica específica se refiere a la masa de una sustancia, la capacidad calorífica molar (C_m) eleva este concepto a un nivel molecular, refiriéndose a la cantidad de calor necesaria para elevar la temperatura de un mol de una sustancia en un grado Celsius (o Kelvin). Sus unidades son J/(mol·°C) o J/(mol·K). Esta es la medida más útil cuando se trabaja con reacciones químicas o procesos que involucran cantidades estequiométricas de sustancias, ya que los cálculos se basan en el número de moles.
La capacidad calorífica molar nos proporciona una comprensión más profunda de cómo la energía térmica se distribuye entre los diferentes modos de movimiento de las moléculas (translación, rotación, vibración). Diferentes sustancias tienen diferentes capacidades caloríficas molares debido a sus estructuras moleculares únicas y cómo estas estructuras interactúan con la energía térmica. Por ejemplo, los gases monoatómicos (como el helio) tienen una capacidad calorífica molar mucho menor que los gases poliatómicos (como el dióxido de carbono), porque los primeros solo pueden almacenar energía en movimientos de traslación, mientras que los segundos también pueden almacenar energía en rotaciones y vibraciones.
¿Cómo se Calcula la Capacidad Calorífica Molar?
La capacidad calorífica molar se puede calcular de varias maneras, dependiendo de la información disponible y el contexto del problema.
1. A partir de la Capacidad Calorífica Específica:
Si conoces la capacidad calorífica específica (c) de una sustancia y su masa molar (M), puedes calcular la capacidad calorífica molar (C_m) usando la siguiente relación:
C_m = c * M
Donde:
C_mes la capacidad calorífica molar (J/(mol·K)).ces la capacidad calorífica específica (J/(g·K)).Mes la masa molar de la sustancia (g/mol).
Ejemplo: La capacidad calorífica específica del agua líquida es aproximadamente 4.18 J/(g·K). La masa molar del agua (H₂O) es aproximadamente 18.015 g/mol.
C_m (agua) = 4.18 J/(g·K) * 18.015 g/mol ≈ 75.3 J/(mol·K)
2. A partir de la Transferencia de Calor y el Cambio de Temperatura:
Si conoces la cantidad de calor (q) absorbida o liberada por una sustancia, el número de moles (n) de esa sustancia y el cambio de temperatura (ΔT), puedes calcular la capacidad calorífica molar utilizando la siguiente fórmula:
q = n * C_m * ΔT
De donde se puede despejar C_m:
C_m = q / (n * ΔT)
Donde:
qes la cantidad de calor absorbida o liberada (en Joules o calorías).nes el número de moles de la sustancia.C_mes la capacidad calorífica molar (J/(mol·K) o cal/(mol·K)).ΔTes el cambio en la temperatura (T_final - T_inicial) en grados Celsius o Kelvin.
Ejemplo: Si 2 moles de una sustancia absorben 1500 J de calor y su temperatura aumenta en 10 K, la capacidad calorífica molar sería:
C_m = 1500 J / (2 mol * 10 K) = 1500 J / 20 mol·K = 75 J/(mol·K)
Calor Molar de Solución (ΔH_sol)
El concepto de capacidad calorífica molar también se extiende al estudio de las soluciones, donde se habla del calor molar de solución (ΔH_sol). Este valor representa la energía térmica absorbida o liberada cuando un mol de soluto se disuelve en una cantidad específica de solvente. Es un tipo particular de entalpía de disolución y es crucial en procesos como la preparación de disoluciones en laboratorio o la comprensión de fenómenos naturales.
El cálculo del calor molar de solución implica dos pasos principales:
1. Cálculo del calor transferido (q) en la disolución:
Esto se calcula generalmente a partir del cambio de temperatura del solvente (o de la solución total, si se asume que su capacidad calorífica es similar a la del solvente puro). La fórmula utilizada es:
q = m_solvente * C_solvente * ΔT
Donde:
qes el calor absorbido o liberado por el solvente (en Joules o calorías).m_solventees la masa del solvente (en gramos).C_solventees la capacidad calorífica específica del solvente (en Joules por gramo por grado Celsius o calorías por gramo por grado Celsius).ΔTes el cambio de temperatura de la solución (T_final - T_inicial) en grados Celsius.
Es importante notar que si la temperatura de la solución aumenta, q será positivo (exotérmico para el solvente, el sistema libera calor); si disminuye, q será negativo (endotérmico para el solvente, el sistema absorbe calor). El signo de q se invierte cuando se considera desde la perspectiva del proceso de disolución.

2. Cálculo del calor molar de solución (ΔH_sol):
Una vez que se ha determinado q, se divide por el número de moles del soluto disuelto (n_soluto):
ΔH_sol = q / n_soluto
El resultado se expresará en Joules por mol (J/mol) o calorías por mol (cal/mol). El signo de ΔH_sol indicará si el proceso de disolución es endotérmico (ΔH_sol > 0, absorbe calor del entorno) o exotérmico (ΔH_sol < 0, libera calor al entorno).
Capacidades Caloríficas Molares a Presión Constante (Cp) y Volumen Constante (Cv)
En termodinámica, la capacidad calorífica molar de un gas puede medirse bajo dos condiciones diferentes, lo que da lugar a dos valores distintos: la capacidad calorífica molar a volumen constante (Cv) y la capacidad calorífica molar a presión constante (Cp). La distinción es crucial porque el trabajo realizado por o sobre el sistema difiere en cada caso.
Termodinámica y Variables de Estado
La termodinámica es la rama de la física que estudia la relación entre el calor, el trabajo, la temperatura y la energía. Se enfoca en la respuesta a gran escala de un sistema que puede ser observado y medido experimentalmente. En el estudio de gases, es común utilizar variables de estado "específicas", que son el valor de la variable dividido por la masa de la sustancia. Esto permite establecer relaciones entre variables sin importar la cantidad total de sustancia. Para convertir estas a valores molares, simplemente se multiplican por la masa molar del gas.
Energía Interna y Entalpía
Para entender Cp y Cv, debemos considerar la energía interna (E o U) y la entalpía (H) de un sistema.
- La energía interna (E) representa toda la energía contenida dentro de un sistema, incluyendo la energía cinética de las moléculas y la energía potencial de sus interacciones. Para un proceso, el cambio en la energía interna (ΔE) se relaciona con el calor (q) y el trabajo (w) por la Primera Ley de la Termodinámica:
ΔE = q - w. - La entalpía (H) es una función de estado definida como
H = E + PV, donde P es la presión y V es el volumen. Es particularmente útil para procesos a presión constante. El cambio en la entalpía (ΔH) se relaciona con el calor absorbido o liberado a presión constante.
Capacidad Calorífica Molar a Volumen Constante (Cv)
Cuando el volumen de un sistema se mantiene constante (ΔV = 0), no se realiza trabajo de expansión o compresión (w = PΔV = 0). En este caso, la Primera Ley de la Termodinámica se simplifica a ΔE = q_v. Esto significa que todo el calor añadido al sistema se destina a aumentar su energía interna.
Por definición, la capacidad calorífica molar a volumen constante (Cv) es la cantidad de calor necesaria para elevar la temperatura de un mol de sustancia en un grado Celsius a volumen constante:
q_v = n * Cv * ΔT
Por lo tanto:
ΔE = n * Cv * ΔT
O, en términos de energía interna molar (e):
Δe = Cv * ΔT
Capacidad Calorífica Molar a Presión Constante (Cp)
Cuando la presión de un sistema se mantiene constante, el sistema puede expandirse o contraerse, realizando o recibiendo trabajo. En este caso, el calor añadido (q_p) no solo aumenta la energía interna, sino que también realiza trabajo.
La entalpía es especialmente útil aquí. Para un proceso a presión constante, el cambio en la entalpía es igual al calor transferido: ΔH = q_p.
Por definición, la capacidad calorífica molar a presión constante (Cp) es la cantidad de calor necesaria para elevar la temperatura de un mol de sustancia en un grado Celsius a presión constante:
q_p = n * Cp * ΔT
Por lo tanto:
ΔH = n * Cp * ΔT
O, en términos de entalpía molar (h):
Δh = Cp * ΔT
La Relación de Mayer: Cp = Cv + R
Una relación fundamental entre Cp y Cv para un gas ideal es la Relación de Mayer:
Cp = Cv + R
Donde R es la constante de los gases ideales (8.314 J/(mol·K)).
Esta relación se deriva de la definición de entalpía (H = E + PV) y la ecuación de estado de los gases ideales (PV = nRT). Para un mol de gas ideal, PV = RT.

Si diferenciamos la entalpía molar (h = e + Pv) con respecto a la temperatura a presión constante:
dh/dT = de/dT + d(Pv)/dT
Sabemos que dh/dT = Cp y de/dT = Cv. También, para un gas ideal, Pv = RT, así que d(Pv)/dT = d(RT)/dT = R.
Sustituyendo esto en la ecuación:
Cp = Cv + R
Esta ecuación demuestra que Cp siempre es mayor que Cv. La diferencia se debe al trabajo de expansión que el gas realiza contra la presión externa cuando se calienta a presión constante. A volumen constante, no se realiza este trabajo, por lo que todo el calor se convierte en energía interna.
El Coeficiente Adiabático (Gamma, γ)
Otra relación importante es el Coeficiente Adiabático, γ (gamma), que es la relación entre Cp y Cv:
γ = Cp / Cv
Este valor es crucial en procesos adiabáticos (donde no hay transferencia de calor) y en la velocidad del sonido en un gas. Para gases monoatómicos (como He, Ne, Ar), γ es aproximadamente 1.67. Para gases diatómicos (como O₂, N₂, aire), γ es aproximadamente 1.40. Para gases poliatómicos, γ es generalmente menor que 1.40.
Factores que Afectan la Capacidad Calorífica Molar
La capacidad calorífica molar de una sustancia no es un valor constante y puede variar significativamente debido a varios factores:
- Temperatura: La capacidad calorífica molar generalmente aumenta con la temperatura, especialmente a bajas temperaturas, a medida que se activan más modos de movimiento molecular (rotación, vibración). A muy altas temperaturas, tiende a estabilizarse.
- Fase de la Sustancia: La capacidad calorífica molar es diferente para la misma sustancia en sus diferentes fases (sólido, líquido, gas). Por ejemplo, el agua líquida tiene una capacidad calorífica molar mucho mayor que el hielo o el vapor. Esto se debe a las diferencias en la libertad de movimiento y las interacciones moleculares.
- Estructura Molecular: La complejidad de la molécula influye directamente. Las moléculas más complejas con más átomos tienen más modos de vibración y rotación, lo que les permite almacenar más energía térmica para un dado aumento de temperatura, resultando en una capacidad calorífica molar más alta.
- Presión y Volumen (para gases): Como se discutió con Cp y Cv, las condiciones bajo las cuales se mide la capacidad calorífica son cruciales para los gases.
Aplicaciones Prácticas de la Capacidad Calorífica Molar
El conocimiento de la capacidad calorífica molar es invaluable en una amplia gama de campos:
- Ingeniería Química: Para el diseño de reactores, intercambiadores de calor y procesos de separación. Permite calcular los requerimientos de energía para calentar o enfriar corrientes de fluidos.
- Diseño de Motores y Turbinas: En la aerodinámica y el diseño de motores a reacción, las capacidades caloríficas de los gases de combustión son esenciales para predecir el rendimiento y la eficiencia.
- Meteorología y Climatología: La capacidad calorífica del aire y del agua influye en los patrones climáticos globales y la formación de fenómenos meteorológicos.
- Ciencia de Materiales: Para entender el comportamiento térmico de los materiales en diferentes aplicaciones, como aislantes o conductores de calor.
- Química Analítica y Bioquímica: En calorimetría, para determinar el calor de reacciones químicas o transiciones de fase.
Tabla Comparativa de Capacidades Caloríficas Molares (Valores Típicos a 25°C y 1 atm)
| Sustancia | Fase | C_m (J/(mol·K)) | Notas |
|---|---|---|---|
| Agua (H₂O) | Líquida | 75.3 | Valor alto debido a puentes de hidrógeno. |
| Hierro (Fe) | Sólido | 25.1 | Típico para metales según la Ley de Dulong-Petit. |
| Cobre (Cu) | Sólido | 24.5 | |
| Aluminio (Al) | Sólido | 24.2 | |
| Helio (He) | Gas (ideal) | 20.8 (Cv), 29.1 (Cp) | Monoatómico |
| Nitrógeno (N₂) | Gas (ideal) | 20.8 (Cv), 29.1 (Cp) | Diatómico (valores de Cv y Cp a bajas temperaturas) |
| Oxígeno (O₂) | Gas (ideal) | 20.8 (Cv), 29.1 (Cp) | Diatómico (valores de Cv y Cp a bajas temperaturas) |
| Dióxido de Carbono (CO₂) | Gas (ideal) | 28.5 (Cv), 37.0 (Cp) | Poliatómico, mayor debido a vibraciones. |
| Aire (aproximado) | Gas | 20.8 (Cv), 29.1 (Cp) | Mezcla de gases diatómicos principalmente. |
Preguntas Frecuentes (FAQs)
¿Cuál es la diferencia entre capacidad calorífica, capacidad calorífica específica y capacidad calorífica molar?
La capacidad calorífica (C) es la cantidad total de calor necesaria para cambiar la temperatura de una muestra completa de una sustancia en un grado. Es una propiedad extensiva y depende de la cantidad de material. La capacidad calorífica específica (c) es la cantidad de calor necesaria para cambiar la temperatura de un gramo de una sustancia en un grado. Es una propiedad intensiva (independiente de la cantidad de masa). Finalmente, la capacidad calorífica molar (C_m) es la cantidad de calor necesaria para cambiar la temperatura de un mol de una sustancia en un grado. También es una propiedad intensiva y es particularmente útil en química.
¿Por qué Cp es siempre mayor que Cv para un gas ideal?
Cuando un gas se calienta a volumen constante (Cv), todo el calor añadido se utiliza para aumentar la energía interna del gas, lo que se manifiesta como un aumento de temperatura. Sin embargo, cuando se calienta el mismo gas a presión constante (Cp), el gas no solo absorbe calor para aumentar su energía interna, sino que también realiza trabajo de expansión contra el entorno al expandirse. Este trabajo adicional requiere energía, por lo que se necesita más calor para lograr el mismo aumento de temperatura a presión constante que a volumen constante. La diferencia entre Cp y Cv es precisamente la energía necesaria para realizar este trabajo de expansión.
¿Puede la capacidad calorífica molar ser negativa?
No, la capacidad calorífica molar, por definición, es una cantidad positiva. Representa la energía necesaria para aumentar la temperatura de una sustancia. Un valor negativo implicaría que la sustancia libera calor cuando su temperatura aumenta, lo cual es físicamente imposible. Sin embargo, el cambio de entalpía (ΔH) de un proceso (como el calor molar de solución) sí puede ser negativo, indicando un proceso exotérmico (liberación de calor).
¿Cuáles son las unidades comunes para la capacidad calorífica molar?
Las unidades más comunes para la capacidad calorífica molar son Joules por mol por Kelvin (J/(mol·K)) o Joules por mol por grado Celsius (J/(mol·°C)). Dado que un cambio de un grado Kelvin es igual a un cambio de un grado Celsius, estas unidades son intercambiables en este contexto. También se pueden encontrar en calorías por mol por Kelvin (cal/(mol·K)).
¿Afecta la fase de la sustancia a su capacidad calorífica molar?
Sí, la fase de la sustancia tiene un impacto significativo en su capacidad calorífica molar. Por ejemplo, la capacidad calorífica molar del agua líquida es de aproximadamente 75.3 J/(mol·K), mientras que la del hielo (agua sólida) es de alrededor de 37.6 J/(mol·K) y la del vapor de agua es de unos 33.6 J/(mol·K) (a presión constante y 100°C). Estas diferencias se deben a las distintas formas en que las moléculas pueden almacenar energía en las diferentes fases (movimiento, vibraciones, etc.) y a las fuerzas intermoleculares presentes.
Si quieres conocer otros artículos parecidos a Capacidad Calorífica Molar: Conceptos y Cálculo puedes visitar la categoría Cálculos.
