17/07/2024
En el vasto y complejo universo de la química, los ácidos y las bases juegan un papel fundamental, influyendo en innumerables procesos biológicos e industriales. Comprender su comportamiento y su fuerza es crucial para científicos, estudiantes y cualquier persona interesada en la composición de las sustancias. Dentro de este campo, la constante de disociación ácida, conocida como Ka, emerge como una herramienta indispensable, especialmente cuando se trata de ácidos débiles.
A diferencia de los ácidos fuertes que se disocian completamente en solución, los ácidos débiles solo lo hacen de manera parcial, estableciendo un equilibrio dinámico entre su forma molecular y sus iones disociados. La constante Ka es precisamente la medida cuantitativa de este equilibrio, indicándonos cuán extenso es el grado de disociación de un ácido y, por ende, su verdadera fuerza. Este artículo exhaustivo te guiará paso a paso a través de los conceptos esenciales y los métodos prácticos para calcular Ka, desde la comodidad de tus datos hasta las aplicaciones en el laboratorio. Exploraremos diversas aproximaciones, desde el uso de concentraciones molares y el pH de una solución, hasta la interpretación de curvas de titulación y la relación con la constante de basicidad (Kb) de su par conjugado. Prepárate para desentrañar los secretos detrás de la fuerza ácida y dominar este concepto químico esencial.
¿Qué es la Constante de Disociación Ácida (Ka)?
La constante de disociación ácida (Ka) es una constante de equilibrio que mide la extensión en la que un ácido se disocia en una solución acuosa. Es particularmente relevante para los ácidos débiles, que, a diferencia de los ácidos fuertes, no se disocian completamente en iones cuando se disuelven en agua. En su lugar, establecen un equilibrio químico dinámico. Para un ácido débil genérico, HA, la reacción de disociación puede representarse de la siguiente manera:
HA(aq) ⇌ H⁺(aq) + A⁻(aq)
En esta expresión, HA representa la forma molecular del ácido, H⁺ son los iones de hidrógeno (o protones) liberados, y A⁻ es la base conjugada del ácido. La doble flecha indica que la reacción es reversible y que coexisten en equilibrio tanto el ácido no disociado como sus iones. La expresión de la constante de disociación ácida (Ka) para esta reacción se define como el producto de las concentraciones de los iones disociados dividido por la concentración del ácido no disociado, todas ellas en el equilibrio:
Ka = [H⁺][A⁻] / [HA]
Donde los corchetes [ ] denotan las concentraciones molares en equilibrio, generalmente en mol dm⁻³ (moles por decímetro cúbico). El valor de Ka es una medida directa de la fuerza del ácido: cuanto menor sea el valor de Ka, menos se disocia el ácido en solución, lo que indica que es un ácido más débil. Por el contrario, un valor de Ka más alto significa que el ácido se disocia en mayor medida, lo que lo convierte en un ácido más fuerte. Es importante destacar que el valor de Ka es constante para un ácido particular a una temperatura específica, lo que lo convierte en una propiedad intrínseca útil para caracterizar y comparar diferentes ácidos.
Métodos para Calcular la Constante de Disociación Ácida (Ka)
La determinación del valor de Ka es fundamental para comprender y predecir el comportamiento de los ácidos en diversas aplicaciones químicas. Afortunadamente, existen varios enfoques para calcular esta constante, cada uno adaptado a diferentes tipos de información disponible o situaciones experimentales. A continuación, exploraremos los métodos más comunes y efectivos para calcular Ka.
1. Cálculo de Ka a partir de la Molaridad y Concentraciones en Equilibrio
La forma más directa de calcular Ka se basa en su definición, si conocemos las concentraciones de todas las especies involucradas en el equilibrio de disociación. Para cualquier reacción de equilibrio, la constante de equilibrio se define como el cociente de las concentraciones de los productos sobre los reactivos, elevadas a sus respectivos coeficientes estequiométricos. Para la disociación de un ácido débil HA:
HA ⇌ H⁺ + A⁻
La ecuación para Ka es simplemente:
Ka = [H⁺][A⁻] / [HA]
Si las concentraciones de equilibrio de los iones H⁺, la base conjugada A⁻ y el ácido no disociado HA son conocidas, simplemente se sustituyen estos valores en la expresión para obtener el valor de Ka. A menudo, estas concentraciones se determinan experimentalmente o se calculan utilizando tablas ICE (Inicial, Cambio, Equilibrio), que ayudan a rastrear cómo las concentraciones cambian desde el estado inicial hasta el equilibrio.
2. Cálculo de Ka a partir del pH de la Solución
Uno de los métodos más comunes y accesibles para calcular Ka es a partir del pH de una solución de ácido débil. El pH es una medida de la concentración de iones hidrógeno en una solución y está directamente relacionado con la fuerza del ácido. La relación fundamental es:
pH = -log₁₀[H⁺]
De esta ecuación, podemos derivar la concentración de iones hidrógeno:
[H⁺] = 10⁻ᵖᴴ
Para calcular Ka a partir del pH, se siguen los siguientes pasos:
- Escribir la expresión para Ka: Para el ácido débil HA, Ka = [H⁺][A⁻]/[HA].
- Encontrar [H⁺] utilizando el pH dado: Utiliza la fórmula [H⁺] = 10⁻ᵖᴴ.
- Determinar [A⁻]: Para un ácido monoprótico (que libera un solo protón por molécula), la concentración de la base conjugada [A⁻] en el equilibrio es igual a la concentración de iones H⁺ [H⁺], ya que se forman en una relación 1:1 durante la disociación.
- Determinar [HA]: Dado que los ácidos débiles se disocian solo parcialmente, una suposición común y válida para cálculos es que la concentración de HA en el equilibrio es aproximadamente igual a la concentración inicial del ácido (antes de la disociación). Esto se debe a que la cantidad de ácido que se disocia es muy pequeña en comparación con la cantidad inicial. Además, se asume que la contribución de los iones H⁺ provenientes de la autoionización del agua es despreciable en comparación con los iones H⁺ liberados por el ácido débil.
- Sustituir los valores y resolver: Una vez que tienes [H⁺], [A⁻] y [HA], sustituye estos valores en la expresión de Ka y calcula el resultado final.
Ejemplo Resuelto: Cálculo del Ka para el Ácido Fluorhídrico (HF)
Calcula el valor de Ka para el ácido fluorhídrico (HF) si 0.02 mol dm⁻³ de HF se disuelven en 1.00 dm³ de agua pura, y la solución resultante tiene un pH de 2.42.
Solución:
1. Primero, escribimos la expresión de Ka para la disociación del HF:
HF(aq) ⇌ H⁺(aq) + F⁻(aq)
Ka = [H⁺][F⁻] / [HF]
2. Ahora, utilizamos el pH dado para encontrar la concentración de iones H⁺:
[H⁺] = 10⁻ᵖᴴ = 10⁻²·⁴² ≈ 3.80 × 10⁻³ mol dm⁻³
3. Dado que HF es un ácido monoprótico, la concentración de iones F⁻ en el equilibrio es igual a la concentración de iones H⁺:
[F⁻] = [H⁺] = 3.80 × 10⁻³ mol dm⁻³
4. Para la concentración de HF en el equilibrio, asumimos que es aproximadamente igual a la concentración inicial, ya que es un ácido débil y se disocia muy poco:
[HF] ≈ Concentración inicial = 0.020 mol dm⁻³
5. Finalmente, sustituimos estos valores en la expresión de Ka y resolvemos:
Ka = (3.80 × 10⁻³)(3.80 × 10⁻³) / 0.020
Ka = 1.444 × 10⁻⁵ / 0.020
Ka ≈ 7.22 × 10⁻⁴ mol dm⁻³
Por lo tanto, el valor de Ka para el ácido fluorhídrico es aproximadamente 7.22 × 10⁻⁴ mol dm⁻³.
3. Cálculo de Ka a partir del pKa
Así como el pH es una escala logarítmica para la concentración de iones H⁺, el pKa es una escala logarítmica para el valor de Ka. Esta relación simplifica la comparación de la fuerza de los ácidos, especialmente cuando sus valores de Ka son muy pequeños o muy grandes. La definición de pKa es:
pKa = -log₁₀Ka
De esta relación, podemos reorganizar la ecuación para calcular Ka si conocemos el valor de pKa:
Ka = 10⁻ᵖᴷᵃ
Esta conversión es directa y muy útil cuando ya se dispone del valor de pKa, que a menudo se encuentra tabulado o se determina experimentalmente por otros medios. Al igual que con el pH, un valor de pKa más pequeño indica un ácido más fuerte (ya que un pKa pequeño corresponde a un Ka grande), mientras que un pKa más grande indica un ácido más débil.
4. Cálculo de Ka a partir de Curvas de Titulación: El Punto de Semi-Neutralización
Las curvas de titulación proporcionan una forma experimental y gráfica de determinar el Ka de un ácido débil. Una curva de titulación es un gráfico que muestra cómo cambia el pH de una solución a medida que se le añade un volumen incremental de una solución de concentración conocida (el titulante). Para un ácido débil titulado con una base fuerte, la curva de titulación tiene una forma característica que permite identificar puntos clave.
Un punto particularmente importante en una curva de titulación ácido débil-base fuerte es el punto de semi-neutralización (o punto de semi-equivalencia). Este es el punto en el que exactamente la mitad del ácido débil inicial ha reaccionado con la base añadida. En este punto, la concentración del ácido débil no disociado ([HA]) es igual a la concentración de su base conjugada ([A⁻]) que se ha formado.
Si observamos la expresión de Ka:
Ka = [H⁺][A⁻] / [HA]
En el punto de semi-neutralización, como [A⁻] = [HA], estos términos se cancelan mutuamente en la ecuación, simplificándola a:
Ka = [H⁺]
Si tomamos el logaritmo negativo de ambos lados de esta ecuación, obtenemos:
-log₁₀Ka = -log₁₀[H⁺]
Lo que se traduce en la relación crucial:
pKa = pH
Esto significa que, en el punto de semi-neutralización de una titulación, el pH de la solución es numéricamente igual al pKa del ácido débil. Para encontrar este punto en una curva de titulación:
- Identificar el punto de equivalencia: Este es el punto medio de la sección vertical más pronunciada de la curva, donde el ácido ha sido completamente neutralizado.
- Determinar el volumen de equivalencia: Es el volumen de titulante necesario para alcanzar el punto de equivalencia.
- Calcular el volumen de semi-neutralización: Es la mitad del volumen de equivalencia.
- Leer el pH en la curva: El pH correspondiente al volumen de semi-neutralización en el eje X es el valor del pKa del ácido. Una vez que se tiene el pKa, se puede calcular Ka usando la relación Ka = 10⁻ᵖᴷᵃ.
Ejemplo Resuelto: Cálculo del Ka para el Ácido Benzoico a partir de una Curva de Titulación
Se necesitan 25 cm³ de NaOH para neutralizar completamente 25 cm³ de ácido benzoico (C₇H₆O₂), dando como resultado una curva de titulación. Utilizando el punto de semi-neutralización de la curva, encuentra el valor de Ka para este ácido (asume que el pH en el punto de semi-neutralización es 4.19).

Solución:
1. Sabemos que en el punto de semi-neutralización, pKa = pH.
2. El volumen del punto de equivalencia de NaOH es 25 cm³.
3. Por lo tanto, el volumen del punto de semi-neutralización es la mitad de esto: 12.5 cm³.
4. Según la información proporcionada (o la lectura de una curva de titulación hipotética), cuando se añaden 12.5 cm³ de NaOH, el pH de la solución es aproximadamente 4.19.
5. Por lo tanto, el pKa del ácido benzoico es:
pKa = 4.19
6. Ahora, podemos utilizar este valor para encontrar Ka:
Ka = 10⁻ᵖᴷᵃ = 10⁻⁴·¹⁹
Ka ≈ 6.46 × 10⁻⁵ mol dm⁻³
Así, el valor de Ka para el ácido benzoico es aproximadamente 6.46 × 10⁻⁵ mol dm⁻³.
5. Cálculo de Ka a partir de Kb (Constante de Basicidad)
Para nuestra última forma de calcular Ka, exploraremos cómo podemos encontrar Ka a partir de Kb (constante de basicidad). Este método implica el concepto de base conjugada y la relación fundamental entre un par ácido-base conjugado y la autoionización del agua.
Un ácido conjugado es una base que ha aceptado un protón de un ácido y ahora puede actuar como un ácido cediendo ese protón. Por otro lado, una base conjugada es un ácido que ha donado un protón a una base y ahora puede actuar como una base aceptando un protón. Cuando un ácido débil (HA) se disocia en solución, forma un protón (H⁺) y su base conjugada (A⁻). La A⁻ puede reaccionar con el agua para formar HA y un ion hidróxido (OH⁻), actuando como una base.
Al igual que Ka mide el grado de disociación de un ácido débil, la constante de equilibrio Kb mide el grado de disociación de una base débil. Existe una relación especial entre el valor de Ka para un ácido débil y el valor de Kb para su base conjugada, mediada por la constante de ionización del agua (Kw):
Ka × Kb = Kw
La constante de ionización del agua, Kw, es un valor constante a una temperatura determinada. A 25 °C (298 K), Kw es igual a 1.00 × 10⁻¹⁴ mol² dm⁻⁶. Esta relación implica que Ka y Kb son inversamente proporcionales: cuanto mayor sea el valor de Ka (ácido más fuerte), menor será el valor de Kb de su base conjugada (base conjugada más débil), y viceversa.
Para entender de dónde viene esta fórmula, consideremos la disociación de nuestro ácido débil general (HA) en agua:
HA(aq) + H₂O(l) ⇌ H₃O⁺(aq) + A⁻(aq)
La expresión de Ka para este equilibrio es:
Ka = [H₃O⁺][A⁻] / [HA]
Ahora, consideremos la reacción de la base conjugada (A⁻) con agua:
A⁻(aq) + H₂O(l) ⇌ HA(aq) + OH⁻(aq)
La expresión de Kb para este equilibrio es:
Kb = [HA][OH⁻] / [A⁻]
Si multiplicamos las expresiones de Ka y Kb, observaremos una cancelación de términos:
Ka × Kb = ([H₃O⁺][A⁻] / [HA]) × ([HA][OH⁻] / [A⁻])
Los términos [HA] y [A⁻] se cancelan del numerador y del denominador, dejándonos con:
Ka × Kb = [H₃O⁺][OH⁻]
Y sabemos que el producto de las concentraciones de iones hidronio e hidróxido es igual a Kw:
Kw = [H₃O⁺][OH⁻]
Por lo tanto:
Ka × Kb = Kw
Para calcular Ka a partir de Kb, simplemente reorganizamos la ecuación:
Ka = Kw / Kb
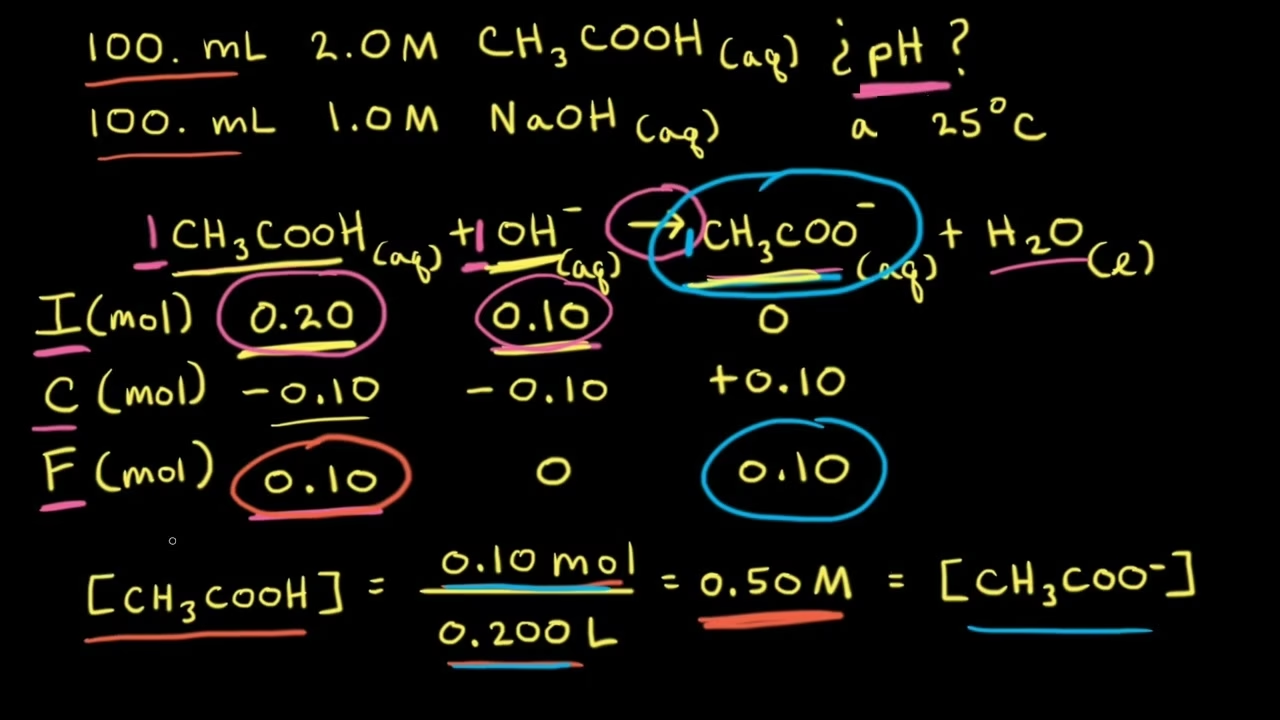
Ejemplo Resuelto: Cálculo del Ka para el Ácido Acético (CH₃COOH)
La base conjugada del ácido débil CH₃COOH es CH₃COO⁻. A 25 °C, el CH₃COO⁻ tiene un valor de Kb de 5.70 × 10⁻¹⁰ mol dm⁻³. Encuentra el valor de Ka para el CH₃COOH a la misma temperatura.
Solución:
Sabemos que para un par ácido-base conjugado, Ka × Kb = Kw. A 25 °C, el valor de Kw es 1.00 × 10⁻¹⁴ mol² dm⁻⁶.

Podemos reorganizar la fórmula para despejar Ka:
Ka = Kw / Kb
Sustituimos los valores conocidos:
Ka = (1.00 × 10⁻¹⁴) / (5.70 × 10⁻¹⁰)
Ka ≈ 1.75 × 10⁻⁵ mol dm⁻³
Este es el valor de Ka para el ácido acético a 25 °C.
¿Cómo se Mide la Acidez de una Solución en la Práctica?
Además de comprender cómo calcular Ka, es igualmente importante saber cómo se mide la acidez de una solución en un entorno práctico. Estos métodos nos permiten obtener los datos necesarios (como el pH) para luego aplicar los cálculos de Ka. Existen varios dispositivos y sustancias que permiten determinar la acidez:
1. pHmetro
Un pHmetro es un instrumento electrónico de alta precisión que se utiliza para medir la acidez o alcalinidad (pH) de una solución. Es uno de los dispositivos más confiables y exactos disponibles en el laboratorio. Su funcionamiento se basa en la medición de la diferencia de potencial eléctrico entre un electrodo de vidrio (sensible a los iones H⁺) y un electrodo de referencia. Esta diferencia de potencial se relaciona directamente con la concentración de iones H⁺ en la solución, siguiendo la ecuación de Nernst. La lectura del pH se muestra digitalmente.
Para asegurar la exactitud de las mediciones, es crucial calibrar el pHmetro antes de cada uso con, al menos, dos soluciones tampón (buffers) de pH conocido. Esta calibración compensa cualquier desviación del electrodo y asegura que las lecturas sean precisas y fiables.
2. Indicador Ácido-Base
Si no se dispone de un pHmetro o se necesita una estimación rápida del pH, se puede utilizar un indicador ácido-base. Un indicador ácido-base es una sustancia (generalmente un ácido o una base orgánica débil) que cambia de color en un rango específico de pH. Estos indicadores tienen diferentes estructuras químicas a diferentes valores de pH, lo que se traduce en un cambio de color visible.
Al añadir unas pocas gotas de un indicador ácido-base a una solución de pH desconocido, el color resultante de la solución puede compararse con una tabla de referencia del indicador para estimar el pH. Por ejemplo, el papel tornasol es un tipo de indicador, pero existen muchos otros como la fenolftaleína, el azul de bromotimol o el rojo de metilo, cada uno con un rango de cambio de color particular. Aunque son útiles para una estimación rápida, una desventaja es que, al ser sustancias ácidas o básicas, pueden alterar ligeramente el pH de la solución original, especialmente si esta es muy diluida.
3. Papel Tornasol
El papel tornasol es una de las herramientas más sencillas y rápidas para obtener una estimación aproximada del pH de una solución. Consiste en una tira de papel impregnada con una mezcla de indicadores ácido-base. Cuando se pone en contacto con una solución, el papel tornasol cambia a un color específico (generalmente rojo para ácidos y azul para bases, aunque existen versiones más avanzadas que muestran un espectro de colores para diferentes rangos de pH).
Para usarlo, basta con sumergir una pequeña porción del papel en la solución o aplicar una gota de la solución sobre el papel. El color resultante se compara con una tabla de colores proporcionada por el fabricante para determinar el pH aproximado. El papel tornasol es ideal para pruebas rápidas y cualitativas, ya que no altera la composición de la solución y es muy fácil de usar, aunque su precisión es mucho menor que la de un pHmetro.
Tabla Comparativa de Métodos para Calcular Ka
Para facilitar la elección del método más adecuado, presentamos una tabla comparativa que resume las características principales de cada enfoque para calcular Ka, destacando la información requerida, sus ventajas y sus posibles desventajas:
| Método | Información Requerida | Ventajas | Desventajas |
|---|---|---|---|
| Molaridad/Concentraciones | Concentraciones de equilibrio de HA, H⁺, A⁻ | Conceptualmente directo, basado en la definición de equilibrio. | Requiere conocer todas las concentraciones en equilibrio, lo cual puede ser difícil de determinar directamente. |
| pH | pH inicial de la solución y concentración inicial de HA | Método común y accesible con un pHmetro; relativamente sencillo. | Requiere suposiciones sobre la disociación del ácido débil y la contribución del agua. |
| pKa | Valor de pKa | Conversión directa y simple si el pKa es conocido. | El pKa debe ser conocido o determinado previamente por otros métodos. |
| Curva de Titulación | Datos de titulación (pH vs. volumen de titulante) | Determina Ka experimentalmente; útil para ácidos de concentración desconocida. | Requiere equipos de laboratorio y una titulación cuidadosa; interpretación de la curva. |
| Kb | Valor de Kb de la base conjugada y Kw (constante del agua) | Relación fundamental que permite el cálculo cruzado entre ácidos y bases conjugados. | Requiere conocer el Kb de la base conjugada, que también debe ser determinado. |
Preguntas Frecuentes (FAQs)
¿Qué es Ka?
Ka, o constante de disociación ácida, es una medida estándar utilizada para cuantificar la fuerza de un ácido en una solución acuosa. Determina el grado en que un ácido se disocia para liberar iones de hidrógeno (H⁺). Se utiliza comúnmente para distinguir entre ácidos fuertes y ácidos débiles: un valor de Ka más alto indica una mayor disociación del ácido y, por lo tanto, un ácido más fuerte, mientras que un Ka más bajo sugiere un ácido débil con una disociación limitada.
¿Cómo se encuentra el Ka de un ácido?
El Ka de un ácido puede determinarse utilizando diversos parámetros y métodos. Entre los más comunes se incluyen: la utilización de las concentraciones molares de equilibrio de los reactivos y productos de la disociación; el cálculo a partir del pH de la solución, aplicando la relación [H⁺] = 10⁻ᵖᴴ y las suposiciones de disociación; la conversión directa si se conoce el valor de pKa (Ka = 10⁻ᵖᴷᵃ); y mediante el análisis de curvas de titulación, identificando el punto de semi-neutralización donde pH = pKa. También es posible calcular Ka si se conoce el valor de Kb de su base conjugada, utilizando la relación fundamental Ka × Kb = Kw.
¿Qué mide la Ka de un ácido débil?
La Ka de un ácido débil mide el grado de disociación o la extensión en que un ácido se ioniza en una solución acuosa. Dado que los ácidos débiles solo se disocian parcialmente, la Ka nos proporciona una indicación cuantitativa de qué tan completa es esa disociación. Un valor de Ka pequeño significa que el ácido se disocia muy poco en iones H⁺ y A⁻, permaneciendo en su mayoría en su forma molecular (HA), lo que lo clasifica como un ácido débil. Por el contrario, un valor de Ka más grande indica una mayor tendencia del ácido a disociarse, lo que resulta en una mayor concentración de iones H⁺ en solución y, por lo tanto, un ácido más fuerte.
Si quieres conocer otros artículos parecidos a Descifrando el Ka: La Clave para la Fuerza de los Ácidos puedes visitar la categoría Química.

