14/03/2025
Desde el aire que respiramos hasta los objetos más sólidos que nos rodean, todo está compuesto por diminutas partículas llamadas átomos y moléculas. Aunque invisibles a simple vista, la capacidad de cuantificarlos es fundamental para la ciencia, la tecnología y nuestra comprensión del universo. ¿Alguna vez te has preguntado cuántos átomos hay en una gota de agua o en un gramo de azúcar? La química nos proporciona las herramientas y los conceptos necesarios para adentrarnos en este mundo microscópico y desvelar sus misterios. Acompáñanos en este viaje para descubrir cómo se calcula la cantidad de átomos y moléculas, una habilidad esencial para cualquier entusiasta de la ciencia.
- La Base de Todo: El Número de Avogadro y los Moles
- Desentrañando la Fórmula Molecular: Contando Átomos en un Compuesto
- La Identidad del Átomo: Protones y el Número Atómico (Z)
- Masa Atómica vs. Número Másico: Comprendiendo el Peso del Átomo
- Los Isótopos: Variaciones del Mismo Elemento
- La Firma Única de Cada Elemento: Espectros Atómicos
- Mujeres Pioneras en la Comprensión del Átomo
- Preguntas Frecuentes (FAQs)
La Base de Todo: El Número de Avogadro y los Moles
Para empezar a contar átomos, primero debemos familiarizarnos con dos conceptos cruciales en química: el mol y el Número de Avogadro. Imagina que necesitas contar granos de arena en una playa; sería una tarea imposible uno por uno. De manera similar, los átomos son tan increíblemente pequeños y numerosos que necesitamos una unidad de conteo masiva. Aquí es donde entra el mol.
Un mol es simplemente una cantidad específica de sustancia que contiene el mismo número de unidades elementales (como átomos, moléculas o iones) que hay en 12 gramos de carbono-12. Esta cantidad, definida experimentalmente, es el famoso Número de Avogadro, cuyo valor es aproximadamente 6.023 x 1023 unidades por mol. Para ponerlo en perspectiva, si tuvieras un mol de canicas, ¡cubrirían la Tierra entera con una capa de kilómetros de profundidad!
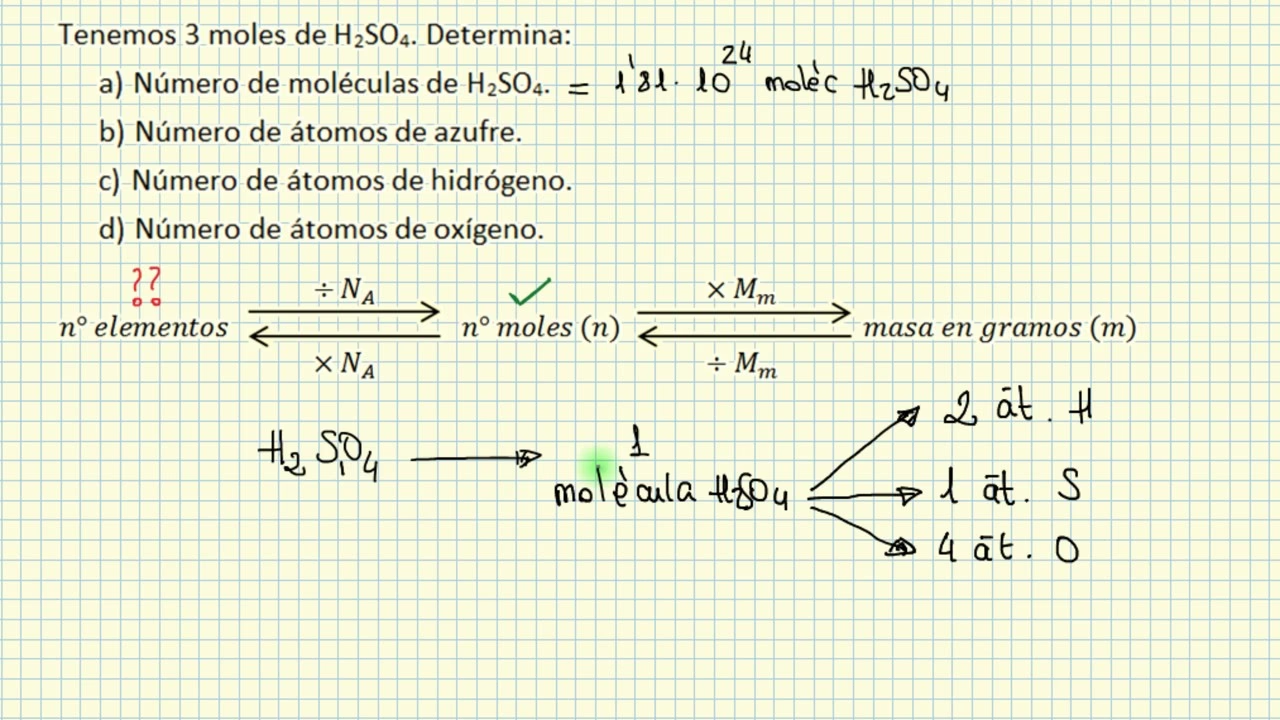
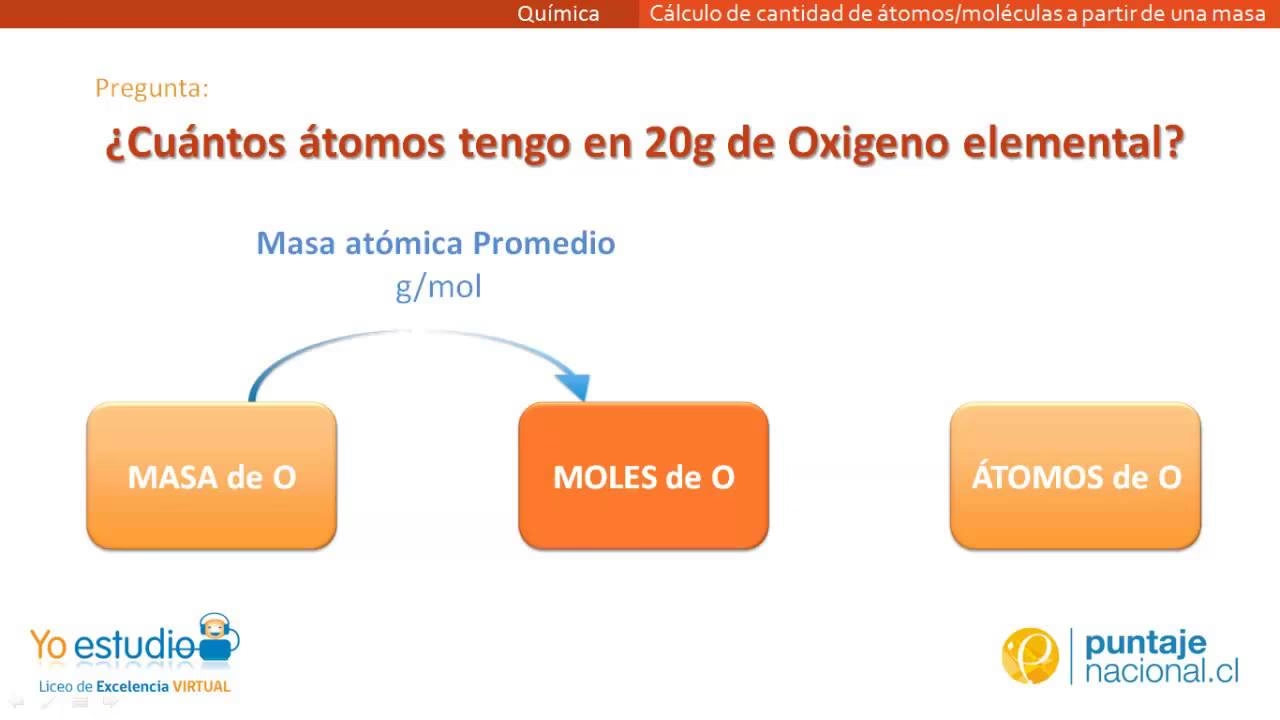
Ahora, ¿cómo utilizamos esto para calcular el número de átomos o moléculas en una muestra dada? El proceso es sorprendentemente directo. Si tienes una masa conocida de una sustancia pura, el primer paso es determinar cuántos moles de esa sustancia hay. Esto se logra dividiendo la masa de tu muestra por la masa molar de la sustancia (que es la masa de un mol de esa sustancia, expresada en gramos/mol y numéricamente igual a su masa atómica o molecular en unidades de masa atómica, u). Una vez que tienes el número de moles, simplemente lo multiplicas por el Número de Avogadro.
Número de Átomos/Moléculas = (Masa de la muestra / Masa molar) × Número de Avogadro
Por ejemplo, si quisieras saber cuántos átomos de oro (Au) hay en una joya de 10 gramos, y sabes que la masa molar del oro es aproximadamente 197 g/mol, el cálculo sería:
Moles de Au = 10 g / 197 g/mol ≈ 0.05076 moles
Número de átomos de Au = 0.05076 moles × (6.023 x 1023 átomos/mol) ≈ 3.058 x 1022 átomos
Este método nos permite cuantificar lo impensable, conectando el mundo macroscópico de las masas con el mundo microscópico de los átomos.
Desentrañando la Fórmula Molecular: Contando Átomos en un Compuesto
Una cosa es contar átomos individuales de un elemento, y otra muy distinta es contar los átomos que componen una molécula o un compuesto. Aquí es donde la fórmula molecular se convierte en nuestra guía. La fórmula molecular nos indica el tipo y el número de átomos de cada elemento presentes en una molécula de ese compuesto.
Para averiguar el número total de átomos de cada elemento en una molécula específica o en un compuesto, debemos observar los subíndices y, si los hay, los coeficientes estequiométricos. Un subíndice es el pequeño número que aparece después del símbolo de un elemento en una fórmula química y que indica cuántos átomos de ese elemento están presentes en una sola molécula. Si no hay un subíndice, se asume que es 1.
Consideremos el ejemplo más común: la molécula de agua, H2O. En esta fórmula, el subíndice '2' junto al hidrógeno (H) nos dice que hay dos átomos de hidrógeno. Como no hay subíndice junto al oxígeno (O), asumimos que hay un átomo de oxígeno. Por lo tanto, una molécula de agua contiene un total de 2 + 1 = 3 átomos.
Otro ejemplo más complejo es la glucosa, cuya fórmula molecular es C6H12O6. Desglosémosla:
- Carbono (C): El subíndice '6' indica 6 átomos de carbono.
- Hidrógeno (H): El subíndice '12' indica 12 átomos de hidrógeno.
- Oxígeno (O): El subíndice '6' indica 6 átomos de oxígeno.
Sumando todos los átomos, una molécula de glucosa contiene 6 + 12 + 6 = 24 átomos. Es fundamental conocer la fórmula molecular de un compuesto para determinar con precisión el número de átomos que lo constituyen.
Cuando trabajamos con reacciones químicas, a veces vemos un número grande delante de una fórmula molecular, conocido como coeficiente. Este coeficiente multiplica todos los átomos dentro de la molécula. Por ejemplo, 2H2O significaría que tenemos dos moléculas de agua. En este caso, tendríamos 2 x 2 = 4 átomos de hidrógeno y 2 x 1 = 2 átomos de oxígeno, para un total de 6 átomos en dos moléculas de agua.
La Identidad del Átomo: Protones y el Número Atómico (Z)
Si los átomos son tan pequeños, ¿cómo podemos diferenciar uno de otro? Así como las huellas dactilares son únicas para cada persona, los átomos poseen una "huella" distintiva que los identifica: el número de protones en su núcleo. Esta característica fundamental es lo que define a un elemento químico y se conoce como Número Atómico, representado por la letra Z.
El átomo, en su forma más básica, está compuesto por tres partículas subatómicas principales: protones, neutrones (ambos ubicados en el núcleo, la parte central y densa del átomo) y electrones (que orbitan alrededor del núcleo). Los protones tienen una carga eléctrica positiva, los electrones una carga negativa, y los neutrones, como su nombre lo indica, no tienen carga.
La importancia del Número Atómico radica en que cada elemento químico tiene un número de protones único y constante. Por ejemplo, todo átomo con 6 protones es carbono, todo átomo con 8 protones es oxígeno, y así sucesivamente. Esta es la base de la organización de la tabla periódica de los elementos, donde los elementos se ordenan de forma creciente según su Número Atómico, de izquierda a derecha y de arriba abajo.
En un átomo eléctricamente neutro, el número de protones es igual al número de electrones. Esto asegura que las cargas positivas y negativas se cancelen mutuamente, dejando el átomo sin carga neta. Por ejemplo, el berilio (Be) tiene un Número Atómico de 4. Esto significa que un átomo de berilio neutro posee 4 protones en su núcleo y 4 electrones girando a su alrededor.
Es importante recordar que, aunque la identidad de un átomo se define por sus protones, los átomos en la naturaleza rara vez se encuentran aislados. Comúnmente forman enlaces químicos entre sí para crear moléculas y compuestos más complejos, buscando estabilidad.
Masa Atómica vs. Número Másico: Comprendiendo el Peso del Átomo
Además del número atómico, existen otros valores clave para describir un átomo, como su masa. Aquí debemos diferenciar entre dos términos que a menudo se confunden: el número másico y la Masa Atómica.
El número másico, representado por la letra A, es simplemente la suma total de protones y neutrones presentes en el núcleo de un átomo. Dado que protones y neutrones son las partículas subatómicas con masa significativa (los electrones tienen una masa despreciable en comparación), el núcleo concentra casi toda la masa del átomo. Por lo tanto, el número másico es siempre un número entero y se calcula con la fórmula:
Número Másico (A) = Protones (Z) + Neutrones (n°)
Si conocemos el número másico y el Número Atómico de un elemento, podemos fácilmente determinar el número de neutrones. Por ejemplo, el uranio (U) tiene un número másico (A) de 238 y un Número Atómico (Z) de 92. Para encontrar el número de neutrones:
Neutrones (n°) = A - Z = 238 - 92 = 146 neutrones
Por otro lado, la Masa Atómica que encontramos en la tabla periódica es un concepto ligeramente diferente y más complejo. A diferencia del número másico, la Masa Atómica suele ser un número con decimales. Esto se debe a que la Masa Atómica reportada es una masa promedio ponderada de todos los Isótopos naturales de un elemento, tomando en cuenta la masa de cada isótopo y su abundancia relativa en la Tierra.
Para calcular la Masa Atómica promedio de un elemento, se multiplican las masas de sus diferentes Isótopos por su abundancia porcentual (convertida a decimal), y luego se suman estos productos. Esta es la razón por la cual los valores de la Masa Atómica en la tabla periódica no son números enteros exactos, sino promedios que reflejan la mezcla natural de los Isótopos de cada elemento.

Los Isótopos: Variaciones del Mismo Elemento
El concepto de Isótopos es fascinante y crucial para entender la diversidad de los átomos. Como mencionamos, el número de protones (Z) define la identidad de un elemento. Sin embargo, no todos los átomos de un mismo elemento son idénticos en su núcleo. Los Isótopos son átomos de un mismo elemento que tienen el mismo número de protones pero difieren en el número de neutrones. Consecuentemente, tienen el mismo Número Atómico pero diferente número másico (A).
El hidrógeno, el elemento más ligero y abundante en el universo, nos ofrece un ejemplo perfecto de Isótopos:
| Nombre del Isótopo | Símbolo | Protones (Z) | Neutrones (n°) | Número Másico (A) | Estabilidad | Abundancia en la Tierra |
|---|---|---|---|---|---|---|
| Protio | 1H | 1 | 0 | 1 | Estable | ~99.99% |
| Deuterio | 2H (D) | 1 | 1 | 2 | Estable | ~0.01% |
| Tritio | 3H (T) | 1 | 2 | 3 | Radiactivo | Traza (~0.000001%) |
Otro ejemplo común es el carbono. Un átomo de carbono neutro siempre tiene 6 protones y 6 electrones. Sin embargo, puede tener 6, 7 u 8 neutrones, dando lugar a los Isótopos12C, 13C y 14C, respectivamente. El carbono-14 es particularmente conocido por su uso en la datación por radiocarbono.
Los Isótopos se clasifican principalmente en dos tipos: estables y radiactivos (o radioisótopos). Los Isótopos estables no se desintegran con el tiempo, mientras que los radiactivos son inestables y emiten radiación a medida que se transforman en Isótopos más estables. Esta propiedad de los radioisótopos tiene innumerables aplicaciones:
- Medicina:Isótopos como el cobalto-60 se usan en radioterapia para tratar el cáncer. Otros se emplean como trazadores en el cuerpo para diagnosticar enfermedades, monitorear el flujo sanguíneo o identificar tumores.
- Industria: Se utilizan para medir el grosor de materiales, esterilizar equipos médicos, detectar fugas en tuberías o en la inspección de soldaduras.
- Energía: Los Isótopos inestables de uranio (como el uranio-235) son el combustible principal en las centrales nucleares, donde su fisión genera enormes cantidades de energía.
- Datación: Además del carbono-14, otros radioisótopos se usan para determinar la edad de rocas, fósiles y artefactos arqueológicos.
- Armamento: Lamentablemente, Isótopos de uranio, plutonio e hidrógeno también se utilizan en la fabricación de armamento nuclear.
El estudio de los Isótopos nos permite no solo entender la composición de la materia, sino también aplicar sus propiedades en beneficio de la humanidad o, en algunos casos, con fines destructivos.
La Firma Única de Cada Elemento: Espectros Atómicos
Así como podemos identificar a una persona por sus huellas dactilares, los elementos químicos tienen una "firma" única que permite diferenciarlos: sus Espectros Atómicos. Cuando los átomos son excitados (por ejemplo, al calentarlos o pasar una corriente eléctrica a través de ellos), emiten luz en longitudes de onda muy específicas. Este patrón de líneas brillantes es lo que se conoce como espectro de emisión. De manera inversa, si la luz blanca pasa a través de un gas, los átomos de ese gas absorberán ciertas longitudes de onda, creando un espectro de absorción con líneas oscuras.
Cada elemento produce su propio conjunto característico de líneas espectrales, único y diferente al de cualquier otro elemento. Esto es como un código de barras lumínico que revela su identidad. Esta propiedad ha sido crucial para el descubrimiento de elementos y para entender la composición de objetos celestes. De hecho, el helio (He) fue descubierto por primera vez en el espectro de la luz del Sol en 1868, casi tres décadas antes de ser encontrado en la Tierra.
Estos Espectros Atómicos son una manifestación de cómo los electrones se mueven entre diferentes niveles de energía dentro del átomo. La luz emitida o absorbida forma parte del espectro electromagnético, que incluye desde ondas de radio y microondas hasta luz visible, rayos ultravioleta, rayos X y rayos gamma. La única diferencia entre estas formas de radiación electromagnética es su longitud de onda y frecuencia, pero todas viajan a la velocidad de la luz y son una forma de energía.
Mujeres Pioneras en la Comprensión del Átomo
La historia de la química y la física está llena de mentes brillantes, y es importante reconocer las contribuciones de mujeres extraordinarias que, a menudo, no recibieron el mismo reconocimiento que sus colegas masculinos. Desde Hipatia de Alejandría, una filósofa y matemática de la antigüedad, hasta las científicas que desentrañaron los secretos del átomo en la era moderna, su legado es inmenso.
En el desarrollo de la tabla periódica y nuestra comprensión de la estructura atómica, figuras como Marie Curie son ampliamente conocidas por sus dos premios Nobel y el descubrimiento de elementos como el polonio y el radio. Sin embargo, su hija, Irene Joliot-Curie, también fue una destacada química y física nuclear que, junto a su esposo, descubrió la radiactividad artificial, un avance fundamental.

Otras mujeres como Harriet Brooks, pionera en el estudio de la radiactividad; Ida Tacke-Noddack, codescubridora del renio y primera en proponer la idea de la fisión nuclear; Marguerite Perey, descubridora del francio; y Lise Meitner, quien jugó un papel crucial en la explicación teórica de la fisión nuclear, realizaron aportaciones esenciales que cimentaron nuestro conocimiento actual del átomo y sus interacciones. Su trabajo colectivo ha sido indispensable para que la tabla periódica sea tal y como la conocemos hoy y para el desarrollo de la física nuclear.
Preguntas Frecuentes (FAQs)
A continuación, respondemos algunas de las preguntas más comunes sobre el conteo y la naturaleza de los átomos:
¿Por qué es importante calcular la cantidad de átomos?
Calcular la cantidad de átomos es fundamental en diversas áreas. En química, permite predecir y controlar reacciones, determinar rendimientos, y diseñar nuevos materiales. En medicina, es crucial para la dosificación de medicamentos y el uso de Isótopos en diagnóstico y tratamiento. En la industria, ayuda en el control de calidad y en la fabricación precisa. Básicamente, nos permite entender y manipular la materia a nivel fundamental.
¿Qué es el Número de Avogadro y por qué es tan grande?
El Número de Avogadro (aproximadamente 6.023 x 1023) es el número de unidades elementales (átomos, moléculas, etc.) que hay en un mol de cualquier sustancia. Es tan grande porque los átomos son increíblemente pequeños. Necesitamos una cantidad tan vasta para poder trabajar con ellos a una escala macroscópica y medible en gramos.
¿Un átomo siempre tiene el mismo número de protones y neutrones?
No. Un átomo del mismo elemento siempre tendrá el mismo número de protones (ese es su Número Atómico y define su identidad). Sin embargo, puede tener un número variable de neutrones. Estos átomos con el mismo número de protones pero diferente número de neutrones se llaman Isótopos. Por ejemplo, el carbono siempre tiene 6 protones, pero puede tener 6, 7 u 8 neutrones.
¿Todos los átomos de un mismo elemento son idénticos?
No, no son completamente idénticos debido a la existencia de los Isótopos. Aunque todos los átomos de un elemento tienen el mismo número de protones y, por lo tanto, las mismas propiedades químicas, pueden diferir en su número de neutrones y, consecuentemente, en su masa. Esto no afecta la identidad del elemento, pero sí puede influir en propiedades físicas o en su estabilidad (radiactividad).
¿Para qué se utilizan los Isótopos en la vida real?
Los Isótopos tienen aplicaciones muy diversas. Los radioisótopos se usan en medicina nuclear para diagnósticos (como PET scans) y tratamientos (radioterapia). En la industria, se emplean para esterilizar equipos, medir espesores y en generadores de energía nuclear. En ciencia, son cruciales para la datación arqueológica (carbono-14) y para investigar mecanismos de reacciones químicas.
Contar lo invisible, es decir, calcular la cantidad de átomos y moléculas, es una piedra angular de la química y de nuestra comprensión del mundo material. Desde el Número de Avogadro que nos permite manejar cantidades astronómicas de partículas, hasta la Masa Atómica que refleja la diversidad de los Isótopos, cada concepto nos acerca más a la esencia de la materia. Comprender la estructura del átomo, la importancia de los protones y neutrones, y cómo estas partículas definen la identidad y el comportamiento de los elementos, nos abre las puertas a un universo de conocimiento. La capacidad de cuantificar y caracterizar estas diminutas unidades es lo que ha impulsado avances revolucionarios en medicina, tecnología y nuestra exploración del cosmos, demostrando que incluso lo más pequeño puede tener el impacto más grande.
Si quieres conocer otros artículos parecidos a Contando lo Invisible: Calculando Átomos y Moléculas puedes visitar la categoría Química.

