07/06/2023
En el fascinante mundo de la química, las reacciones son el corazón de todo proceso, desde la formación de compuestos simples hasta la creación de materiales complejos. Pero, ¿cómo medimos la eficacia de estas transformaciones? Aquí es donde entra en juego el concepto de rendimiento, una medida crucial que nos indica qué tan bien se ha producido un nuevo material a partir de los elementos y compuestos iniciales. Comprender el rendimiento es fundamental para cualquier químico, ya que permite evaluar la eficiencia de un experimento, optimizar procesos y predecir resultados con mayor precisión.
- Las Ecuaciones Químicas y sus Componentes Esenciales
- Tipos de Rendimiento en Química
- Cálculo del Rendimiento en Química: Un Proceso Paso a Paso
- Factores que Afectan el Rendimiento de una Reacción Química
- Importancia del Rendimiento Porcentual en la Comunidad Científica
- Tabla Comparativa de los Tipos de Rendimiento
- Preguntas Frecuentes sobre el Rendimiento Químico
- ¿Por qué el rendimiento real es casi siempre menor que el teórico?
- ¿Qué significa un rendimiento porcentual del 100%?
- ¿Es posible tener un rendimiento porcentual superior al 100%?
- ¿Qué es un reactivo limitante y por qué es importante para el rendimiento?
- ¿Cómo se puede optimizar el rendimiento de una reacción química?
Las Ecuaciones Químicas y sus Componentes Esenciales
Antes de sumergirnos en los tipos de rendimiento, es vital comprender la base de toda reacción química: la ecuación química. Una ecuación química es una representación simbólica de lo que ocurre durante una reacción, mostrando las sustancias que reaccionan y las que se forman. En ella, identificamos dos componentes principales:
- Reactivos: Son las sustancias iniciales que se combinan o interactúan. Se encuentran a la izquierda de la flecha en la ecuación.
- Productos: Son las nuevas sustancias que se forman como resultado de la reacción. Se ubican a la derecha de la flecha.
Es crucial que toda ecuación química esté balanceada. Esto significa que el número de átomos de cada elemento debe ser el mismo en ambos lados de la flecha de reacción. Este principio se rige por la Ley de Conservación de la Masa, que establece que la masa no se crea ni se destruye en un proceso químico, solo se transforma. Si una ecuación no está balanceada, no representa con precisión la realidad de la reacción y, por lo tanto, cualquier cálculo de rendimiento sería incorrecto.
Consideremos un ejemplo clásico: la reacción entre el ácido sulfúrico (H₂SO₄) y el hidróxido de sodio (NaOH) para formar sulfato de sodio (Na₂SO₄) y agua (H₂O). La ecuación balanceada es la siguiente:
H₂SO₄ + 2NaOH → Na₂SO₄ + 2H₂O
En esta ecuación, podemos verificar que hay la misma cantidad de átomos de hidrógeno, azufre, oxígeno y sodio en ambos lados, asegurando el cumplimiento de la Ley de Conservación de la Masa y proporcionando la base para cálculos estequiométricos precisos.
Tipos de Rendimiento en Química
En el estudio de las reacciones químicas, los científicos se basan en tres tipos de rendimiento para calcular y comprender los resultados:
Rendimiento Teórico
El rendimiento teórico, también conocido como rendimiento predicho, representa la cantidad máxima de producto que se podría obtener si una reacción química se llevara a cabo bajo condiciones óptimas y perfectas, es decir, si todos los reactivos se convirtieran completamente en productos sin ninguna pérdida. Este valor se calcula antes de realizar el experimento, utilizando la estequiometría de la ecuación química balanceada y las cantidades iniciales de los reactivos. Es una predicción idealizada que asume una eficiencia del 100%.
Para determinar el rendimiento teórico, es fundamental identificar el reactivo limitante. El reactivo limitante es aquel que se consume por completo en una reacción y, por lo tanto, determina la cantidad máxima de producto que se puede formar. Una vez identificado, la cantidad de producto se calcula a partir de la cantidad del reactivo limitante, utilizando las relaciones molares de la ecuación balanceada.
Rendimiento Real
El rendimiento real es la cantidad de producto que se obtiene y se mide experimentalmente después de llevar a cabo una reacción química en el laboratorio. A diferencia del rendimiento teórico, el rendimiento real es el resultado tangible y definitivo de un experimento. Generalmente, el rendimiento real es menor que el rendimiento teórico. Esto se debe a una variedad de factores que impiden que la reacción alcance una eficiencia del 100%.

Algunas de las razones comunes por las que el rendimiento real difiere del teórico incluyen:
- Reacciones incompletas: No todos los reactivos se convierten en productos.
- Reacciones secundarias (o paralelas): Los reactivos pueden combinarse de formas inesperadas para formar subproductos no deseados, consumiendo parte del reactivo limitante.
- Pérdidas durante la purificación y manipulación: Durante los procesos de filtración, transferencia de materiales, evaporación, cromatografía u otras técnicas de purificación, siempre se pierde una pequeña cantidad de producto.
- Equilibrio químico: Algunas reacciones alcanzan un estado de equilibrio en el que tanto los reactivos como los productos coexisten, impidiendo la conversión completa de los reactivos.
- Impurezas en los reactivos: Si los materiales de partida no son puros, parte de la masa de los reactivos no contribuirá a la formación del producto deseado.
Es importante destacar que el concepto de "pérdida" de material en una reacción química no significa que la sustancia se destruya, lo cual violaría la Ley de Conservación de la Masa. Más bien, implica que la sustancia no se transformó de la manera deseada, se quedó sin reaccionar, se convirtió en un subproducto o se perdió físicamente durante el proceso de aislamiento.
Rendimiento Porcentual
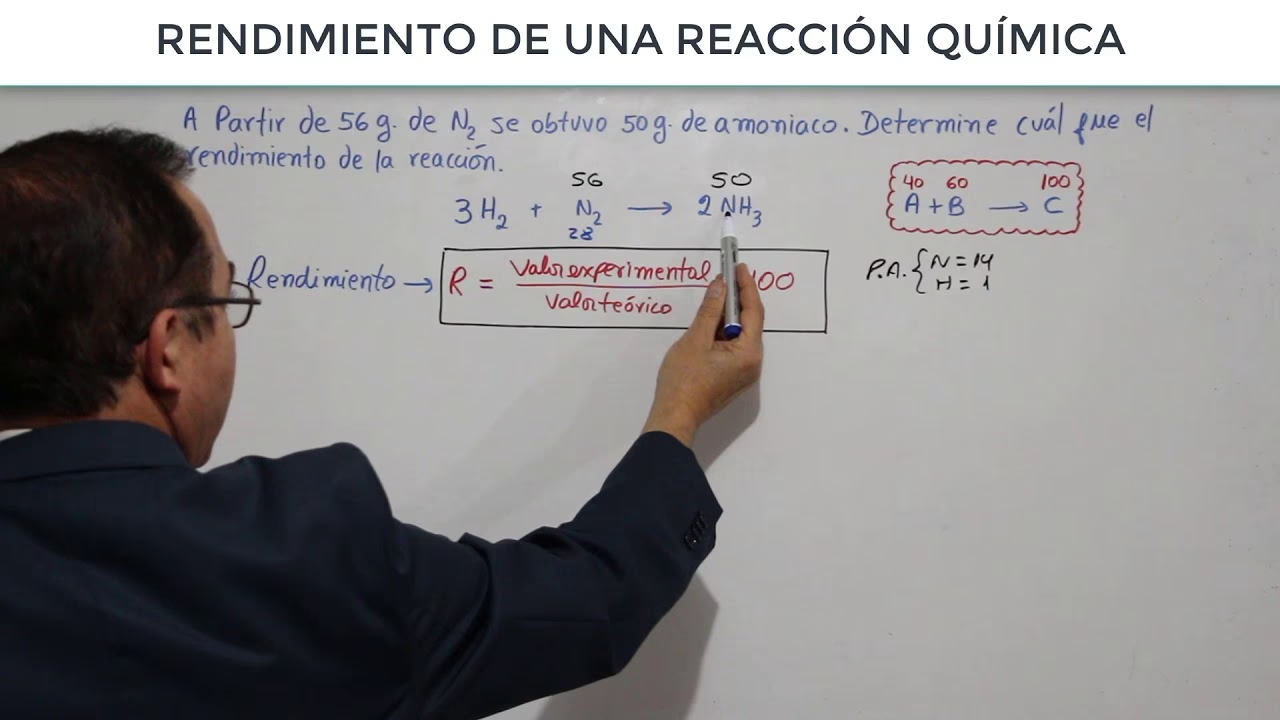
El rendimiento porcentual es una medida de la eficiencia de una reacción química. Se calcula dividiendo el rendimiento real por el rendimiento teórico y multiplicando el resultado por 100 para expresarlo como un porcentaje. Este valor nos indica qué tan cerca estuvo el experimento de alcanzar su potencial químico máximo.
La fórmula para calcular el rendimiento porcentual es:
Rendimiento Porcentual = (Rendimiento Real / Rendimiento Teórico) × 100
Un rendimiento porcentual alto indica que la reacción fue muy eficiente en la conversión de reactivos a productos deseados, mientras que un rendimiento bajo sugiere ineficiencia o problemas en el proceso. Los rendimientos cercanos al 100% son considerados excelentes, aunque en la práctica son difíciles de alcanzar debido a los factores mencionados anteriormente.
Cálculo del Rendimiento en Química: Un Proceso Paso a Paso
Para calcular los tres tipos de rendimiento de una reacción química, se sigue un proceso sistemático:
Paso 1: Balancear la Ecuación Química
Como se mencionó anteriormente, el primer y más crucial paso es asegurarse de que la ecuación química esté balanceada. Esto garantiza que se respeten las leyes de la estequiometría y la conservación de la masa.
Paso 2: Determinar el Rendimiento Teórico
Una vez balanceada la ecuación, se utiliza la estequiometría para calcular el rendimiento teórico. Esto implica:
- Convertir las masas de los reactivos conocidos a moles usando sus masas molares.
- Identificar el reactivo limitante. Este es el reactivo que producirá la menor cantidad de producto, y por lo tanto, el que se agotará primero.
- Usar la cantidad de moles del reactivo limitante y las proporciones molares de la ecuación balanceada para calcular los moles del producto deseado.
- Convertir los moles del producto deseado a gramos (o la unidad de masa relevante) usando su masa molar. Este valor es el rendimiento teórico.
Ejemplo: Volviendo a la reacción entre H₂SO₄ y NaOH. Supongamos que un químico tiene 6.9 gramos de ácido sulfúrico. Usando cálculos estequiométricos (y suponiendo que el ácido sulfúrico es el reactivo limitante o que hay suficiente NaOH), podría predecir que se podrían crear potencialmente 10 gramos de sulfato de sodio (Na₂SO₄). Estos 10 gramos representan el rendimiento teórico para este producto específico.

Paso 3: Medir el Rendimiento Real
Este paso se realiza experimentalmente en el laboratorio. Después de llevar a cabo la reacción y purificar el producto, se pesa la cantidad obtenida. Este es el rendimiento real.
Ejemplo: El químico realiza el experimento y, después de la purificación, encuentra que solo se han producido 7.2 gramos de sulfato de sodio. Esta cifra más baja, resultado de diversas "pérdidas" o ineficiencias, es el rendimiento real.
Paso 4: Calcular el Rendimiento Porcentual
Con el rendimiento real y el teórico ya determinados, se aplica la fórmula del rendimiento porcentual:
Rendimiento Porcentual = (Rendimiento Real / Rendimiento Teórico) × 100
Ejemplo: Para el sulfato de sodio, el cálculo sería:
Rendimiento Porcentual = (7.2 g / 10 g) × 100
Rendimiento Porcentual = 0.72 × 100
Rendimiento Porcentual = 72%
Esto significa que el rendimiento real del sulfato de sodio fue el 72% del rendimiento teórico, indicando la eficiencia de este proceso particular.
Factores que Afectan el Rendimiento de una Reacción Química
Como se mencionó, el rendimiento real rara vez es idéntico al teórico. Varios factores pueden influir en el resultado final de una reacción:
- Condiciones de la reacción: La temperatura, la presión, la concentración de los reactivos y la presencia de catalizadores pueden afectar la velocidad y la extensión de una reacción. Condiciones subóptimas pueden llevar a rendimientos más bajos.
- Reacciones secundarias: Es común que, además de la reacción principal deseada, ocurran otras reacciones paralelas que consumen reactivos y producen subproductos no deseados, reduciendo así la cantidad de producto principal.
- Equilibrio químico: Muchas reacciones son reversibles y alcanzan un estado de equilibrio dinámico donde la velocidad de la reacción directa es igual a la de la inversa. En este punto, la reacción no procede hasta la conversión completa de los reactivos.
- Pérdidas durante la manipulación: En cada etapa del proceso experimental (mezclado, calentamiento, enfriamiento, transferencia entre recipientes, filtración, lavado), hay una probabilidad de perder una pequeña cantidad de material.
- Técnicas de purificación: La purificación del producto es esencial para obtener un material puro, pero a menudo implica pérdidas. Por ejemplo, en la recristalización, parte del producto puede permanecer disuelto en el solvente. En la cromatografía, el producto puede dispersarse o adherirse al material estacionario.
- Pureza de los reactivos: Los reactivos que contienen impurezas reducirán el rendimiento, ya que la masa de las impurezas se cuenta como parte del reactivo inicial pero no participa en la formación del producto deseado.
- Habilidad experimental: La experiencia y la precisión del experimentador juegan un papel significativo en la maximización del rendimiento real.
Importancia del Rendimiento Porcentual en la Comunidad Científica
El rendimiento porcentual es una herramienta invaluable en la comunidad científica por varias razones:
- Evaluación de la eficiencia: Permite a los químicos evaluar la eficiencia de sus métodos y procedimientos experimentales. Un rendimiento porcentual alto indica un proceso bien controlado y optimizado.
- Comparación de métodos: Facilita la comparación entre diferentes vías sintéticas o condiciones de reacción para producir el mismo compuesto. Los investigadores pueden determinar cuál es el método más eficiente.
- Reproducibilidad: Al documentar los rendimientos teóricos, reales y porcentuales, los químicos proporcionan información crucial a sus colegas, permitiendo que otros reproduzcan sus experimentos y anticipen los resultados.
- Optimización de procesos: Un rendimiento porcentual bajo puede señalar la necesidad de optimizar las condiciones de la reacción, la pureza de los reactivos o las técnicas de purificación para mejorar la producción.
- Relevancia industrial: En la industria, un alto rendimiento porcentual es directamente proporcional a la rentabilidad. Minimizar las pérdidas y maximizar la producción es vital para la fabricación a gran escala.
Tabla Comparativa de los Tipos de Rendimiento
| Tipo de Rendimiento | Descripción | Cómo se Determina | Importancia |
|---|---|---|---|
| Rendimiento Teórico | Cantidad máxima de producto que se podría obtener bajo condiciones ideales. | Cálculo estequiométrico a partir de la ecuación balanceada y el reactivo limitante. | Establece el límite superior de producción, una referencia ideal. |
| Rendimiento Real | Cantidad de producto obtenida experimentalmente en el laboratorio. | Medición directa (pesaje) del producto aislado y purificado. | Representa la cantidad de producto tangible obtenida en la práctica. |
| Rendimiento Porcentual | Medida de la eficiencia de la reacción; relación entre el rendimiento real y el teórico. | Fórmula: (Rendimiento Real / Rendimiento Teórico) × 100. | Evalúa la eficacia del experimento, permite optimización y comparación. |
Preguntas Frecuentes sobre el Rendimiento Químico
¿Por qué el rendimiento real es casi siempre menor que el teórico?
El rendimiento real es casi siempre menor que el teórico debido a una combinación de factores como reacciones incompletas, la ocurrencia de reacciones secundarias que forman subproductos no deseados, pérdidas de material durante las etapas de purificación y manipulación, y la presencia de impurezas en los reactivos iniciales. Además, algunas reacciones alcanzan un equilibrio químico, lo que impide la conversión completa de los reactivos.
¿Qué significa un rendimiento porcentual del 100%?
Un rendimiento porcentual del 100% significa que la cantidad de producto obtenida experimentalmente (rendimiento real) es exactamente igual a la cantidad máxima de producto que se predijo estequiométricamente (rendimiento teórico). En la práctica, esto es muy difícil de lograr debido a las inevitables pérdidas y complejidades de las reacciones reales.

¿Es posible tener un rendimiento porcentual superior al 100%?
Teóricamente, no es posible tener un rendimiento porcentual superior al 100% si el producto es completamente puro. Sin embargo, en un laboratorio, un rendimiento aparente superior al 100% puede indicar que el producto obtenido no está completamente puro y contiene impurezas (como solventes residuales, subproductos no eliminados o reactivos sin reaccionar) que aumentan su masa medida, haciendo que el rendimiento real parezca mayor de lo que realmente es para el producto puro.
¿Qué es un reactivo limitante y por qué es importante para el rendimiento?
El reactivo limitante es el reactivo que se consume por completo en una reacción química, deteniendo la formación de más producto. Es importante porque la cantidad del reactivo limitante determina la cantidad máxima de producto que se puede formar, es decir, el rendimiento teórico de la reacción. Si se tiene un exceso de otros reactivos, estos simplemente no reaccionarán una vez que el reactivo limitante se haya agotado.
¿Cómo se puede optimizar el rendimiento de una reacción química?
Para optimizar el rendimiento de una reacción, los químicos pueden ajustar varios parámetros: controlar cuidadosamente la temperatura, la presión y la concentración de los reactivos; usar catalizadores adecuados; minimizar las reacciones secundarias; refinar las técnicas de purificación para reducir las pérdidas; y asegurar la alta pureza de los reactivos de partida. Un diseño experimental cuidadoso y una ejecución precisa son clave.
En conclusión, el rendimiento en química es un concepto multifacético que va más allá de un simple cálculo. Es una medida fundamental que permite a los químicos evaluar la eficiencia de sus procesos, comprender las limitaciones de las reacciones y trabajar hacia la optimización. Al dominar el cálculo y la interpretación del rendimiento real, rendimiento teórico y rendimiento porcentual, los científicos pueden desentrañar los misterios de las transformaciones químicas y avanzar en la creación de nuevos materiales y tecnologías. Es un pilar esencial en el laboratorio y en la industria, que impulsa la innovación y la eficiencia en el vasto campo de la química.
Si quieres conocer otros artículos parecidos a ¿Cómo se Calcula el Rendimiento en Química? puedes visitar la categoría Química.
