15/02/2025
En el vasto y complejo universo de la química, existen fenómenos que desafían la intuición y las técnicas de separación convencionales. Uno de los más intrigantes es el conocido como azeótropo. Imagina una mezcla de líquidos que, al ser calentada, se comporta como si fuera una sustancia pura, hirviendo a una temperatura constante y produciendo un vapor con la misma composición que el líquido original. Esta peculiaridad impide su separación mediante la simple destilación, una técnica fundamental en laboratorios e industrias. Pero, ¿qué es exactamente un azeótropo y por qué se comporta de esta manera? Acompáñanos en este recorrido para desentrañar los secretos de estas mezclas de punto de ebullición constante y las ingeniosas estrategias desarrolladas para su separación.
El término azeótropo, acuñado en 1911 por los químicos ingleses John Wade y Richard William Merriman, tiene sus raíces en el griego, combinando 'a-' (sin), 'zeein' (hervir) y 'tropos' (cambio), lo que se traduce como 'sin cambio al hervir'. Esta etimología capta perfectamente la esencia de estas mezclas: su composición no se altera durante la destilación, de ahí que también se les conozca como mezclas de punto de ebullición constante.
- ¿Qué es un Azeótropo y por qué son Especiales?
- Tipos de Azeótropos: Desviaciones de la Ley de Raoult
- Homogeneidad y Heterogeneidad: Azeótropos Homogéneos y Heterogéneos
- El Número de Componentes en un Azeótropo
- Condiciones para la Existencia de un Azeótropo
- Superando el Desafío: Métodos de Separación de Azeótropos
- Preguntas Frecuentes
¿Qué es un Azeótropo y por qué son Especiales?
Un azeótropo es, en esencia, una mezcla de dos o más líquidos que exhibe un punto de ebullición constante debido a que la composición del vapor en equilibrio es idéntica a la composición de la mezcla líquida. Esta característica es lo que los hace tan desafiantes para la separación convencional. En una destilación normal, los componentes de una mezcla se separan porque tienen diferentes puntos de ebullición, lo que permite que el componente más volátil se evapore preferentemente. Sin embargo, en un azeótropo, esta diferencia de volatilidad desaparece en un punto específico de composición, creando un cuello de botella en el proceso de separación.
El punto de ebullición de una mezcla azeotrópica puede ser sorprendentemente superior o inferior al de cualquiera de sus componentes puros. Esta desviación del comportamiento ideal es clave para entender su formación y clasificación.
Tipos de Azeótropos: Desviaciones de la Ley de Raoult
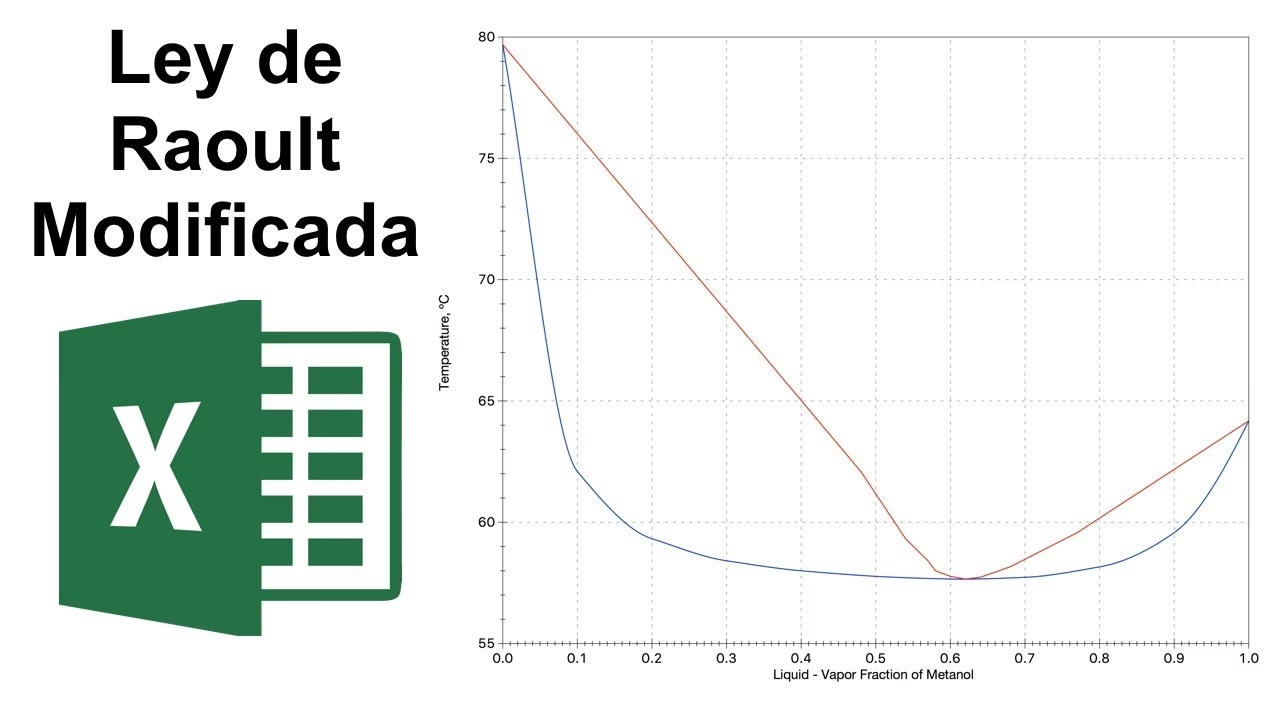
La existencia de los azeótropos se explica por las desviaciones que una mezcla real presenta respecto a la Ley de Raoult. Esta ley predice el comportamiento de las presiones de vapor en mezclas ideales, donde las interacciones entre moléculas de diferentes componentes son similares a las interacciones entre moléculas del mismo componente. Cuando hay una "desafinidad" o una "afinidad" inusual entre los componentes, se producen desviaciones que pueden llevar a la formación de azeótropos.
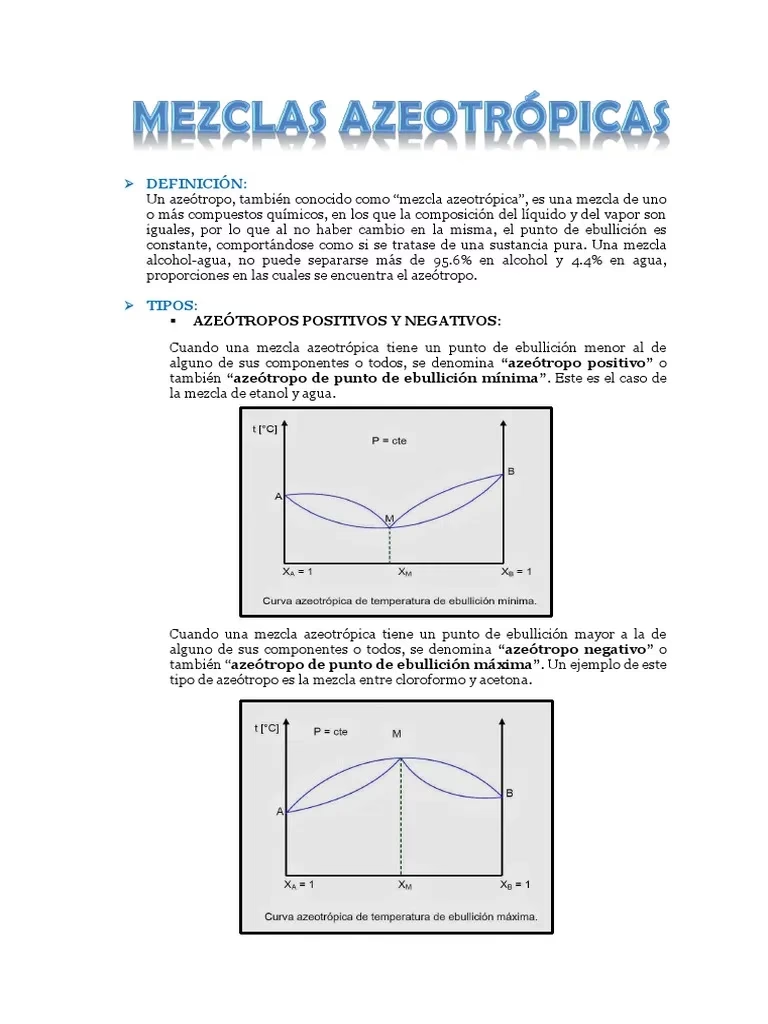
Azeótropos de Mínimo Punto de Ebullición (Desviación Positiva)
Estos azeótropos se forman cuando una solución muestra una gran desviación positiva de la Ley de Raoult. Esto significa que los componentes de la mezcla tienen una "desafinidad" entre sí; las moléculas de X prefieren unirse a otras moléculas de X, y las moléculas de Y prefieren unirse a otras moléculas de Y, más que unirse entre sí (X-Y). Como resultado, las moléculas escapan más fácilmente de la fase líquida a la fase de vapor, lo que se traduce en una presión de vapor total mayor de lo esperado.
El punto de ebullición de un azeótropo de mínimo punto de ebullición es siempre más bajo que el de cualquiera de sus constituyentes puros. Un ejemplo clásico es la mezcla de etanol y agua. El etanol puro hierve a 78.4 °C y el agua a 100 °C. Sin embargo, una mezcla de 95.63% de etanol y 4.37% de agua (en masa) hierve a 78.2 °C, una temperatura inferior a la de ambos componentes. Alcanzada esta composición, el líquido y el vapor tienen la misma composición, impidiendo una mayor separación por destilación simple.
En un diagrama de fases, donde el eje vertical representa la temperatura y el horizontal la composición, un azeótropo de mínimo punto de ebullición se manifiesta como un punto donde las curvas de líquido y vapor se tocan en un mínimo de temperatura. Al destilar una mezcla no azeotrópica, el vapor se enriquece en el componente más volátil, acercándose progresivamente a la composición del azeótropo. Sin embargo, una vez que se alcanza la composición azeotrópica, ya no es posible separar más los componentes mediante destilación.
Azeótropos de Máximo Punto de Ebullición (Desviación Negativa)
Por el contrario, los azeótropos de máximo punto de ebullición surgen de una gran desviación negativa de la Ley de Raoult. En este caso, los componentes de la mezcla tienen una fuerte "afinidad" entre sí; las moléculas de X y Y se unen más fuertemente entre sí (X-Y) que a las moléculas de su propio tipo (X-X o Y-Y). Esta mayor atracción molecular hace que sea más difícil para las moléculas escapar de la fase líquida a la fase de vapor, resultando en una presión de vapor total menor de lo predicho por la Ley de Raoult.
El punto de ebullición de un azeótropo de máximo punto de ebullición es siempre superior al de cualquiera de sus constituyentes puros. Un ejemplo notable es la mezcla de ácido nítrico y agua. El ácido nítrico puro hierve a 83 °C y el agua a 100 °C, pero una mezcla azeotrópica de aproximadamente 68% de ácido nítrico y 32% de agua hierve a 120.4 °C. Otro ejemplo es el ácido clorhídrico acuoso (20.2% HCl y 79.8% agua), que hierve a 110 °C, muy por encima de los puntos de ebullición del HCl (-85 °C) y del agua (100 °C).
En un diagrama de fases, este tipo de azeótropo se muestra como un punto donde las curvas de líquido y vapor se tocan en un máximo de temperatura. A diferencia de los azeótropos de mínimo, la destilación de estas mezclas hace que el destilado se aleje de la composición azeotrópica, mientras que el residuo se acerca a ella.
Para comprender mejor las diferencias fundamentales entre los azeótropos de mínimo y máximo punto de ebullición, podemos observar la siguiente tabla comparativa:
| Característica | Azeótropo de Mínimo Punto de Ebullición | Azeótropo de Máximo Punto de Ebullición |
|---|---|---|
| Desviación de la Ley de Raoult | Positiva (mayor presión de vapor) | Negativa (menor presión de vapor) |
| Punto de Ebullición | Inferior al de cualquiera de sus componentes puros | Superior al de cualquiera de sus componentes puros |
| Afinidad Molecular | Los componentes se "prefieren" a sí mismos (X-X, Y-Y) más que entre sí (X-Y) | Los componentes se "prefieren" entre sí (X-Y) más que a sí mismos (X-X, Y-Y) |
| Ejemplo Típico | Etanol (95.63%) y Agua (4.37%) | Ácido Nítrico (68%) y Agua (32%) |
Otros Tipos de Azeótropos
La complejidad de los azeótropos no se limita a los tipos de mínimo y máximo punto de ebullición:
- Azeótropos Dobles: Son sistemas más complejos que presentan tanto un punto de ebullición mínimo como uno máximo. Un ejemplo es la mezcla de benceno y hexafluorobenceno.
- Azeótropos de Silla (Complejos): Estos azeótropos no encajan en las categorías de mínimo o máximo punto de ebullición. Su punto de ebullición cae entre los puntos de ebullición de sus componentes. Solo pueden formarse en sistemas de tres o más componentes. Un ejemplo conocido es el azeótropo ternario formado por 30% acetona, 47% cloroformo y 23% metanol, que hierve a 57.5 °C.
Homogeneidad y Heterogeneidad: Azeótropos Homogéneos y Heterogéneos
La miscibilidad de los componentes en una mezcla también influye en el tipo de azeótropo formado:
- Azeótropos Homogéneos: Se forman cuando los componentes son completamente miscibles en todas las proporciones, es decir, forman una única fase líquida. Los azeótropos de etanol-agua o ácido nítrico-agua son ejemplos de azeótropos homogéneos.
- Azeótropos Heterogéneos (Heteroazeótropos): Se encuentran cuando los componentes de la mezcla no son completamente miscibles y, por lo tanto, forman dos fases líquidas separadas. Curiosamente, los heteroazeótropos solo se conocen en combinación con un comportamiento azeotrópico de temperatura mínima. Un ejemplo es la mezcla de cloroformo y agua. Si se calientan juntas, esta mezcla bifásica hierve a 53.3 °C (inferior a los puntos de ebullición del cloroformo 61.2 °C y del agua 100 °C). El vapor resultante tendrá una composición fija (97.0% cloroformo y 3.0% agua), independientemente de las proporciones de las fases líquidas presentes.
Es importante distinguir los azeótropos de las mezclas zeotrópicas. Las mezclas zeotrópicas son aquellas que no forman azeótropos en ninguna proporción y, por lo tanto, sus componentes sí pueden separarse completamente por destilación fraccionada. Irónicamente, los azeótropos son útiles para separar mezclas zeotrópicas difíciles. Por ejemplo, la separación de ácido acético puro del agua es económicamente inviable por destilación simple debido a que cada destilación sucesiva es menos efectiva. Sin embargo, añadiendo acetato de etilo como entrenador, se forma un azeótropo con el agua que hierve a 70.4 °C, permitiendo destilar el agua y dejar un ácido acético casi puro como residuo.
El Número de Componentes en un Azeótropo
Los azeótropos pueden clasificarse también por el número de componentes que los forman:
- Azeótropos Binarios: Consisten en dos componentes, como la mezcla de dietil éter y halotano, usada en anestesia.
- Azeótropos Ternarios: Compuestos por tres constituyentes, como el azeótropo de acetona, metanol y cloroformo.
- También existen azeótropos con más de tres componentes, aunque son menos comunes.
Condiciones para la Existencia de un Azeótropo
La condición fundamental para que se forme un azeótropo es que la mezcla se desvíe de la Ley de Raoult. En el punto azeotrópico, la composición del líquido y del vapor en equilibrio son idénticas. Matemáticamente, esto implica que en un diagrama de presión de vapor total versus fracción molar, debe existir un máximo o un mínimo local. Esta es una consecuencia directa de la ecuación de Gibbs-Duhem.

- Una desviación positiva de la Ley de Raoult (cuando la afinidad X-Y es menor que X-X o Y-Y) conduce a una presión de vapor total mayor de lo esperado, y si esta desviación es suficientemente grande, se forma un azeótropo de mínimo punto de ebullición (máximo de presión de vapor).
- Una desviación negativa (cuando la afinidad X-Y es mayor que X-X o Y-Y) conduce a una presión de vapor total menor de lo esperado, y si la desviación es lo suficientemente grande, se forma un azeótropo de máximo punto de ebullición (mínimo de presión de vapor).
Superando el Desafío: Métodos de Separación de Azeótropos
Dado que la destilación simple es ineficaz para separar azeótropos, se han desarrollado métodos ingeniosos para "romper" estas mezclas y obtener los componentes puros. La dificultad de esta separación llevó a algunos investigadores a creer inicialmente que los azeótropos eran compuestos químicos, pero su composición no sigue proporciones estequiométricas simples y puede variar con la presión, lo que desmiente esta idea.
Destilación por Cambio de Presión (Pressure Swing Distillation)
Este método explota el hecho de que la composición de un azeótropo puede variar significativamente con la presión. Se destila la mezcla a una presión, se obtiene un destilado que se acerca al azeótropo de esa presión, y luego se somete ese destilado a una presión diferente. Al cambiar la presión, la composición del azeótropo se desplaza, permitiendo que la mezcla original, que antes era azeotrópica, ya no lo sea a la nueva presión. Esto permite que una nueva destilación a la segunda presión separe aún más los componentes. Un ejemplo es la separación de agua y tetrahidrofurano, que puede separarse económicamente mediante un cambio de presión entre 1 atm y 8 atm.
Destilación Azeotrópica (Azeotropic Distillation)
Este es quizás el método más conocido para romper azeótropos. Consiste en añadir un tercer agente, llamado entrenador, a la mezcla azeotrópica binaria. Este entrenador forma un nuevo azeótropo (ternario) con uno o ambos componentes originales, que tiene un punto de ebullición más bajo. Por ejemplo, para separar el azeótropo etanol-agua, se puede añadir benceno o ciclohexano. Con ciclohexano como entrenador, se forma un azeótropo ternario de 7% agua, 17% etanol y 76% ciclohexano, que hierve a 62.1 °C. Al destilar, este azeótropo ternario se vaporiza, dejando un residuo de etanol casi puro.
Separación por Acción Química
Otro enfoque implica la adición de un agente que tiene una fuerte afinidad química por uno de los constituyentes del azeótropo, reaccionando con él para formar un compuesto no volátil. Por ejemplo, para el azeótropo agua-etanol, se puede agitar la mezcla con óxido de calcio, que reacciona con el agua para formar hidróxido de calcio no volátil. Tras la filtración del hidróxido de calcio, el etanol restante puede ser destilado hasta alcanzar una pureza del 100%. Otros agentes desecantes, como el cloruro de calcio anhidro, son útiles para secar una variedad de solventes.
Destilación con Sal Disuelta (Salt-effect Distillation)
Cuando una sal se disuelve en un solvente, su efecto es siempre aumentar el punto de ebullición de ese solvente, es decir, disminuir su volatilidad. Si la sal es fácilmente soluble en un componente de la mezcla azeotrópica pero no en el otro, se reduce la volatilidad del componente en el que es soluble, mientras que el otro componente no se ve afectado. Esto altera el equilibrio de fases y permite la separación. Por ejemplo, se puede romper el azeótropo agua-etanol disolviendo acetato de potasio en la mezcla y luego destilando.
Destilación Extractiva (Extractive Distillation)
Similar a la destilación azeotrópica, pero en este caso, el entrenador añadido es menos volátil que cualquiera de los componentes del azeótropo. El entrenador se añade en cantidades significativas y forma una fase líquida separada o modifica las volatilidades relativas de los componentes originales de tal manera que permite su separación. Por ejemplo, el azeótropo de 20% acetona y 80% cloroformo puede romperse añadiendo agua, que forma una capa separada en la que la acetona se disuelve preferentemente, permitiendo que el destilado sea más rico en cloroformo.
Pervaporación y Otros Métodos de Membrana
Estos métodos utilizan membranas selectivas que son más permeables a un componente que a otro. En la pervaporación, la mezcla líquida pasa a través de una membrana y se vaporiza selectivamente. En la permeación de vapor, los componentes pasan a través de la membrana completamente en la fase de vapor. En ambos casos, la membrana separa el fluido en un permeado (lo que pasa) y un retenido (lo que queda), enriqueciendo uno de los componentes en el permeado.
En resumen, los azeótropos representan un fascinante desafío en la química de las separaciones. Su comportamiento de punto de ebullición constante, derivado de desviaciones de la Ley de Raoult, exige soluciones innovadoras más allá de la simple destilación. Desde la manipulación de la presión hasta la introducción de agentes externos, los químicos e ingenieros han desarrollado una variedad de técnicas sofisticadas para dominar estas mezclas y lograr la pureza deseada de sus componentes, demostrando la constante búsqueda de la eficiencia y la precisión en los procesos químicos.
Preguntas Frecuentes
¿Por qué no se pueden separar los azeótropos por destilación simple?
Los azeótropos no pueden separarse por destilación simple porque en su punto de ebullición constante, la composición del vapor que se forma es idéntica a la composición de la mezcla líquida. Esto significa que al evaporarse y condensarse, la proporción de los componentes no cambia, impidiendo la separación.
¿Todos los azeótropos tienen un punto de ebullición más bajo que sus componentes?
No. Los azeótropos pueden ser de mínimo punto de ebullición (donde el punto de ebullición es inferior al de cualquiera de sus componentes puros, como el etanol-agua) o de máximo punto de ebullición (donde el punto de ebullición es superior al de cualquiera de sus componentes puros, como el ácido nítrico-agua).
¿Un azeótropo es un compuesto químico?
No. Aunque se comportan como sustancias puras durante la destilación, los azeótropos no son compuestos químicos. Su composición molar no sigue proporciones estequiométricas simples y, a diferencia de los compuestos químicos, su composición puede variar con la presión y la temperatura, lo que demuestra que son mezclas y no nuevas sustancias con enlaces químicos.
Si quieres conocer otros artículos parecidos a El Punto Azeotrópico: Un Desafío en la Química puedes visitar la categoría Química.