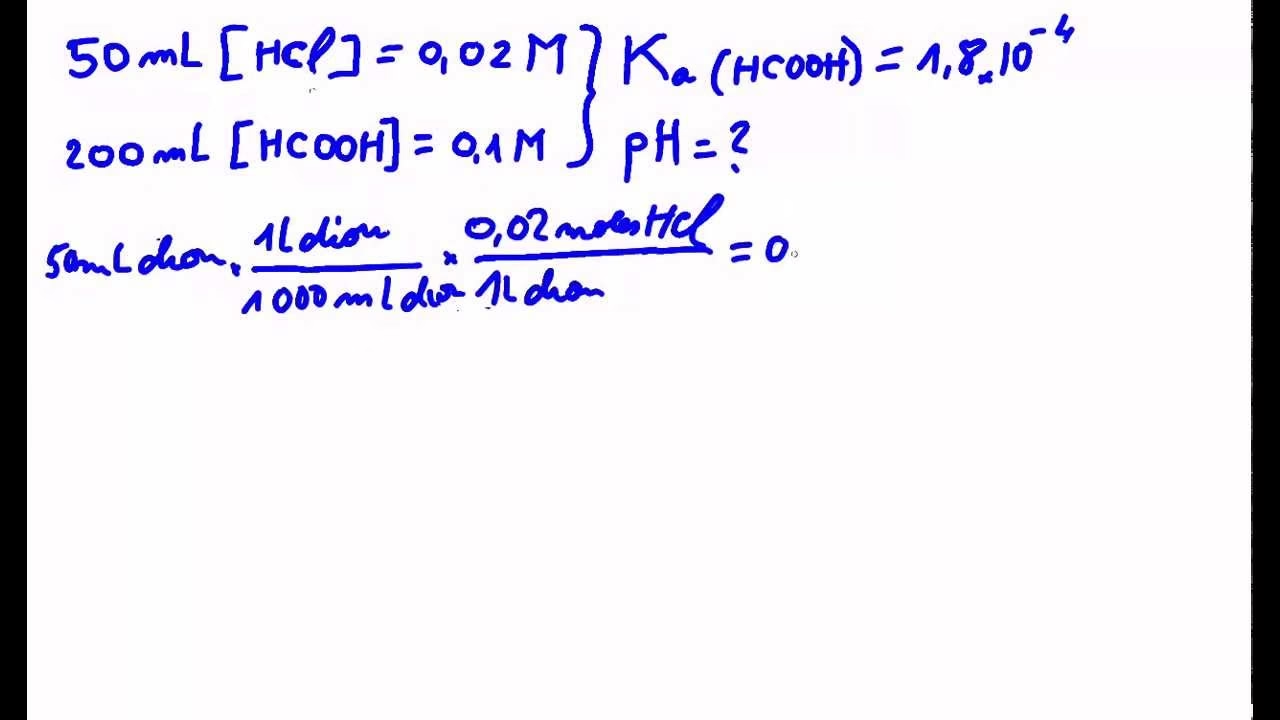07/06/2023
El pH es una medida fundamental en química que nos indica la acidez o alcalinidad de una solución. Mientras que determinar el pH de una solución con un solo ácido puede ser relativamente sencillo, la complejidad aumenta significativamente cuando nos enfrentamos a mezclas de ácidos. Comprender cómo los diferentes tipos de ácidos interactúan y contribuyen a la concentración total de iones hidronio (H₃O⁺) es crucial para realizar cálculos precisos. Este artículo explora los métodos para determinar el pH de diversas mezclas de ácidos, desde combinaciones de ácidos fuertes y débiles hasta mezclas de dos ácidos fuertes o dos ácidos débiles, desglosando los principios químicos subyacentes y ofreciendo ejemplos prácticos para una comprensión completa.

- Entendiendo la Disociación de los Ácidos
- Cálculo del pH en una Mezcla de un Ácido Fuerte y un Ácido Débil
- Cálculo del pH en una Mezcla de Dos Ácidos Fuertes
- Cálculo del pH en una Mezcla de Dos Ácidos Débiles
- ¿Qué Sucede al Mezclar Dos Ácidos?
- Tabla Comparativa de Métodos de Cálculo de pH en Mezclas de Ácidos
- Preguntas Frecuentes (FAQs)
- ¿Siempre se pueden ignorar las contribuciones de los ácidos débiles o la autoionización del agua en mezclas?
- ¿Cómo afecta la temperatura al pH de una mezcla de ácidos?
- ¿Es lo mismo mezclar ácidos que mezclar un ácido y una base?
- ¿Por qué es importante el concepto de constante de disociación ácida (Ka) para calcular el pH de mezclas?
- ¿Existen herramientas o software que ayuden a calcular el pH de mezclas complejas?
- Conclusión
Entendiendo la Disociación de los Ácidos
Antes de sumergirnos en las mezclas, es vital recordar qué hace que un ácido sea fuerte o débil. Un ácido fuerte se disocia completamente en agua, liberando todos sus iones de hidrógeno como iones hidronio (H₃O⁺). Ejemplos comunes incluyen el ácido clorhídrico (HCl), el ácido nítrico (HNO₃) y el ácido sulfúrico (H₂SO₄). Por otro lado, un ácido débil solo se disocia parcialmente en agua, estableciendo un equilibrio químico entre la forma molecular no disociada y sus iones. La extensión de esta disociación se mide por su constante de disociación ácida (Ka), un valor que nos indica qué tan fuerte es un ácido débil. Cuanto mayor sea el valor de Ka, más fuerte será el ácido débil.
La concentración de iones hidronio es el factor determinante del pH de una solución, ya que el pH se calcula como el logaritmo negativo de la concentración molar de iones hidronio (pH = -log[H₃O⁺]). En una mezcla de ácidos, la clave es determinar la concentración total de H₃O⁺ que proviene de todas las fuentes.
Cálculo del pH en una Mezcla de un Ácido Fuerte y un Ácido Débil
Cuando se mezclan un ácido fuerte y un ácido débil, el ácido fuerte domina la concentración de iones hidronio en la solución. Esto se debe a que el ácido fuerte se disocia por completo, liberando una gran cantidad de H₃O⁺, mientras que el ácido débil solo se disocia parcialmente. Además, la alta concentración de iones hidronio producida por el ácido fuerte suprime aún más la disociación del ácido débil.
Este fenómeno se explica por el principio de Le Chatelier, que establece que cuando un sistema en equilibrio es perturbado, el sistema se ajusta para minimizar esa perturbación. En este caso, el exceso de H₃O⁺ proveniente del ácido fuerte empuja el equilibrio de disociación del ácido débil hacia la izquierda (hacia la forma no disociada), reduciendo aún más la ya limitada producción de iones hidronio por parte del ácido débil. Como resultado, la contribución del ácido débil a la concentración total de H₃O⁺ se vuelve insignificante y puede ignorarse en la mayoría de los casos prácticos.

Ejemplo Práctico:
Consideremos una mezcla de ácido clorhídrico (HCl), un ácido fuerte, y ácido fórmico (HCHO₂), un ácido débil. Si la concentración inicial de HCl en la mezcla es 0.0020 M, podemos calcular el pH de la solución de la siguiente manera:
Dado que el HCl es un ácido fuerte, se disocia completamente:
HCl(ac) → H⁺(ac) + Cl⁻(ac)Por lo tanto, la concentración de iones H⁺ (o H₃O⁺) producida por el HCl es igual a su concentración inicial:
[H⁺] = 0.0020 MEl pH se calcula como:
pH = -log[H⁺] pH = -log(0.0020) pH ≈ 2.70En este ejemplo, la contribución de los iones hidronio producida por el ácido fórmico y la autoionización del agua es tan pequeña en comparación con la del HCl que se puede despreciar con seguridad. El cálculo de pH se simplifica enormemente al considerar solo la concentración del ácido fuerte.
Cálculo del pH en una Mezcla de Dos Ácidos Fuertes
Cuando se mezclan dos ácidos fuertes, ambos se disocian completamente en la solución, aportando iones hidronio. El enfoque aquí es determinar la concentración total de H₃O⁺ sumando las contribuciones de ambos ácidos. Es crucial considerar los volúmenes y las diluciones que ocurren al mezclar las soluciones.
Pasos para el Cálculo:
- Calcular los moles de H₃O⁺ de cada ácido fuerte: Para cada ácido, multiplique su concentración molar inicial por su volumen.
- Sumar los moles totales de H₃O⁺: Sume los moles de H₃O⁺ obtenidos de cada ácido.
- Determinar el volumen total de la solución: Sume los volúmenes de las soluciones ácidas mezcladas.
- Calcular la concentración molar total de H₃O⁺: Divida los moles totales de H₃O⁺ por el volumen total de la solución.
- Calcular el pH: Aplique la fórmula pH = -log[H₃O⁺].
Ejemplo Ilustrativo:
Supongamos que mezclamos 50 mL de una solución de HCl 0.1 M con 50 mL de una solución de HNO₃ 0.05 M.
- Moles de H₃O⁺ del HCl:
Moles HCl = 0.1 M * 0.050 L = 0.005 moles H₃O⁺ - Moles de H₃O⁺ del HNO₃:
Moles HNO₃ = 0.05 M * 0.050 L = 0.0025 moles H₃O⁺ - Moles totales de H₃O⁺:
Moles totales = 0.005 + 0.0025 = 0.0075 moles H₃O⁺ - Volumen total de la solución:
Volumen total = 50 mL + 50 mL = 100 mL = 0.100 L - Concentración total de H₃O⁺:
[H₃O⁺] = 0.0075 moles / 0.100 L = 0.075 M - Calcular el pH:
pH = -log(0.075)
pH ≈ 1.12
Cálculo del pH en una Mezcla de Dos Ácidos Débiles
El cálculo del pH para una mezcla de dos ácidos débiles es el más complejo de los tres escenarios, ya que ambos ácidos se disocian parcialmente y sus equilibrios pueden influirse mutuamente. La aproximación más común y práctica depende de las constantes de disociación (Ka) relativas de los dos ácidos.
Casos Posibles:
- Si un ácido débil es significativamente más fuerte que el otro (es decir, su Ka es al menos 1000 veces mayor): En este caso, el ácido débil más fuerte será la fuente principal de iones hidronio. Su disociación suprimirá la disociación del ácido débil más débil de manera similar a como lo haría un ácido fuerte. Por lo tanto, el pH puede calcularse principalmente basándose en el ácido débil más fuerte, utilizando su expresión de Ka y resolviendo para [H₃O⁺] (a menudo mediante una ecuación cuadrática o aproximaciones si la disociación es muy pequeña).
- Si ambos ácidos débiles tienen constantes de disociación (Ka) comparables: Aquí, ambos ácidos contribuyen significativamente a la concentración total de H₃O⁺, y sus equilibrios están interconectados. El cálculo exacto requiere resolver un sistema de ecuaciones de equilibrio simultáneas, lo que puede ser bastante laborioso y a menudo implica el uso de métodos numéricos o software especializado. En la práctica, para fines educativos, a menudo se asume que la contribución del ácido más débil es despreciable si la diferencia de Ka es considerable, o se resuelven problemas simplificados.
Consideraciones Clave:
- La autoionización del agua (H₂O ⇌ H⁺ + OH⁻) generalmente se ignora a menos que las concentraciones de los ácidos sean extremadamente bajas (por debajo de 10⁻⁷ M).
- Los cálculos exactos para dos ácidos débiles con Ka similares pueden requerir la consideración de todas las especies en equilibrio y la resolución de ecuaciones cúbicas o de mayor grado.
¿Qué Sucede al Mezclar Dos Ácidos?
Una pregunta común es si ocurre una reacción química cuando se mezclan dos ácidos. En general, si hablamos de una reacción de neutralización donde un ácido reacciona con una base para formar sal y agua, la respuesta es no. Los ácidos, por definición, son donadores de protones (H⁺). Cuando se mezclan dos donadores de protones, no hay una base significativa con la que reaccionar para formar una sal en el sentido tradicional de una reacción ácido-base entre ellos.

Sin embargo, es importante aclarar que, aunque no ocurre una reacción de neutralización entre ellos, sí hay una interacción a nivel de sus equilibrios de disociación. Como se explicó con el principio de Le Chatelier, la presencia de un ácido más fuerte (ya sea fuerte o un ácido débil con un Ka mucho mayor) puede suprimir la disociación de un ácido más débil. Esta interacción afecta la concentración final de iones hidronio y, por lo tanto, el pH de la mezcla.
La idea de que un "ácido débil puede actuar como una base" cuando se mezcla con un ácido fuerte se refiere más a su capacidad de aceptar protones de un ácido mucho más fuerte en un contexto de equilibrio, que a una reacción de neutralización clásica. La reacción principal sigue siendo la disociación de los ácidos en agua, y cómo estas disociaciones se influyen mutuamente para determinar la concentración final de H₃O⁺.
Tabla Comparativa de Métodos de Cálculo de pH en Mezclas de Ácidos
| Tipo de Mezcla de Ácidos | Método de Cálculo Principal | Consideraciones Clave |
|---|---|---|
| Ácido Fuerte + Ácido Débil | El pH se determina casi exclusivamente por la concentración del ácido fuerte. | El ácido fuerte suprime la disociación del ácido débil (Principio de Le Chatelier). La contribución del ácido débil es insignificante. |
| Dos Ácidos Fuertes | Sumar los moles de H₃O⁺ de ambos ácidos y dividir por el volumen total de la mezcla. | Ambos ácidos se disocian completamente. Es crucial considerar los volúmenes para calcular la concentración final. |
| Dos Ácidos Débiles | Depende de las Ka relativas: - Si una Ka es mucho mayor: Calcular pH basado en el ácido débil más fuerte. - Si las Ka son comparables: Requiere resolver un sistema de ecuaciones de equilibrio simultáneas (más complejo). | Ambos ácidos se disocian parcialmente. Los equilibrios se influyen mutuamente. La autoionización del agua suele ser insignificante. |
Preguntas Frecuentes (FAQs)
¿Siempre se pueden ignorar las contribuciones de los ácidos débiles o la autoionización del agua en mezclas?
No siempre. La autoionización del agua solo se ignora cuando la concentración de H₃O⁺ de los ácidos es significativamente mayor que 10⁻⁷ M. La contribución de un ácido débil solo se ignora si hay un ácido mucho más fuerte presente (ya sea fuerte o un ácido débil con una Ka mucho mayor) que domine la concentración de H₃O⁺. En el caso de dos ácidos débiles con Ka comparables, la contribución de ambos debe ser considerada.
¿Cómo afecta la temperatura al pH de una mezcla de ácidos?
La temperatura afecta tanto la constante de disociación ácida (Ka) de los ácidos débiles como la constante de autoionización del agua (Kw). Un aumento en la temperatura generalmente aumenta la disociación de los ácidos débiles y la autoionización del agua, lo que puede llevar a un cambio en el pH. Los cálculos de pH que hemos discutido se asumen a una temperatura constante, típicamente 25°C, a menos que se especifique lo contrario.

¿Es lo mismo mezclar ácidos que mezclar un ácido y una base?
No, son procesos fundamentalmente diferentes. Al mezclar un ácido y una base, ocurre una reacción de neutralización vigorosa que forma una sal y agua, y el pH final dependerá de la estequiometría de la reacción y de las fuerzas relativas del ácido y la base. Al mezclar dos ácidos, como se explicó, no hay una reacción de neutralización entre ellos; más bien, sus disociaciones interactúan en la solución acuosa para determinar la concentración final de iones hidronio.
¿Por qué es importante el concepto de constante de disociación ácida (Ka) para calcular el pH de mezclas?
La Ka es crucial para los ácidos débiles porque cuantifica su fuerza y el grado de su disociación en solución. Para mezclas que involucran ácidos débiles, la Ka nos permite determinar la concentración de iones hidronio que el ácido débil contribuye al sistema, especialmente cuando su disociación no es despreciable. Es la base para establecer el equilibrio y calcular el pH en estos casos complejos.
¿Existen herramientas o software que ayuden a calcular el pH de mezclas complejas?
Sí, para mezclas muy complejas, especialmente aquellas con múltiples equilibrios interconectados (como varios ácidos débiles o la presencia de sales que actúan como ácidos o bases conjugadas), los químicos suelen utilizar software de modelado de equilibrio químico. Estas herramientas pueden resolver sistemas complejos de ecuaciones para predecir con precisión las concentraciones de todas las especies y el pH final de la solución.
Conclusión
El cálculo del pH en mezclas de ácidos es una habilidad esencial en química, que requiere una comprensión clara de la fuerza de los ácidos y cómo sus disociaciones interactúan en solución. Ya sea que se trate de la dominancia de un ácido fuerte, la suma directa de contribuciones de dos ácidos fuertes, o la intrincada resolución de equilibrios para ácidos débiles, el objetivo final es determinar la concentración total de iones hidronio. Dominar estos métodos no solo mejora la precisión de los cálculos, sino que también profundiza la comprensión de los principios fundamentales del equilibrio químico y las propiedades ácido-base en soluciones acuosas.
Si quieres conocer otros artículos parecidos a Calculando el pH en Mezclas de Ácidos puedes visitar la categoría Química.