08/03/2025
En el vasto universo de la química, comprender la masa de los átomos es fundamental. Sin embargo, no todos los átomos de un mismo elemento son idénticos. Aquí es donde entran en juego conceptos cruciales como el peso atómico promedio y la masa molar. Estas no son solo cifras abstractas en una tabla periódica, sino herramientas esenciales que permiten a científicos y estudiantes realizar cálculos precisos, predecir reacciones y comprender la composición de la materia que nos rodea. Desde la balanza de un laboratorio hasta la formulación de nuevos compuestos, el conocimiento de estas magnitudes es la clave para desentrañar los misterios del mundo atómico y molecular.

¿Qué es la Masa Atómica?
Para entender el peso atómico promedio, primero debemos comprender la masa atómica de un solo átomo. En el corazón de cada átomo residen los protones y los neutrones, partículas subatómicas que son los principales contribuyentes a su masa. Cada protón y cada neutrón tienen una masa aproximadamente igual, que se define arbitrariamente como una unidad de masa atómica (uma) o un Dalton. Esta cantidad es extremadamente pequeña, alrededor de 1.67 × 10-24 gramos. Por otro lado, los electrones, aunque son componentes esenciales del átomo, son considerablemente más ligeros, pesando solo alrededor de 9.11 × 10-28 gramos, o aproximadamente 1/1800 de una unidad de masa atómica. Debido a su masa insignificante en comparación con los protones y neutrones, la contribución de los electrones a la masa atómica total de un elemento es habitualmente ignorada. Por lo tanto, al considerar la masa atómica de un átomo individual, se calcula principalmente sumando el número de protones y neutrones presentes en su núcleo.
El Rol Crucial de los Isótopos y el Cálculo del Peso Atómico Promedio
Si bien la masa atómica de un solo átomo puede ser sencilla de definir, la realidad es que la mayoría de los elementos que se encuentran en la naturaleza no existen en una única forma. En cambio, están compuestos por una mezcla de isótopos. Los isótopos son átomos del mismo elemento que tienen el mismo número de protones, pero difieren en el número de neutrones. Esta diferencia en el número de neutrones resulta en una variación en su masa atómica. Por ejemplo, el carbono tiene isótopos como el carbono-12 y el carbono-14, cada uno con una masa ligeramente diferente.
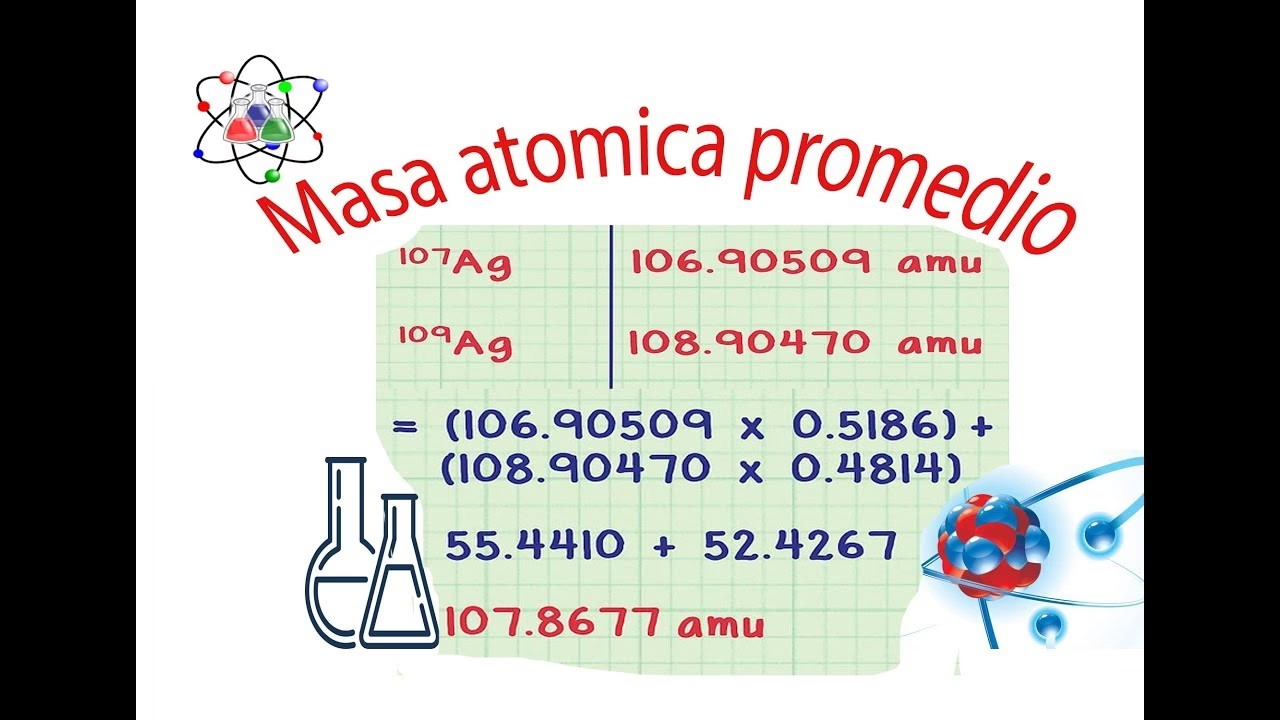
Dado que los isótopos de un elemento no son igualmente abundantes en la naturaleza, no podemos simplemente promediar sus masas. En su lugar, es fundamental considerar tanto la masa de cada isótopo como su abundancia natural relativa. El peso atómico promedio (también conocido como masa atómica relativa o peso atómico estándar) se calcula como una media ponderada de las masas de todos los isótopos de un elemento, donde el "peso" de cada isótopo en el promedio es su abundancia porcentual en la naturaleza. La fórmula para calcular el peso atómico promedio es la siguiente:
Peso Atómico Promedio = Σ (masa del isótopoi × abundancia fraccional del isótopoi)
Donde la suma (Σ) se realiza sobre todos los isótopos presentes de un elemento. La abundancia fraccional es la abundancia porcentual dividida por 100. Por ejemplo, si un elemento tiene dos isótopos, el isótopo A con una masa MA y una abundancia del X%, y el isótopo B con una masa MB y una abundancia del Y% (donde X + Y = 100), el peso atómico promedio sería:
Peso Atómico Promedio = (MA × X/100) + (MB × Y/100)
Este cálculo asegura que el valor del peso atómico promedio que encontramos en la tabla periódica refleje con precisión la composición isotópica natural del elemento, lo cual es vital para los cálculos estequiométricos y muchas otras aplicaciones químicas.

¿Qué es la Masa Molar y Por Qué es Importante?
Mientras que el peso atómico promedio se refiere a la masa de un solo átomo (promediada por sus isótopos), la masa molar introduce el concepto del "mol", una unidad fundamental en química que nos permite trabajar con cantidades macroscópicas de sustancias. Los químicos a menudo utilizan la unidad "mol" para determinar el número de átomos o moléculas de un compuesto que participan en una reacción química. Un mol de un elemento es numéricamente igual a su peso atómico en gramos. De manera similar, un mol de un compuesto es la suma de los pesos atómicos de sus componentes, lo que se conoce como peso molecular o masa molecular.
La masa molar se define como la relación entre la masa y la cantidad de sustancia (medida en moles) de cualquier muestra de un compuesto. Esto significa que, ya sea que intente determinar cuánto carbono, titanio o cobalto necesita para un experimento, comprender la masa molar es esencial. Permite a los científicos pasar de la escala atómica (uma) a la escala de laboratorio (gramos), haciendo posible medir cantidades precisas de sustancias.
Consideremos el ejemplo de la glucosa, con la fórmula química C6H12O6. Para calcular su masa molecular (y, por lo tanto, su masa molar), sumamos las masas atómicas de sus componentes:
- El peso atómico del carbono (C) es 12.011 gramos/mol. Como hay seis átomos de carbono en la glucosa, la contribución total del carbono es 12.011 g/mol × 6 = 72.066 gramos/mol.
- Para el hidrógeno (H), con un peso atómico de aproximadamente 1.008 gramos/mol y 12 átomos, la contribución es 1.008 g/mol × 12 = 12.096 gramos/mol.
- Para el oxígeno (O), con un peso atómico de aproximadamente 15.999 gramos/mol y 6 átomos, la contribución es 15.999 g/mol × 6 = 95.994 gramos/mol.
Sumando estas contribuciones, la masa molecular de la glucosa es 72.066 + 12.096 + 95.994 = 180.156 gramos/mol. Esto significa que un mol de glucosa pesa 180.156 gramos. Esta capacidad de convertir entre moles y gramos es una piedra angular de la estequiometría, permitiendo a los químicos predecir y controlar las cantidades de reactivos y productos en las reacciones.
El Caso Específico del Hidrógeno: Masa Molar y Características
El hidrógeno es el elemento más abundante en el universo y el más ligero, lo que lo convierte en un excelente ejemplo para ilustrar los conceptos de masa atómica y molar. La masa molar del hidrógeno molecular (H2) es de 2.01568 g/mol. Se calcula multiplicando el peso atómico del hidrógeno (aproximadamente 1.00784 unidades de masa atómica) por dos, ya que el gas hidrógeno se forma a partir de dos átomos de hidrógeno (H) unidos. Así, 1.00784 × 2 = 2.01568 gramos/mol.
Características del Hidrógeno:
- Ligereza: Como el hidrógeno consta de un solo protón en su núcleo (y generalmente ningún neutrón en su isótopo más común, el protio), su número atómico es 1. Cuantos más protones tiene un átomo en su núcleo, mayor es su número atómico y más pesado se vuelve el elemento. Esto significa que, en general, el hidrógeno es un elemento extremadamente "ligero".
- Reactividad: El hidrógeno es muy reactivo. Debido a esta reactividad, los átomos de hidrógeno atómico (H) se combinan entre sí para formar moléculas de dos átomos (H2). Así es como se forman las moléculas de hidrógeno.
- Estabilidad del H2: Aunque el hidrógeno atómico es reactivo, la molécula de hidrógeno (H2) puede reaccionar con muchos elementos y compuestos, pero a temperatura ambiente, la reacción ocurre a un ritmo tan lento que es casi insignificante. Debido a esta aparente inercia, la molécula de H2 puede considerarse una molécula muy estable a temperatura ambiente.
Usos de la Masa Molar del Hidrógeno en la Educación
Conocer la masa molar del hidrógeno abre un mundo de oportunidades en términos de educación sobre este elemento. Los estudiantes pueden comprender, por ejemplo, el proceso de generación de hidrógeno (electrólisis) con mayor profundidad. Un ejemplo clásico es la electrólisis del agua (H2O) para producir hidrógeno y oxígeno. La ecuación balanceada es 2H2O → 2H2 + O2.
A menudo surge la pregunta: ¿Por qué un generador de hidrógeno (electrolizador) produce aproximadamente 8 veces más oxígeno que hidrógeno en masa? La respuesta radica en las masas molares. La masa molar de 2 moléculas de agua (2 H2O) es 2 × (2 × 1.008 + 15.999) = 2 × 18.015 = 36.03 gramos/mol. Una vez que el generador de hidrógeno divide el agua en hidrógeno y oxígeno, el hidrógeno (H2), al tener una masa molar baja, solo tiene una masa de 2.016 g/mol, mientras que el oxígeno (O2) tiene una masa molar de 31.998 g/mol (aproximadamente 16 × 2). Al observar la relación estequiométrica de 2H2 y 1O2, se producen 2 moles de H2 (2 × 2.016 = 4.032 g) y 1 mol de O2 (31.998 g). La relación en masa es 31.998 / 4.032 ≈ 7.93. Es decir, por cada unidad de masa de hidrógeno producida, se crean casi 8 unidades de masa de oxígeno. Este tipo de análisis, basado en la masa molar, es fundamental para comprender las proporciones de las reacciones químicas.
Tabla Comparativa de Masas Molares
Para contextualizar la masa molar del hidrógeno, aquí presentamos una tabla comparativa con las masas molares de otros elementos comunes:
| Elemento | Fórmula Química | Masa Molar (g/mol) |
|---|---|---|
| Hidrógeno | H | 1.00784 |
| Sodio | Na | 22.98977 |
| Nitrógeno | N | 14.007 |
| Cloro | Cl | 35.45 |
| Carbono | C | 12.011 |
| Oxígeno | O | 15.9994 |
| Yodo | I | 126.9045 |
| Zinc | Zn | 65.4 |
Es importante notar que la masa molar del hidrógeno en esta tabla se refiere a un solo átomo de hidrógeno (H), mientras que en el ejemplo de la molécula de gas hidrógeno (H2) se duplicó el valor para reflejar la naturaleza diatómica de la molécula.
Preguntas Frecuentes sobre Masa Atómica y Molar
- ¿Cuál es la diferencia entre masa atómica y peso atómico promedio?
- La masa atómica se refiere a la masa de un átomo individual, generalmente expresada en unidades de masa atómica (uma). El peso atómico promedio, por otro lado, es una media ponderada de las masas de todos los isótopos naturales de un elemento, considerando sus abundancias relativas. Es el valor que normalmente se encuentra en la tabla periódica.
- ¿Por qué se ignoran los electrones al calcular la masa atómica?
- Los electrones tienen una masa significativamente menor que los protones y los neutrones (aproximadamente 1/1800 de una uma). Su contribución a la masa total del átomo es tan pequeña que, para la mayoría de los cálculos químicos, se considera despreciable y se ignora para simplificar.
- ¿Cómo se relaciona el mol con el peso atómico?
- Un mol de un elemento es la cantidad de sustancia que contiene un número de Avogadro (aproximadamente 6.022 x 1023) de átomos. Numéricamente, la masa en gramos de un mol de un elemento es igual a su peso atómico promedio expresado en unidades de masa atómica. Por ejemplo, si el peso atómico promedio del carbono es 12.011 uma, un mol de carbono pesa 12.011 gramos.
- ¿Puede un elemento tener diferentes masas atómicas?
- Sí, un elemento puede tener diferentes masas atómicas debido a la existencia de isótopos. Cada isótopo de un elemento tiene una masa atómica ligeramente diferente debido a su distinto número de neutrones. El peso atómico que vemos en la tabla periódica es el promedio ponderado de estas masas isotópicas.
- ¿La masa molar del hidrógeno es 1.00784 g/mol o 2.01568 g/mol?
- Ambos valores son correctos, pero se refieren a entidades diferentes. 1.00784 g/mol es la masa molar de un átomo individual de hidrógeno (H), que es su peso atómico. 2.01568 g/mol es la masa molar de una molécula de hidrógeno diatómico (H2), que es la forma en que el hidrógeno existe comúnmente como gas a temperatura ambiente. Es crucial especificar si se habla de H o H2.
Si quieres conocer otros artículos parecidos a Desvelando el Peso Atómico Promedio: Guía Completa puedes visitar la categoría Química.

