14/02/2022
Desde el café que nos despierta por la mañana hasta los materiales que componen nuestra tecnología más avanzada, las mezclas están en todas partes. Comprender su composición es fundamental para predecir su comportamiento y propiedades. Sin embargo, no todas las mezclas se abordan de la misma manera. Mientras que para una bebida o una solución química simple nos interesa la proporción de sus componentes, en la ciencia de los materiales, especialmente en aleaciones complejas, necesitamos adentrarnos en parámetros termodinámicos como la entalpía de mezcla. Este artículo explorará ambos mundos: la práctica y accesible medición de la concentración en porcentaje, y la compleja pero crucial evaluación de la entalpía de mezcla para el diseño de materiales.
Fundamentos de la Concentración de Mezclas: El Lenguaje del Porcentaje
La concentración de una disolución es una medida de la cantidad de soluto disuelto en una cantidad determinada de disolvente o de disolución total. Es una forma esencial de cuantificar la composición de una mezcla homogénea, permitiéndonos comprender y predecir sus propiedades. La química cotidiana, la industria alimentaria, la farmacéutica y muchas otras disciplinas dependen directamente de la precisión en la determinación y control de estas concentraciones.
¿Qué es el Soluto y el Disolvente?
En una disolución, el soluto es la sustancia que se disuelve, y generalmente se encuentra en menor proporción. El disolvente, por otro lado, es la sustancia que disuelve al soluto y suele estar en mayor proporción. Por ejemplo, al preparar una bebida de jamaica, el concentrado de jamaica y el azúcar actúan como solutos, mientras que el agua es el disolvente. La cantidad de estos componentes afecta directamente la intensidad del sabor y el color de nuestra bebida.
Concentración por Porcentaje en Masa (% m/m)
Una de las formas más comunes de expresar la concentración es el porcentaje en masa, que indica la masa de soluto presente en 100 unidades de masa de la disolución. Su fórmula es sencilla y directa:
Porcentaje en masa = (Masa del soluto / Masa de la disolución) × 100%
La masa de la disolución es la suma de la masa del soluto y la masa del disolvente.
Ejemplo Práctico: Sal en Agua
Imaginemos que deseamos calcular el porcentaje de sal en una disolución preparada con 5 gramos de cloruro de sodio (sal de mesa) y 95 gramos de agua. Primero, sumamos las masas para obtener la masa total de la disolución: 5 g (soluto) + 95 g (disolvente) = 100 g (disolución).
Aplicando la fórmula:
Porcentaje en masa = (5 g de NaCl / 100 g de disolución) × 100% = 5%
Esto significa que la disolución contiene un 5% de cloruro de sodio en masa. Este tipo de cálculos es fundamental en la cocina, en laboratorios y en la industria para asegurar la calidad y consistencia de los productos.
Otro Ejemplo: Tu Café Matutino
Si preparas tu café con 15 gramos de café (soluto) y 175 gramos de agua caliente (disolvente), la masa total de la disolución es 15 g + 175 g = 190 g. El porcentaje de café en tu taza sería:
Porcentaje en masa = (15 g de café / 190 g de disolución) × 100% ≈ 7.89%
Este pequeño cálculo nos muestra que aproximadamente el 7.89% de tu café es realmente café, y el resto es agua.
Concentración por Porcentaje en Volumen (% v/v)
Cuando tanto el soluto como el disolvente son líquidos, es más práctico expresar la concentración como porcentaje en volumen. Este método es común en la preparación de soluciones alcohólicas o mezclas de líquidos miscibles.
Porcentaje en volumen = (Volumen del soluto / Volumen de la disolución) × 100%
Al igual que con la masa, el volumen de la disolución es la suma de los volúmenes del soluto y el disolvente.
Ejemplo Práctico: Alcohol y Agua
Si se prepara una mezcla con 70 ml de alcohol y 30 ml de agua, el volumen total de la disolución es 70 ml + 30 ml = 100 ml.
Aplicando la fórmula:
Porcentaje en volumen = (70 ml de alcohol / 100 ml de disolución) × 100% = 70%
Esta mezcla es una disolución de alcohol al 70%, comúnmente utilizada como desinfectante.
Tipos de Disoluciones según su Concentración
Además de cuantificar la concentración, podemos clasificar las disoluciones según la cantidad de soluto que pueden disolver:
- Disoluciones Insaturadas: Contienen una cantidad de soluto menor a la máxima que el disolvente puede admitir a una temperatura y presión dadas. Aún pueden disolver más soluto.
- Disoluciones Saturadas: Contienen la cantidad máxima de soluto que el disolvente puede disolver a una temperatura y presión dadas. El soluto disuelto está en equilibrio con el soluto sin disolver.
- Disoluciones Sobresaturadas: Contienen una cantidad de soluto mayor a la que el disolvente puede disolver en condiciones normales. Son inestables y el exceso de soluto puede precipitarse si se altera la disolución.
Impacto de la Concentración en las Propiedades de las Mezclas
La concentración no es solo un número; tiene un impacto directo y observable en las propiedades físicas y químicas de una mezcla. Uno de los ejemplos más claros es la densidad.
La Densidad y la Flotabilidad
Consideremos el experimento del huevo en agua salada. Un huevo se hunde en agua pura porque su densidad es mayor que la del agua. Sin embargo, al añadir sal al agua, la densidad de la disolución aumenta. Cuanta más sal se disuelve, mayor es la densidad. Llegará un punto en que la densidad de la disolución supera la del huevo, haciendo que este flote. Este principio explica por qué es más fácil flotar en el mar Muerto, con su elevadísima concentración de sales, que en una piscina con agua dulce.
Cambios de Color y Propiedades en Aleaciones
Las aleaciones, que son mezclas sólidas de metales, también exhiben cambios de propiedades y apariencia según la concentración de sus componentes. El latón, por ejemplo, una aleación de cobre y zinc, puede variar drásticamente de color. Si contiene entre 91% y 94% de cobre, se ve rojizo. Pero si se mezcla 60% de cobre con 40% de zinc, adquiere un color amarillo característico. Incluso pequeñas adiciones de otros metales, como el oro, pueden modificar su apariencia, creando el apreciado color dorado.
Concentración y Salud Pública
La concentración de sustancias en el aire que respiramos o en los alimentos que consumimos tiene implicaciones directas en nuestra salud. El aire, una mezcla de gases, tiene una composición ideal de aproximadamente 78% nitrógeno, 20.9% oxígeno, 0.9% argón, entre otros. Alteraciones en estas proporciones, como el aumento de monóxido de carbono debido a la combustión incompleta, pueden tener efectos severos, desde dolores de cabeza hasta la muerte, al reducir la disponibilidad de oxígeno en nuestro cuerpo. De manera similar, la concentración de alcohol en la sangre afecta directamente las funciones cerebrales y motoras, con consecuencias graves a partir de ciertos umbrales.
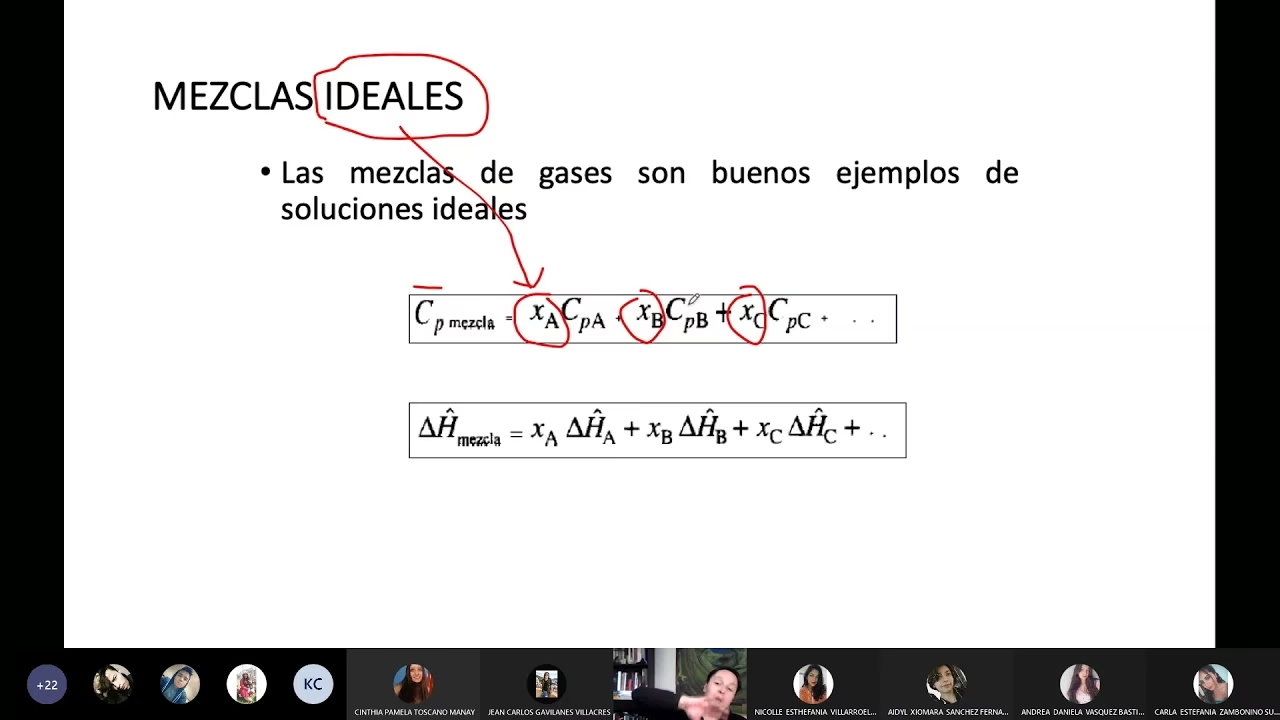
La Entalpía de Mezcla: Un Parámetro Termodinámico en Materiales Avanzados
Mientras que el porcentaje de concentración es fundamental para mezclas cotidianas, el estudio de materiales avanzados, como las aleaciones de alta entropía (HEAs) y los vidrios metálicos a granel (BMGs), requiere un enfoque termodinámico más profundo. Aquí, la entalpía de mezcla (ΔHmix) emerge como un parámetro crítico para predecir la formación de fases y, por ende, las propiedades del material.
La entalpía de mezcla representa el cambio de energía térmica que ocurre cuando dos o más sustancias se mezclan para formar una solución. Un valor negativo de ΔHmix indica que la mezcla es un proceso exotérmico (libera calor), lo que generalmente favorece la estabilidad de la solución. Un valor positivo indica un proceso endotérmico (requiere calor), lo que puede llevar a la separación de fases.
Es importante destacar que la entalpía de mezcla no se calcula con una fórmula universal simple aplicable a cualquier sistema, como en el caso del porcentaje de concentración. En cambio, su valor se deriva de modelos termodinámicos complejos (como el método CALPHAD, CALculation of PHAse Diagrams) o de datos experimentales específicos para cada par de elementos o sistema multicomponente. Lo que la investigación nos proporciona son los rangos de valores de ΔHmix (junto con otros parámetros) que son favorables para la formación de ciertas fases.
Parámetros Termodinámicos y Topológicos Clave
Para predecir la formación de soluciones sólidas o vidrios metálicos en aleaciones multicomponentes, los científicos utilizan una combinación de parámetros. Además de la entalpía de mezcla (ΔHmix), se consideran:
- Entropía de Mezcla (ΔSmix): Mide el grado de desorden o aleatoriedad introducido al mezclar los elementos. Una alta entropía de mezcla a menudo favorece la formación de soluciones sólidas.
- Diferencia de Tamaño Atómico (δ): Un parámetro topológico que cuantifica la disparidad en los tamaños atómicos de los elementos constituyentes. Una δ pequeña favorece soluciones sólidas, mientras que una grande puede inducir distorsión de la red y favorecer fases amorfas o intermetálicas. Se define como:
δ = 100 * ∑ (ci * (1 - ri / r̄)²)
donde ci es la composición, ri es el radio atómico del elemento i, y r̄ es el radio atómico promedio.
- Entropía de Desajuste (ΔSσ): También relacionada con la diferencia de tamaño atómico, pero con un enfoque más termodinámico sobre la deformación elástica de la red.
- Parámetro Ω (Omega): Un parámetro termodinámico que combina la temperatura de fusión hipotética (Tm), la entropía de mezcla y la entalpía de mezcla. Se define como:
Ω = | Tm * ΔSmix / ΔHmix |
donde Tm = ∑ (Xi * (Tm)i) es la temperatura de fusión hipotética de la mezcla, calculada como la suma ponderada de las temperaturas de fusión de los elementos puros (Xi es la fracción molar y (Tm)i es la temperatura de fusión del elemento i).
Criterios para la Formación de Fases
Diferentes estudios han propuesto criterios basados en estos parámetros para predecir la formación de soluciones sólidas, compuestos intermetálicos o fases amorfas en HEAs. Aunque existen algunas inconsistencias entre los criterios de distintos grupos de investigación, todos proporcionan valiosas directrices para el diseño de materiales.
| Criterio | ΔHmix (kJ/mol) | ΔSmix (J/K mol) | δ (%) | Ω | Fase Predicha |
|---|---|---|---|---|---|
| Zhang et al. (2008b) | -20 a 5 | 12 a 17.5 | ≤ 6.4 | N/A | Solución Sólida Simple |
| Zhang et al. (2008b) (Desordenadas) | ≥ -15 | N/A | ≤ 4.6 | N/A | Fases Desordenadas |
| Zhang et al. (2012c) | N/A | N/A | ≤ 6.6 | ≥ 1.1 | Solución Sólida Simple |
| Guo & Liu (2011) | -22 a 7 | 11 a 19.5 | 0 a 8.5 | N/A | Solución Sólida |
| Guo & Liu (2011) | -49 a -5.5 | 7 a 16 | ≥ 9 | N/A | Vidrio Metálico a Granel (BMG) |
| Guo et al. (2013a) | -11.6 a 3.2 | N/A | ≤ 6.6 | N/A | Solución Sólida |
| Guo et al. (2013a) | < -12.2 | N/A | > 6.4 | N/A | Fase Amorfa |
| Ren et al. (2013) | ≥ -8.8 | N/A | ≤ 2.77 | N/A | Solución Sólida |
Estos criterios, aunque a veces contradictorios en sus límites exactos, ilustran cómo la entalpía de mezcla, junto con la entropía de mezcla y la diferencia de tamaño atómico, guía a los científicos en la creación de materiales con propiedades específicas. Por ejemplo, se ha observado que las fases cúbicas centradas en el cuerpo (BCC) se favorecen cuando la diferencia de tamaño atómico es mayor (mayor ΔSσ/k) y la ΔHmix es más negativa, lo que sugiere que estas estructuras abiertas pueden acomodar mayor deformación y no idealidad. Por otro lado, las fases cúbicas centradas en las caras (FCC) se estabilizan con una ΔSσ/k muy pequeña y una ΔHmix cercana a cero, indicando una solución más ideal.
La Importancia de la Minimización de la Energía Libre
Aunque los parámetros individuales como ΔHmix y ΔSmix son cruciales, algunos estudios, como el de Otto et al. (2013b), sugieren que la formación de fases en aleaciones multicomponentes se rige por la minimización de la energía libre de Gibbs, que considera el equilibrio entre la entalpía y la entropía. Esto significa que maximizar solo la entropía configuracional no garantiza la formación de soluciones sólidas de una sola fase; las interacciones atractivas o repulsivas entre los elementos (reflejadas en ΔHmix) también son vitales y pueden conducir a la formación de intermetálicos o a la separación de fases. La diferencia de tamaño atómico también juega un papel determinante, especialmente en la distinción entre soluciones sólidas cristalinas y fases amorfas.
Preguntas Frecuentes
Aquí respondemos algunas de las preguntas más comunes sobre la concentración y la entalpía de mezcla.
¿Qué es la concentración de una mezcla?
La concentración de una mezcla es una medida que expresa la cantidad de soluto (la sustancia que se disuelve) presente en una cantidad determinada de disolvente o de disolución total. Permite cuantificar la composición y es fundamental para entender las propiedades de la mezcla.
¿Para qué sirve calcular el porcentaje de una mezcla?
Calcular el porcentaje de una mezcla es útil para innumerables aplicaciones prácticas: desde preparar recetas con precisión, formular medicamentos con la dosis correcta, asegurar la calidad de productos industriales, hasta comprender la composición del aire que respiramos o las aleaciones de las monedas. Nos permite replicar mezclas y predecir su comportamiento.
¿Qué es la entalpía de mezcla (ΔHmix)?
La entalpía de mezcla es un parámetro termodinámico que mide el cambio de energía térmica (calor) que ocurre cuando diferentes sustancias se mezclan para formar una solución o aleación. Un valor negativo indica que la mezcla es energéticamente favorable (exotérmica), mientras que un valor positivo sugiere que es desfavorable (endotérmica).
¿Por qué es importante la entalpía de mezcla en las aleaciones?
En el campo de la ciencia de materiales, especialmente en el diseño de aleaciones avanzadas, la entalpía de mezcla es crucial porque ayuda a predecir la estabilidad y la formación de diferentes fases (soluciones sólidas, intermetálicos, fases amorfas). Junto con otros parámetros termodinámicos y topológicos, permite a los ingenieros y científicos diseñar materiales con propiedades específicas y deseadas.
¿Cómo afecta la concentración a las propiedades de una mezcla?
La concentración afecta directamente propiedades físicas como la densidad, el punto de ebullición y el punto de congelación. Por ejemplo, una mayor concentración de sal en agua aumenta su densidad y eleva su punto de ebullición. En el caso de las aleaciones, la concentración de los elementos puede cambiar el color, la dureza, la resistencia a la corrosión y otras propiedades mecánicas.
Conclusión
La capacidad de cuantificar la composición de las mezclas es una piedra angular en la ciencia y la ingeniería. Ya sea que estemos calculando la concentración porcentual de una solución de uso diario o investigando la compleja entalpía de mezcla en el desarrollo de materiales de vanguardia, estos cálculos nos proporcionan una comprensión profunda de la materia. Desde la simple aritmética que nos asegura la proporción perfecta en una receta, hasta las intrincadas ecuaciones termodinámicas que modelan la creación de nuevas aleaciones, el conocimiento de cómo se comportan y se mezclan los elementos es fundamental para innovar y mejorar nuestro mundo.
Si quieres conocer otros artículos parecidos a Cálculo de Mezclas: Entalpía y Concentración puedes visitar la categoría Química.

