11/09/2022
En el vasto universo de la ciencia, y particularmente en la química, pocos conceptos son tan fundamentales y a la vez tan susceptibles de ser malinterpretados como la masa. A menudo confundida con el peso, la masa es una propiedad intrínseca de la materia que nos permite cuantificar la cantidad de sustancia presente en un objeto o muestra. Comprender qué es la masa y cómo se relaciona con otras propiedades es crucial para cualquiera que desee adentrarse en el estudio de los elementos, compuestos y sus interacciones. Pero, ¿existe una única “fórmula de masa”? Y, ¿qué significa realmente calcular el “porcentaje en masa” en un compuesto? Este artículo desglosará estas preguntas, proporcionando una guía completa y accesible para entender uno de los pilares de la química.
A lo largo de estas líneas, exploraremos no solo las definiciones básicas, sino también las distintas aplicaciones y cálculos que involucran la masa, desde la determinación de la composición de un elemento en un compuesto hasta su relevancia en la industria y la vida cotidiana. Prepárese para descubrir cómo la masa, más allá de ser un simple número, es una clave para desvelar los secretos de la materia que nos rodea.
- La Masa: Más Allá de una Simple Medida
- ¿Existe una Única “Fórmula de Masa”? Desmitificando el Concepto
- El Porcentaje en Masa: Una Herramienta Crucial en Química
- Importancia y Aplicaciones del Porcentaje en Masa
- Comparativa de Conceptos de Masa
- Preguntas Frecuentes (FAQ)
- ¿Cuál es la diferencia entre masa y peso?
- ¿Cómo se calcula la masa molar de un compuesto?
- ¿Por qué es importante el porcentaje en masa en la química?
- ¿Se aplica el porcentaje en masa solo a compuestos químicos?
- ¿Qué significa “masa atómica”?
- ¿Cuál es la “fórmula de masa” más usada en un laboratorio de química?
La Masa: Más Allá de una Simple Medida
Para empezar, es vital establecer una distinción clara: la masa y el peso no son lo mismo. Mientras que el peso es una medida de la fuerza de la gravedad sobre un objeto (y por lo tanto varía según la ubicación, por ejemplo, en la Tierra o en la Luna), la masa es la cantidad de materia que contiene un objeto y es una propiedad constante, independientemente de dónde se mida. Es una medida de la inercia de un objeto, es decir, su resistencia a ser acelerado.
En el Sistema Internacional de Unidades (SI), la unidad básica de masa es el kilogramo (kg), aunque en química es más común trabajar con gramos (g) y miligramos (mg) para cantidades más pequeñas, o con la unidad de masa atómica (uma) para átomos y moléculas individuales. La conservación de la masa es uno de los principios más importantes en la química, postulado por Antoine Lavoisier: la masa no se crea ni se destruye en una reacción química ordinaria, solo se transforma.
¿Existe una Única “Fórmula de Masa”? Desmitificando el Concepto
Cuando se pregunta por la “fórmula de masa”, la respuesta no es tan directa como se podría esperar. A diferencia de fórmulas específicas como E=mc² (energía es igual a masa por la velocidad de la luz al cuadrado), no existe una única fórmula universal llamada “fórmula de masa” que se aplique a todos los contextos. En cambio, la masa puede ser calculada o relacionada con otras propiedades a través de diversas fórmulas, dependiendo del escenario específico. Estas son algunas de las más relevantes:
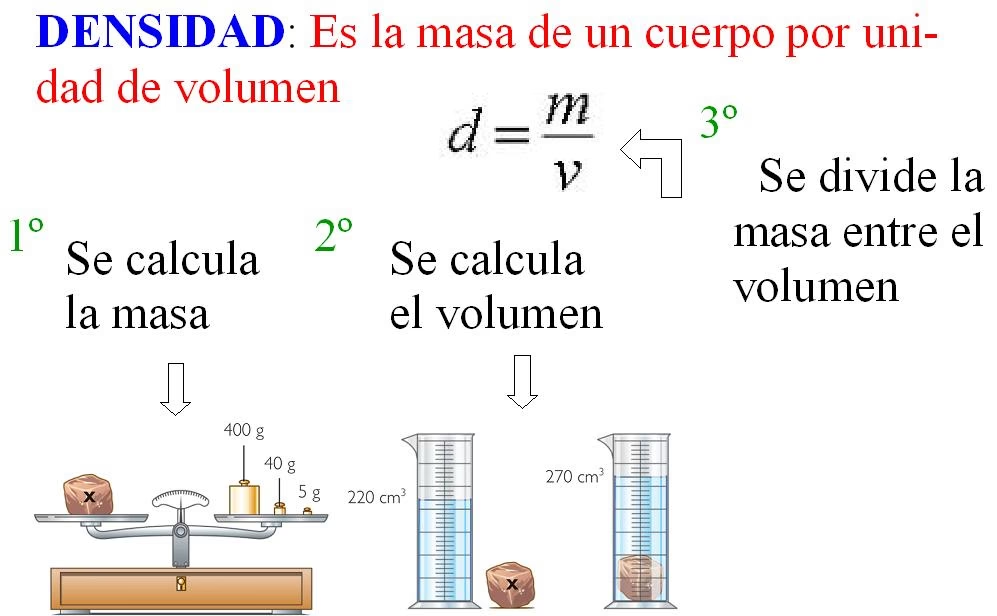
- Masa a partir de Densidad y Volumen: Una de las formas más comunes de calcular la masa de una sustancia es utilizando su densidad y su volumen. La densidad (ρ) se define como la masa por unidad de volumen. Por lo tanto, si conocemos la densidad de una sustancia y el volumen que ocupa, podemos calcular su masa con la siguiente relación:
Masa (m) = Densidad (ρ) × Volumen (V)
Esta fórmula es extremadamente útil en laboratorios y en la industria para determinar la masa de líquidos o sólidos de forma indirecta. - Masa a partir de Moles y Masa Molar: En química, es frecuente trabajar con moles, que representan una cantidad específica de partículas (átomos, moléculas, iones). La masa molar (M) de una sustancia es la masa de un mol de esa sustancia, expresada generalmente en gramos por mol (g/mol). Si conocemos la cantidad de moles (n) de una sustancia y su masa molar, podemos calcular la masa total de esa sustancia:
Masa (m) = Moles (n) × Masa Molar (M)
Esta es una fórmula fundamental para cálculos estequiométricos, permitiendo convertir entre la cantidad de sustancia y su masa. - Masa a partir de Fuerza y Aceleración (Segunda Ley de Newton): Aunque más relacionada con la física, es importante mencionar que la masa también se define en el contexto de la Segunda Ley de Newton, que establece que la fuerza (F) aplicada a un objeto es igual al producto de su masa (m) por su aceleración (a). De esta ley, podemos despejar la masa:
Masa (m) = Fuerza (F) / Aceleración (a)
Este enfoque nos permite entender la masa como una medida de la inercia.
Como se puede observar, la “fórmula de masa” se refiere más bien a un conjunto de relaciones que nos permiten calcular la masa en diferentes situaciones, en lugar de una única ecuación universal.
El Porcentaje en Masa: Una Herramienta Crucial en Química
Ahora, adentrémonos en el concepto de “porcentaje en masa”, que es una herramienta indispensable en la química analítica y en muchas aplicaciones industriales. El porcentaje en masa de un componente (ya sea un elemento en un compuesto o una sustancia en una mezcla) nos indica la proporción de la masa de ese componente con respecto a la masa total del compuesto o mezcla, expresada como un porcentaje.
La fórmula general para calcular el porcentaje en masa es la siguiente:
Porcentaje en Masa = (Masa del componente / Masa total del compuesto o mezcla) × 100%
Este cálculo es fundamental para:
- Determinar la composición elemental de un compuesto: Saber qué porcentaje de cada elemento constituye un compuesto es vital para la identificación y caracterización de sustancias.
- Analizar la concentración de soluciones y mezclas: En la industria farmacéutica, alimentaria o química, es crucial conocer el porcentaje en masa de un ingrediente activo o un contaminante.
- Control de calidad: Asegurar que los productos tengan la composición deseada.
Cálculo del Porcentaje en Masa de un Elemento en un Compuesto: Paso a Paso
La información proporcionada al inicio de este artículo se refiere específicamente a este cálculo. Para determinar el porcentaje en masa de un elemento en un compuesto puro, seguimos estos pasos:
- Paso 1: Identificar la fórmula química del compuesto. Esto nos permitirá saber qué elementos lo componen y en qué proporción.
- Paso 2: Calcular la masa molar del compuesto. La masa molar es la suma de las masas atómicas de todos los átomos presentes en la fórmula química, multiplicando cada masa atómica por su subíndice. Las masas atómicas se obtienen de la tabla periódica.
- Paso 3: Calcular la masa total del elemento de interés en un mol del compuesto. Multiplique la masa atómica del elemento por el número de veces que aparece en la fórmula del compuesto. Si el elemento aparece en varios iones dentro del compuesto, sume todas sus contribuciones.
- Paso 4: Aplicar la fórmula del porcentaje en masa. Divida la masa total del elemento calculada en el Paso 3 entre la masa molar del compuesto (Paso 2) y multiplique el resultado por 100.
Ejemplo Práctico: Porcentaje en Masa de Oxígeno en el Agua (H₂O)
Vamos a calcular el porcentaje en masa de oxígeno en una molécula de agua (H₂O).
- Fórmula química: H₂O
- Masas atómicas (aproximadas): H = 1.008 g/mol; O = 15.999 g/mol
- Paso 2: Masa molar de H₂O:
(2 × 1.008 g/mol H) + (1 × 15.999 g/mol O) = 2.016 g/mol + 15.999 g/mol = 18.015 g/mol H₂O - Paso 3: Masa de Oxígeno en 1 mol de H₂O:
1 × 15.999 g/mol O = 15.999 g/mol - Paso 4: Calcular el porcentaje en masa de Oxígeno:
Porcentaje en masa de O = (Masa de O / Masa molar de H₂O) × 100
Porcentaje en masa de O = (15.999 g/mol / 18.015 g/mol) × 100
Porcentaje en masa de O ≈ 0.8881 × 100 ≈ 88.81%Esto significa que aproximadamente el 88.81% de la masa de una molécula de agua proviene del oxígeno, mientras que el resto proviene del hidrógeno.
Cálculo del Porcentaje en Masa de un Componente en una Mezcla
El mismo principio se aplica a las mezclas. Si tenemos una mezcla y queremos saber el porcentaje en masa de uno de sus componentes, simplemente dividimos la masa de ese componente entre la masa total de la mezcla y multiplicamos por 100.
Ejemplo Práctico: Porcentaje en Masa de Sal en una Solución Salina
Supongamos que preparamos una solución disolviendo 5 gramos de sal (NaCl) en 95 gramos de agua.

Por ello, se define la llamada unidad de masa atómica (uma) que es la doceava parte de la masa del isótopo de carbono 12 (1 uma = masa del carbono-12/12). - Masa del componente (NaCl): 5 g
- Masa del solvente (agua): 95 g
- Masa total de la solución: 5 g (NaCl) + 95 g (agua) = 100 g
- Calcular el porcentaje en masa de NaCl:
Porcentaje en masa de NaCl = (Masa de NaCl / Masa total de la solución) × 100
Porcentaje en masa de NaCl = (5 g / 100 g) × 100
Porcentaje en masa de NaCl = 5%
Esta solución es una solución salina al 5% en masa.
Importancia y Aplicaciones del Porcentaje en Masa
La capacidad de calcular el porcentaje en masa es de una utilidad inmensa en diversas áreas:
- Nutrición y Alimentos: Las etiquetas nutricionales de los alimentos a menudo muestran el contenido de grasas, proteínas, carbohidratos, etc., como porcentajes en masa. Esto ayuda a los consumidores a entender la composición de lo que ingieren.
- Farmacología: En la fabricación de medicamentos, el porcentaje en masa del principio activo es crítico para garantizar la dosificación correcta y la eficacia del fármaco.
- Metalurgia: La composición de las aleaciones (como el acero, que es una aleación de hierro y carbono) se expresa comúnmente en porcentaje en masa para definir sus propiedades.
- Análisis Ambiental: Para medir la concentración de contaminantes en muestras de agua, suelo o aire.
- Química Industrial: En la producción de productos químicos, polímeros, fertilizantes y más, el control de la composición porcentual es esencial para la calidad y el rendimiento.
Comparativa de Conceptos de Masa
Concepto Descripción Unidad Común Fórmula Clave Aplicación Típica Masa (general) Cantidad de materia en un objeto, medida de inercia. Kilogramo (kg), Gramo (g) m = ρ × V ; m = n × M Cuantificar materia, cálculos básicos. Masa Molar Masa de un mol de una sustancia. Gramos por mol (g/mol) Suma de masas atómicas en la fórmula. Conversión entre moles y masa. Masa Atómica Masa promedio de un átomo de un elemento (considerando isótopos). Unidad de masa atómica (uma) (No es una fórmula de cálculo general) Base para calcular masa molar. Porcentaje en Masa Proporción de la masa de un componente respecto a la masa total, expresada en %. Porcentaje (%) (Masa componente / Masa total) × 100 Análisis de composición, control de calidad. Densidad Masa por unidad de volumen de una sustancia. Gramos por mililitro (g/mL), kg/m³ ρ = m / V Identificación de sustancias, cálculos de volumen/masa. Preguntas Frecuentes (FAQ)
¿Cuál es la diferencia entre masa y peso?
La masa es la cantidad de materia en un objeto y es constante. El peso es la fuerza de la gravedad sobre un objeto y puede variar según la gravedad del lugar donde se mida.
¿Cómo se calcula la masa molar de un compuesto?
Se suman las masas atómicas de todos los átomos presentes en la fórmula química del compuesto. Por ejemplo, para el CO₂, sumas la masa atómica de un carbono y dos veces la masa atómica de un oxígeno.
¿Por qué es importante el porcentaje en masa en la química?
Es importante porque permite determinar la composición exacta de sustancias, lo cual es crucial para la investigación, el desarrollo de nuevos materiales, el control de calidad en la industria y el análisis de pureza.
¿Se aplica el porcentaje en masa solo a compuestos químicos?
No, el porcentaje en masa se aplica tanto a compuestos (para determinar la proporción de elementos) como a mezclas (para determinar la proporción de componentes, como en soluciones o aleaciones).
¿Qué significa “masa atómica”?
La masa atómica es la masa de un átomo de un elemento. Se mide en unidades de masa atómica (uma) y es el promedio ponderado de las masas de los isótopos de ese elemento, teniendo en cuenta su abundancia natural.
¿Cuál es la “fórmula de masa” más usada en un laboratorio de química?
En un laboratorio de química, las fórmulas más usadas que involucran la masa son:
Masa = Moles × Masa Molar(para convertir entre moles y masa) y la fórmula delPorcentaje en Masa(para análisis de composición).En resumen, la masa es un concepto central y multifacético en la ciencia. Aunque no exista una única “fórmula de masa” universal, su comprensión se deriva de diversas relaciones que nos permiten cuantificar la materia en diferentes contextos. El porcentaje en masa, en particular, emerge como una herramienta analítica de valor incalculable, facilitando la comprensión de la composición de todo, desde la molécula más simple hasta los productos que utilizamos a diario. Dominar estos conceptos no solo enriquece nuestro conocimiento de la química, sino que también nos capacita para interpretar mejor el mundo material que nos rodea.
Si quieres conocer otros artículos parecidos a ¿Qué es la Masa y Cómo se Calcula? puedes visitar la categoría Química.

