25/08/2025
En el vasto universo de la termodinámica, el concepto de trabajo es fundamental para comprender cómo la energía se transforma y se transfiere en los sistemas físicos. Sin embargo, no todo el trabajo realizado por o sobre un sistema es igualmente ‘útil’ para nuestros propósitos. Aquí es donde entra en juego la noción de trabajo útil, una métrica crucial que nos permite cuantificar la energía aprovechable en diversos procesos, desde reacciones químicas hasta la generación de electricidad en celdas electroquímicas.

Este artículo explora en profundidad el trabajo útil, sus fórmulas, su relación con las funciones de estado termodinámicas y cómo se diferencia de otras formas de trabajo. Acompáñanos en este recorrido para desentrañar los misterios de la eficiencia energética y la capacidad de los sistemas para realizar trabajo aprovechable.
- ¿Qué es el Trabajo Termodinámico? Una Perspectiva General
- La Esencia del Trabajo Útil en Termodinámica
- Las Energías Libres: Helmholtz y Gibbs como Medidas del Trabajo Útil
- Aplicación Práctica: Celdas Galvánicas y el Trabajo Eléctrico
- Preguntas Frecuentes sobre el Trabajo Útil en Termodinámica
- ¿Cuál es la diferencia entre trabajo y trabajo útil?
- ¿Por qué se relaciona el trabajo útil con las energías de Gibbs y Helmholtz?
- ¿Siempre se puede obtener el trabajo útil máximo de un sistema?
- ¿El trabajo útil es siempre positivo o negativo?
- ¿Qué significa que la energía de Gibbs no es 'energía' en el sentido estricto de conservación?
- Conclusión
¿Qué es el Trabajo Termodinámico? Una Perspectiva General
Antes de sumergirnos en el trabajo útil, es imperativo comprender el concepto general de trabajo en termodinámica. El trabajo termodinámico se refiere a la energía transferida entre un sistema y sus alrededores debido a una fuerza que causa un desplazamiento. Es una forma de transferencia de energía que no es calor.
La primera ley de la termodinámica establece que el cambio en la energía interna (ΔU) de un sistema es igual al calor (Q) añadido al sistema menos el trabajo (W) realizado por el sistema. O, alternativamente, si W es el trabajo realizado sobre el sistema: ΔU = Q + W.
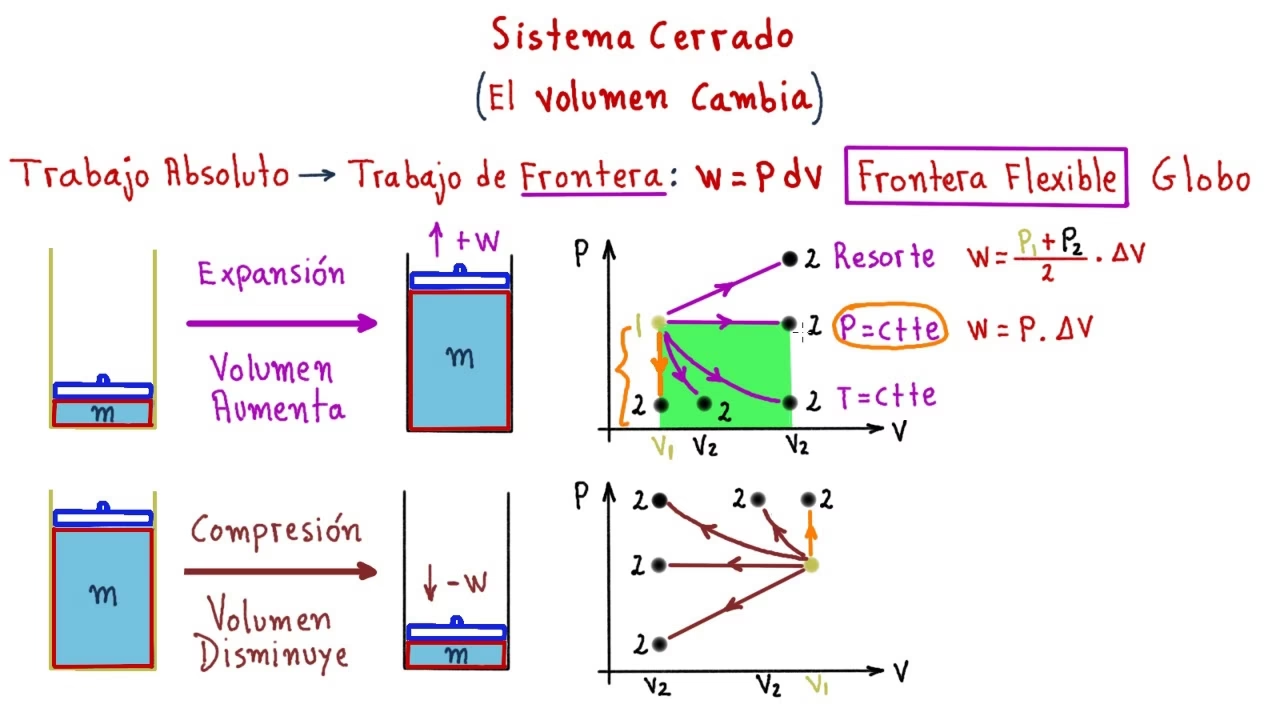
En su forma más general, para un proceso que implica un cambio de volumen, el trabajo se calcula como:
W = ∫ P dV
Donde W es el trabajo, P es la presión y dV es el cambio diferencial de volumen. Esta integral se calcula desde un volumen inicial (Vi) hasta un volumen final (Vf). Es crucial recordar la convención de signos: si el sistema realiza trabajo sobre los alrededores (por ejemplo, expandiéndose), el trabajo es negativo (W < 0). Si los alrededores realizan trabajo sobre el sistema (por ejemplo, comprimiéndolo), el trabajo es positivo (W > 0).
Tipos de Procesos Termodinámicos y sus Fórmulas de Trabajo
La forma en que se calcula el trabajo termodinámico depende del tipo de proceso que experimenta el sistema. A continuación, se detallan los procesos más comunes:
- Proceso Isobárico: Ocurre a presión constante. En este caso, la fórmula del trabajo se simplifica considerablemente.
- Proceso Isotérmico: Se lleva a cabo a temperatura constante. Para un gas ideal, esto implica una relación inversa entre presión y volumen.
- Proceso Adiabático: No hay intercambio de calor con el ambiente (Q = 0). Todo el cambio de energía interna se manifiesta como trabajo.
- Proceso Isocórico (o Isométrico): El volumen del sistema se mantiene constante.
La siguiente tabla resume las fórmulas de trabajo para estos procesos:
| Proceso | Condición | Fórmula del Trabajo (W) | Notas |
|---|---|---|---|
| Isobárico | Presión constante (P) | W = P(Vf - Vi) | Trabajo realizado por expansión o compresión. |
| Isotérmico | Temperatura constante (T) | W = nRT ln(Vf/Vi) | Para un gas ideal, n es moles, R es cte. de gases. |
| Adiabático | Sin intercambio de calor (Q = 0) | W = (PiViγ - PfVfγ) / (1 - γ) | γ es el coeficiente adiabático (Cp/Cv). También W = ΔU. |
| Isocórico | Volumen constante (V) | W = 0 | No hay desplazamiento, por lo tanto no hay trabajo P-V. |
Estos tipos de trabajo son esenciales, pero ¿qué sucede con el trabajo que no implica cambios de volumen?
La Esencia del Trabajo Útil en Termodinámica
El trabajo útil (Wútil) en termodinámica se refiere a cualquier forma de trabajo que no sea el trabajo de expansión-compresión (PΔV). Es el trabajo adicional que un sistema puede realizar, más allá del simple cambio de volumen contra una presión externa. Este tipo de trabajo es particularmente relevante porque representa la porción de energía que puede ser directamente aprovechada para realizar una tarea específica, como generar electricidad, mover un motor que no sea por expansión, o realizar un trabajo químico.
Consideremos la primera ley de la termodinámica nuevamente: ΔU = Q + Wtotal. Si dividimos el trabajo total (Wtotal) en trabajo de expansión (Wexp) y trabajo útil (Wútil), tenemos:
Wtotal = Wexp + Wútil
Donde Wexp = -PΔV (trabajo realizado por el sistema sobre los alrededores debido a un cambio de volumen, si se expande, PΔV es positivo, y Wexp es negativo). Por lo tanto, Wútil es el trabajo que queda después de contabilizar el trabajo de volumen.
La importancia del trabajo útil radica en que, en un proceso reversible, representa el máximo trabajo que un sistema puede realizar para un propósito específico. Los procesos reversibles son idealizaciones en las que el sistema está siempre en equilibrio y el trabajo se realiza de la manera más eficiente posible, sin pérdidas por irreversibilidades como la fricción o la transferencia de calor a través de una diferencia finita de temperatura.
Las Energías Libres: Helmholtz y Gibbs como Medidas del Trabajo Útil
En el estudio de la termodinámica, dos funciones de estado son de particular importancia para cuantificar el trabajo útil: la energía de Helmholtz (A) y la energía de Gibbs (G). Ambas se conocen históricamente como 'energías libres' porque representan la parte de la energía interna o entalpía de un sistema que está 'libre' o disponible para realizar trabajo útil bajo ciertas condiciones.

Energía de Helmholtz (A): Trabajo Útil a Temperatura y Volumen Constantes
La energía de Helmholtz se define como:
A = U - TS
Donde U es la energía interna, T es la temperatura absoluta y S es la entropía.
Para un proceso reversible que ocurre a temperatura constante (T) y volumen constante (V), el cambio en la energía de Helmholtz (ΔA) es igual al trabajo útil realizado sobre el sistema:
wútil = ΔU - TΔS = Δ(U - TS) = ΔA
Esto significa que si el volumen del sistema no cambia, cualquier trabajo realizado es trabajo útil. Si ΔA es negativo, el sistema puede realizar esa cantidad de trabajo útil sobre el entorno.
Energía de Gibbs (G): Trabajo Útil a Temperatura y Presión Constantes
La energía de Gibbs es quizás la función más utilizada en química y bioquímica, ya que muchos procesos ocurren a temperatura y presión constantes. Se define como:
G = H - TS
Donde H es la entalpía, T es la temperatura absoluta y S es la entropía.
Para un proceso reversible que ocurre a temperatura constante (T) y presión constante (P), el cambio en la energía de Gibbs (ΔG) es igual al trabajo útil realizado sobre el sistema:
wútil = ΔH - TΔS = Δ(H - TS) = ΔG
Al igual que con la energía de Helmholtz, si ΔG es negativo para un proceso espontáneo, esto indica que el sistema puede realizar una cantidad de trabajo útil equivalente a -ΔG. Es la máxima cantidad de trabajo no P-V que se puede extraer del sistema bajo estas condiciones.
Es importante señalar que, aunque históricamente se les llamó 'energías libres', el uso del término 'energía' para G y A puede generar confusión. Como se ha argumentado en la literatura especializada, estas funciones son más precisamente 'funciones de estado' que cuantifican el trabajo útil máximo, en lugar de ser 'energía' en el sentido de una cantidad que se conserva. Ni la entalpía ni el producto TS son estrictamente 'energía' en un sentido conservativo, por lo que su diferencia tampoco lo es. Sin embargo, su valor práctico para calcular el trabajo útil es innegable.
Aplicación Práctica: Celdas Galvánicas y el Trabajo Eléctrico
Un ejemplo sobresaliente de trabajo útil es el trabajo eléctrico producido por una celda galvánica (o pila). Una celda galvánica es un dispositivo que convierte la energía química liberada por una reacción redox espontánea en energía eléctrica.
Para una celda galvánica, el trabajo eléctrico (Weléctrico) realizado por la celda se relaciona con el potencial de la celda (E) y el número de moles de electrones (n) transferidos, así como con la constante de Faraday (F), que es la carga de un mol de electrones (aproximadamente 96485 C/mol):
Weléctrico = -nFE
El signo negativo indica que el trabajo es realizado *por* el sistema (la celda). Cuanto mayor sea E, mayor será el trabajo eléctrico que la celda puede realizar.
Como se mencionó anteriormente, el trabajo útil máximo a temperatura y presión constantes es igual al cambio en la energía de Gibbs (ΔG) para el proceso reversible. En el caso de una celda galvánica funcionando de manera reversible (es decir, con una corriente infinitesimalmente pequeña), el trabajo eléctrico es el trabajo útil. Por lo tanto, podemos igualar las dos expresiones:
ΔG = Weléctrico = -nFE
Esta ecuación fundamental, conocida como la ecuación de Nernst-Gibbs, establece una relación directa entre la termodinámica (ΔG) y la electroquímica (E). Si la reacción en la celda es espontánea, ΔG será negativo, lo que resulta en un potencial E positivo, indicando que la celda puede generar electricidad (realizar trabajo útil).
A condiciones estándar (298.15 K, 1 bar de presión para gases, y 1 M de concentración para soluciones), la ecuación se convierte en:
ΔG° = -nFE°
Donde ΔG° es el cambio de energía de Gibbs estándar y E° es el potencial estándar de la celda. Esta relación permite calcular uno a partir del otro, utilizando datos termoquímicos (ΔH°, ΔS°) o electroquímicos (E°).
Por ejemplo, en la celda de Daniell (Zn/ZnSO4 || CuSO4/Cu), el cinc se oxida y el cobre se reduce. La reacción global es:
Zn(s) + Cu2+(aq) → Zn2+(aq) + Cu(s)
Para esta reacción, se transfieren 2 moles de electrones (n=2). Conociendo el E° de la celda, se puede calcular el ΔG° y, por ende, el trabajo eléctrico útil máximo que puede generar la celda.
Preguntas Frecuentes sobre el Trabajo Útil en Termodinámica
¿Cuál es la diferencia entre trabajo y trabajo útil?
El trabajo termodinámico general incluye todas las formas de trabajo, siendo la más común el trabajo de expansión-compresión (PΔV). El trabajo útil es la porción del trabajo total que no es trabajo de expansión-compresión y que puede ser aprovechada para fines específicos, como el trabajo eléctrico, mecánico no volumétrico o químico.
¿Por qué se relaciona el trabajo útil con las energías de Gibbs y Helmholtz?
Las energías de Gibbs (G) y Helmholtz (A) son funciones de estado que permiten determinar la espontaneidad de un proceso y el máximo trabajo útil que se puede obtener de un sistema bajo condiciones específicas (T y P constantes para G; T y V constantes para A) en un proceso reversible. Ellas cuantifican la capacidad de un sistema para realizar trabajo, excluyendo el trabajo de expansión.
¿Siempre se puede obtener el trabajo útil máximo de un sistema?
No. El trabajo útil máximo (cuantificado por -ΔG o -ΔA) solo se puede obtener en un proceso reversible, que es una idealización. En la realidad, todos los procesos son irreversibles en algún grado, lo que significa que siempre hay pérdidas de energía (por ejemplo, en forma de calor disipado) y el trabajo útil real extraído es menor que el máximo teórico. La eficiencia de un proceso es la relación entre el trabajo útil real y el trabajo útil máximo.
¿El trabajo útil es siempre positivo o negativo?
El signo del trabajo útil depende de la convención utilizada. Si se define como el trabajo realizado sobre el sistema (W > 0), entonces para un proceso espontáneo que realiza trabajo (como una pila), el ΔG es negativo, lo que implica que el Wútil es negativo (trabajo realizado por el sistema). Si nos referimos a la *cantidad* de trabajo que el sistema *puede realizar*, a menudo se habla de su magnitud, |ΔG|.
¿Qué significa que la energía de Gibbs no es 'energía' en el sentido estricto de conservación?
Aunque la energía de Gibbs tiene dimensiones de energía y se usa para calcular trabajo, algunos enfoques termodinámicos argumentan que no es una cantidad que se conserva universalmente como la energía interna. Más bien, es una función de estado que disminuye en procesos espontáneos a T y P constantes, reflejando la capacidad de un sistema para realizar trabajo. A diferencia de la energía interna, la energía de Gibbs no se conserva en todos los procesos, especialmente en los irreversibles, lo que la diferencia de la definición más estricta de 'energía' como una cantidad conservada.
Conclusión
El concepto de trabajo útil es una piedra angular en la termodinámica, especialmente en el diseño y análisis de sistemas que buscan convertir eficientemente la energía. Al diferenciar entre el trabajo de expansión y el trabajo que realmente podemos aprovechar para fines específicos, obtenemos una comprensión más profunda de la eficiencia y las limitaciones de los procesos energéticos. Las funciones de estado como la energía de Helmholtz y, particularmente, la energía de Gibbs, se erigen como herramientas matemáticas poderosas para cuantificar este trabajo útil máximo bajo condiciones controladas. Comprender estas fórmulas y sus implicaciones no solo es fundamental para académicos e ingenieros, sino también para cualquier persona interesada en la ciencia detrás de la conversión y el aprovechamiento de la energía en nuestro mundo.
Si quieres conocer otros artículos parecidos a El Trabajo Útil en Termodinámica: Conceptos y Fórmulas puedes visitar la categoría Cálculos.