19/09/2025
En el fascinante mundo de la química, las reacciones son el corazón de la transformación de la materia. Desde la producción de medicamentos hasta la fabricación de materiales avanzados, cada proceso implica una serie de cambios químicos. Sin embargo, no todas las reacciones ocurren con una eficiencia perfecta. Aquí es donde entra en juego la estequiometría, la rama de la química que estudia las relaciones cuantitativas entre reactivos y productos en una reacción química. Comprender cómo calcular el rendimiento de una reacción es fundamental para cualquier químico, ingeniero o estudiante que busque optimizar procesos, predecir resultados y minimizar el desperdicio. Este artículo te guiará a través de los conceptos esenciales y los pasos prácticos para dominar el cálculo del rendimiento en estequiometría.

La estequiometría nos permite predecir cuánto producto podemos obtener a partir de una cantidad dada de reactivos. Sin embargo, en la práctica, la cantidad de producto obtenida es a menudo menor de lo que las predicciones teóricas sugieren. Esta diferencia se debe a varios factores que exploraremos más adelante. La capacidad de cuantificar esta eficiencia es lo que conocemos como el cálculo del rendimiento.
- Fundamentos Esenciales para el Cálculo del Rendimiento
- Guía Paso a Paso para Calcular el Rendimiento
- Factores que Afectan el Rendimiento de una Reacción
- Importancia del Cálculo del Rendimiento en la Industria y la Investigación
- Tabla Comparativa: Conceptos de Rendimiento
- Preguntas Frecuentes sobre el Cálculo del Rendimiento
- ¿Por qué el rendimiento real es casi siempre menor que el rendimiento teórico?
- ¿Puede el rendimiento porcentual ser mayor del 100%?
- ¿Qué unidades se utilizan para el rendimiento?
- ¿Es siempre necesario identificar el reactivo limitante para calcular el rendimiento?
- ¿Cómo puedo mejorar el rendimiento de una reacción en el laboratorio?
Fundamentos Esenciales para el Cálculo del Rendimiento
Antes de sumergirnos en los cálculos, es crucial entender algunos conceptos clave que son la base de cualquier análisis estequiométrico de rendimiento:
El Reactivo Limitante: La Clave de la Predicción
En la mayoría de las reacciones químicas, los reactivos no se consumen en proporciones exactas. Uno de los reactivos se agotará primero, deteniendo la reacción y limitando la cantidad de producto que se puede formar. Este reactivo se conoce como el reactivo limitante. Es el componente que determina la máxima cantidad de producto que se puede generar. Identificarlo correctamente es el primer paso crítico para calcular el rendimiento teórico de una reacción. El otro reactivo, que queda en exceso una vez que la reacción ha cesado, se denomina reactivo en exceso.
Rendimiento Teórico: El Ideal Inalcanzable
El rendimiento teórico es la cantidad máxima de producto que podría formarse a partir de una cantidad dada de reactivo limitante, asumiendo que la reacción procede a la perfección y con una eficiencia del 100%. Se calcula utilizando la estequiometría de la ecuación química balanceada. Representa el ideal, la cantidad máxima posible de producto que se puede obtener si no hubiera pérdidas, subproductos o reacciones secundarias. Este valor es puramente teórico y se obtiene a través de cálculos matemáticos basados en las masas molares y las proporciones estequiométricas.
Rendimiento Real o Experimental: La Realidad de Laboratorio
El rendimiento real, también conocido como rendimiento experimental o rendimiento actual, es la cantidad de producto que se obtiene verdaderamente en el laboratorio o en un proceso industrial. Esta cantidad casi siempre es menor que el rendimiento teórico. Se determina a través de la medición directa del producto después de que la reacción ha concluido y el producto ha sido aislado y purificado. Este valor es el resultado de las imperfecciones inherentes a cualquier proceso químico experimental.
Rendimiento Porcentual: La Medida de la Eficiencia
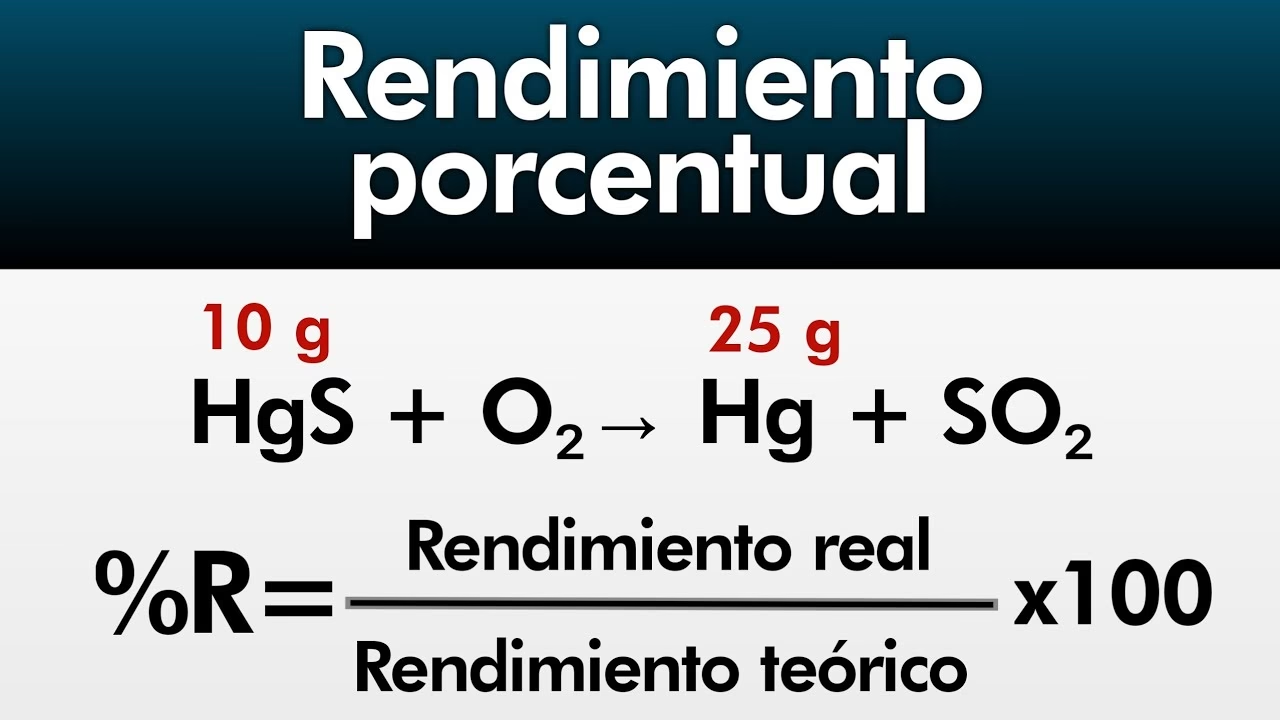
El rendimiento porcentual es una medida de la eficiencia de una reacción química. Expresa el rendimiento real como un porcentaje del rendimiento teórico. Nos dice qué tan cerca estuvo la cantidad de producto obtenida experimentalmente de la cantidad máxima que se podría haber obtenido. Se calcula utilizando la siguiente fórmula:
Rendimiento Porcentual = (Rendimiento Real / Rendimiento Teórico) x 100%
Un alto rendimiento porcentual indica una reacción eficiente, mientras que un bajo rendimiento porcentual sugiere pérdidas significativas o problemas en el proceso. Es una métrica crucial para evaluar la viabilidad y la optimización de una síntesis química.
Guía Paso a Paso para Calcular el Rendimiento
El cálculo del rendimiento en estequiometría sigue una serie de pasos lógicos y sistemáticos. Aquí te presentamos una guía detallada:
Paso 1: Escribir y Balancear la Ecuación Química
El primer y más fundamental paso es tener la ecuación química correctamente balanceada. Una ecuación balanceada asegura que la ley de conservación de la masa se cumple y que las proporciones molares entre reactivos y productos son correctas. Sin una ecuación balanceada, todos los cálculos estequiométricos subsiguientes serán incorrectos.
Paso 2: Convertir las Cantidades Dadas a Moles
Generalmente, las cantidades de reactivos se proporcionan en unidades de masa (gramos, kilogramos) o volumen (litros, mililitros, especialmente para soluciones con concentraciones). Para realizar cálculos estequiométricos, es indispensable convertir estas cantidades a moles utilizando las masas molares de las sustancias o la concentración y el volumen para soluciones.
Paso 3: Identificar el Reactivo Limitante
Este es un paso crucial si se te dan las cantidades de más de un reactivo. Para identificar el reactivo limitante, puedes seguir uno de los siguientes métodos:
- Método de Comparación de Moles de Producto: Calcula la cantidad de producto que se podría formar con cada uno de los reactivos, asumiendo que es el reactivo limitante. El reactivo que produce la menor cantidad de producto es el reactivo limitante.
- Método de Comparación de Moles Necesarios: Calcula cuántos moles de un reactivo se necesitarían para reaccionar completamente con la cantidad dada del otro reactivo. Compara esta cantidad con la cantidad de moles que realmente tienes. Si tienes menos de lo que necesitas, ese es el reactivo limitante.
El reactivo limitante es el que se consumirá por completo y determinará la cantidad máxima de producto que se puede obtener.
Paso 4: Calcular el Rendimiento Teórico del Producto
Una vez identificado el reactivo limitante, utiliza su cantidad en moles y las proporciones estequiométricas de la ecuación balanceada para calcular la cantidad de moles del producto deseado que se formaría. Luego, convierte esos moles de producto a la unidad de masa (generalmente gramos) utilizando la masa molar del producto. Esta es tu cantidad de rendimiento teórico.
Paso 5: Determinar el Rendimiento Real o Experimental
El rendimiento real es la cantidad de producto que se ha medido experimentalmente. Esta información normalmente se proporciona en los problemas de estequiometría o se obtiene directamente de los datos experimentales de laboratorio. Es importante que tanto el rendimiento real como el teórico estén en las mismas unidades (por ejemplo, gramos).
Paso 6: Calcular el Rendimiento Porcentual
Finalmente, utiliza la fórmula del rendimiento porcentual para calcular la eficiencia de la reacción:
Rendimiento Porcentual = (Rendimiento Real / Rendimiento Teórico) x 100%
Este valor te dará una idea clara de qué tan exitosa fue la reacción en términos de producción de producto.
Factores que Afectan el Rendimiento de una Reacción
Es fundamental comprender por qué el rendimiento real casi siempre es menor que el rendimiento teórico. Varios factores contribuyen a esta discrepancia:
- Reacciones Incompletas: No todos los reactivos pueden reaccionar completamente. Esto puede deberse a condiciones de reacción desfavorables (temperatura, presión), equilibrio químico que favorece a los reactivos, o simplemente a que la reacción se detiene antes de que se complete.
- Reacciones Secundarias o Colaterales: A menudo, junto con la reacción deseada, ocurren otras reacciones que producen subproductos no deseados. Esto consume parte de los reactivos disponibles que de otro modo se habrían convertido en el producto principal.
- Pérdidas Durante la Manipulación y Purificación: Durante el proceso de aislamiento y purificación del producto (filtración, decantación, evaporación, cristalización, etc.), siempre hay alguna pérdida de material. Parte del producto puede quedarse adherido al material de vidrio, no disolverse completamente, o evaporarse.
- Impurezas en los Reactivos: Los reactivos utilizados pueden no ser 100% puros. Las impurezas no reaccionarán o reaccionarán de manera diferente, reduciendo la cantidad efectiva del reactivo deseado.
- Errores Experimentales: Medidas inexactas de masa o volumen, problemas con la temperatura o la presión, o cualquier otro error humano o instrumental durante el experimento pueden afectar negativamente el rendimiento.
Importancia del Cálculo del Rendimiento en la Industria y la Investigación
El cálculo del rendimiento no es solo un ejercicio académico; tiene implicaciones profundas y prácticas en el mundo real. Es una métrica vital para:
- Optimización de Procesos: Al conocer el rendimiento porcentual, los químicos e ingenieros pueden identificar áreas de mejora en un proceso. Un bajo rendimiento indica que se deben investigar y ajustar las condiciones de reacción, la pureza de los reactivos o los métodos de purificación.
- Eficiencia Económica: En la industria, el rendimiento afecta directamente los costos de producción. Un mayor rendimiento significa que se gasta menos reactivo para producir la misma cantidad de producto, lo que se traduce en ahorro de costos y menor generación de residuos.
- Investigación y Desarrollo: En la investigación, el rendimiento es un indicador de la viabilidad de una nueva síntesis. Un método con un rendimiento consistentemente bajo puede no ser práctico para la producción a gran escala.
- Control de Calidad: Monitorear el rendimiento a lo largo del tiempo puede ayudar a detectar problemas en la producción, asegurando la consistencia y la calidad del producto.
- Sostenibilidad: Un rendimiento más alto implica un uso más eficiente de los recursos y una menor cantidad de subproductos o residuos, lo que contribuye a procesos más sostenibles y amigables con el medio ambiente.
Tabla Comparativa: Conceptos de Rendimiento
| Concepto | Definición | Cómo se Determina | Consideraciones Clave |
|---|---|---|---|
| Rendimiento Teórico | Cantidad máxima de producto que se puede obtener si la reacción es 100% eficiente, basada en el reactivo limitante. | Cálculos estequiométricos a partir de la ecuación balanceada y las cantidades de reactivos. | Es un valor ideal, no se alcanza en la práctica. |
| Rendimiento Real | Cantidad de producto obtenida experimentalmente en el laboratorio o en un proceso industrial. | Medición directa del producto aislado y purificado. | Siempre es menor que el rendimiento teórico debido a pérdidas y reacciones secundarias. |
| Rendimiento Porcentual | Relación entre el rendimiento real y el rendimiento teórico, expresada como porcentaje. | (Rendimiento Real / Rendimiento Teórico) x 100% | Mide la eficiencia de la reacción. Un valor alto indica un proceso eficiente. |
Preguntas Frecuentes sobre el Cálculo del Rendimiento
¿Por qué el rendimiento real es casi siempre menor que el rendimiento teórico?
El rendimiento real es casi siempre menor debido a factores como reacciones incompletas, la ocurrencia de reacciones secundarias no deseadas, pérdidas de material durante la manipulación y purificación del producto, y errores experimentales. El rendimiento teórico asume condiciones ideales que rara vez se replican perfectamente en la práctica.
¿Puede el rendimiento porcentual ser mayor del 100%?
Teóricamente, no. Un rendimiento porcentual superior al 100% indicaría que se obtuvo más producto del que es estequiométricamente posible. Si esto ocurre en un experimento, es un fuerte indicio de un error en la medición (por ejemplo, el producto aún contiene solvente, impurezas o no está completamente seco), o un error en los cálculos del rendimiento teórico o real. Es una señal de que algo salió mal en el experimento o en la contabilidad de la masa.
¿Qué unidades se utilizan para el rendimiento?
El rendimiento teórico y el rendimiento real deben expresarse en las mismas unidades de masa, comúnmente gramos (g) o kilogramos (kg). El rendimiento porcentual, como su nombre lo indica, se expresa como un porcentaje (%).
¿Es siempre necesario identificar el reactivo limitante para calcular el rendimiento?
Sí, es absolutamente necesario si se te proporcionan las cantidades de más de un reactivo. El rendimiento teórico de una reacción siempre se basa en la cantidad de reactivo limitante, ya que este es el que determinará cuánta cantidad de producto se puede formar. Si solo se proporciona la cantidad de un reactivo, se asume que los demás están en exceso y el cálculo del rendimiento teórico se basa en ese único reactivo dado.
¿Cómo puedo mejorar el rendimiento de una reacción en el laboratorio?
Mejorar el rendimiento implica optimizar las condiciones de reacción (temperatura, presión, concentración, tiempo de reacción), utilizar reactivos de mayor pureza, desarrollar técnicas de purificación más eficientes para minimizar las pérdidas, y asegurarse de que la reacción se agite adecuadamente para garantizar el contacto entre los reactivos. También, la prevención de reacciones secundarias y el monitoreo cuidadoso del progreso de la reacción son clave.
En conclusión, el cálculo del rendimiento en estequiometría es una habilidad fundamental que va más allá de la mera aritmética. Permite a los químicos comprender la eficiencia de sus procesos, diagnosticar problemas y buscar vías para la optimización. Al dominar los conceptos de reactivo limitante, rendimiento teórico, real y porcentual, se adquiere una herramienta poderosa para la predicción, la evaluación y la mejora continua en el vasto campo de la química.
Si quieres conocer otros artículos parecidos a Cálculo del Rendimiento en Estequiometría puedes visitar la categoría Química.