19/03/2023
La comprensión de cómo las sustancias cambian con el tiempo es fundamental en campos tan diversos como la química, la biología, la ingeniería y la física. En el corazón de esta comprensión se encuentran los conceptos de cinética de reacción y el comportamiento de los sistemas. Dentro de este vasto dominio, las reacciones y sistemas de primer orden ocupan un lugar privilegiado debido a su simplicidad matemática y a la ubicuidad de su comportamiento en la naturaleza y la tecnología. Este artículo desglosará las características, fórmulas y métodos para identificar estos procesos, brindando una visión clara y profunda que va más allá de los libros de texto.
Desde la desintegración radiactiva hasta el crecimiento poblacional o la respuesta de un circuito electrónico, el patrón de 'primer orden' emerge repetidamente. Su estudio no solo nos permite predecir el futuro de una reacción o sistema, sino también diseñar procesos más eficientes y seguros. Prepárate para explorar las ecuaciones que rigen estos fenómenos y descubrir por qué su patrón es tan fundamental.
- ¿Qué son las Reacciones de Primer Orden?
- La Ley de Velocidad Diferencial de Primer Orden
- Derivación de la Ley de Velocidad Integrada de Primer Orden
- Interpretación Gráfica y Determinación Experimental
- La Forma Exponencial de la Ley de Velocidad
- Aplicaciones y Significado de las Leyes Exponenciales
- Sistemas de Primer Orden en Otros Campos
- Identificación de Ecuaciones Diferenciales Lineales de Primer Orden
- Tabla Comparativa: Leyes de Velocidad Diferenciales vs. Integradas
- Preguntas Frecuentes (FAQ)
¿Qué son las Reacciones de Primer Orden?
Una reacción de primer orden es un tipo de reacción química en la que la velocidad a la que procede depende linealmente de la concentración de un solo reactivo. Esto significa que si duplicamos la concentración de ese reactivo, la velocidad de la reacción también se duplicará. Si la reducimos a la mitad, la velocidad se reducirá a la mitad. Esta relación directa es lo que define su 'primer orden'.
La velocidad de una reacción se mide en unidades de concentración por unidad de tiempo (por ejemplo, moles por litro por segundo, M/s). La relación entre la velocidad de reacción y la concentración del reactivo se expresa a través de una constante de proporcionalidad, conocida como la constante de velocidad de la reacción, denotada por k. Las unidades de k varían según el orden de la reacción; para una reacción de primer orden, las unidades de k son de tiempo-1 (por ejemplo, s-1 o min-1).
La Ley de Velocidad Diferencial de Primer Orden
Para una reacción genérica de primer orden donde un reactivo A se convierte en productos (A → productos), la ley de velocidad diferencial se expresa de la siguiente manera:
Velocidad = - d[A]/dt = k[A]
Aquí, d[A]/dt representa el cambio instantáneo en la concentración del reactivo A con respecto al tiempo (t). El signo negativo indica que la concentración de A disminuye a medida que avanza la reacción. [A] es la concentración molar del reactivo A en un momento dado, y k es la constante de velocidad de primer orden. Esta ecuación nos dice la velocidad de la reacción en cualquier instante, basándose en la concentración actual del reactivo.
Derivación de la Ley de Velocidad Integrada de Primer Orden
Mientras que la ley de velocidad diferencial describe lo que ocurre a nivel molecular en un instante, la ley de velocidad integrada es una herramienta invaluable para determinar el orden de una reacción y el valor de su constante de velocidad a partir de mediciones experimentales a lo largo del tiempo. Nos permite predecir la concentración de un reactivo en cualquier momento futuro o calcular el tiempo necesario para alcanzar una cierta concentración.

La derivación de la ley de velocidad integrada para una reacción de primer orden comienza con la ley de velocidad diferencial y utiliza cálculo integral:
Reorganizar la ecuación diferencial:
Comenzamos con la ley diferencial:
- d[A]/dt = k[A]Reorganizamos para separar las variables, colocando los términos de concentración en un lado y los términos de tiempo en el otro:
d[A]/[A] = - k dtIntegrar ambos lados de la ecuación:
Ahora integramos ambos lados de la ecuación. La integración se realiza desde la concentración inicial
[A]₀(en el tiempo t = 0) hasta la concentración[A](en un tiempo t) y desde el tiempo 0 hasta el tiempo t.∫[A]₀[A] (1/[A]) d[A] = ∫0t -k dtRecordemos de cálculo que la integral de
1/xes el logaritmo natural dex(ln(x)).Aplicando esta regla, obtenemos:
ln[A] - ln[A]₀ = -ktReorganizar para obtener la ley de velocidad integrada:
Esta ecuación se puede reorganizar de varias maneras para facilitar su uso. Una forma común es:
ln[A] = -kt + ln[A]₀Esta forma es particularmente útil porque se asemeja a la ecuación de una línea recta (y = mx + b), donde:
y = ln[A](el logaritmo natural de la concentración en el tiempo t)m = -k(la pendiente de la línea, que es el negativo de la constante de velocidad)x = t(el tiempo)b = ln[A]₀(la ordenada al origen, que es el logaritmo natural de la concentración inicial)
Otra forma útil, obtenida de las propiedades de los logaritmos (ln(a) - ln(b) = ln(a/b)), es:
ln([A]/[A]₀) = -ktEsta última ecuación es muy compacta y a menudo se utiliza para calcular la fracción de reactivo restante después de un cierto tiempo.
Interpretación Gráfica y Determinación Experimental
La forma ln[A] = -kt + ln[A]₀ es clave para determinar si una reacción es de primer orden a partir de datos experimentales. Si graficamos el logaritmo natural de la concentración del reactivo ln[A] en el eje Y contra el tiempo t en el eje X, y obtenemos una línea recta con una pendiente negativa, entonces la reacción es de primer orden.
La pendiente de esta línea recta será igual a -k. Por lo tanto, la constante de velocidad k se puede determinar directamente a partir de la pendiente del gráfico. La ordenada al origen (el valor de ln[A] cuando t=0) nos dará ln[A]₀, permitiéndonos encontrar la concentración inicial si no se conoce directamente.
Dado que los logaritmos de los números no tienen unidades, el producto -kt tampoco debe tenerlas. Esto implica que la unidad de k en una reacción de primer orden debe ser de tiempo-1 (por ejemplo, s-1, min-1, h-1), lo que es consistente con la definición de la constante de velocidad.

La Forma Exponencial de la Ley de Velocidad
Además de la forma logarítmica, la ley de velocidad integrada de primer orden también puede expresarse en una forma exponencial, que es muy intuitiva para comprender el proceso de decaimiento. Partiendo de ln([A]/[A]₀) = -kt, podemos elevar ambos lados de la ecuación a la base exponencial e:
eln([A]/[A]₀) = e-kt
Dado que eln(x) = x, simplificamos el lado izquierdo para obtener la segunda forma de la ley de velocidad:
[A] = [A]₀e-kt
Esta ecuación es la representación directa del decaimiento exponencial. Nos muestra cómo la concentración del reactivo [A] disminuye exponencialmente con el tiempo a partir de su concentración inicial [A]₀, modulada por la constante de velocidad k. Esta relación es fundamental porque describe cómo una cantidad cambia a una velocidad que depende de su valor instantáneo, un patrón que se encuentra en innumerables fenómenos naturales.
Aplicaciones y Significado de las Leyes Exponenciales
La relación exponencial, donde una cantidad cambia a una tasa que depende de su valor instantáneo, es una de las leyes más fundamentales y extendidas en la ciencia y más allá. Aunque la hemos derivado en el contexto de las reacciones químicas, su aplicación es mucho más amplia:
- Decaimiento Radiactivo: La desintegración de isótopos radiactivos sigue una ley de decaimiento exponencial, donde la cantidad de material radiactivo disminuye con el tiempo de acuerdo con una constante de desintegración (análoga a k).
- Crecimiento Poblacional: En condiciones ideales, el crecimiento de una población de organismos (bacterias, animales) puede seguir una ley de crecimiento exponencial, donde la tasa de crecimiento es proporcional al tamaño actual de la población.
- Interés Compuesto Continuo: El crecimiento del dinero en una cuenta bancaria con interés compuesto continuamente también sigue una ley de crecimiento exponencial.
- Descarga de Condensadores: En un circuito RC, la descarga de un condensador se describe mediante una función exponencial decreciente.
La razón por la que la función exponencial y=ex describe tan eficientemente estos cambios es que su derivada dy/dx = ex; es decir, ex es su propia derivada. Esto significa que la tasa de cambio de y es idéntica a su valor en cualquier punto, lo cual es la definición misma de un proceso de primer orden.
Sistemas de Primer Orden en Otros Campos
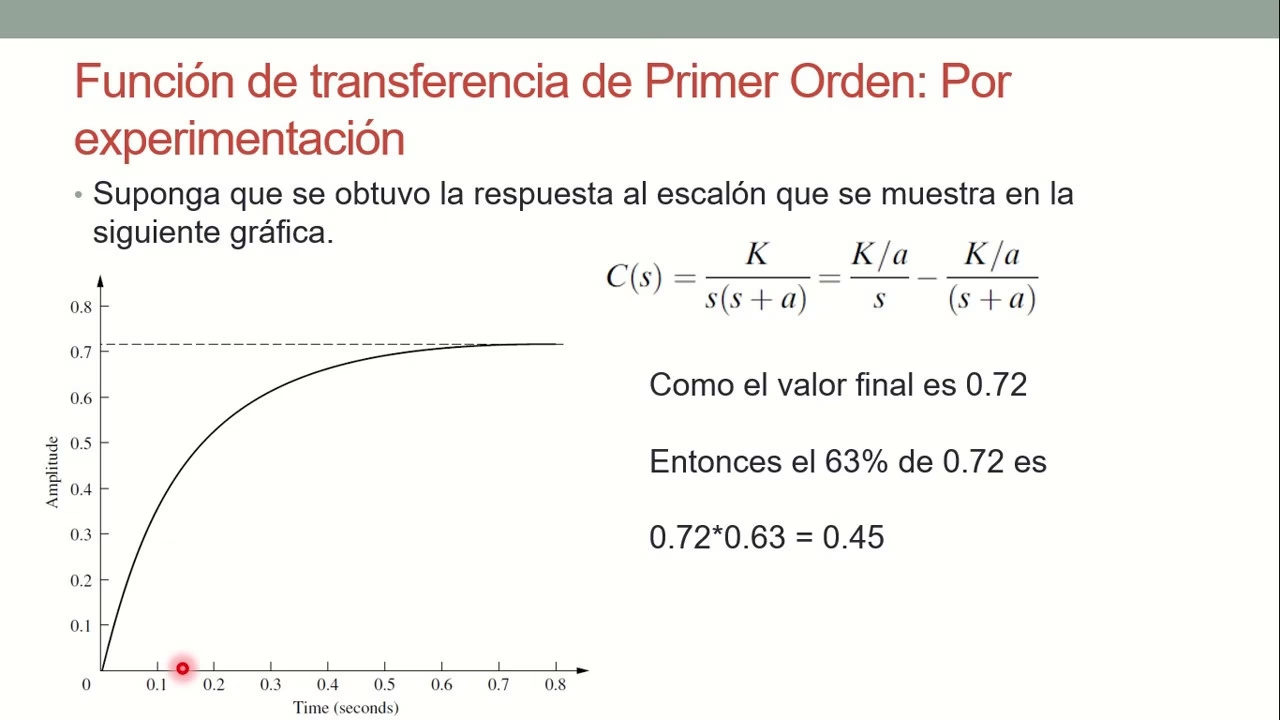
El concepto de 'primer orden' no se limita solo a la química. En ingeniería, especialmente en control de sistemas, se habla de 'sistemas de primer orden' para describir aquellos cuya dinámica puede ser modelada por una ecuación diferencial de primer orden. Un ejemplo clásico es la respuesta al escalón de un sistema de primer orden.
La ecuación de salida para la respuesta al escalón (cuando la entrada cambia abruptamente de cero a un valor constante) de un sistema de primer orden es:
c(t) = K(1 - e-t/T)
Donde c(t) es la salida del sistema en el tiempo t, K es la ganancia final del sistema (el valor estacionario al que tiende la salida), y T es la constante de tiempo del sistema. La constante de tiempo T es análoga a 1/k en la cinética química y representa el tiempo que tarda el sistema en alcanzar aproximadamente el 63.2% de su valor final. Esta fórmula muestra cómo el sistema se acerca exponencialmente a su nuevo estado de equilibrio después de una perturbación.
Identificación de Ecuaciones Diferenciales Lineales de Primer Orden
En el ámbito de las matemáticas puras, una ecuación diferencial lineal de primer orden es aquella que puede expresarse en la forma general:
dy/dx + p(x)y = f(x)
Aquí, dy/dx es la derivada de la función y con respecto a x, y p(x) y f(x) son funciones continuas de x. La característica 'lineal' se refiere a que la función dependiente y y su derivada dy/dx aparecen con una potencia de uno y no se multiplican entre sí. El 'primer orden' se refiere a la derivada de mayor orden presente en la ecuación (en este caso, la primera derivada).

Si f(x) ≡ 0, la ecuación se denomina homogénea. Las ecuaciones diferenciales de primer orden son fundamentales para modelar una vasta gama de fenómenos físicos, biológicos y económicos, y las reacciones de primer orden son un caso específico de estas ecuaciones, donde p(x) = k (una constante) y f(x) = 0 (homogénea).
Tabla Comparativa: Leyes de Velocidad Diferenciales vs. Integradas
| Característica | Ley de Velocidad Diferencial | Ley de Velocidad Integrada |
|---|---|---|
| Propósito Principal | Describe la velocidad instantánea de la reacción en función de las concentraciones. | Relaciona las concentraciones de reactivos con el tiempo transcurrido. |
| Uso Principal | Comprender el mecanismo molecular y la dependencia de la velocidad en un instante dado. | Determinar el orden de reacción y la constante de velocidad a partir de datos experimentales de concentración vs. tiempo. |
| Forma para Primer Orden | Velocidad = -d[A]/dt = k[A] | ln[A] = -kt + ln[A]₀ o [A] = [A]₀e-kt |
| Tipo de Datos Requeridos | Velocidades iniciales o instantáneas para diferentes concentraciones. | Concentraciones de reactivos medidas en diferentes intervalos de tiempo. |
| Representación Gráfica | No es directamente lineal para determinar el orden (requiere análisis de pendientes o log-log). | ln[A] vs. t da una línea recta para reacciones de primer orden. |
Preguntas Frecuentes (FAQ)
¿Cuál es la fórmula para una reacción de primer orden?
La fórmula principal, conocida como la ley de velocidad integrada para una reacción de primer orden (A → productos), es ln[A]t = -kt + ln[A]₀. Aquí, [A]t es la concentración del reactivo A en el tiempo t, [A]₀ es la concentración inicial de A, y k es la constante de velocidad. Esta ecuación también puede expresarse en su forma exponencial como [A]t = [A]₀e-kt.
¿Cómo determinar si una reacción es de primer orden?
Para determinar si una reacción es de primer orden, se deben medir las concentraciones del reactivo a diferentes tiempos. Luego, se grafica el logaritmo natural de la concentración del reactivo (ln[A]) en el eje Y contra el tiempo (t) en el eje X. Si el gráfico resultante es una línea recta con una pendiente negativa, la reacción es de primer orden. La pendiente de esta línea será igual a -k (el negativo de la constante de velocidad).
¿Cuál es la fórmula para la respuesta al escalón de un sistema de primer orden?
La fórmula para la salida c(t) de la respuesta al escalón de un sistema de primer orden es c(t) = K(1 - e-t/T). En esta ecuación, K representa la ganancia o valor final al que tiende la salida del sistema, t es el tiempo, y T es la constante de tiempo del sistema, que indica la rapidez con la que el sistema responde al cambio en la entrada.
¿Cómo se identifica una ecuación diferencial lineal de primer orden?
Una ecuación diferencial lineal de primer orden se identifica por su forma estándar: dy/dx + p(x)y = f(x). Aquí, dy/dx es la primera derivada de la función y con respecto a x. Las funciones p(x) y f(x) deben ser continuas. La clave es que y y su derivada dy/dx aparecen con una potencia de uno y no están multiplicadas entre sí, y la derivada de mayor orden presente es la primera.
Si quieres conocer otros artículos parecidos a Reacciones y Sistemas de Primer Orden: Guía Completa puedes visitar la categoría Química.
