28/07/2023
En el vasto y fascinante mundo de la química, los enlaces entre átomos son los cimientos sobre los que se construye toda la materia. Pero estos enlaces no siempre son iguales; algunos son como un tira y afloja equilibrado, mientras que otros son una lucha desigual por los electrones. Esta característica, fundamental para entender el comportamiento de las sustancias, se conoce como la polaridad de un enlace. Comprender cómo calcularla no solo es clave para los estudiantes de química, sino para cualquiera que desee desentrañar los misterios de cómo interactúan las moléculas.
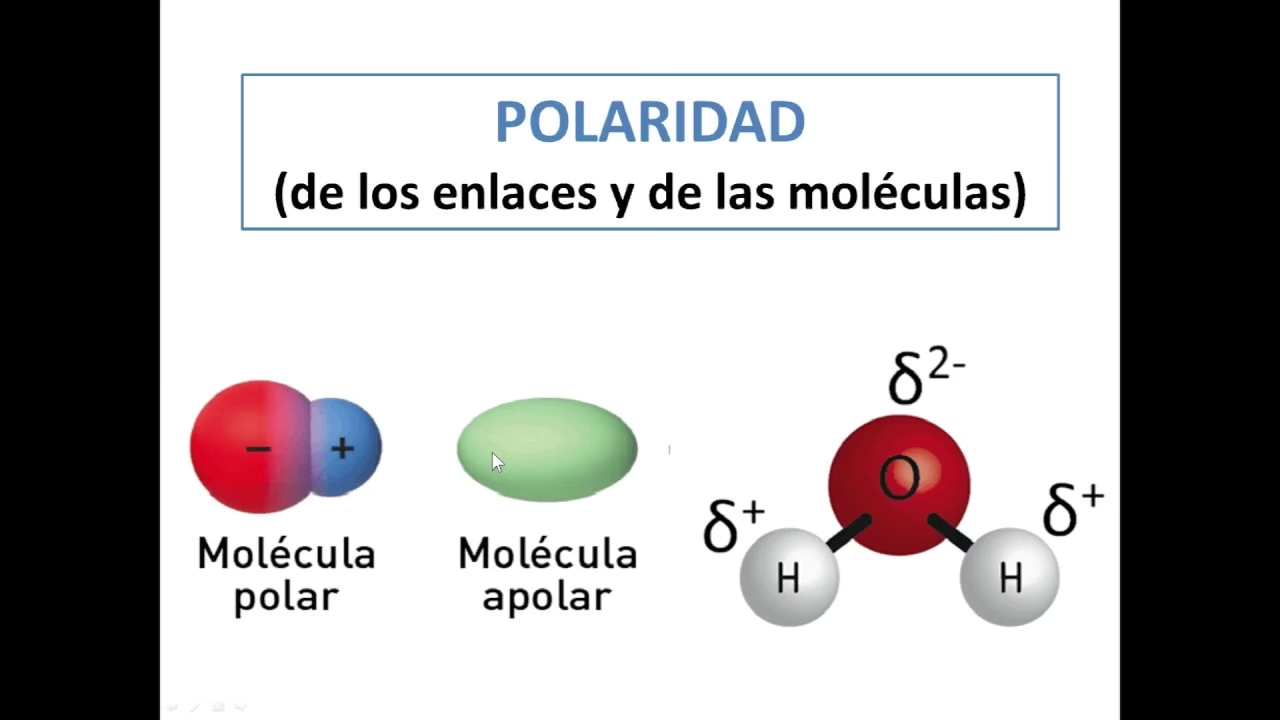
La polaridad es una propiedad que describe la separación de cargas eléctricas dentro de una molécula o, más específicamente, dentro de un enlace entre dos átomos. Esta separación de cargas se debe a una distribución desigual de los electrones que participan en el enlace. Imagina un par de electrones compartidos entre dos átomos: si ambos átomos los atraen con la misma fuerza, los electrones se mantendrán centrados. Sin embargo, si uno de los átomos tiene una “sed” mayor por los electrones, los atraerá más hacia sí, creando una región con una ligera carga negativa y dejando al otro átomo con una ligera carga positiva. Esta asimetría es lo que define la polaridad y es el punto de partida para entender por qué el agua, la sal o el aceite se comportan de maneras tan diferentes.
¿Qué es la Polaridad de un Enlace Químico?
La polaridad de un enlace se refiere a la naturaleza de la distribución de la densidad electrónica entre los dos átomos que lo forman. En un enlace covalente, los átomos comparten pares de electrones para alcanzar una configuración electrónica más estable. Sin embargo, esta compartición no siempre es equitativa. La capacidad de un átomo para atraer hacia sí los electrones compartidos en un enlace se conoce como electronegatividad. Es una propiedad periódica fundamental que nos permite predecir la polaridad de un enlace.
Cuando dos átomos se unen, la diferencia en sus valores de electronegatividad determina la naturaleza del enlace. Si los átomos tienen electronegatividades muy similares o idénticas, los electrones se comparten de manera equitativa, resultando en un enlace covalente no polar. Un ejemplo clásico es la molécula de oxígeno (O₂), donde ambos átomos de oxígeno tienen la misma electronegatividad y los electrones se comparten por igual. No hay una separación de carga significativa.
Por otro lado, si los átomos tienen electronegatividades diferentes, el átomo más electronegativo atraerá con mayor fuerza el par de electrones compartidos. Esto provoca que los electrones pasen más tiempo cerca del átomo más electronegativo, generando una densidad de carga parcial negativa (δ-) en ese átomo y una densidad de carga parcial positiva (δ+) en el átomo menos electronegativo. Esta separación de cargas dentro del enlace se denomina dipolo eléctrico, y el enlace se clasifica como covalente polar. El agua (H₂O) es un ejemplo perfecto: el oxígeno es más electronegativo que el hidrógeno, atrayendo los electrones de los enlaces O-H hacia sí y creando dipolos.

En casos extremos, cuando la diferencia de electronegatividad es muy grande, el átomo más electronegativo “arranca” completamente los electrones del átomo menos electronegativo, formando iones. Este tipo de enlace se conoce como enlace iónico, y aunque no es un enlace covalente en el sentido estricto de compartir electrones, es el resultado de una polaridad extrema.
Cómo Calcular la Polaridad de un Enlace
La forma más directa y común de determinar la polaridad de un enlace es calculando la diferencia de electronegatividad entre los dos átomos involucrados. Para ello, se utilizan escalas de electronegatividad, siendo la escala de Pauling la más ampliamente aceptada y utilizada. En esta escala, al flúor (el elemento más electronegativo) se le asigna un valor de 4.0, y los valores disminuyen progresivamente hacia el cesio y el francio (los menos electronegativos, con valores de aproximadamente 0.7).
Una vez que se conocen los valores de electronegatividad de los dos átomos, se resta el valor menor al mayor para obtener la diferencia. Basándose en esta diferencia, se aplican las siguientes pautas generales para clasificar la polaridad del enlace:
| Diferencia de Electronegatividad | Tipo de Enlace | Características |
|---|---|---|
| Menor de 0.5 | Covalente No Polar | Electrones compartidos casi por igual. No hay separación significativa de carga. |
| Entre 0.5 y 1.7 | Covalente Polar | Electrones compartidos de forma desigual. Se forma un dipolo eléctrico. |
| Mayor de 1.7 | Iónico | Transferencia completa de electrones de un átomo a otro, formando iones. |
Es importante recordar que estas son pautas generales y pueden existir algunas excepciones o casos límite. Por ejemplo, un enlace con una diferencia de electronegatividad de 1.7 podría ser considerado polar covalente o iónico dependiendo del contexto y de otras propiedades del compuesto.
Ejemplos de Cálculo de Polaridad de Enlaces:
- Molécula de Cloro (Cl₂): Electronegatividad de Cl = 3.16. Diferencia = 3.16 - 3.16 = 0.0. Enlace no polar.
- Ácido Clorhídrico (HCl): Electronegatividad de H = 2.20, Cl = 3.16. Diferencia = 3.16 - 2.20 = 0.96. Enlace covalente polar. El cloro atrae más los electrones.
- Fluoruro de Hidrógeno (HF): Electronegatividad de H = 2.20, F = 3.98. Diferencia = 3.98 - 2.20 = 1.78. Aunque está justo en el límite, se considera un enlace covalente polar muy fuerte, casi iónico.
- Cloruro de Potasio (KCl): Electronegatividad de K = 0.82, Cl = 3.16. Diferencia = 3.16 - 0.82 = 2.34. Enlace iónico. El cloro “roba” un electrón del potasio.
Electronegatividad: El Motor de la Polaridad
La electronegatividad es una medida de la tendencia de un átomo a atraer un par de electrones de enlace hacia sí mismo. Es una propiedad crucial que se ve influenciada por varios factores atómicos:
- Carga Nuclear: Los protones cargados positivamente en el núcleo atraen a los electrones cargados negativamente. A medida que aumenta el número de protones en el núcleo, la atracción y, por lo tanto, la electronegatividad aumentan.
- Distancia al Núcleo: La fuerza de atracción entre cargas disminuye rápidamente con la distancia. Los electrones de valencia (los que participan en el enlace) que están más lejos del núcleo sienten una atracción menor.
- Apantallamiento (Efecto Pantalla): Los electrones internos “apantallan” o “protegen” a los electrones de valencia de la atracción total del núcleo. Cuantos más electrones internos haya, mayor será el apantallamiento y menor la electronegatividad.
Tendencias de la Electronegatividad en la Tabla Periódica:
- A lo largo de un Periodo (de izquierda a derecha): La electronegatividad generalmente aumenta. Esto se debe a que, a medida que avanzamos en un periodo, el número de protones en el núcleo aumenta, incrementando la carga nuclear efectiva. Los electrones de valencia se encuentran en el mismo nivel de energía (o capa), por lo que el apantallamiento no aumenta significativamente. La mayor carga nuclear atrae con más fuerza a los electrones de enlace. Por ejemplo, en el periodo 3, el sodio es poco electronegativo, mientras que el cloro es muy electronegativo.
- Descendiendo en un Grupo (de arriba a abajo): La electronegatividad generalmente disminuye. Aunque la carga nuclear aumenta, los electrones de valencia se encuentran en capas de energía cada vez más alejadas del núcleo y hay un mayor número de electrones internos que apantallan la carga nuclear. Esto reduce la atracción efectiva del núcleo sobre los electrones de enlace, haciendo que los átomos sean menos electronegativos. El flúor es el elemento más electronegativo, y a medida que descendemos en el grupo de los halógenos (Cl, Br, I), su electronegatividad disminuye.
Polaridad de Moléculas: Más Allá del Enlace
Es crucial entender que la polaridad de un enlace no siempre se traduce directamente en la polaridad de la molécula en su conjunto. Una molécula puede contener enlaces polares y, sin embargo, ser una molécula no polar globalmente. Esto depende de la geometría molecular y de la disposición espacial de los dipolos de los enlaces.
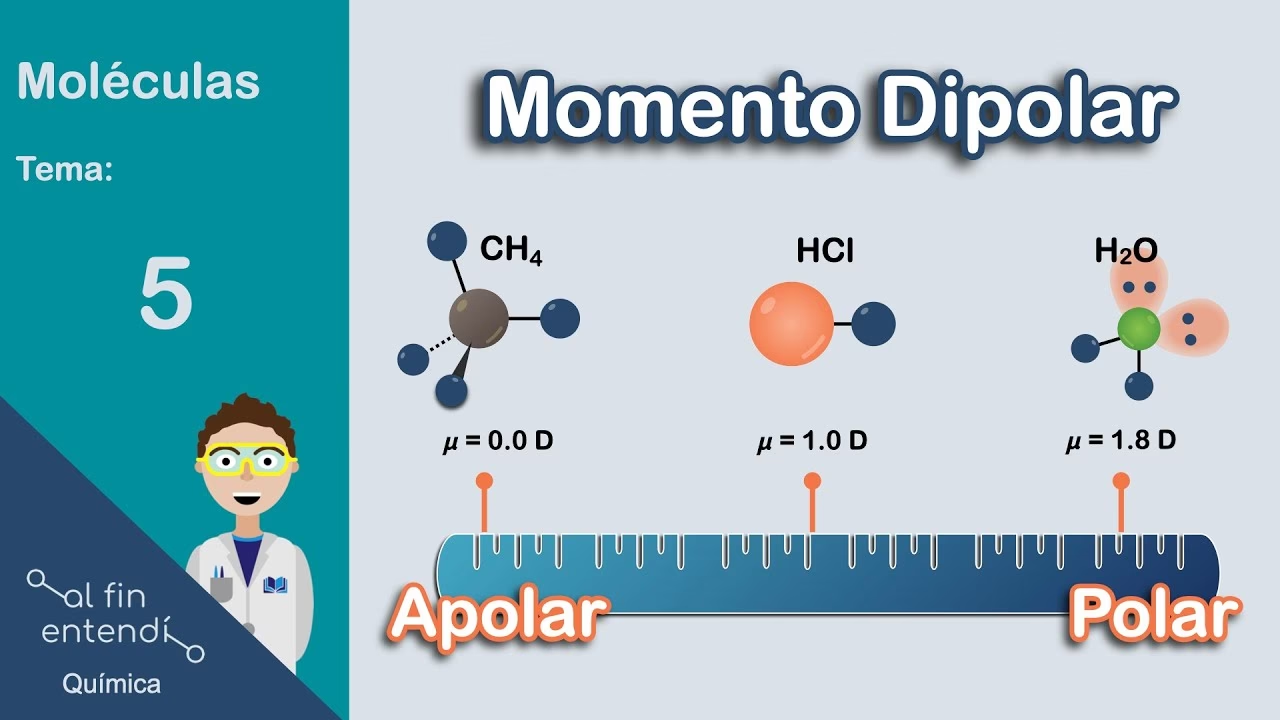
La polaridad de una molécula se determina sumando vectorialmente los momentos dipolares individuales de cada enlace. El momento dipolar eléctrico es una magnitud vectorial que mide la separación de cargas; su dirección va de la carga negativa a la positiva y su módulo es igual al producto de la carga por la distancia que las separa. Si la suma vectorial de todos los momentos dipolares de los enlaces de una molécula es nula (es decir, se cancelan entre sí), la molécula es apolar. Si la suma es diferente de cero, la molécula es polar.
- Moléculas con enlaces no polares: Si una molécula solo contiene enlaces no polares (como O₂ o N₂), su momento dipolar total será nulo, y la molécula será siempre apolar.
- Moléculas con enlaces polares y geometría simétrica: Aquí es donde la distinción es importante. Consideremos el dióxido de carbono (CO₂). Contiene dos enlaces C=O, que son polares debido a la diferencia de electronegatividad entre el carbono y el oxígeno. Sin embargo, la molécula de CO₂ tiene una geometría lineal. Los dos dipolos de enlace están orientados en direcciones opuestas y se cancelan mutuamente, resultando en una molécula de CO₂ no polar en su conjunto. Otro ejemplo es el tetracloruro de carbono (CCl₄), que tiene cuatro enlaces C-Cl polares. Pero, debido a su geometría tetraédrica simétrica, los momentos dipolares de los enlaces se anulan, haciendo que el CCl₄ sea una molécula no polar.
- Moléculas con enlaces polares y geometría asimétrica: El ejemplo más conocido es el agua (H₂O). El agua tiene dos enlaces O-H polares. Sin embargo, la molécula de agua tiene una geometría “angular” o en “V” debido a los pares de electrones no enlazantes en el oxígeno. Esta forma angular impide que los momentos dipolares de los enlaces se cancelen. En cambio, se suman, creando un momento dipolar neto significativo que hace que la molécula de agua sea fuertemente polar. El lado del oxígeno adquiere una carga parcial negativa, y los lados de los hidrógenos adquieren cargas parciales positivas.
En resumen, para determinar la polaridad de una molécula, no solo basta con identificar si tiene enlaces polares, sino que es fundamental considerar su estructura tridimensional y la simetría de la distribución de los dipolos.
La Importancia de la Polaridad en la Química y la Biología
La polaridad, tanto de los enlaces como de las moléculas, es una propiedad de inmensa importancia que influye en casi todas las demás propiedades físicas y químicas de una sustancia. Sus implicaciones son vastas y se manifiestan en diversos fenómenos:
- Solubilidad: Uno de los principios más conocidos en química es “semejante disuelve a semejante”. Esto significa que los solventes polares (como el agua) disuelven sustancias polares o iónicas (como la sal común, NaCl), mientras que los solventes apolares (como el hexano o el aceite) disuelven sustancias apolares (como grasas o ceras). Esta propiedad es crucial en la preparación de soluciones, en la industria farmacéutica y en procesos biológicos.
- Puntos de Fusión y Ebullición: Las moléculas polares, debido a sus cargas parciales, pueden interactuar entre sí a través de fuerzas intermoleculares más fuertes, como las fuerzas dipolo-dipolo y los puentes de hidrógeno (un tipo especial de interacción dipolo-dipolo). Estas fuerzas de atracción son más intensas que las fuerzas de dispersión de London (presentes en todas las moléculas, pero predominantes en las apolares). Para romper estas interacciones y pasar de un estado de agregación a otro (por ejemplo, de líquido a gas), se requiere más energía. Por lo tanto, las sustancias polares tienden a tener puntos de fusión y ebullición más altos que las sustancias apolares de masa molecular comparable.
- Fuerzas Intermoleculares: La polaridad es la base de las fuerzas intermoleculares que mantienen unidas a las moléculas. Estas fuerzas son determinantes en la viscosidad, la tensión superficial y la capilaridad de los líquidos.
- Reconocimiento Molecular: La polaridad permite a las moléculas “reconocerse” y unirse de forma específica. Este es un principio fundamental en la biología, donde enzimas interactúan con sustratos, anticuerpos con antígenos, y receptores con hormonas, todo basado en la complementariedad de forma y polaridad.
- Importancia Biológica (Moléculas Anfipáticas): Las moléculas anfipáticas son un claro ejemplo de la importancia biológica de la polaridad. Estas moléculas poseen regiones tanto polares (hidrofílicas, que “aman” el agua) como apolares (hidrofóbicas, que “odian” el agua). Los fosfolípidos, componentes principales de las membranas celulares, son moléculas anfipáticas. En un entorno acuoso, se autoorganizan en bicapas lipídicas, con las “cabezas” polares hacia el exterior (en contacto con el agua) y las “colas” apolares hacia el interior (alejadas del agua). Esta estructura es la base de la compartimentación celular y es vital para la vida.
- Identificación de Compuestos: La polaridad puede ayudar a diferenciar isómeros o compuestos con estructuras similares pero propiedades muy diferentes, como el cis-dicloroetano (polar) y el trans-dicloroetano (apolar).
Preguntas Frecuentes sobre la Polaridad
¿Qué es un dipolo eléctrico?
Un dipolo eléctrico es una separación de cargas opuestas (una parcial positiva y una parcial negativa) dentro de un enlace o una molécula. Se forma cuando los electrones se distribuyen de manera desigual, creando dos “polos” con cargas opuestas. El momento dipolar es una medida de la magnitud de este dipolo.
¿Siempre que hay enlaces polares, la molécula es polar?
No, no siempre. Una molécula puede contener enlaces polares pero ser no polar en su conjunto si su geometría molecular es simétrica. En estos casos, los momentos dipolares individuales de los enlaces se cancelan entre sí vectorialmente, resultando en un momento dipolar molecular neto de cero. Ejemplos incluyen el CO₂ (lineal) y el CCl₄ (tetraédrico).

¿Cómo afecta la polaridad a la solubilidad?
La polaridad afecta la solubilidad siguiendo la regla “semejante disuelve a semejante”. Las sustancias polares se disuelven bien en solventes polares (como el agua), y las sustancias apolares se disuelven bien en solventes apolares (como el benceno o el éter). Esto se debe a que las interacciones entre soluto y solvente son más fuertes cuando sus polaridades son similares.
¿Qué es la escala de Pauling de electronegatividad?
La escala de Pauling es la escala más utilizada para cuantificar la electronegatividad de los elementos. Fue desarrollada por Linus Pauling y asigna un valor numérico a la capacidad de un átomo para atraer electrones en un enlace químico. El flúor es el elemento con la electronegatividad más alta (4.0 en la escala de Pauling), mientras que el cesio y el francio tienen los valores más bajos (aproximadamente 0.7).
¿Por qué el agua (H₂O) es una molécula tan polar?
El agua es una molécula fuertemente polar debido a dos factores principales: primero, los enlaces O-H son polares porque el oxígeno es significativamente más electronegativo que el hidrógeno. Segundo, la molécula de agua tiene una geometría angular (en “V”), no lineal. Esta forma asimétrica, causada por los dos pares de electrones no enlazantes en el átomo de oxígeno, impide que los momentos dipolares de los dos enlaces O-H se cancelen. En cambio, se suman, creando un momento dipolar molecular neto considerable, con una densidad de carga negativa en el oxígeno y una positiva en los hidrógenos.
Conclusión
La polaridad de los enlaces y de las moléculas es un concepto fundamental en la química que va mucho más allá de una simple clasificación. Al entender cómo calcular la polaridad a través de la diferencia de electronegatividad y cómo la geometría molecular influye en la polaridad global, podemos predecir y explicar una vasta gama de propiedades físicas y químicas de las sustancias. Desde la solubilidad de la sal en agua hasta la formación de las membranas celulares, la polaridad es el motor invisible que rige las interacciones a nivel molecular. Dominar este concepto no solo enriquece nuestra comprensión del mundo microscópico, sino que también nos proporciona herramientas poderosas para manipular y diseñar materiales con propiedades específicas, abriendo un sinfín de posibilidades en la ciencia y la tecnología.
Si quieres conocer otros artículos parecidos a ¿Cómo Calcular la Polaridad de un Enlace? puedes visitar la categoría Química.
