24/02/2026
El pH es una medida fundamental en química que nos permite cuantificar la acidez o alcalinidad de una solución. Desde la química de los alimentos hasta la biología de nuestro propio cuerpo, pasando por innumerables procesos industriales, comprender y calcular el pH es esencial. No es solo un número, sino un indicador crítico que revela la concentración de iones de hidrógeno (H+) en una solución, afectando directamente las propiedades y reacciones de las sustancias.
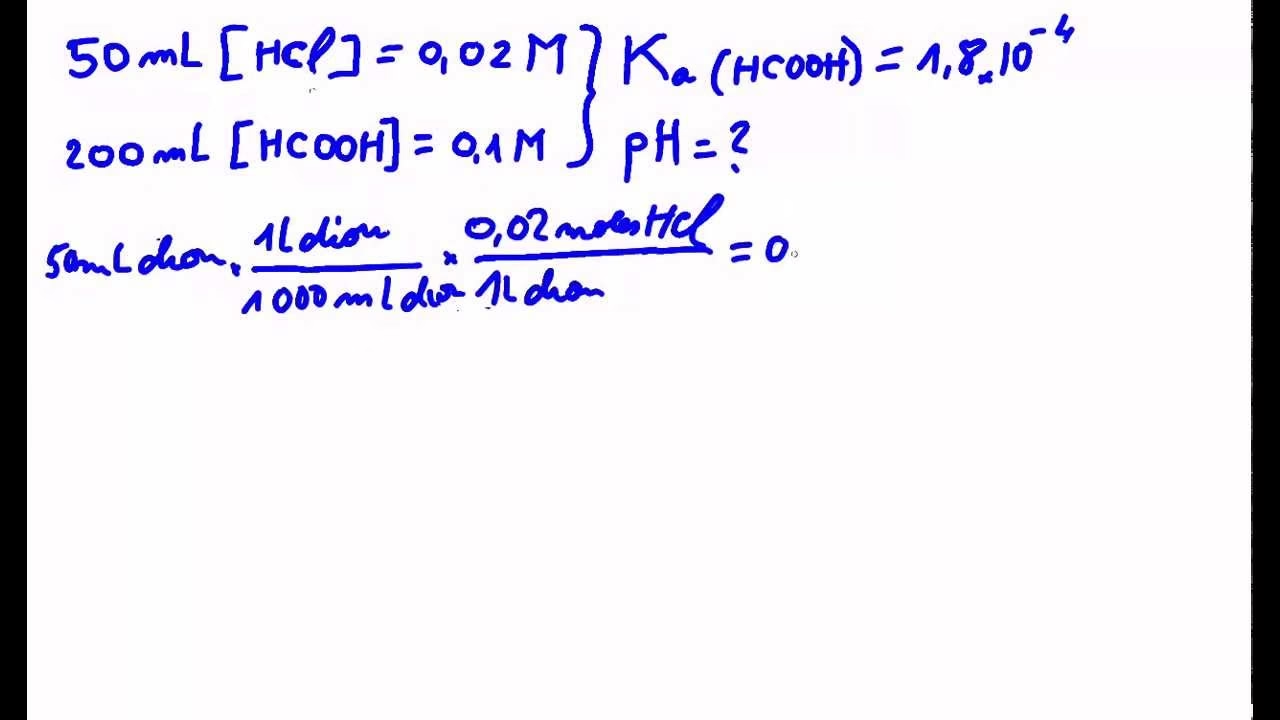
Aunque el concepto de pH parece sencillo, su cálculo puede volverse complejo, especialmente cuando se trata de ácidos o bases débiles, mezclas de diferentes sustancias o cuando se utilizan conceptos como la normalidad. En este artículo, desglosaremos paso a paso cómo abordar estos cálculos, proporcionando una comprensión clara y práctica que te permitirá dominar este aspecto crucial de la química.
- Comprendiendo el pH: Un Indicador Crucial
- Cálculo del pH a partir de Ka y Kb: La Clave para Ácidos y Bases Débiles
- Paso 1: Introducción a las Constantes Ka y Kb
- Paso 2: Entendiendo Ácidos y Bases Débiles en Equilibrio
- Paso 3: Estableciendo la Expresión de Equilibrio
- Paso 4: Realizando Suposiciones para Simplificación
- Paso 5: Resolviendo la Concentración del Ion Hidronio
- Paso 6: Calculando el pH
- Paso 7: Ejemplo de Cálculo
- Relación entre Ka y Kb
- Calculando el pH de una Mezcla: Un Desafío de Equilibrio
- El pH y la Normalidad: Una Perspectiva en Concentración
- Preguntas Frecuentes (FAQ)
- Conclusión
Comprendiendo el pH: Un Indicador Crucial
El término pH fue introducido por el químico danés Søren Peder Lauritz Sørensen en 1909 y se define como el logaritmo negativo de base 10 de la concentración molar de iones de hidrógeno (H+) o iones hidronio (H3O+) en una solución. Matemáticamente, se expresa como:
pH = -log[H+]
De manera análoga, para medir la alcalinidad, utilizamos el pOH, que se relaciona con la concentración de iones hidroxilo (OH-):
pOH = -log[OH-]
En soluciones acuosas a 25°C, existe una relación fundamental entre el pH y el pOH, basada en el producto iónico del agua (Kw), que es 1.0 x 10^-14:
pH + pOH = 14
Esta escala de 0 a 14 nos permite clasificar las soluciones: un pH menor a 7 indica una solución ácida, un pH igual a 7 indica una solución neutra, y un pH mayor a 7 indica una solución básica o alcalina. La precisión en el cálculo del pH es vital para muchas aplicaciones, desde ajustar el pH de una piscina hasta formular medicamentos.
Cálculo del pH a partir de Ka y Kb: La Clave para Ácidos y Bases Débiles
A diferencia de los ácidos y bases fuertes, que se disocian completamente en agua, los ácidos y bases débiles solo se disocian parcialmente. Esta disociación incompleta significa que el equilibrio químico juega un papel fundamental en la determinación de sus concentraciones iónicas y, por ende, de su pH. Aquí es donde entran en juego las constantes de disociación ácida (Ka) y básica (Kb).
Paso 1: Introducción a las Constantes Ka y Kb
La constante de disociación ácida, Ka, es una medida de la fuerza de un ácido débil. Cuanto mayor sea el valor de Ka, más fuerte será el ácido (es decir, mayor será su grado de disociación). Para un ácido débil genérico, HX, que se disocia en agua:
HX(aq) + H2O(l) ⇌ H3O+(aq) + X-(aq)
La expresión de Ka es:
Ka = ([H3O+][X-]) / [HX]
Similarmente, la constante de disociación básica, Kb, mide la fuerza de una base débil. Para una base débil genérica, B:
B(aq) + H2O(l) ⇌ BH+(aq) + OH-(aq)
La expresión de Kb es:
Kb = ([BH+][OH-]) / [B]
Paso 2: Entendiendo Ácidos y Bases Débiles en Equilibrio
Como mencionamos, los ácidos y bases débiles no se disocian completamente en agua. Esta disociación parcial implica que la expresión de equilibrio para ácidos débiles debe considerar tanto el ácido no disociado como los iones producidos. Para ácidos débiles, la disociación general se puede representar como:
HX + H2O ⇌ H3O+ + X-
Donde HX es el ácido débil, H3O+ es el ion hidronio y X- es la base conjugada. La expresión de Ka para este equilibrio es:
Ka = ([H3O+][X-]) / [HX]
Paso 3: Estableciendo la Expresión de Equilibrio
Para encontrar el pH de una solución de ácido débil, comenzamos estableciendo la expresión de equilibrio. Consideremos un ácido débil HX con una concentración inicial 'a'. En el equilibrio, la concentración de HX será 'a - b', donde 'b' es la cantidad que se disocia. Las concentraciones de H3O+ y X- en el equilibrio serán ambas 'b'. Así, la expresión de Ka se convierte en:
Ka = ([H3O+][X-]) / [HX] = b^2 / (a - b)
Paso 4: Realizando Suposiciones para Simplificación
Dado que los ácidos débiles no se disocian completamente, 'b' es típicamente mucho menor que 'a'. Esto nos permite hacer la suposición de que 'a - b' es aproximadamente igual a 'a'. Esto simplifica la expresión de Ka a:
Ka ≈ b^2 / a
Esta suposición es válida para la mayoría de los ácidos débiles, donde el grado de disociación es menor al 5%. Si el grado de disociación es mayor, se debe resolver la ecuación cuadrática completa.
Paso 5: Resolviendo la Concentración del Ion Hidronio
Para encontrar la concentración de H3O+ (que es 'b'), reordenamos la expresión simplificada de Ka:
b^2 = Ka * a
b = √(Ka * a)
Al sustituir los valores conocidos de Ka y 'a', podemos calcular la concentración de H3O+.
Paso 6: Calculando el pH
Una vez que tenemos la concentración de H3O+, podemos encontrar el pH de la solución utilizando la fórmula:
pH = -log[H3O+]
Sustituye el valor de [H3O+] obtenido del paso anterior para calcular el pH.
Paso 7: Ejemplo de Cálculo
Consideremos un ejemplo con ácido metanoico 0.1 M (HCOOH) con un Ka de 1.8 x 10^-4. Usando la expresión simplificada de Ka:
b = √(1.8 x 10^-4 * 0.1)
b = √(1.8 x 10^-5)
b ≈ 4.24 x 10^-3 M
Luego, el pH se calcula como:
pH = -log(4.24 x 10^-3) ≈ 2.37
Relación entre Ka y Kb
Para un par ácido-base conjugado, Ka y Kb están relacionados por el producto iónico del agua (Kw) a una temperatura dada (usualmente 25°C, donde Kw = 1.0 x 10^-14):
Ka * Kb = Kw
Esta relación es crucial. Si conoces el Ka de un ácido débil, puedes calcular el Kb de su base conjugada (y viceversa). Una vez que tienes Kb, el proceso para calcular el pOH (y luego el pH) de una base débil es análogo al cálculo del pH de un ácido débil. Primero, usa Kb para encontrar [OH-], luego calcula pOH = -log[OH-], y finalmente pH = 14 - pOH.
Calculando el pH de una Mezcla: Un Desafío de Equilibrio
Calcular el pH de una solución que contiene una mezcla de ácidos y/o bases puede ser más complejo, ya que las interacciones entre las especies deben ser consideradas. La clave es identificar las especies predominantes y las reacciones de neutralización que puedan ocurrir.
Mezcla de Ácidos Fuertes y Bases Fuertes
Cuando se mezclan un ácido fuerte y una base fuerte, ocurre una reacción de neutralización. El enfoque es determinar cuál de los iones (H+ o OH-) está en exceso después de la reacción. Los pasos son:
- Calcular los moles de H+ aportados por el ácido fuerte y los moles de OH- aportados por la base fuerte.
- Restar los moles del ion limitante de los moles del ion en exceso para encontrar los moles netos del ion remanente.
- Calcular el volumen total de la mezcla.
- Dividir los moles netos del ion remanente por el volumen total para obtener la concentración molar del ion en exceso.
- Calcular el pH o pOH según corresponda.
Por ejemplo, si mezclas 50 mL de HCl 0.1 M con 50 mL de NaOH 0.05 M:
- Moles H+ = 0.050 L * 0.1 mol/L = 0.005 moles
- Moles OH- = 0.050 L * 0.05 mol/L = 0.0025 moles
- Moles H+ en exceso = 0.005 - 0.0025 = 0.0025 moles
- Volumen total = 0.050 L + 0.050 L = 0.100 L
- [H+] = 0.0025 moles / 0.100 L = 0.025 M
- pH = -log(0.025) ≈ 1.60
Mezcla de Ácido Fuerte y Ácido Débil
En la mayoría de los casos, la contribución de H+ del ácido débil es insignificante en comparación con la del ácido fuerte. Por lo tanto, el pH de la mezcla estará determinado casi exclusivamente por el ácido fuerte. Solo en situaciones donde el ácido fuerte es extremadamente diluido y el ácido débil es relativamente concentrado y no tan débil, se debería considerar la contribución del ácido débil, lo cual implicaría un sistema de ecuaciones de equilibrio más complejo.
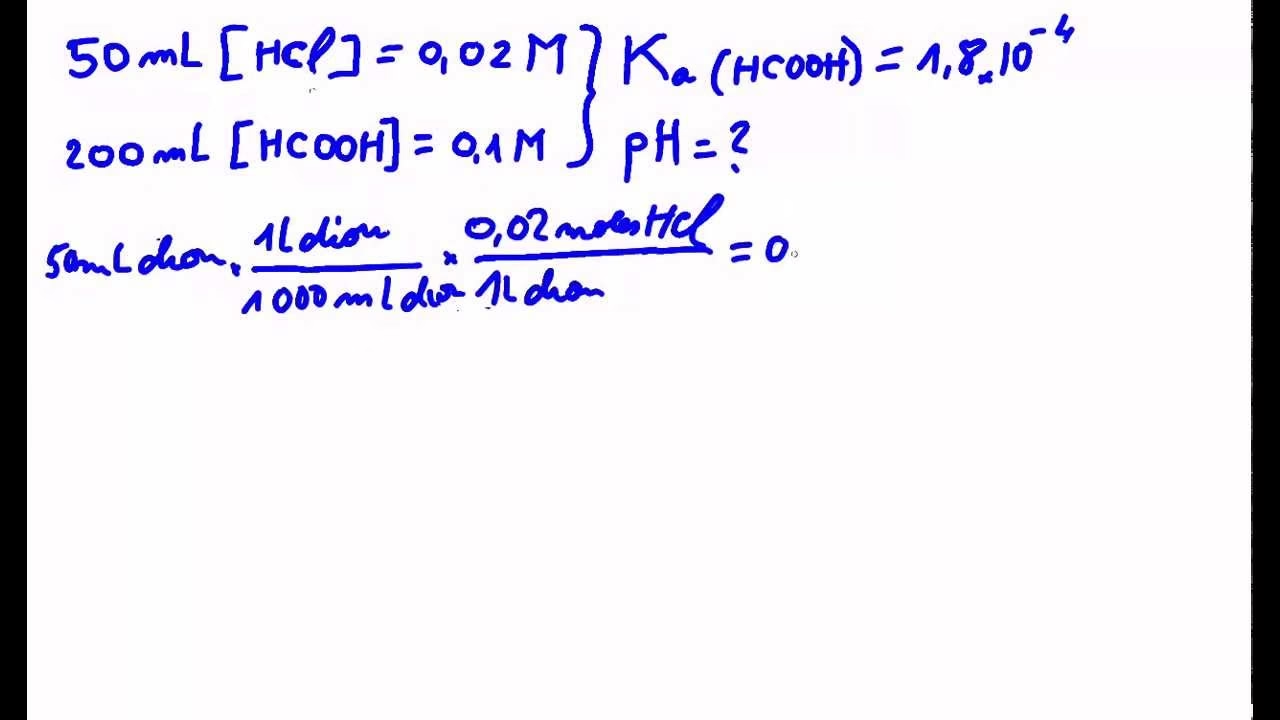
Mezcla de Ácido/Base Débil y su Sal (Soluciones Amortiguadoras o Buffer)
Las soluciones que contienen un ácido débil y su base conjugada (o una base débil y su ácido conjugado) se conocen como soluciones amortiguadoras o buffer. Estas soluciones resisten cambios significativos en el pH al añadir pequeñas cantidades de ácido o base. El pH de estas soluciones se puede calcular utilizando la ecuación de Henderson-Hasselbalch:
Para un ácido débil y su base conjugada:
pH = pKa + log([Base Conjugada] / [Ácido Débil])
Donde pKa = -log(Ka).
Para una base débil y su ácido conjugado:
pOH = pKb + log([Ácido Conjugado] / [Base Débil])
Donde pKb = -log(Kb).
La ecuación de Henderson-Hasselbalch es una herramienta poderosa para predecir y diseñar soluciones buffer, que son fundamentales en bioquímica y muchas otras áreas.
Consideraciones Generales para Mezclas
Al abordar cualquier mezcla, es crucial:
- Identificar todas las especies presentes y sus propiedades (fuerte/débil, ácido/base).
- Escribir las reacciones de neutralización que puedan ocurrir primero.
- Luego, considerar los equilibrios de disociación de ácidos/bases débiles si quedan.
- Recordar que la autoionización del agua ([H+] = [OH-] = 10^-7 M) solo es relevante en soluciones extremadamente diluidas o cercanas a la neutralidad.
El pH y la Normalidad: Una Perspectiva en Concentración
La normalidad (N) es otra unidad de concentración que se utiliza a menudo en química, especialmente en reacciones de neutralización y titulaciones ácido-base. Se define como el número de equivalentes por litro de solución.
¿Qué es un Equivalente?
Para ácidos, un equivalente es la cantidad de ácido que puede donar un mol de iones H+. Para bases, un equivalente es la cantidad de base que puede aceptar un mol de iones H+ o donar un mol de iones OH-.
La relación entre normalidad y molaridad (M) es:
Normalidad (N) = Molaridad (M) * Factor de Equivalencia (n)
El factor de equivalencia (n) es el número de iones H+ (para ácidos) o OH- (para bases) que una molécula puede donar o aceptar en una reacción. Por ejemplo:
- Para HCl (ácido monoprótico): n = 1 (1 H+ por molécula). Entonces, una solución 1 M de HCl es 1 N.
- Para H2SO4 (ácido diprótico): n = 2 (2 H+ por molécula). Entonces, una solución 1 M de H2SO4 es 2 N.
- Para Ca(OH)2 (base con dos OH-): n = 2 (2 OH- por molécula). Entonces, una solución 1 M de Ca(OH)2 es 2 N.
Cálculo del pH Usando Normalidad para Ácidos y Bases Fuertes
Para ácidos y bases fuertes, la normalidad puede simplificar el cálculo del pH porque nos da directamente la concentración de los iones H+ u OH- que son relevantes para el pH.
- Si tienes una solución de un ácido fuerte con normalidad N, entonces [H+] = N. Luego, calculas pH = -log(N).
- Si tienes una solución de una base fuerte con normalidad N, entonces [OH-] = N. Luego, calculas pOH = -log(N) y finalmente pH = 14 - pOH.
Es importante recordar que esta simplificación solo aplica para ácidos y bases fuertes, donde la disociación es completa.
Limitaciones de la Normalidad para Ácidos y Bases Débiles
Aunque se puede expresar la normalidad de una solución de ácido o base débil, no te da directamente la concentración de H+ u OH- disociados. Para ácidos y bases débiles, la normalidad indica la cantidad total de equivalentes que *podrían* reaccionar, pero la cantidad real de H+ u OH- en solución en un momento dado sigue dependiendo de su Ka o Kb y del equilibrio de disociación. Por lo tanto, para ácidos y bases débiles, la molaridad y las constantes Ka/Kb son más útiles para calcular el pH.
La normalidad es particularmente útil en titulaciones, donde la relación de equivalentes es 1:1 en el punto de equivalencia (N1V1 = N2V2), independientemente de la estequiometría de la reacción.
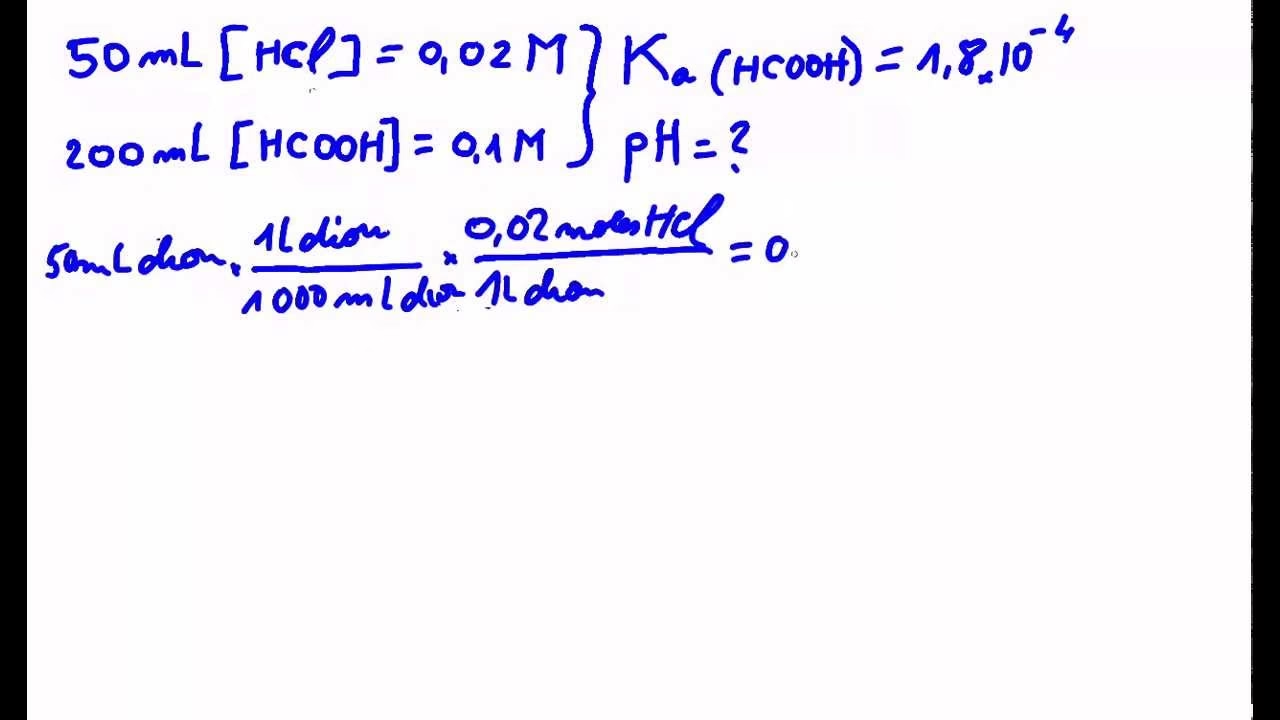
Preguntas Frecuentes (FAQ)
Para consolidar tu comprensión, abordemos algunas preguntas comunes sobre el cálculo del pH.
P: ¿Cuándo puedo usar la suposición de simplificación (a-b ≈ a) al calcular el pH de un ácido débil?
solvents. The assumption that 'a - b' is approximately 'a' (where 'a' is the initial concentration and 'b' is the amount dissociated) is generally valid when the degree of dissociation is less than 5%. Un criterio común es que si la concentración inicial del ácido 'a' es al menos 1000 veces mayor que el valor de Ka (es decir, a/Ka ≥ 1000), la suposición es válida y el error es menor al 5%. Si no se cumple esta condición, deberás resolver la ecuación cuadrática completa para 'b'.
P: ¿Qué sucede si mezclo un ácido fuerte con una base débil?
solvents. Cuando un ácido fuerte se mezcla con una base débil, ocurre una reacción de neutralización. El ácido fuerte protonará a la base débil, convirtiéndola en su ácido conjugado. Si el ácido fuerte es el reactivo limitante, la solución final contendrá la base débil original y su ácido conjugado, formando una solución amortiguadora. Si la base débil es el reactivo limitante, la solución final contendrá un exceso de ácido fuerte y el ácido conjugado de la base débil, y el pH estará dominado por el ácido fuerte restante. El cálculo se vuelve más complejo, involucrando la reacción de neutralización primero y luego un cálculo de equilibrio si se forma una solución buffer.
P: ¿Por qué no se usa la normalidad para calcular el pH de ácidos y bases débiles?
solvents. La normalidad representa el número total de equivalentes por litro, es decir, la capacidad total de un ácido o una base para donar o aceptar protones. Sin embargo, para ácidos y bases débiles, no todos los equivalentes se disocian en iones H+ u OH- en solución. El pH depende directamente de la concentración de iones H+ disociados en equilibrio, que se rige por la constante de disociación (Ka o Kb). Por lo tanto, la molaridad y Ka/Kb son las herramientas apropiadas para calcular el pH de soluciones de ácidos y bases débiles, mientras que la normalidad es más útil para reacciones estequiométricas como las titulaciones.
P: ¿Cómo afecta la temperatura al pH?
solvents. El pH de una solución es sensible a la temperatura. Esto se debe a que la constante de producto iónico del agua (Kw) es dependiente de la temperatura. A medida que la temperatura aumenta, Kw también aumenta, lo que significa que el agua se autoioniza más, produciendo más H+ y OH-. Esto hace que el punto neutro (donde [H+] = [OH-]) cambie. Por ejemplo, a 25°C, el agua pura tiene un pH de 7.0, pero a 60°C, el agua pura tiene un pH de aproximadamente 6.5. Es crucial especificar la temperatura cuando se habla de pH, especialmente si no es a 25°C.
P: ¿Cuál es la diferencia entre un ácido monoprótico y poliprótico?
solvents. Un ácido monoprótico es aquel que puede donar solo un protón (H+) por molécula en solución, como el HCl (ácido clorhídrico) o el HNO3 (ácido nítrico). Un ácido poliprótico, por otro lado, puede donar dos o más protones por molécula. Ejemplos incluyen el H2SO4 (ácido sulfúrico, diprótico) o el H3PO4 (ácido fosfórico, triprótico). Cada disociación de un ácido poliprótico tiene su propia constante de Ka (Ka1, Ka2, etc.), y las disociaciones posteriores son siempre más débiles que las anteriores. El cálculo del pH para ácidos polipróticos puede ser más complejo, a menudo dominado por la primera disociación.
Conclusión
El cálculo del pH es una habilidad fundamental en química que te abre las puertas a una comprensión más profunda de las propiedades de las soluciones. Desde la simple aplicación de la fórmula logarítmica para ácidos y bases fuertes, hasta el manejo de los equilibrios con Ka y Kb para las sustancias débiles, e incluso la complejidad de las mezclas y la aplicación de la normalidad, cada escenario presenta su propio conjunto de desafíos y soluciones.
La clave para dominar estos cálculos reside en una comprensión sólida de los principios subyacentes: la disociación, el equilibrio químico y la estequiometría. Al aplicar los pasos y las consideraciones discutidas en este artículo, estarás bien equipado para abordar una amplia gama de problemas de pH. Recuerda que la práctica es esencial para consolidar estos conocimientos y convertirte en un experto en la determinación de la acidez y alcalinidad de cualquier solución.
Si quieres conocer otros artículos parecidos a Calculando el pH: De Ácidos Débiles a Mezclas puedes visitar la categoría Química.
