29/01/2026
En el vasto universo de la química, el pH es una medida fundamental que nos permite cuantificar la acidez o basicidad de una solución acuosa. Sin embargo, detrás de este valor aparentemente simple se esconden complejas interacciones que involucran constantes de equilibrio como el pKa y el pKb. Comprender la relación entre estas magnitudes es crucial para cualquier estudiante o profesional que trabaje con soluciones, desde la elaboración de medicamentos hasta el análisis ambiental. Este artículo se adentrará en el fascinante mundo de los cálculos ácido-base, enfocándose específicamente en cómo determinar el pH cuando se nos proporciona el pKb de una base, así como su comportamiento en procesos de titulación.
La capacidad de una sustancia para donar o aceptar protones (iones H+) es lo que define su naturaleza ácida o básica. Las bases, en particular, son sustancias que pueden aceptar protones o donar pares de electrones, lo que a menudo se traduce en la producción de iones hidróxido (OH-) en solución acuosa. El pKb es una medida de la fuerza de una base débil, indicando su tendencia a ionizarse en agua. Un valor de pKb bajo indica una base más fuerte, mientras que un valor alto sugiere una base más débil. Adentrémonos en los detalles para desentrañar estas relaciones y dominar los cálculos que nos permiten predecir el comportamiento de estas soluciones.
Entendiendo las Constantes de Equilibrio Ácido-Base: pKa y pKb
Antes de sumergirnos en los cálculos específicos, es vital tener una comprensión clara de las constantes de equilibrio ácido-base. El pH mide la concentración de iones hidrógeno (H+) en una escala logarítmica, mientras que el pOH hace lo mismo para los iones hidróxido (OH-). En soluciones acuosas a 25 °C, siempre se cumple que:
pH + pOH = 14
Esta relación es una piedra angular en los cálculos ácido-base, ya que nos permite interconvertir entre pH y pOH. De manera similar, para un par conjugado ácido-base (por ejemplo, un ácido débil HA y su base conjugada A-, o una base débil B y su ácido conjugado BH+), las constantes de disociación ácida (Ka) y básica (Kb) están relacionadas por el producto iónico del agua (Kw = 1.0 x 10^-14 a 25 °C):
Ka * Kb = Kw
Al tomar el logaritmo negativo de ambos lados de esta ecuación, obtenemos una relación análoga en términos de pKa y pKb:
pKa + pKb = 14
Esta segunda relación es de suma importancia, ya que nos permite determinar el pKa de un ácido conjugado si conocemos el pKb de su base, y viceversa. Esta interconexión es la clave para resolver muchos problemas de pH que involucran bases débiles.
Determinando el pH a partir del pKb de una Base Débil
Para calcular el pH de una solución de una base débil a partir de su pKb, necesitamos seguir una serie de pasos lógicos. Consideremos una base débil genérica, B, que reacciona con agua de la siguiente manera:
B (aq) + H₂O (l) ⇌ BH⁺ (aq) + OH⁻ (aq)
La constante de basicidad (Kb) para esta reacción se expresa como:
Kb = [BH⁺][OH⁻] / [B]
El pKb se define como el logaritmo negativo de Kb:
pKb = -log(Kb)
Por lo tanto, si conocemos el pKb, podemos calcular Kb:
Kb = 10^(-pKb)
Ahora, para determinar la concentración de iones OH- ([OH-]) en una solución de una base débil, podemos utilizar una tabla ICE (Inicial, Cambio, Equilibrio) o una aproximación si la base es lo suficientemente débil y la concentración inicial es considerable. Suponiendo que la concentración inicial de la base es C₀ y que la cantidad de B que se ioniza es 'x':
| | B | BH⁺ | OH⁻ |
|-------------|---------|---------|---------|
| Inicial | C₀ | 0 | 0 |
| Cambio | -x | +x | +x |
| Equilibrio | C₀ - x | x | x |
Sustituyendo estos valores en la expresión de Kb:
Kb = (x)(x) / (C₀ - x) = x² / (C₀ - x)
Para bases débiles, 'x' (la concentración de OH-) es generalmente mucho menor que C₀, por lo que podemos simplificar la ecuación a:
Kb ≈ x² / C₀
De donde, x = [OH⁻] = √(Kb * C₀)
Una vez que hemos calculado [OH-], podemos determinar el pOH:
pOH = -log[OH⁻]
Finalmente, usando la relación fundamental entre pH y pOH:
pH = 14 - pOH
Este es el proceso completo para determinar el pH de una solución de una base débil a partir de su pKb y su concentración inicial. Es un método esencial en el análisis químico.
Ejemplo Práctico: Cálculo del pH de una solución de amoniaco
Consideremos una solución de amoniaco (NH₃) 0.1 M. El pKb del amoniaco es 4.75.
- Calcular Kb a partir de pKb:
Kb = 10^(-pKb) = 10^(-4.75) ≈ 1.78 x 10⁻⁵ - Calcular [OH⁻] utilizando la aproximación:
[OH⁻] = √(Kb * C₀) = √(1.78 x 10⁻⁵ * 0.1) = √(1.78 x 10⁻⁶) ≈ 1.33 x 10⁻³ M - Calcular pOH:
pOH = -log(1.33 x 10⁻³) ≈ 2.88 - Calcular pH:
pH = 14 - pOH = 14 - 2.88 = 11.12
Así, el pH de una solución de amoniaco 0.1 M es aproximadamente 11.12, lo cual es coherente con una solución básica.
El pH en la Titulación de una Base Débil
Las titulaciones son procedimientos analíticos que nos permiten determinar la concentración de una sustancia (el analito) mediante la adición controlada de una solución de concentración conocida (el titulante). Cuando titulamos una base débil con un ácido fuerte, el pH de la solución cambia de manera característica a lo largo del proceso. Comprender estos cambios es vital para la precisión en el laboratorio.

Punto Inicial (Antes de añadir ácido)
En este punto, solo tenemos la base débil en solución. El pH se calcula como se describió anteriormente, utilizando el pKb y la concentración inicial de la base.
Durante la Titulación (Antes del Punto de Equivalencia)
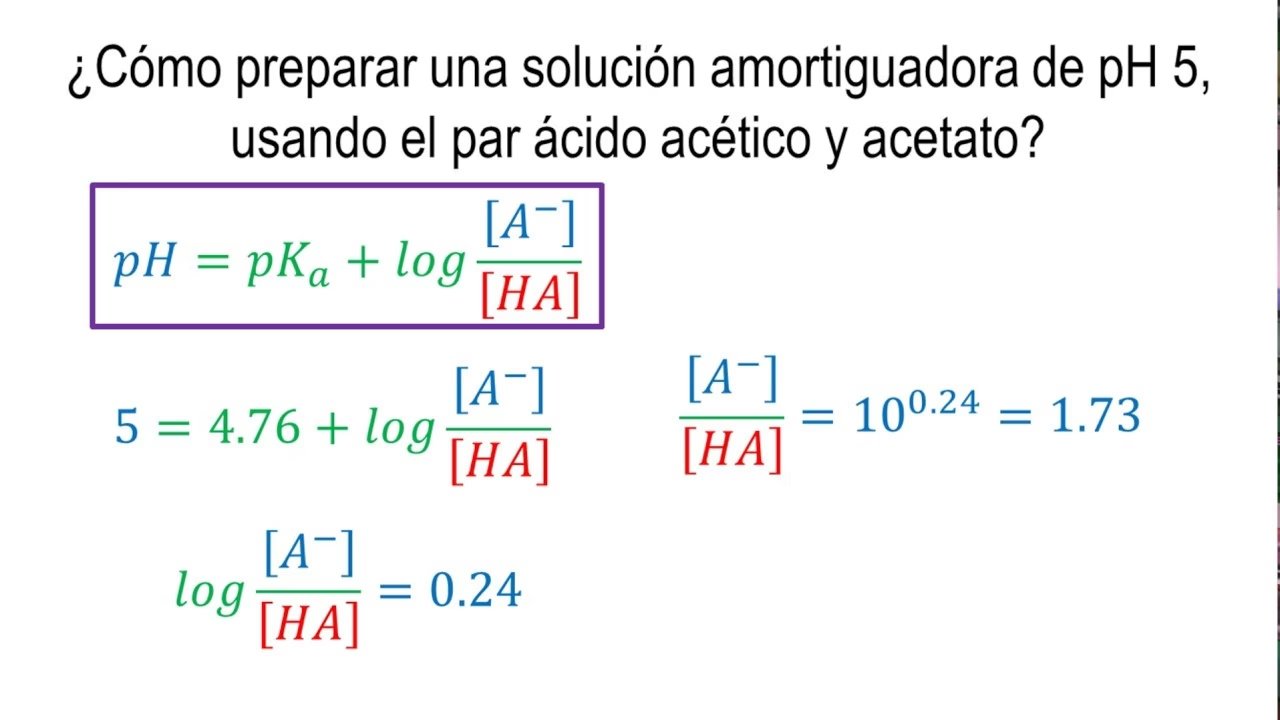
A medida que se añade el ácido fuerte, este reacciona con la base débil para formar su ácido conjugado. Se forma una solución amortiguadora (buffer) que contiene la base débil y su ácido conjugado. El pH en esta región puede calcularse utilizando la ecuación de Henderson-Hasselbalch para bases (o su forma ácida, si trabajamos con el pKa del ácido conjugado):
pOH = pKb + log([BH⁺]/[B])
Alternativamente, y a menudo más conveniente, se puede usar la forma ácida de la ecuación de Henderson-Hasselbalch, recordando que pH = 14 - pOH y pKa = 14 - pKb:
pH = pKa(BH⁺) + log([B]/[BH⁺])
Donde pKa(BH+) es el pKa del ácido conjugado de la base débil.
Punto de Semiequivalencia
Un punto particularmente importante durante la titulación de una base débil es el punto de semiequivalencia. Este ocurre cuando se ha añadido la mitad del volumen de ácido fuerte necesario para alcanzar el punto de equivalencia. En este punto, la concentración de la base débil ([B]) es igual a la concentración de su ácido conjugado ([BH+]).
Si [B] = [BH+], entonces el término log([B]/[BH+]) = log(1) = 0. Por lo tanto, en el punto de semiequivalencia:
pH = pKa(BH⁺)
Esta es una relación muy útil, ya que permite determinar experimentalmente el pKa del ácido conjugado (y por ende el pKb de la base) a partir de la curva de titulación. El pH en el punto de semititulación es, efectivamente, igual al pKa del ácido débil, BH+. Para obtener el pKb de la base (B), es necesario restar el pKa de 14. Esto se debe a que el pOH es lo que equivale al pKb. Por lo tanto, pKb = 14 - pKa del H+ en exceso añadido (o más precisamente, pKb = 14 - pKa del ácido conjugado).
Punto de Equivalencia
En el punto de equivalencia, todo el ácido débil ha reaccionado con la base fuerte. La solución contiene principalmente el ácido conjugado de la base débil (BH+). Como BH+ es un ácido débil, hidrolizará el agua para producir iones H+, haciendo que la solución sea ligeramente ácida. Por lo tanto, el pH en el punto de equivalencia de la titulación de una base débil con un ácido fuerte será menor que 7 (pH < 7). Para calcular el pH en este punto, se debe tratar al ácido conjugado como un ácido débil y usar su pKa (o Ka) para determinar [H+] y luego el pH.
Después del Punto de Equivalencia
Una vez que se ha superado el punto de equivalencia, el exceso de ácido fuerte añadido domina el pH de la solución. El pH se calculará directamente a partir de la concentración de este exceso de ácido fuerte.
Cálculo del pH a partir de pKa (Para Ácidos Débiles)
Aunque nuestro enfoque principal es el pKb, es útil recordar cómo se calcula el pH a partir del pKa para ácidos débiles, ya que ambos conceptos están intrínsecamente relacionados. Para un ácido débil genérico, HA, que se disocia en agua:
HA (aq) + H₂O (l) ⇌ H₃O⁺ (aq) + A⁻ (aq)
La constante de acidez (Ka) se expresa como:
Ka = [H₃O⁺][A⁻] / [HA]
El pKa se define como el logaritmo negativo de Ka:
pKa = -log(Ka)
Por lo tanto, si conocemos el pKa, podemos calcular Ka:
Ka = 10^(-pKa)
De manera análoga al cálculo para bases débiles, si la concentración inicial del ácido es C₀ y 'x' es la cantidad que se disocia, entonces [H₃O⁺] = x. Para ácidos débiles, si la disociación es pequeña, podemos aproximar:
Ka ≈ x² / C₀
De donde, x = [H₃O⁺] = √(Ka * C₀)
Y finalmente, el pH es:
pH = -log[H₃O⁺]
Este es el proceso para determinar el pH de una solución de un ácido débil a partir de su pKa y su concentración inicial.

Tabla Comparativa de Constantes Ácido-Base
Para reforzar el entendimiento de estas relaciones, la siguiente tabla resume los conceptos clave:
| Concepto | Definición | Relación con pH/pOH | Fuerza |
|---|---|---|---|
| pH | -log[H+] | Medida de acidez/basicidad | Menor pH = Más ácido |
| pOH | -log[OH-] | Medida de basicidad/acidez | Menor pOH = Más básico |
| pKa | -log(Ka) | Para ácidos débiles (HA) | Menor pKa = Ácido más fuerte |
| pKb | -log(Kb) | Para bases débiles (B) | Menor pKb = Base más fuerte |
| Ka | Constante de disociación ácida | Determina [H+] de un ácido débil | Mayor Ka = Ácido más fuerte |
| Kb | Constante de disociación básica | Determina [OH-] de una base débil | Mayor Kb = Base más fuerte |
| pH + pOH | 14 (a 25 °C) | Interconversión entre acidez y basicidad | |
| pKa + pKb | 14 (para pares conjugados) | Interconversión entre fuerza de ácido y base conjugada |
Preguntas Frecuentes (FAQ)
¿Cuál es la diferencia entre Ka y pKa?
Ka es la constante de disociación ácida, un valor directo que indica la fuerza de un ácido. Cuanto mayor sea Ka, más fuerte será el ácido. pKa es el logaritmo negativo de Ka (pKa = -log Ka). Se usa por conveniencia para manejar números muy pequeños y más fácilmente comparables. Cuanto menor sea pKa, más fuerte será el ácido.
¿Por qué pH + pOH = 14?
Esta relación se deriva del producto iónico del agua (Kw = [H+][OH-] = 1.0 x 10^-14 a 25 °C). Al aplicar el logaritmo negativo a esta ecuación, se obtiene -log(Kw) = -log([H+]) + -log([OH-]), lo que se simplifica a pKw = pH + pOH. Dado que pKw es 14, resulta en pH + pOH = 14.
¿Qué significa un pKb bajo?
Un pKb bajo significa que la constante de basicidad (Kb) es un número grande (ya que pKb = -log Kb). Esto indica que la base es fuerte, es decir, tiene una gran tendencia a aceptar protones y producir iones hidróxido en solución. Por ejemplo, una base con pKb = 1 es mucho más fuerte que una con pKb = 9.
¿Cómo afecta la concentración inicial al pH de una solución de base débil?
La concentración inicial de la base débil (C₀) tiene un impacto directo en el pH. Como se vio en la fórmula [OH⁻] = √(Kb * C₀), una mayor concentración inicial de la base (C₀) resultará en una mayor concentración de iones OH- en el equilibrio, lo que a su vez se traduce en un pOH menor y, por lo tanto, un pH más alto (más básico). Sin embargo, la disociación fraccional de la base disminuye a medida que aumenta la concentración inicial.
¿Puede una base débil tener un pH menor que 7?
Normalmente, una solución acuosa de una base débil tendrá un pH mayor que 7. Sin embargo, en un contexto de titulación, después de añadir suficiente ácido fuerte para reaccionar completamente con la base débil (en el punto de equivalencia o más allá), la solución resultante puede tener un pH menor que 7 debido a la formación del ácido conjugado y/o el exceso de ácido titulante.
Conclusión
La capacidad de determinar el pH a partir del pKb es una habilidad crucial en la química ácido-base. A través de la comprensión de las relaciones entre pH, pOH, pKa y pKb, y la aplicación de las ecuaciones de equilibrio, podemos predecir con precisión la acidez o basicidad de una solución. Las titulaciones, en particular, ofrecen una aplicación práctica de estos principios, permitiéndonos analizar y caracterizar sustancias químicas. Dominar estos conceptos no solo es fundamental para el éxito académico en química, sino también para diversas aplicaciones en la investigación, la industria y la vida cotidiana.
Si quieres conocer otros artículos parecidos a pH a partir de pKb: Guía Completa de Cálculo puedes visitar la categoría Química.

