04/08/2025
La titulación es una técnica analítica fundamental en química, utilizada para determinar la concentración desconocida de un analito en una solución. En su esencia, implica la adición controlada de una solución de concentración conocida (el titulante) a una solución de concentración desconocida (el analito) hasta que la reacción entre ambos se completa. Uno de los parámetros más críticos que se monitorean y calculan durante este proceso es el pH, ya que su variación a lo largo de la titulación revela información invaluable sobre la naturaleza de las sustancias involucradas y el progreso de la reacción.
El cálculo preciso del pH en diferentes etapas de una titulación no es solo un ejercicio académico, sino una habilidad esencial para químicos, biólogos y cualquier profesional que trabaje en laboratorios. Permite predecir el comportamiento de las soluciones, seleccionar indicadores adecuados y, en última instancia, asegurar la exactitud de los resultados analíticos. Comprender cómo el pH evoluciona desde el inicio hasta después del punto de equivalencia es clave para dominar esta técnica.
El pH inicial: La base de la curva de titulación
El primer paso para entender cualquier titulación es determinar el pH inicial de la solución que se va a valorar. Este valor es crucial porque establece el punto de partida de la curva de titulación y depende directamente de la naturaleza y concentración del analito.
Cálculo para Ácidos Fuertes
Si la solución inicial es un ácido fuerte, como el ácido clorhídrico (HCl) o el ácido nítrico (HNO₃), se disocia completamente en agua, liberando una concentración de iones hidronio (H₃O⁺) igual a la concentración inicial del ácido. En este caso, el cálculo es directo:
pH = -log[H₃O⁺]
Donde [H₃O⁺] es la concentración molar inicial del ácido. Por ejemplo, si tienes una solución 0.1 M de HCl, el pH inicial será -log(0.1) = 1.
Cálculo para Bases Fuertes
Si el analito es una base fuerte, como el hidróxido de sodio (NaOH) o el hidróxido de potasio (KOH), también se disocia completamente en agua, liberando iones hidróxido (OH⁻). Primero se calcula el pOH, y luego se convierte a pH:
pOH = -log[OH⁻]
pH = 14 - pOH (a 25°C)
Donde [OH⁻] es la concentración molar inicial de la base. Por ejemplo, una solución 0.05 M de NaOH tendrá un pOH de -log(0.05) = 1.30, y por lo tanto, un pH de 14 - 1.30 = 12.70.
Cálculo para Ácidos o Bases Débiles
Cuando el analito es un ácido débil (como el ácido acético, CH₃COOH) o una base débil (como el amoníaco, NH₃), la disociación en agua no es completa. Esto significa que se establece un equilibrio químico. Para calcular el pH inicial en estos casos, es necesario utilizar la constante de acidez (Ka) para ácidos débiles o la constante de basicidad (Kb) para bases débiles, y a menudo se recurre a una tabla ICE (Initial, Change, Equilibrium).
Para un ácido débil genérico HA, la reacción de equilibrio es:
HA (aq) ⇌ H⁺ (aq) + A⁻ (aq)
La expresión de la constante de equilibrio es:
Ka = [H⁺][A⁻] / [HA]
Usando una tabla ICE, se establecen las concentraciones iniciales, el cambio 'x' debido a la disociación, y las concentraciones en el equilibrio. Generalmente, se asume que 'x' es pequeño en comparación con la concentración inicial del ácido o base, lo que simplifica la ecuación a resolver (a menudo una ecuación cuadrática si la aproximación no es válida). Una vez que se encuentra [H⁺] (o [OH⁻]), el pH se calcula como se indicó anteriormente.
Los cambios de pH a lo largo de la titulación
Una vez que comienza la adición del titulante, el pH de la solución cambia progresivamente, lo que da lugar a la característica curva de titulación. Esta curva es un gráfico del pH en función del volumen de titulante añadido y se divide en varias regiones distintas.

Región Antes del Punto de Equivalencia
En esta fase, el titulante reacciona con el analito. El pH varía de manera relativamente gradual al principio. La forma exacta de esta región depende de la fuerza del ácido o base que se está titulando:
- Titulación de Ácido Fuerte con Base Fuerte: El pH aumenta lentamente a medida que los iones H₃O⁺ se neutralizan. La concentración de H₃O⁺ disminuye, pero sigue siendo la especie dominante que determina el pH.
- Titulación de Ácido Débil con Base Fuerte: Esta región es particularmente interesante porque se forma un sistema amortiguador (también conocido como buffer). A medida que la base fuerte reacciona con el ácido débil, se produce la sal conjugada del ácido. La mezcla de un ácido débil y su base conjugada resiste los cambios drásticos de pH. El pH en esta región se puede calcular utilizando la ecuación de Henderson-Hasselbalch:
pH = pKa + log([A⁻] / [HA])Donde [A⁻] es la concentración de la base conjugada formada y [HA] es la concentración del ácido débil remanente.
El Punto de Equivalencia
El punto de equivalencia es el corazón de la titulación, el momento en que la cantidad de titulante añadido es estequiométricamente igual a la cantidad de analito presente en la muestra. En este punto, la reacción se ha completado. El pH en el punto de equivalencia es crucial y varía según el tipo de titulación:
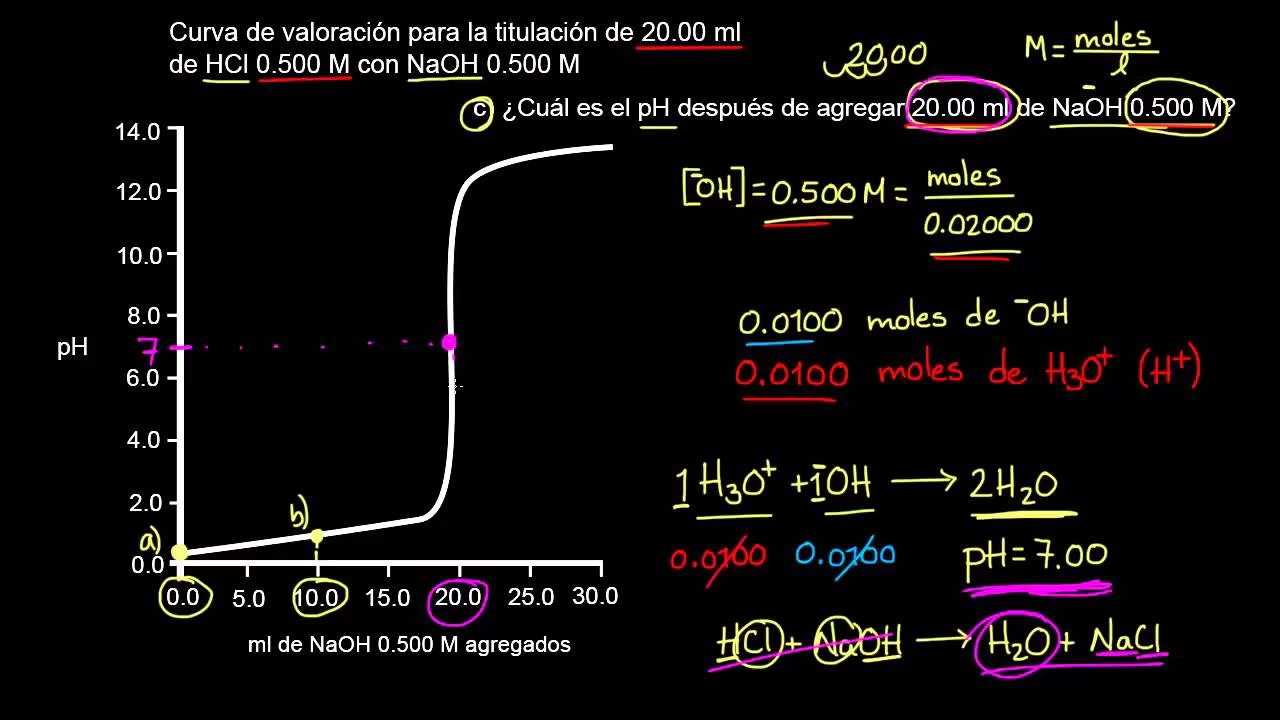
- Ácido Fuerte vs. Base Fuerte: El pH en el punto de equivalencia es aproximadamente 7 (neutro), ya que los productos de la neutralización son una sal que no hidroliza (como NaCl) y agua.
- Ácido Débil vs. Base Fuerte: El pH en el punto de equivalencia será mayor que 7 (básico). Esto se debe a que la base conjugada del ácido débil (A⁻) es una base relativamente fuerte que hidroliza el agua, produciendo iones OH⁻:
A⁻ (aq) + H₂O (l) ⇌ HA (aq) + OH⁻ (aq)El pH se calcula utilizando la constante de basicidad de la base conjugada (Kb = Kw/Ka) y una tabla ICE para determinar [OH⁻]. - Base Débil vs. Ácido Fuerte: El pH en el punto de equivalencia será menor que 7 (ácido). En este caso, el ácido conjugado de la base débil hidroliza el agua, produciendo iones H₃O⁺. El pH se calcula utilizando la constante de acidez del ácido conjugado (Ka = Kw/Kb).
Región Después del Punto de Equivalencia
Una vez que se ha superado el punto de equivalencia, el pH está determinado principalmente por el exceso de titulante añadido. Los cálculos se simplifican nuevamente:
- Exceso de Base Fuerte: El pH se calcula a partir de la concentración del exceso de iones OH⁻.
- Exceso de Ácido Fuerte: El pH se calcula a partir de la concentración del exceso de iones H₃O⁺.
El cambio de pH en esta región es nuevamente más gradual, pero en la dirección opuesta a la fase inicial.
Factores que influencian la forma de la curva de titulación
La forma y la magnitud del cambio de pH en una curva de titulación no son constantes. Varios factores pueden alterarlas significativamente:
- Las concentraciones del reactivo valorante y del analito: Como se mencionó en la información proporcionada, las concentraciones iniciales del ácido y la base tienen un impacto directo en la nitidez del salto de pH alrededor del punto de equivalencia. Cuanto mayores sean estas concentraciones, más pronunciado será el cambio de pH en la región del punto de equivalencia. Esto se debe a que una mayor concentración inicial significa que se necesita menos volumen de titulante para cambiar drásticamente la relación molar de los iones H⁺ y OH⁻. Si las soluciones son muy diluidas, el salto de pH puede ser menos definido, dificultando la identificación precisa del punto de equivalencia.
- La fuerza del ácido o la base: La fuerza de los reactivos (si son fuertes o débiles) determina el pH inicial, la presencia de una región amortiguadora y el pH en el punto de equivalencia. Las titulaciones que involucran al menos un reactivo débil (ácido débil/base fuerte, base débil/ácido fuerte) presentan una región de amortiguación antes del punto de equivalencia y un pH de equivalencia que se desvía de 7.
- Temperatura: La constante de ionización del agua (Kw) y las constantes de equilibrio (Ka, Kb) son dependientes de la temperatura. Aunque a menudo se asumen a 25°C, las variaciones de temperatura pueden afectar sutilmente los cálculos de pH.
La importancia de calcular el pH en titulaciones
El meticuloso cálculo del pH en cada etapa de una titulación trasciende el ámbito puramente teórico. Tiene implicaciones prácticas significativas en una variedad de campos:
- Análisis Cuantitativo: Es fundamental para determinar con precisión la concentración de sustancias en muestras químicas, biológicas o ambientales. Desde la calidad del agua potable hasta la concentración de principios activos en medicamentos, el control de pH en titulaciones es crucial.
- Control de Calidad: En la industria, las titulaciones se utilizan rutinariamente para verificar la pureza y concentración de materias primas y productos finales. Un pH calculado incorrectamente podría llevar a productos defectuosos o no conformes.
- Investigación y Desarrollo: En laboratorios de investigación, el entendimiento de las curvas de titulación ayuda a caracterizar nuevas sustancias, estudiar sus propiedades ácido-base y diseñar nuevos procesos químicos.
- Bioquímica y Biología: El pH es vital para los sistemas biológicos. Las titulaciones ayudan a entender el comportamiento de proteínas, aminoácidos y otros biomoléculas que actúan como amortiguadores en sistemas vivos.
Preguntas Frecuentes (FAQ)
¿Por qué es importante conocer el pH inicial de una titulación?
El pH inicial establece el punto de partida de la curva de titulación y es crucial para predecir la forma general de la curva y el pH esperado en el punto de equivalencia. Además, ayuda a seleccionar el indicador de pH adecuado para la titulación.
¿Qué es exactamente el punto de equivalencia en una titulación?
El punto de equivalencia es el momento teórico durante una titulación en el que la cantidad de titulante añadido es estequiométricamente equivalente a la cantidad original del analito en la muestra. Es el punto donde la reacción de neutralización se ha completado.
¿Cómo sé qué fórmula debo usar para calcular el pH inicial?
Debes identificar si el analito es un ácido fuerte, una base fuerte, un ácido débil o una base débil. Para fuertes, usa las fórmulas directas de -log[H⁺] o 14 - (-log[OH⁻]). Para débiles, necesitarás usar la constante de equilibrio (Ka o Kb) y una tabla ICE.
¿Qué es una tabla ICE y cuándo se usa?
Una tabla ICE (Initial, Change, Equilibrium) es una herramienta para organizar las concentraciones de reactivos y productos en una reacción en equilibrio. Se usa para calcular las concentraciones de equilibrio (incluyendo [H⁺] o [OH⁻]) en soluciones de ácidos débiles, bases débiles o sales que hidrolizan.
¿Las concentraciones iniciales solo afectan el pH inicial?
No, las concentraciones iniciales afectan la nitidez del salto de pH alrededor del punto de equivalencia. Soluciones más concentradas producirán un salto de pH más pronunciado y fácil de observar, mientras que soluciones muy diluidas pueden tener un salto menos definido.
En resumen, el cálculo del pH en las titulaciones es un pilar de la química analítica. Desde el pH inicial de la solución hasta el complejo comportamiento de la región amortiguadora y la determinación del punto de equivalencia, cada cálculo contribuye a una comprensión profunda de las interacciones ácido-base. La capacidad de predecir y entender estos cambios de pH es lo que permite a los químicos llevar a cabo análisis precisos, asegurar la calidad de los productos y avanzar en la investigación científica.
Si quieres conocer otros artículos parecidos a El Arte de Calcular el pH en Titulaciones puedes visitar la categoría Química.

