15/06/2022
En el vasto universo de la química, el pH es una medida fundamental que nos permite comprender la acidez o basicidad de una solución. Mientras que calcular el pH de un ácido monoprótico (aquel que cede un solo protón) puede parecer una tarea sencilla, el desafío aumenta exponencialmente cuando nos enfrentamos a los ácidos polipróticos. Estos compuestos, capaces de donar dos o más protones, presentan un comportamiento de disociación escalonado que requiere un enfoque más detallado y un entendimiento profundo de sus propiedades.

Este artículo explorará en detalle cómo abordar el cálculo del pH para soluciones de ácidos polipróticos, desglosando cada paso y ofreciendo una visión clara de los principios subyacentes. Desde la identificación de las constantes de disociación hasta la aplicación de las tablas ICE y la consideración de las sales derivadas, te guiaremos para que domines este aspecto crucial de la química ácido-base.
- ¿Qué Son los Ácidos Polipróticos y Por Qué son Especiales?
- El Proceso Detallado para Calcular el pH de un Ácido Poliprótico
- La Importancia de la Aproximación en Ácidos Polipróticos
- El pH de una Sal Poliprótica: Más Allá del Ácido Puro
- Tabla Comparativa: Ácidos Monopróticos vs. Polipróticos
- Preguntas Frecuentes (FAQ)
- Conclusión
¿Qué Son los Ácidos Polipróticos y Por Qué son Especiales?
Los ácidos polipróticos son, en esencia, moléculas que poseen la capacidad de ceder dos o más de sus protones (iones H+) a otras especies químicas en una solución acuosa. A diferencia de los ácidos monopróticos, como el ácido clorhídrico (HCl) o el ácido nítrico (HNO3), que solo cuentan con un átomo de hidrógeno ionizable, los ácidos polipróticos presentan múltiples hidrógenos ácidos que se liberan de manera secuencial. Ejemplos comunes incluyen el ácido sulfúrico (H2SO4), el ácido carbónico (H2CO3), y el ácido fosfórico (H3PO4).
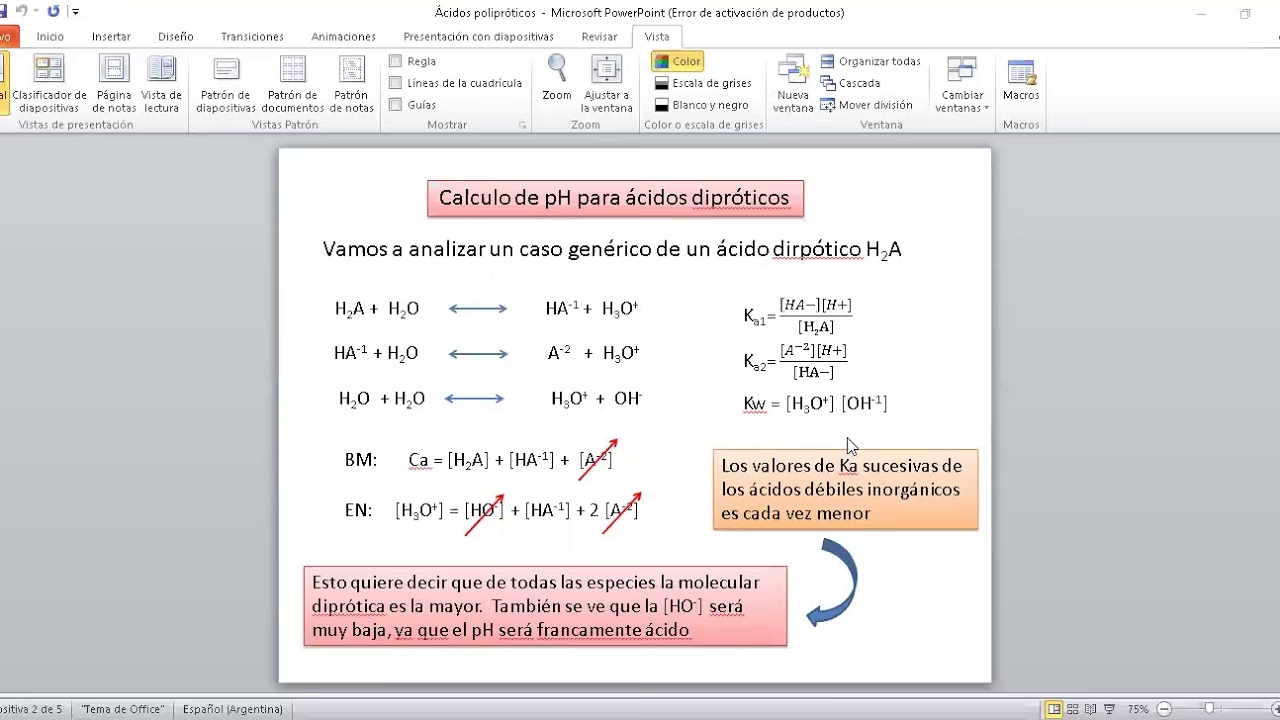
La característica que los hace especiales y, a la vez, más complejos para el cálculo del pH, es su disociación por etapas. Cada protón se libera en una etapa de ionización separada, y cada una de estas etapas tiene su propia constante de disociación ácida (Ka). Por ejemplo, un ácido diprótico (que libera dos protones) tendrá dos constantes de disociación, Ka1 y Ka2. Un ácido triprótico tendrá Ka1, Ka2 y Ka3. Es crucial entender que la fuerza de la disociación disminuye drásticamente con cada etapa sucesiva, lo que significa que Ka1 siempre será significativamente mayor que Ka2, y Ka2 mayor que Ka3. Esto se debe a que, una vez que el primer protón se ha ido, la especie restante tiene una carga negativa que dificulta la liberación de otro protón cargado positivamente debido a la atracción electrostática.
El Proceso Detallado para Calcular el pH de un Ácido Poliprótico
Calcular el pH de una solución de ácido poliprótico requiere un enfoque sistemático que considera cada etapa de disociación. Los pasos a seguir son los siguientes, profundizando en cada uno para una comprensión completa:
1. Determinación de las Constantes de Disociación Ácida (Ka)
El primer paso fundamental es identificar y recopilar las constantes de disociación ácida (Ka1, Ka2, etc.) para cada etapa de ionización del ácido poliprótico en cuestión. Estos valores son específicos para cada ácido y se encuentran comúnmente en tablas de referencia química. Por ejemplo, para el ácido fosfórico (H3PO4):
- Ka1 = 7.11 × 10-3
- Ka2 = 6.34 × 10-8
- Ka3 = 4.2 × 10-13
La diferencia de magnitud entre estas constantes es un indicador clave de cómo cada etapa contribuirá a la concentración final de iones H+.
2. Escritura de las Ecuaciones Químicas Balanceadas
Para cada etapa de ionización, debes escribir la ecuación química balanceada correspondiente. Esto ayuda a visualizar cómo el ácido se disocia y qué especies se forman en cada paso. Utilizando el ácido sulfúrico (H2SO4) como ejemplo:
Primera etapa de ionización:
H2SO4 (ac) ⇌ H+ (ac) + HSO4- (ac) (Ka1 es muy grande, a menudo se considera un ácido fuerte en esta etapa)
Segunda etapa de ionización:
HSO4- (ac) ⇌ H+ (ac) + SO42- (ac) (Ka2 = 1.2 × 10-2)
Es importante notar que el ácido sulfúrico es un caso especial, ya que su primera disociación es completa (como un ácido fuerte), mientras que la segunda es parcial (como un ácido débil).

3. Configuración de Tablas ICE (Inicial, Cambio, Equilibrio)
Las tablas ICE son una herramienta indispensable para resolver problemas de equilibrio químico. Debes configurar una tabla ICE para cada etapa de ionización que contribuya significativamente a la concentración de H+.
Etapa 1: Comienza con la concentración inicial del ácido poliprótico y asume una disociación inicial para la primera etapa.
| Especie | Inicial (I) | Cambio (C) | Equilibrio (E) |
|---|---|---|---|
| H2A | [H2A]inicial | -x | [H2A]inicial - x |
| H+ | 0 | +x | x |
| HA- | 0 | +x | x |
Utiliza la expresión de Ka1 para resolver para 'x', que representará la concentración de H+ y de la especie mono-aniónica (HA-) en el equilibrio de la primera etapa.
Etapa 2 (y subsiguientes): La concentración de HA- y H+ resultante de la primera etapa se convierte en las concentraciones 'iniciales' para la segunda tabla ICE. Esto es crucial porque la concentración de H+ ya no es cero al inicio de la segunda etapa.
| Especie | Inicial (I) | Cambio (C) | Equilibrio (E) |
|---|---|---|---|
| HA- | [HA-]de etapa 1 | -y | [HA-]de etapa 1 - y |
| H+ | [H+]de etapa 1 | +y | [H+]de etapa 1 + y |
| A2- | 0 | +y | y |
Utiliza la expresión de Ka2 para resolver para 'y'. A menudo, debido a que Ka2 es mucho menor que Ka1, la contribución de H+ de la segunda etapa (y subsiguientes) es mucho menor que la de la primera. En muchos casos, se puede hacer una aproximación y considerar que la contribución de H+ de las etapas subsiguientes es insignificante, y el pH se determina principalmente por la primera disociación. Sin embargo, esto debe ser verificado.
4. Cálculo de la Concentración Total de Iones H+
Una vez que hayas resuelto las concentraciones de equilibrio de H+ para cada etapa (o las que consideres significativas), debes sumar estas contribuciones para obtener la concentración total de iones H+ en la solución. Es importante recordar que la H+ de la primera disociación afectará el equilibrio de las disociaciones posteriores, por lo que la suma no es simplemente la 'x' y la 'y' independientes, sino el valor de equilibrio final de [H+] de la última tabla ICE considerada.
5. Cálculo del pH Final
Finalmente, una vez que tengas la concentración total de iones H+ en el equilibrio, utiliza la fórmula universal del pH:
pH = -log[H+]
Este valor representará el pH de la solución de ácido poliprótico.
La Importancia de la Aproximación en Ácidos Polipróticos
Como se mencionó, las constantes de disociación disminuyen drásticamente con cada etapa. Esta marcada diferencia a menudo permite una simplificación significativa en los cálculos. Si Ka1 es al menos 1000 veces mayor que Ka2 (Ka1 / Ka2 > 1000), o si la concentración inicial del ácido es relativamente alta, la contribución de H+ de la segunda etapa (y posteriores) suele ser tan pequeña que puede ignorarse sin un error significativo. En tales casos, el pH de la solución puede ser aproximado considerando solo la primera etapa de ionización. Sin embargo, para ácidos donde las Ka son más cercanas (como en el ácido sulfúrico, donde Ka1 es muy grande y Ka2 es considerable), o para soluciones muy diluidas, es necesario realizar los cálculos para cada etapa.
El pH de una Sal Poliprótica: Más Allá del Ácido Puro
El comportamiento ácido-base no se limita a los ácidos y bases puros; también se extiende a sus sales. Las sales pueden considerarse derivadas de la neutralización de un ácido y una base. Cuando una sal se disuelve en agua, sus iones pueden hidrolizarse (reaccionar con el agua para producir H+ o OH-), afectando el pH de la solución.
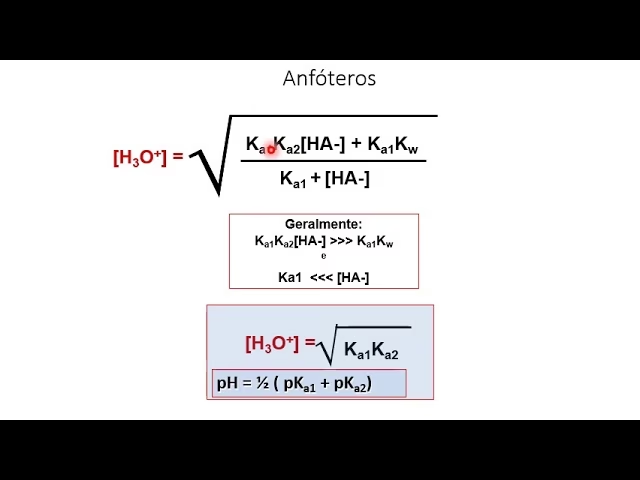
Para calcular el pH de una solución de una sal poliprótica (derivada de un ácido poliprótico), necesitamos considerar la hidrólisis de los aniones resultantes. Por ejemplo, si tenemos una sal como NaH2PO4 (dihidrógeno fosfato de sodio), el anión H2PO4- puede actuar tanto como ácido (donando un protón) como base (aceptando un protón). Su comportamiento dependerá de la comparación entre su Ka (para la disociación adicional) y su Kb (para la hidrólisis como base).
Las reglas generales para la hidrólisis de sales (aplicables a aniones de ácidos polipróticos) son:
- Si un ion no puede afectar el pH (como Na+ o Cl-), la solución es neutra.
- Si solo el catión de la sal es ácido, la solución es ácida.
- Si solo el anión de la sal es básico, la solución será básica.
- Si una sal tiene un catión ácido y un anión básico (como en el caso de un anión intermedio de un ácido poliprótico), el pH de la solución se determina por las fuerzas relativas del ácido y la base:
- Si Ka = Kb para el ion, entonces no hay efecto neto sobre el pH (pH neutro).
- Si Ka > Kb, entonces la solución es ligeramente ácida.
- Si Kb > Ka, entonces la solución es ligeramente básica.
Para determinar la Kb de un anión conjugado de un ácido poliprótico, se utiliza la relación Kw = Ka × Kb, donde Kw es la constante de autoionización del agua (1.0 × 10-14 a 25°C). Por ejemplo, para el anión H2PO4-, su Ka sería Ka2 del ácido fosfórico (6.34 × 10-8), y su Kb se calcularía usando Ka1 del ácido fosfórico y la relación Kw/Ka1. La comparación de estos valores determinará si el anión se comporta predominantemente como ácido o como base y, por lo tanto, el pH de la solución salina.

Tabla Comparativa: Ácidos Monopróticos vs. Polipróticos
| Característica | Ácido Monoprótico | Ácido Poliprótico |
|---|---|---|
| Número de Protones Ionizables | Uno | Dos o más |
| Constantes de Disociación (Ka) | Una (Ka) | Múltiples (Ka1, Ka2, ...) |
| Disociación | Una sola etapa | Múltiples etapas secuenciales |
| Cálculo del pH | Generalmente más directo, una tabla ICE | Requiere considerar múltiples tablas ICE (o aproximaciones), sumando contribuciones de H+ |
| Fuerza de Disociación | Constante para su única etapa | Disminuye drásticamente en cada etapa sucesiva (Ka1 >> Ka2 >> ...) |
| Ejemplos | HCl, HNO3, CH3COOH | H2SO4, H3PO4, H2CO3 |
Preguntas Frecuentes (FAQ)
¿Cómo saber si un ácido es poliprótico?
Un ácido es poliprótico si su fórmula química indica que puede ceder dos o más de sus protones. Visualmente, esto se traduce en la presencia de dos o más átomos de hidrógeno que son capaces de ionizarse en solución acuosa. Por ejemplo, H2SO4 (dos hidrógenos), H3PO4 (tres hidrógenos). Los ácidos que liberan solo un protón, como HCl o HNO3, se denominan ácidos monopróticos.
¿Por qué las constantes de disociación disminuyen en cada etapa?
Las constantes de disociación (Ka) disminuyen progresivamente en cada etapa de ionización de un ácido poliprótico debido a un efecto electrostático. Después de que el primer protón (H+) se ha disociado, la especie restante adquiere una carga negativa. Liberar un segundo protón, que también es positivo, de una especie ya cargada negativamente se vuelve energéticamente menos favorable y, por lo tanto, más difícil. La atracción electrostática entre el protón saliente y la carga negativa remanente en el anión dificulta su separación, resultando en una Ka menor para las etapas subsiguientes.
¿Cuándo puedo ignorar las etapas subsiguientes al calcular el pH?
Puedes ignorar las contribuciones de las etapas subsiguientes de disociación (Ka2, Ka3, etc.) y basar el cálculo del pH casi exclusivamente en la primera etapa (Ka1) cuando la constante de disociación de la primera etapa es al menos 1000 veces mayor que la de la segunda etapa (es decir, Ka1 / Ka2 > 1000). En estos casos, la cantidad de H+ adicional liberada por las etapas posteriores es insignificante en comparación con la de la primera etapa, lo que simplifica considerablemente los cálculos sin comprometer la precisión.
¿Es diferente el cálculo del pH para una base poliprótica?
Sí, el principio es similar pero se aplican las constantes de basicidad (Kb) en lugar de las Ka. Las bases polipróticas aceptan protones en etapas, cada una con su propia Kb (Kb1, Kb2, etc.). Al igual que con los ácidos, las Kb disminuyen en cada etapa. El cálculo implica el uso de tablas ICE para determinar la concentración de iones OH- en el equilibrio, a partir de la cual se puede calcular el pOH y luego el pH (pH = 14 - pOH). Los ejemplos incluyen el ion carbonato (CO32-) o la hidrazina (N2H4).
Conclusión
El cálculo del pH de soluciones de ácidos polipróticos es un desafío químico que revela la complejidad y la sutileza de los equilibrios ácido-base. A través de la comprensión de las constantes de disociación escalonadas, la aplicación meticulosa de las tablas ICE y la consideración de las aproximaciones válidas, es posible determinar con precisión la acidez de estas soluciones. Además, reconocer cómo las sales de ácidos polipróticos pueden hidrolizarse y afectar el pH es esencial para una comprensión completa del comportamiento de estas especies en solución. Dominar estos conceptos no solo mejora nuestra capacidad de predecir y controlar reacciones químicas, sino que también profundiza nuestra apreciación por la intrincada danza de protones en el mundo molecular.
Si quieres conocer otros artículos parecidos a El Enigma del pH: Ácidos Polipróticos y su Cálculo puedes visitar la categoría Química.