19/11/2023
El pH es un concepto fundamental en la química, la biología y numerosas industrias, sirviendo como una medida crucial de la acidez o alcalinidad de una solución acuosa. Desde el equilibrio delicado de nuestro propio cuerpo hasta la calidad del agua que bebemos o la efectividad de los productos de limpieza, el pH juega un papel omnipresente. Comprender qué es el pH y cómo se relaciona con la concentración de iones en una solución no solo es esencial para estudiantes y profesionales de la ciencia, sino también para cualquier persona interesada en entender mejor el mundo que nos rodea. A menudo, la relación entre el pH y los iones protón, así como los iones hidroxilo, puede parecer compleja, pero con una explicación clara y ejemplos prácticos, se convierte en un concepto totalmente accesible y fascinante.
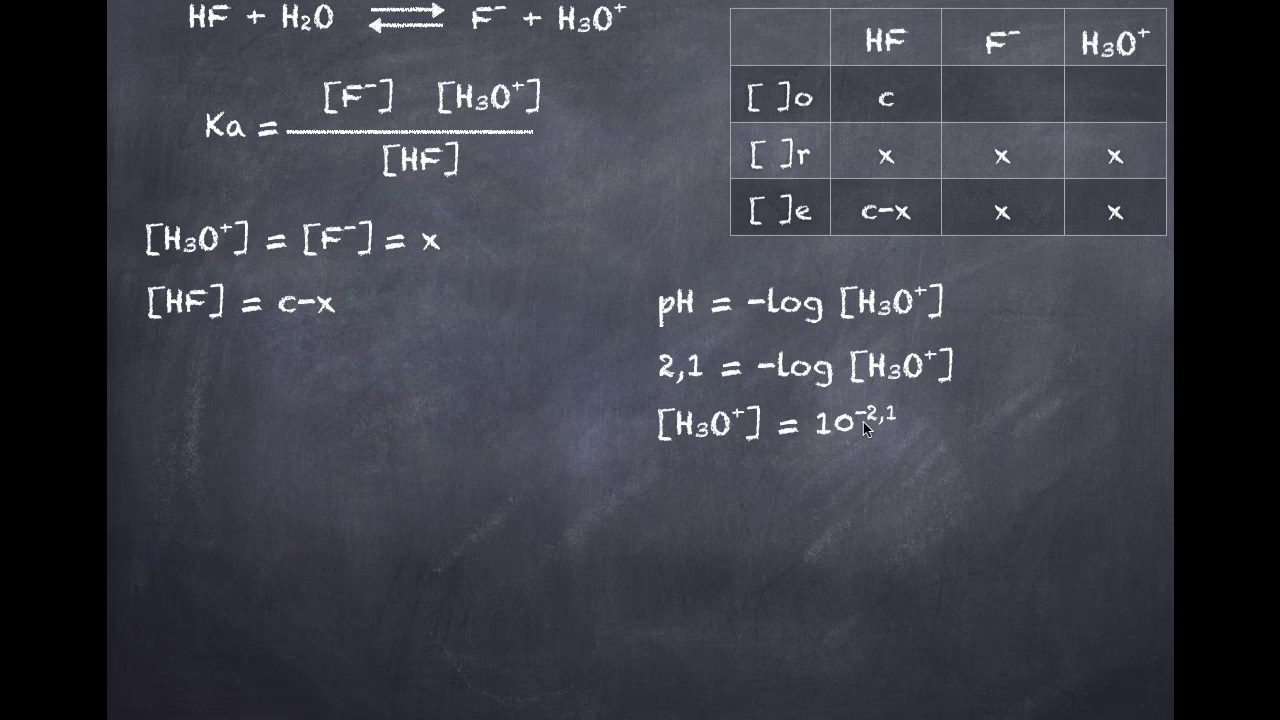
- La Esencia del pH: Concentración de Iones Protón (H+)
- El Papel Crucial del Agua: Autodisociación y Kw
- Cálculo del pH a partir de la Concentración de Iones Hidroxilo (OH-)
- Importancia y Aplicaciones Prácticas del pH
- Tabla Comparativa: pH, [H+] y [OH-] en Diferentes Soluciones
- Preguntas Frecuentes sobre el pH y las Concentraciones Iónicas
- Conclusión
La Esencia del pH: Concentración de Iones Protón (H+)
En el corazón de la definición de pH se encuentra la concentración de iones de hidrógeno, a menudo representados como H+ o, más precisamente en soluciones acuosas, como iones hidronio (H3O+). La forma en que medimos la acidez o alcalinidad de una solución se expresa a través de una escala logarítmica, lo que permite manejar un rango muy amplio de concentraciones de iones de hidrógeno de una manera más manejable. La fórmula universalmente aceptada para el pH es:
pH = -log[H+]
Aquí, [H+] representa la concentración molar de iones de hidrógeno en moles por litro (mol/L). El término "logaritmo" se refiere al logaritmo en base 10. Lo que esta fórmula nos indica es una relación inversamente proporcional: a medida que la concentración de iones H+ aumenta, el valor del pH disminuye, indicando una solución más ácida. Por el contrario, si la concentración de H+ disminuye, el pH aumenta, lo que significa que la solución se vuelve más básica o alcalina.
Por ejemplo, una solución con una concentración de [H+] = 1 x 10-3 M tendrá un pH de 3 (ácido). Una solución con [H+] = 1 x 10-7 M tendrá un pH de 7 (neutro), y una con [H+] = 1 x 10-11 M tendrá un pH de 11 (básico). Esta escala logarítmica es lo que permite que un cambio de una unidad en el pH represente un cambio de diez veces en la concentración de iones de hidrógeno.
El Papel Crucial del Agua: Autodisociación y Kw
Para comprender completamente la relación entre pH, iones protón y iones hidroxilo, es fundamental entender cómo se comporta el agua. El agua pura, aunque a menudo se considera una sustancia estable, experimenta un proceso de autodisociación, donde algunas moléculas de agua se disocian en iones de hidrógeno (H+) e iones hidroxilo (OH-).
H2O(l) ⇌ H+(aq) + OH-(aq)
Este proceso ocurre en muy pequeña medida, pero es constante. A una temperatura de 25°C, el producto de las concentraciones de estos dos iones en agua pura es una constante conocida como el producto iónico del agua, simbolizado como Kw:
Kw = [H+][OH-] = 1.0 x 10-14
Esta constante es de suma importancia porque establece una relación directa entre las concentraciones de iones H+ y OH- en cualquier solución acuosa. Si conocemos la concentración de uno de ellos, podemos fácilmente calcular la concentración del otro. Por ejemplo, en agua pura, donde [H+] = [OH-], ambas concentraciones son 1.0 x 10-7 M, lo que resulta en un pH de 7 (neutro).
Esta relación es la clave para poder calcular el pH incluso cuando solo conocemos la concentración de iones hidroxilo (OH-), ya que nos permite primero determinar la concentración de iones protón (H+) o, alternativamente, utilizar el concepto de pOH.
Cálculo del pH a partir de la Concentración de Iones Hidroxilo (OH-)
En muchas ocasiones, especialmente cuando se trabaja con soluciones básicas o alcalinas, la concentración que se mide o se conoce directamente es la de los iones hidroxilo (OH-). Aunque la fórmula del pH se basa en [H+], la relación de Kw nos proporciona las herramientas necesarias para realizar la conversión. Existen dos métodos principales para calcular el pH a partir de la concentración de OH-:
Método 1: Usando Kw para Encontrar [H+] Primero
- Paso 1: Calcular [H+] usando Kw.
Dado que
Kw = [H+][OH-], podemos reorganizar la fórmula para encontrar [H+]:[H+] = Kw / [OH-]Recuerda que Kw es 1.0 x 10-14 a 25°C.
- Paso 2: Calcular el pH usando la fórmula del pH.
Una vez que tienes [H+], simplemente aplica la fórmula del pH:
pH = -log[H+]
Ejemplo práctico: Supongamos que tienes una solución de hidróxido de sodio (NaOH) con una concentración de iones OH- de 1.0 x 10-2 M.
- Primero, calcula [H+]:
[H+] = (1.0 x 10-14) / (1.0 x 10-2) = 1.0 x 10-12 M - Luego, calcula el pH:
pH = -log(1.0 x 10-12) = 12
Este resultado tiene sentido, ya que las soluciones de hidróxido de sodio son altamente básicas, y un pH de 12 confirma esto.
Método 2: Usando pOH
Este método es a menudo más directo y se basa en el concepto de pOH, que es análogo al pH pero para los iones hidroxilo:
pOH = -log[OH-]
La relación entre pH y pOH se deriva directamente de la constante Kw. Si aplicamos el logaritmo negativo a ambos lados de la ecuación de Kw:
-log(Kw) = -log([H+][OH-])
-log(Kw) = -log[H+] + (-log[OH-])
Dado que -log(Kw) es -log(1.0 x 10-14) = 14 (a 25°C), y que -log[H+] es pH y -log[OH-] es pOH, obtenemos la relación fundamental:
14 = pH + pOH
Por lo tanto, los pasos para calcular el pH a partir de [OH-] usando pOH son:
- Paso 1: Calcular el pOH.
Usa la concentración de OH- dada para encontrar el pOH:
pOH = -log[OH-] - Paso 2: Calcular el pH.
Usa la relación
pH = 14 - pOHpara encontrar el pH:pH = 14 - pOH
Ejemplo práctico: Usando la misma solución de hidróxido de sodio con una concentración de iones OH- de 1.0 x 10-2 M.

- Primero, calcula el pOH:
pOH = -log(1.0 x 10-2) = 2 - Luego, calcula el pH:
pH = 14 - 2 = 12
Ambos métodos producen el mismo resultado, lo que demuestra la coherencia de los principios de la química ácido-base. La elección del método a menudo depende de la preferencia personal o del contexto del problema.
Importancia y Aplicaciones Prácticas del pH
Entender el pH y su cálculo no es solo un ejercicio académico; tiene profundas implicaciones en una multitud de campos y aspectos de nuestra vida diaria. Aquí exploramos algunas de las aplicaciones más relevantes:
En Biología y Medicina
- Cuerpo Humano: El mantenimiento del pH en el cuerpo humano es vital. La sangre, por ejemplo, tiene un pH muy estrechamente regulado entre 7.35 y 7.45. Desviaciones significativas de este rango pueden ser mortales. Otros fluidos corporales, como el jugo gástrico (muy ácido, pH 1.5-3.5) o la orina (pH variable), también tienen rangos de pH específicos para su función óptima.
- Enzimas: Las enzimas, proteínas que catalizan reacciones biológicas, funcionan de manera óptima dentro de rangos de pH muy específicos. Un pH fuera de este rango puede desnaturalizar la enzima, haciendo que pierda su estructura y función.
- Cultivos Celulares: En laboratorios, el control del pH es crucial para el crecimiento y mantenimiento de cultivos celulares y microorganismos, asegurando un ambiente propicio para su desarrollo.
En Agricultura y Ciencias del Suelo
- Disponibilidad de Nutrientes: El pH del suelo afecta directamente la disponibilidad de nutrientes para las plantas. Algunos nutrientes son más solubles y accesibles en suelos ácidos, mientras que otros lo son en suelos alcalinos. Por ejemplo, el hierro y el manganeso son más disponibles en suelos ácidos, mientras que el calcio y el magnesio lo son en suelos más neutros o alcalinos.
- Crecimiento de Cultivos: Diferentes cultivos tienen rangos de pH óptimos para su crecimiento. Los agricultores a menudo ajustan el pH del suelo (mediante la adición de cal para aumentar el pH o azufre para disminuirlo) para maximizar el rendimiento de sus cosechas.
En la Industria
- Industria Alimentaria: El pH es un factor crítico en la conservación de alimentos, la seguridad alimentaria y el sabor. Por ejemplo, el pH bajo de los cítricos ayuda a su conservación, mientras que el pH es monitoreado en la producción de quesos, cervezas y productos lácteos para asegurar la calidad y prevenir el crecimiento de microorganismos indeseables.
- Industria Cosmética: Los productos para el cuidado de la piel y el cabello están formulados para tener un pH compatible con el pH natural de la piel (aproximadamente 5.5, ligeramente ácido) para evitar irritaciones y mantener la salud de la piel y el cabello.
- Tratamiento de Aguas: El pH del agua es monitoreado y ajustado en plantas de tratamiento de agua potable y aguas residuales. Un pH adecuado es esencial para la efectividad de los procesos de coagulación, desinfección y para prevenir la corrosión de las tuberías.
- Procesos Químicos: Muchas reacciones químicas en la industria requieren un pH específico para proceder eficientemente o para producir los productos deseados. El control del pH es fundamental en la síntesis de fármacos, la producción de polímeros y la fabricación de productos químicos en general.
En el Medio Ambiente
- Lluvia Ácida: Las emisiones de óxidos de azufre y nitrógeno a la atmósfera pueden reaccionar con el agua para formar ácidos, dando lugar a la lluvia ácida. Un pH bajo en la lluvia puede dañar bosques, lagos, edificios y monumentos.
- Salud de Ecosistemas Acuáticos: El pH de los ríos, lagos y océanos es vital para la supervivencia de la vida acuática. Pequeños cambios en el pH pueden tener efectos devastadores en peces, anfibios e invertebrados. La acidificación de los océanos, causada por la absorción de dióxido de carbono atmosférico, es una preocupación creciente.
Tabla Comparativa: pH, [H+] y [OH-] en Diferentes Soluciones
Para ilustrar la relación entre el pH y las concentraciones iónicas, la siguiente tabla presenta ejemplos de soluciones comunes y sus valores aproximados a 25°C. Observa cómo un cambio en el pH refleja cambios exponenciales en las concentraciones de H+ y OH-.
| Sustancia | pH Aproximado | [H+] Aproximado (M) | [OH-] Aproximado (M) | Clasificación |
|---|---|---|---|---|
| Ácido de batería | 0 | 1.0 x 100 | 1.0 x 10-14 | Fuertemente Ácido |
| Jugo gástrico | 1.5 | 3.2 x 10-2 | 3.2 x 10-13 | Muy Ácido |
| Jugo de limón | 2.0 | 1.0 x 10-2 | 1.0 x 10-12 | Ácido |
| Vinagre | 2.9 | 1.3 x 10-3 | 7.7 x 10-12 | Ácido |
| Refresco | 3.0 | 1.0 x 10-3 | 1.0 x 10-11 | Ácido |
| Café negro | 5.0 | 1.0 x 10-5 | 1.0 x 10-9 | Ligeramente Ácido |
| Leche | 6.5 | 3.2 x 10-7 | 3.2 x 10-8 | Ligeramente Ácido |
| Agua pura | 7.0 | 1.0 x 10-7 | 1.0 x 10-7 | Neutro |
| Sangre humana | 7.4 | 4.0 x 10-8 | 2.5 x 10-7 | Ligeramente Básico |
| Bicarbonato de sodio | 8.4 | 4.0 x 10-9 | 2.5 x 10-6 | Básico |
| Leche de magnesia | 10.5 | 3.2 x 10-11 | 3.2 x 10-4 | Básico |
| Amoníaco doméstico | 11.5 | 3.2 x 10-12 | 3.2 x 10-3 | Básico |
| Blanqueador (lejía) | 12.5 | 3.2 x 10-13 | 3.2 x 10-2 | Muy Básico |
| Limpiador de desagües | 14.0 | 1.0 x 10-14 | 1.0 x 100 | Fuertemente Básico |
Preguntas Frecuentes sobre el pH y las Concentraciones Iónicas
¿Qué significa un pH de 7?
Un pH de 7 indica una solución neutra. En este punto, la concentración de iones de hidrógeno (H+) es exactamente igual a la concentración de iones hidroxilo (OH-). A 25°C, ambas concentraciones son 1.0 x 10-7 M. El agua pura es el ejemplo clásico de una solución neutra.
¿Puede el pH ser negativo o mayor que 14?
Sí, teóricamente es posible, aunque es menos común encontrar soluciones con pH fuera del rango 0-14 en la vida cotidiana. El rango de 0 a 14 es el más práctico para la mayoría de las soluciones acuosas diluidas. Sin embargo, para soluciones muy concentradas de ácidos fuertes (como ácido clorhídrico 10 M), la concentración de H+ puede ser mayor que 1 M, lo que resultaría en un pH negativo (por ejemplo, si [H+] = 10 M, pH = -log(10) = -1). De manera similar, soluciones muy concentradas de bases fuertes pueden tener un pH mayor que 14 (por ejemplo, si [OH-] = 10 M, pOH = -1, entonces pH = 14 - (-1) = 15).
¿Cómo afecta la temperatura al pH?
La temperatura afecta el pH principalmente a través de su impacto en la constante de autodisociación del agua (Kw). A medida que la temperatura aumenta, la autodisociación del agua se incrementa, lo que significa que Kw aumenta. Esto hace que las concentraciones de H+ y OH- en agua pura aumenten, y por lo tanto, el pH del agua neutra disminuye (se vuelve ligeramente más ácida en términos de valor numérico, pero sigue siendo neutra porque [H+] = [OH-]). Por ejemplo, a 0°C, el pH del agua pura es 7.47, mientras que a 100°C, es 6.14. Es crucial especificar la temperatura al reportar valores de pH para una precisión química.
¿Cuál es la diferencia entre un ácido fuerte y un ácido débil?
La diferencia radica en su grado de disociación en agua:
- Ácido Fuerte: Se disocia completamente (o casi completamente) en iones H+ cuando se disuelve en agua. Ejemplos incluyen el ácido clorhídrico (HCl), el ácido nítrico (HNO3) y el ácido sulfúrico (H2SO4). Esto significa que la concentración inicial del ácido es directamente la concentración de H+.
- Ácido Débil: Solo se disocia parcialmente en iones H+ en agua. Existe un equilibrio entre la forma no disociada del ácido y sus iones. Ejemplos son el ácido acético (CH3COOH, componente principal del vinagre) y el ácido carbónico (H2CO3). Para calcular el pH de un ácido débil, se requiere el uso de su constante de disociación ácida (Ka) y a menudo un cálculo de equilibrio.
Una base fuerte y una base débil se definen de manera análoga, en función de su grado de disociación en iones OH-.
¿Por qué la escala de pH es logarítmica?
La escala de pH es logarítmica porque la concentración de iones H+ en soluciones acuosas puede variar en un rango extremadamente amplio, desde aproximadamente 10 M (ácidos muy fuertes) hasta 10-15 M (bases muy fuertes). Si usáramos una escala lineal, sería muy difícil representar y comparar estas concentraciones. La escala logarítmica comprime este vasto rango en una escala más manejable (generalmente de 0 a 14), donde cada unidad de pH representa un cambio de diez veces en la concentración de H+. Esto facilita la comprensión y el trabajo con las variaciones de acidez y alcalinidad.
Conclusión
El pH es mucho más que un simple número; es una medida fundamental que rige innumerables procesos en la naturaleza, la tecnología y la vida diaria. Comprender su relación directa con la concentración de iones protón (H+) y su vínculo indirecto, pero igualmente crucial, con la concentración de iones hidroxilo (OH-) a través de la constante de Kw, es esencial para cualquier persona que interactúe con el mundo químico. Ya sea que estemos hablando de la salud del suelo para nuestros cultivos, la seguridad de nuestros alimentos o el delicado equilibrio de nuestro propio cuerpo, el pH es un indicador clave.
Las calculadoras, tanto las físicas como las integradas en software, son herramientas invaluables para realizar estos cálculos de pH y pOH de manera rápida y precisa, permitiéndonos aplicar estos principios químicos en contextos prácticos sin errores manuales. Dominar estos conceptos nos empodera para entender y manipular mejor las propiedades de las soluciones, abriendo puertas a innovaciones y soluciones en diversos campos científicos e industriales. La próxima vez que uses una calculadora para resolver un problema de pH, recordarás la profundidad de la química que hay detrás de cada número.
Si quieres conocer otros artículos parecidos a La Relación pH, Protones y su Cálculo puedes visitar la categoría Química.

