28/04/2024
En el vasto y complejo universo de la química, comprender la estructura interna de los átomos es fundamental para desentrañar el comportamiento de la materia. Durante mucho tiempo, modelos atómicos como el de Bohr proporcionaron una visión simplificada, utilizando un solo número cuántico para describir la órbita de los electrones. Sin embargo, con el advenimiento de la mecánica cuántica y el modelo de Schrödinger, se hizo evidente que los electrones no solo se mueven en órbitas fijas, sino que ocupan un espacio tridimensional complejo, conocido como orbitales. Para describir estos orbitales y, en última instancia, la posición y energía de los electrones, necesitamos una serie de valores numéricos precisos: los números cuánticos.

Los números cuánticos son como las coordenadas GPS de un electrón dentro de un átomo, proporcionando información detallada sobre su energía, la forma del espacio que ocupa y su orientación en el espacio. Son la base para entender cómo se organizan los electrones y cómo interactúan con otros átomos, lo que a su vez determina las propiedades químicas de los elementos. Al adentrarnos en estos conceptos, descubriremos las reglas que gobiernan el mundo subatómico y cómo se construyen las configuraciones electrónicas que definen cada elemento en la tabla periódica.
Los Cuatro Pilares Cuánticos: Tipos de Números Cuánticos
Existen cuatro números cuánticos principales, cada uno aportando una pieza crucial al rompecabezas de la ubicación y el estado de un electrón. Derivados de las ecuaciones de onda de Schrödinger (con la adición del número de espín), estos números son el principal, el azimutal o secundario, el magnético y el de espín.
El Número Cuántico Principal (n): Tamaño y Energía
El primer número cuántico es el número cuántico principal, denotado por la letra ‘n’. Este número describe el tamaño del orbital y, de forma indirecta, la energía del electrón. Cuanto mayor sea el valor de ‘n’, mayor será el tamaño del orbital y, por lo general, mayor será la energía del electrón dentro de ese orbital. Los electrones con ‘n = 2’ están, por ejemplo, más lejos del núcleo y tienen más energía que aquellos con ‘n = 1’. Los valores permitidos para ‘n’ son enteros positivos: 1, 2, 3, 4, y así sucesivamente. Cada valor de ‘n’ corresponde a una capa electrónica o nivel de energía principal.
El Número Cuántico Azimutal o Secundario (l): Forma del Orbital
El segundo número cuántico es el número cuántico azimutal (o secundario), representado por la letra ‘l’. Este número define la forma del orbital. A diferencia del modelo de Bohr con sus órbitas circulares, los orbitales cuánticos pueden tener formas diversas. Los valores de ‘l’ dependen del valor de ‘n’; puede tomar cualquier valor entero desde 0 hasta ‘n - 1’.
- Si ‘l = 0’, el orbital tiene forma esférica y se denomina orbital ‘s’.
- Si ‘l = 1’, el orbital tiene forma polar (como un lóbulo doble) y se denomina orbital ‘p’.
- Si ‘l = 2’, el orbital tiene forma de trébol (o más compleja) y se denomina orbital ‘d’.
- Si ‘l = 3’, el orbital tiene formas aún más complejas y se denomina orbital ‘f’.
Estas letras (s, p, d, f) son convencionales y se utilizan para identificar las subcapas dentro de una capa principal.
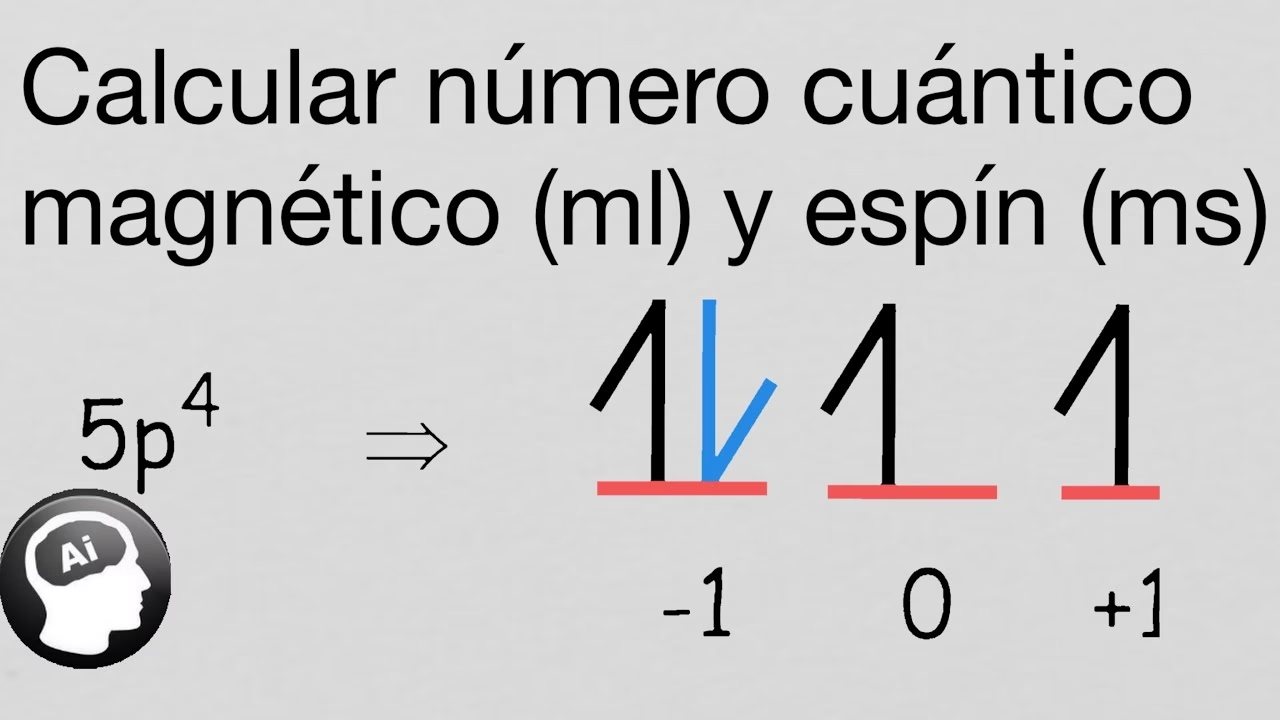
El Número Cuántico Magnético (m_l): Orientación en el Espacio
El tercer número cuántico es el número cuántico magnético, simbolizado por ‘m_l’ (o simplemente ‘m’). Este número describe la orientación espacial del orbital. Mientras que un orbital esférico (l=0) solo puede tener una orientación, los orbitales con formas más complejas (p, d, f) pueden apuntar en diferentes direcciones en el espacio. El valor de ‘m_l’ depende del valor de ‘l’; puede tomar cualquier valor entero desde ‘-l’ hasta ‘+l’, incluyendo el cero.
- Para ‘l = 0’ (orbital s), ‘m_l’ solo puede ser 0 (1 orientación).
- Para ‘l = 1’ (orbital p), ‘m_l’ puede ser -1, 0, +1 (3 orientaciones: p_x, p_y, p_z).
- Para ‘l = 2’ (orbital d), ‘m_l’ puede ser -2, -1, 0, +1, +2 (5 orientaciones).
El nombre ‘magnético’ proviene de la observación original de que diferentes orientaciones de los orbitales se manifestaban en presencia de un campo magnético.
El Número Cuántico de Spin (m_s): El Giro del Electrón
El cuarto y último número cuántico es el número cuántico de spin, denotado por ‘m_s’ (o ‘s’). Este número no se deriva de la ecuación de Schrödinger, sino que fue introducido experimentalmente para explicar ciertas propiedades de los electrones. Describe una propiedad intrínseca del electrón, similar a un giro o rotación sobre su propio eje, que genera un pequeño campo magnético. Solo hay dos valores posibles para ‘m_s’:
- +1/2 (generalmente representado como ‘espín arriba’ ↑)
- -1/2 (generalmente representado como ‘espín abajo’ ↓)
Este número es crucial porque el Principio de Exclusión de Pauli establece que no puede haber dos electrones en un mismo átomo con los mismos cuatro números cuánticos idénticos. Por lo tanto, un orbital puede contener un máximo de dos electrones, y si los contiene, deben tener espines opuestos.
Reglas que Gobiernan las Combinaciones de Números Cuánticos
La combinación de los valores de ‘n’, ‘l’ y ‘m_l’ define un orbital atómico, mientras que los cuatro números cuánticos (incluyendo ‘m_s’) definen el estado de un electrón específico dentro de ese orbital. Las reglas para sus valores permitidos son estrictas:
- n (Número Cuántico Principal): Debe ser un entero positivo (1, 2, 3, ...). Nunca puede ser cero.
- l (Número Cuántico Azimutal): Puede ser cualquier entero desde 0 hasta ‘n - 1’. Esto significa que el número de subcapas dentro de una capa es igual a ‘n’. Por ejemplo, si ‘n = 3’, ‘l’ puede ser 0, 1 o 2.
- m_l (Número Cuántico Magnético): Puede ser cualquier entero desde ‘-l’ hasta ‘+l’. El número de orbitales dentro de una subcapa es ‘2l + 1’.
- m_s (Número Cuántico de Spin): Solo puede ser +1/2 o -1/2.
Estas reglas implican que cada valor de ‘n’ tiene ‘n’ subcapas, y cada subcapa ‘l’ tiene ‘2l + 1’ orbitales. El número total de orbitales en una capa es ‘n^2’.
Ejemplos de Combinaciones Permitidas
Veamos algunas combinaciones posibles de números cuánticos para las primeras capas:
Capa n = 1
Para n = 1:
- l solo puede ser 0 (porque l debe ser de 0 a n-1, es decir, de 0 a 0).
- Si l = 0, m_l solo puede ser 0 (porque m_l debe ser de -l a +l, es decir, de 0 a 0).
Esto significa que en la capa n=1, solo existe un tipo de orbital: el 1s.
| n | l | m_l | Notación Subcapa | Número de Orbitales |
|---|---|---|---|---|
| 1 | 0 | 0 | 1s | 1 |
Capa n = 2
Para n = 2:
- l puede ser 0 o 1.
- Si l = 0, m_l = 0 (orbital 2s).
- Si l = 1, m_l puede ser -1, 0, +1 (orbitales 2p).
En la capa n=2, hay un orbital 2s y tres orbitales 2p (2p_x, 2p_y, 2p_z).
| n | l | m_l | Notación Subcapa | Número de Orbitales |
|---|---|---|---|---|
| 2 | 0 | 0 | 2s | 1 |
| 2 | 1 | -1, 0, +1 | 2p | 3 |
Capa n = 3
Para n = 3:
- l puede ser 0, 1 o 2.
- Si l = 0, m_l = 0 (orbital 3s).
- Si l = 1, m_l = -1, 0, +1 (orbitales 3p).
- Si l = 2, m_l = -2, -1, 0, +1, +2 (orbitales 3d).
En la capa n=3, hay un orbital 3s, tres orbitales 3p y cinco orbitales 3d.
| n | l | m_l | Notación Subcapa | Número de Orbitales |
|---|---|---|---|---|
| 3 | 0 | 0 | 3s | 1 |
| 3 | 1 | -1, 0, +1 | 3p | 3 |
| 3 | 2 | -2, -1, 0, +1, +2 | 3d | 5 |
Cada uno de estos orbitales puede albergar un máximo de dos electrones, cada uno con un espín opuesto (+1/2 y -1/2). Así, el número máximo de electrones en una subcapa es ‘2 * (2l + 1)’, y en una capa es ‘2 * n^2’.
Configuraciones Electrónicas: Llenando los Orbitales
La configuración electrónica de un átomo describe la distribución de sus electrones en los diferentes orbitales. Para determinar esta configuración, se siguen tres principios fundamentales:
1. Principio de Aufbau (Principio de Construcción)
Este principio establece que los electrones ocupan los orbitales disponibles de menor energía antes de ocupar los de mayor energía. Es como llenar un edificio de apartamentos: primero se ocupan los pisos más bajos. La energía de un orbital está determinada principalmente por su número cuántico principal (n) y, en átomos multielectrónicos, también por su número cuántico azimutal (l).

La regla general de energía es que, para una misma capa, los orbitales ‘s’ tienen menor energía que los ‘p’, que a su vez tienen menor energía que los ‘d’, y así sucesivamente (s < p < d < f). Sin embargo, para átomos con múltiples electrones, el orden de llenado puede ser más complejo debido a interacciones electrón-electrón, lo que a veces lleva a que orbitales de una capa superior (mayor n) tengan menor energía que orbitales de una capa inferior (menor n) pero con un ‘l’ más alto (por ejemplo, 4s se llena antes que 3d).
Existe un diagrama mnemotécnico popular, la regla de las diagonales, que ayuda a recordar el orden de llenado de los orbitales:
1s
2s 2p
3s 3p 3d
4s 4p 4d 4f
5s 5p 5d 5f
6s 6p 6d
7s 7p
Siguiendo las flechas diagonales de arriba a abajo, el orden de llenado es: 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f < 5d < 6p < 7s < 5f < 6d < 7p...
2. Principio de Exclusión de Pauli
Como mencionamos, este principio establece que no puede haber dos electrones en un mismo átomo que tengan el mismo conjunto de cuatro números cuánticos. Esto significa que un orbital atómico (definido por n, l y m_l) puede contener un máximo de dos electrones, y si contiene dos, deben tener espines opuestos (uno con m_s = +1/2 y el otro con m_s = -1/2).
3. Regla de Hund (Regla de Máxima Multiplicidad)
Cuando hay orbitales degenerados (orbitales con la misma energía, como los tres orbitales 2p o los cinco orbitales 3d), la regla de Hund establece que los electrones llenarán estos orbitales individualmente con espines paralelos (el mismo valor de m_s) antes de que cualquier orbital sea ocupado por un segundo electrón. Solo después de que todos los orbitales degenerados contengan un electrón cada uno, los electrones adicionales comenzarán a aparearse con los electrones existentes, ocupando los mismos orbitales pero con espín opuesto.
Por ejemplo, para el carbono (Z=6), su configuración electrónica es 1s² 2s² 2p². Los dos electrones en los orbitales 2p se distribuyen en orbitales diferentes (por ejemplo, 2p_x¹ 2p_y¹) con espines paralelos, en lugar de aparearse en un solo orbital (2p_x²).
Excepciones a las Configuraciones Predichas
Si bien el principio de Aufbau predice con precisión la configuración electrónica de la mayoría de los elementos, existen algunas excepciones, especialmente en los metales de transición. Los casos más notables son el cromo (Cr) y el cobre (Cu). En estos elementos, la configuración experimentalmente determinada difiere de la predicha por el diagrama de Aufbau. Por ejemplo, para el cromo (Z=24), se esperaría [Ar] 4s² 3d⁴, pero la configuración real es [Ar] 4s¹ 3d⁵. Para el cobre (Z=29), se esperaría [Ar] 4s² 3d⁹, pero es [Ar] 4s¹ 3d¹⁰.
Estas excepciones se deben a la estabilidad adicional que se logra cuando los orbitales ‘d’ están medio llenos (d⁵) o completamente llenos (d¹⁰), lo que es energéticamente más favorable que tener orbitales ‘s’ y ‘d’ parcialmente llenos. La diferencia de energía entre los orbitales 4s y 3d es lo suficientemente pequeña como para permitir que un electrón se transfiera en estos casos.

La Relación entre Configuraciones Electrónicas y la Tabla Periódica
La organización de la tabla periódica es un reflejo directo de las configuraciones electrónicas de los elementos. Los elementos se agrupan en bloques y períodos basados en qué orbitales están siendo llenados:
- Bloque s: Las dos primeras columnas (Grupos 1 y 2) corresponden al llenado de los orbitales ‘s’.
- Bloque p: Las seis columnas de la derecha (Grupos 13 a 18) corresponden al llenado de los orbitales ‘p’.
- Bloque d: Los diez grupos de metales de transición en el centro (Grupos 3 a 12) corresponden al llenado de los orbitales ‘d’.
- Bloque f: Las dos filas separadas en la parte inferior (lantánidos y actínidos) corresponden al llenado de los orbitales ‘f’.
Esta relación es fundamental porque las propiedades químicas de un elemento están determinadas en gran medida por la configuración de sus electrones más externos (electrones de valencia), que residen en los orbitales de la capa más energética.
Preguntas Frecuentes sobre los Números Cuánticos
¿Cómo se calcula el número cuántico?
Los números cuánticos no se “calculan” en el sentido de una operación matemática directa como una suma o una multiplicación. Más bien, son valores que se determinan o asignan a un electrón en un átomo basándose en un conjunto de reglas fundamentales que derivan de la mecánica cuántica. Se obtienen al resolver la ecuación de onda de Schrödinger para el átomo, que describe el comportamiento de los electrones. Una vez que se conoce el número cuántico principal (n), los valores posibles para los otros números cuánticos (l, m_l, m_s) se restringen según las reglas previamente mencionadas.
¿Cuál es la regla para los números cuánticos?
Las reglas que rigen los números cuánticos son:
- n (principal): Enteros positivos (1, 2, 3, ...). Indica el nivel de energía y el tamaño del orbital.
- l (azimutal/secundario): Enteros desde 0 hasta ‘n - 1’. Indica la forma del orbital (s, p, d, f).
- m_l (magnético): Enteros desde ‘-l’ hasta ‘+l’, incluyendo el 0. Indica la orientación espacial del orbital.
- m_s (spin): Solo +1/2 o -1/2. Indica la dirección del ‘giro’ del electrón.
Además, el Principio de Exclusión de Pauli establece que no hay dos electrones en un mismo átomo que puedan tener el mismo conjunto de los cuatro números cuánticos.
¿Cómo se calcula el número cuántico de espín?
El número cuántico de espín (m_s) no se “calcula” a partir de una fórmula o integral en el contexto de la asignación a un electrón en un átomo. Es una propiedad intrínseca del electrón que solo puede tomar uno de dos valores discretos: +1/2 o -1/2. Estos valores se asignan para distinguir los dos posibles estados de espín de un electrón dentro de un orbital. Si un orbital contiene dos electrones, uno se asigna arbitrariamente como +1/2 y el otro como -1/2 para cumplir con el Principio de Exclusión de Pauli.
¿Cuáles son los 4 números cuánticos?
Los cuatro números cuánticos son:
- Número Cuántico Principal (n): Define el nivel de energía principal del electrón y el tamaño del orbital.
- Número Cuántico Azimutal o Secundario (l): Define la forma del orbital y la subcapa a la que pertenece (s, p, d, f).
- Número Cuántico Magnético (m_l): Define la orientación del orbital en el espacio.
- Número Cuántico de Spin (m_s): Define la dirección intrínseca del ‘giro’ del electrón (arriba o abajo).
Estos cuatro números trabajan en conjunto para describir de manera única el estado cuántico de cada electrón en un átomo.
Conclusión
Los números cuánticos son herramientas esenciales en la química y la física modernas. Nos permiten trascender las representaciones simplistas del átomo y adentrarnos en la verdadera complejidad de la distribución electrónica. Comprender estos números y las reglas que los rigen es fundamental para predecir las propiedades de los elementos, explicar la formación de enlaces químicos y, en última instancia, descifrar el comportamiento de la materia a nivel fundamental. Desde la reactividad de un elemento hasta las propiedades de los materiales, todo comienza con la precisa descripción de sus electrones a través de los números cuánticos.
Si quieres conocer otros artículos parecidos a Los Números Cuánticos: La Clave de los Átomos puedes visitar la categoría Química.
