28/05/2022
La presión es una de las propiedades más fundamentales y omnipresentes en el estudio de la materia, especialmente cuando se trata de mezclas. Comprender cómo se comportan los gases, líquidos y sólidos cuando se combinan es esencial para una vasta gama de aplicaciones, desde la ingeniería química hasta la meteorología y la seguridad ambiental. ¿Alguna vez te has preguntado por qué el agua hierve a una temperatura más baja en la montaña o cómo se calcula la concentración de un vapor tóxico en el aire? La respuesta a estas preguntas reside en el estudio de las presiones en mezclas.

Este artículo te guiará a través de los principios clave que rigen la presión de mezclas, abordando tanto la ley de los gases ideales como el complejo mundo de la presión de vapor en líquidos y sólidos. Exploraremos las leyes fundamentales, las ecuaciones prácticas para su cálculo y las implicaciones de estas propiedades en el mundo real.
- Presión en Mezclas Gaseosas: La Ley de Dalton
- La Presión de Vapor: Un Concepto Fundamental
- Estimación de la Presión de Vapor: La Ecuación de Antoine
- Presión en Mezclas Líquidas: La Ley de Raoult
- Presión de Vapor en Sólidos
- Importancia y Aplicaciones de la Presión en Mezclas
- Preguntas Frecuentes (FAQ)
Presión en Mezclas Gaseosas: La Ley de Dalton
Cuando hablamos de una mezcla de gases, la intuición podría sugerir que la presión total es el resultado de una interacción compleja entre las moléculas de cada gas. Sin embargo, para los gases ideales (un modelo que se aproxima muy bien a muchos gases reales bajo condiciones normales), la realidad es sorprendentemente simple. La Ley de Dalton de las Presiones Parciales establece que la presión total ejercida por una mezcla de gases ideales es simplemente la suma de las presiones que cada gas ejercería si ocupara el volumen total por sí solo.
Matemáticamente, esto se expresa como:
P(total) = P1 + P2 + P3 + ... + Pn
Donde P(total) es la presión total de la mezcla, y P1, P2, P3, ..., Pn son las presiones parciales de cada gas componente en la mezcla. La presión parcial de un gas es la presión que ese gas ejercería si fuera el único gas presente en el mismo volumen y a la misma temperatura que la mezcla.
Esta ley es de suma importancia en campos como la química atmosférica, la ingeniería de procesos y la medicina (por ejemplo, en la mezcla de gases para anestesia o buceo). Nos permite desglosar la contribución de cada componente gaseoso a la presión general de un sistema.
Cálculo de Presiones Parciales
Para gases ideales, la presión parcial de un componente también se puede relacionar con su fracción molar. La fracción molar (Xi) de un gas es la relación entre el número de moles de ese gas (ni) y el número total de moles de todos los gases en la mezcla (ntotal):
Xi = ni / ntotal
Entonces, la presión parcial de un gas (Pi) es igual a la fracción molar de ese gas multiplicada por la presión total de la mezcla:
Pi = Xi * P(total)
Esta relación es extremadamente útil, ya que permite determinar la presión de un componente específico incluso si solo conocemos su cantidad relativa en la mezcla y la presión total del sistema.
La Presión de Vapor: Un Concepto Fundamental
Más allá de las mezclas gaseosas, la presión de vapor es un concepto crucial que describe el equilibrio entre una fase condensada (líquida o sólida) y su fase gaseosa. Imagina un líquido en un recipiente cerrado: sus moléculas están constantemente escapando a la fase de vapor (evaporación) y regresando a la fase líquida (condensación). Cuando las tasas de evaporación y condensación se igualan, se establece un equilibrio dinámico, y la presión ejercida por las moléculas en la fase gaseosa sobre el líquido se conoce como presión de vapor.
Medición y Unidades de la Presión de Vapor
La presión de vapor se mide en unidades estándar de presión. La unidad del Sistema Internacional (SI) es el pascal (Pa), que equivale a un newton por metro cuadrado (N·m⁻²). Sin embargo, otras unidades como milímetros de mercurio (mmHg) o atmósferas (atm) son también comunes.
La medición experimental de la presión de vapor es un procedimiento que puede variar en complejidad. Para presiones entre 1 y 200 kPa, es relativamente sencillo. Se obtienen resultados más exactos cerca del punto de ebullición de la sustancia. Un procedimiento común implica purificar la sustancia, aislarla en un contenedor sellado para evitar gases indeseados, y luego medir la presión de equilibrio de la fase gaseosa a diferentes temperaturas. Herramientas como el isoteniscopio pueden mejorar la precisión de estas mediciones.
Factores que Afectan la Presión de Vapor
Temperatura: Es el factor más influyente. A medida que la temperatura de un líquido (o sólido) aumenta, sus moléculas adquieren más energía cinética. Esto les permite superar con mayor facilidad las fuerzas intermoleculares y escapar a la fase de vapor, aumentando así la presión de vapor. Por ejemplo, el agua a 20 °C tiene una presión de vapor de aproximadamente 23.4 mbar, mientras que a 40 °C, esta se eleva a 73.8 mbar. Este aumento exponencial explica por qué ambientes tropicales (cálidos y húmedos) se sienten tan agobiantes: hay una mayor concentración de vapor de agua en el aire.
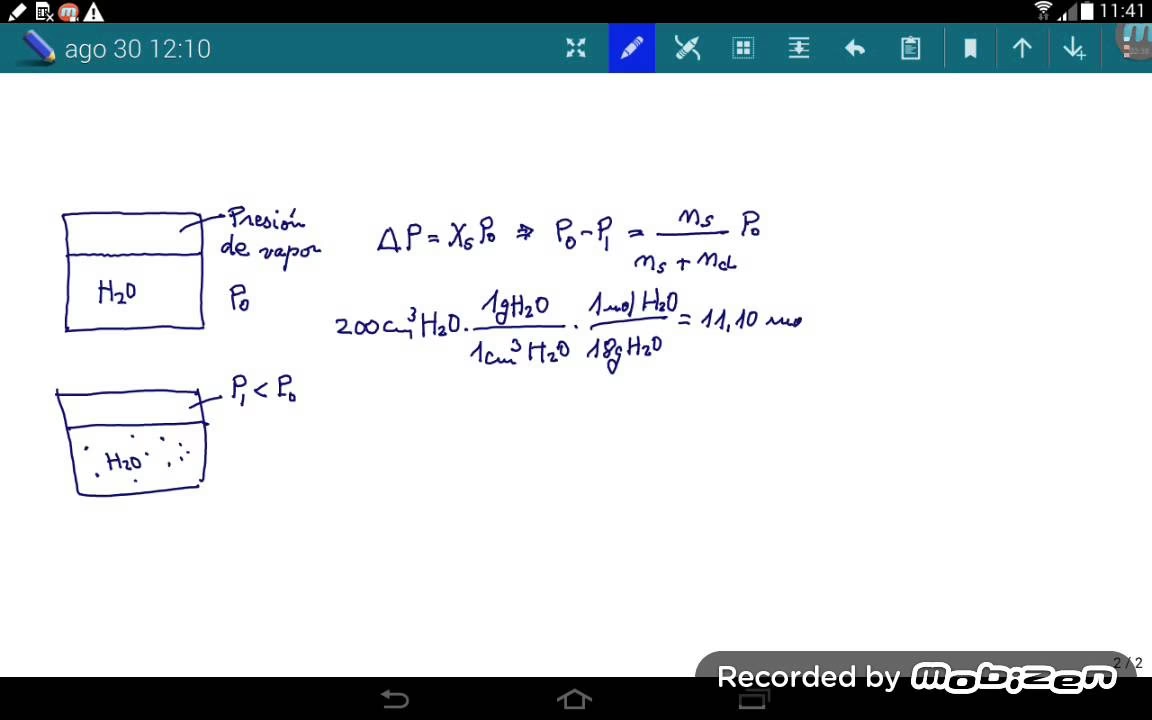
La presión de vapor de un líquido es la presión del gas sobre el líquido resultante de la evaporación cuando el líquido y el gas están en equilibrio dinámico en un recipiente cerrado. La presión de vapor de la solución es siempre menor que la del disolvente puro. Naturaleza de la Sustancia: Cada sustancia tiene una presión de vapor intrínseca que depende de la fuerza de sus fuerzas intermoleculares. Las sustancias con fuerzas intermoleculares débiles (como el clorometano o el propano) tienen presiones de vapor más altas a una temperatura dada en comparación con aquellas con fuerzas intermoleculares fuertes (como el agua). Esto también explica por qué diferentes líquidos tienen diferentes puntos de ebullición; el punto de ebullición es la temperatura a la cual la presión de vapor de un líquido iguala a la presión externa (generalmente la presión atmosférica).
Estimación de la Presión de Vapor: La Ecuación de Antoine
Dado que la relación entre la presión de vapor y la temperatura no es lineal, los científicos han desarrollado ecuaciones empíricas para modelarla. Una de las más utilizadas es la Ecuación de Antoine. Esta ecuación es una expresión matemática pragmática que relaciona la presión de vapor (P) y la temperatura (T) de sustancias líquidas o sólidas puras. Se obtiene por ajuste de curvas a datos experimentales y es ampliamente utilizada en ingeniería química.
La forma básica de la ecuación es:
log P = A - B / (C + T)
Donde:
Pes la presión de vapor.Tes la temperatura.A, B, Cson coeficientes específicos para cada sustancia, obtenidos experimentalmente.logpuede ser el logaritmo decimal (log₁₀) o el logaritmo natural (logₑ).
A veces se utiliza una forma más simple con solo dos coeficientes: log P = A - B / T.
Limitaciones y Precisión
Aunque la Ecuación de Antoine es muy útil, tiene sus limitaciones:
- Cada conjunto de parámetros (A, B, C) es aplicable solo en un intervalo de temperatura específico. Para muchas sustancias volátiles, existen varios conjuntos de parámetros para diferentes rangos.
- Su precisión es baja cuando se usa desde el punto de fusión de un compuesto hasta su temperatura crítica.
- También es poco precisa cuando la presión de vapor es inferior a 10 Torr, debido a las limitaciones del equipo utilizado para establecer los parámetros.
Para una mayor precisión, especialmente en rangos amplios, se utilizan ecuaciones más complejas como la Ecuación de Wagner, que se ajusta mejor a los datos experimentales.
Presión en Mezclas Líquidas: La Ley de Raoult
El comportamiento de la presión de vapor en mezclas líquidas es más complejo que en las mezclas gaseosas, ya que las interacciones entre las moléculas de los diferentes componentes juegan un papel crucial. La Ley de Raoult proporciona una aproximación fundamental para la presión de vapor de mezclas líquidas, especialmente cuando uno de los componentes es un soluto no volátil.
El Efecto de un Soluto No Volátil
Cuando se añade un soluto no volátil (uno cuya presión de vapor es insignificante, como la glucosa en agua) a un solvente volátil (como el agua), la presión de vapor del solvente disminuye. Esto se puede entender cualitativamente: una parte de la superficie del líquido ahora está ocupada por moléculas de soluto no volátiles. Esto significa que hay menos moléculas de solvente en la superficie que pueden escapar a la fase de vapor por unidad de tiempo. Mientras tanto, la tasa a la que las moléculas de solvente en la fase de vapor colisionan con la superficie y regresan al líquido no se ve afectada. El efecto neto es un desplazamiento del equilibrio dinámico, resultando en una menor concentración de moléculas de solvente en la fase de vapor y, por lo tanto, una menor presión de vapor de la solución en comparación con el solvente puro.
Formulación de la Ley de Raoult
Si las partículas del soluto tienen un tamaño similar al del solvente y ambos tienen probabilidades aproximadamente iguales de estar en la superficie, el efecto del soluto sobre la presión de vapor del solvente es proporcional al número de sitios ocupados por las partículas de soluto en la superficie. La Ley de Raoult se expresa como:
P_A = X_A * P°_A
Donde:
P_Aes la presión de vapor del componente A (el solvente) en la solución.X_Aes la fracción molar del componente A en la fase líquida.P°_Aes la presión de vapor del componente A puro.
Si la solución contiene un solo soluto no volátil (B), entonces X_A + X_B = 1. Podemos reordenar la ley para expresar la disminución de la presión de vapor (ΔP_A = P°_A - P_A):
ΔP_A = X_B * P°_A
Esto significa que la disminución de la presión de vapor es directamente proporcional a la fracción molar del soluto no volátil.
Desviaciones de la Ley de Raoult
La Ley de Raoult es ideal para soluciones ideales, donde las interacciones entre las moléculas de soluto y solvente (A-B) son similares a las interacciones entre las moléculas de soluto (A-A) y solvente (B-B) en sus estados puros. Sin embargo, en la realidad, muchas mezclas líquidas muestran desviaciones debido a interacciones moleculares más complejas. Estas desviaciones son cruciales para entender el comportamiento real de las mezclas.
| Tipo de Desviación | Interacciones Moleculares | Presión de Vapor Observada | Punto de Ebullición del Azeótropo | Ejemplo |
|---|---|---|---|---|
| Desviación Positiva | Atracción A-B más débil que A-A o B-B | Mayor que la predicha por Raoult | Menor que los componentes puros (azeótropo de ebullición mínima) | Etanol + Agua |
| Desviación Negativa | Atracción A-B más fuerte que A-A o B-B | Menor que la predicha por Raoult | Mayor que los componentes puros (azeótropo de ebullición máxima) | Cloroformo + Acetona |
Las desviaciones positivas sugieren que las moléculas están "retenidas" con menos fuerza en la fase líquida en la mezcla que en los componentes puros. Las desviaciones negativas, por otro lado, indican que las moléculas se "retienen" con más fuerza en el líquido cuando hay una segunda molécula presente. Estas desviaciones se utilizan para determinar los coeficientes de actividad termodinámica de los componentes en las mezclas, lo que permite refinar los cálculos de presión de vapor para sistemas reales.
Ejemplo Práctico: Cálculo de Presión de Vapor con Etilenglicol
Consideremos un ejemplo práctico para aplicar la Ley de Raoult. El etilenglicol (HOCH₂CH₂OH) es el ingrediente principal del anticongelante automotriz y reduce la presión de vapor del líquido del radiador, lo que a su vez eleva su punto de ebullición. A 100°C, la presión de vapor del agua pura es de 760 mmHg. Calculemos la presión de vapor de una solución acuosa que contiene 30.2% de etilenglicol en masa.

Paso 1: Calcular los moles de cada componente.
Asumimos 1000 g de solución para simplificar. Esto significa 302 g de etilenglicol y 698 g de agua.
- Masa molar del etilenglicol (EG): 62.07 g/mol
- Masa molar del agua (H₂O): 18.02 g/mol
Moles de EG = 302 g / 62.07 g/mol = 4.87 mol EG
Moles de H₂O = 698 g / 18.02 g/mol = 38.7 mol H₂O
Paso 2: Calcular la fracción molar del agua (solvente).
Moles totales = 4.87 mol EG + 38.7 mol H₂O = 43.57 mol
Fracción molar de H₂O (X_H₂O) = 38.7 mol H₂O / 43.57 mol = 0.888
Paso 3: Aplicar la Ley de Raoult.
P_H₂O (solución) = X_H₂O * P°_H₂O (pura)
P_H₂O (solución) = 0.888 * 760 mmHg = 675 mmHg
La presión de vapor de la solución es de 675 mmHg. Esto demuestra cómo la adición de un soluto no volátil reduce significativamente la presión de vapor del solvente.
Presión de Vapor en Sólidos
Aunque a menudo se asocia la presión de vapor con líquidos, los sólidos también poseen una presión de vapor de equilibrio. Para un sólido, esto se define como la presión alcanzada cuando la velocidad de sublimación (paso directo de sólido a vapor) coincide con la velocidad de deposición (paso de vapor a sólido). Para la mayoría de los sólidos, esta presión es extremadamente baja a temperaturas ambiente, lo que dificulta su medición. Sin embargo, hay excepciones notables como el naftaleno (bolas de naftalina), el hielo y el hielo seco (CO₂ sólido), que tienen presiones de vapor significativas.
La presión de vapor del hielo seco, por ejemplo, es de 5.73 MPa (aproximadamente 56.5 atm) a 20 °C, lo que explica por qué debe manipularse con cuidado y en recipientes adecuados, ya que puede romper la mayoría de los contenedores sellados.
Estimación de Presión de Sublimación
Existen métodos para calcular la presión de sublimación de un sólido. Uno de ellos implica extrapolar la presión de vapor del líquido sobreenfriado y utilizar el calor de fusión, aplicando una forma particular de la relación de Clausius-Clapeyron:
ln P_s_sub = ln P_l_sub - (ΔfusH / R) * (1/T_sub - 1/T_fus)
Donde:
P_s_subes la presión de sublimación del sólido aT_sub.P_l_subes la presión de vapor del líquido sobreenfriado aT_sub.ΔfusHes el calor de fusión.Res la constante de los gases.T_subes la temperatura de sublimación yT_fuses la temperatura de fusión.
Este método supone que el calor de fusión es independiente de la temperatura y proporciona una estimación razonable para temperaturas no muy alejadas del punto de fusión.
Importancia y Aplicaciones de la Presión en Mezclas
El conocimiento y la capacidad de calcular las presiones en mezclas tienen implicaciones profundas en diversas áreas:
Derecho Ambiental y Seguridad: La presión de vapor es un factor crítico para determinar el índice de peligrosidad (Ip) de una sustancia. Este índice se calcula como el cociente entre la presión de vapor de la sustancia y su Concentración Máxima Permitida (CMP) en condiciones estándar. Un Ip alto indica una mayor probabilidad de que una sustancia se volatilice en el ambiente, lo que es vital para evaluar la viabilidad de su uso en ciertas actividades y para implementar medidas de seguridad adecuadas.
Meteorología: En meteorología, el término presión de vapor se utiliza para referirse a la presión parcial del vapor de agua en la atmósfera, incluso si no está en equilibrio. La "presión de vapor de saturación" es la presión de vapor de equilibrio del agua sobre una superficie plana. La humedad relativa, por ejemplo, es una medida directa de la cantidad de vapor de agua presente en relación con la cantidad máxima posible (presión de vapor de saturación) a una temperatura dada. Comprender estos conceptos es fundamental para el pronóstico del tiempo, el estudio del clima y la comprensión de fenómenos como la formación de nubes y la precipitación.
Industria Química y Farmacéutica: El diseño de procesos de destilación, evaporación, secado y formulación de productos requiere un conocimiento preciso de las presiones de vapor de los componentes de las mezclas. Esto permite optimizar la separación de sustancias, controlar la pureza de los productos y asegurar la estabilidad de las formulaciones.
Preguntas Frecuentes (FAQ)
- ¿Qué es la presión parcial?
- La presión parcial es la presión que un gas individual ejercería si ocupara el mismo volumen total que la mezcla de gases, y a la misma temperatura.
- ¿Cómo afecta la temperatura a la presión de vapor?
- La presión de vapor aumenta significativamente con la temperatura. A mayor temperatura, las moléculas tienen más energía para escapar a la fase de vapor, aumentando la presión ejercida por el vapor.
- ¿Qué es la Ley de Raoult y cuándo se aplica?
- La Ley de Raoult describe cómo la presión de vapor de un solvente en una solución disminuye proporcionalmente a la fracción molar de un soluto no volátil. Se aplica idealmente a soluciones diluidas y mezclas donde las interacciones moleculares son muy similares a las de los componentes puros.
- ¿Qué son las desviaciones de la Ley de Raoult?
- Las desviaciones ocurren cuando las interacciones entre las moléculas de soluto y solvente son significativamente diferentes de las interacciones entre las moléculas de los componentes puros. Una desviación positiva significa una presión de vapor mayor a la esperada, mientras que una negativa indica una presión de vapor menor.
- ¿Por qué es importante conocer la presión de vapor de una sustancia?
- Es crucial para entender y predecir el comportamiento de las sustancias en diferentes condiciones. Permite calcular puntos de ebullición, diseñar procesos industriales, evaluar riesgos ambientales y comprender fenómenos atmosféricos, entre otros.
En resumen, la presión en mezclas es un campo de estudio dinámico y fundamental en la química y la física. Desde la simplicidad de la Ley de Dalton para gases ideales hasta la complejidad de las interacciones en mezclas líquidas regidas por la Ley de Raoult y las propiedades de sublimación de los sólidos, comprender estos principios es clave para innumerables aplicaciones prácticas. Ya sea que estés diseñando un proceso industrial, analizando la calidad del aire o simplemente entendiendo por qué el agua hierve de manera diferente en la montaña, el conocimiento de cómo calcular y predecir la presión en mezclas te proporciona una herramienta invaluable.
Si quieres conocer otros artículos parecidos a Calcular la Presión en Mezclas: Guía Completa puedes visitar la categoría Química.

