13/08/2023
En el vasto universo de la química, comprender la composición de una mezcla es tan crucial como conocer los elementos que la componen. Cuando hablamos de soluciones, una de las formas más fundamentales y utilizadas para expresar su composición es a través de la concentración en moles, comúnmente conocida como concentración molar o molaridad. Esta medida nos permite cuantificar la cantidad de una sustancia disuelta en un volumen determinado de disolución, proporcionando una base sólida para realizar cálculos estequiométricos precisos y entender las reacciones químicas a un nivel más profundo. Si alguna vez te has preguntado cómo los científicos y los químicos preparan soluciones con una precisión asombrosa, la respuesta reside en el dominio de esta sencilla pero poderosa fórmula.

La concentración molar es una medida de la cantidad de soluto (la sustancia que se disuelve) en un volumen dado de disolución (la mezcla homogénea resultante del soluto y el disolvente). Su importancia radica en que las reacciones químicas a menudo dependen de la cantidad de moles de los reactivos presentes, no de su masa o volumen directamente. Por lo tanto, expresar la concentración en términos de moles por volumen facilita enormemente los cálculos en el laboratorio y la industria.
La Fórmula Maestra: Moles por Litro
La fórmula para calcular la concentración en moles es una de las más fundamentales en química cuantitativa. Es directa y fácil de recordar:
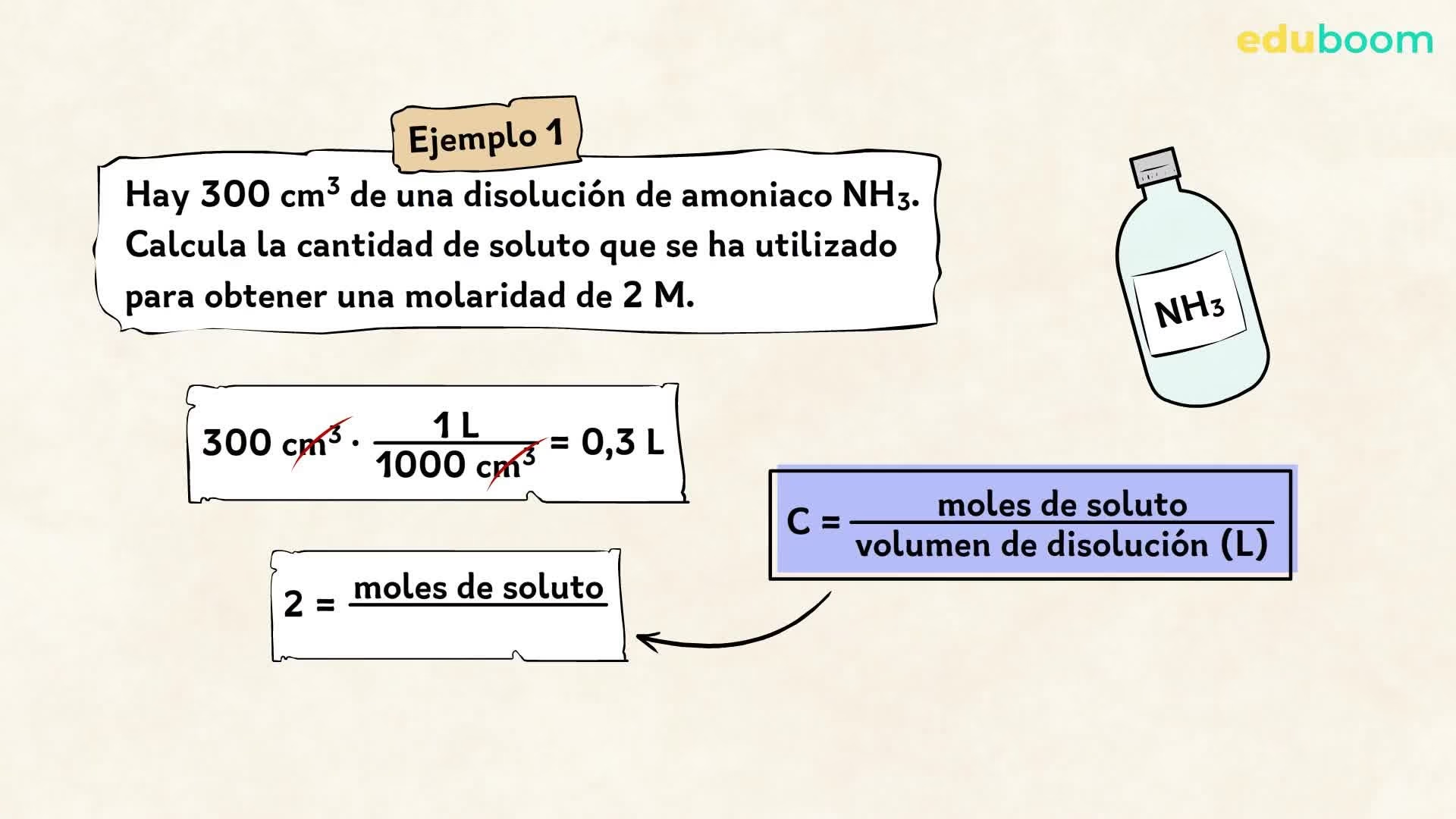
Concentración Molar (M) = Moles de Soluto / Volumen de Disolución (en Litros)
Desglosando cada componente:
- Moles de Soluto: Esta es la cantidad de sustancia del soluto, medida en moles (mol). Un mol es una unidad fundamental en química que representa aproximadamente 6.022 x 1023 partículas (átomos, moléculas, iones, etc.). Para calcular los moles de una sustancia, generalmente se utiliza la siguiente relación:
- Volumen de Disolución (en Litros): Este es el volumen total de la solución, es decir, el volumen del soluto más el volumen del disolvente, medido en litros (L). Es crucial que el volumen esté en litros, ya que la unidad estándar de la concentración molar es moles por litro (mol/L). Si el volumen está dado en mililitros (mL), debe convertirse a litros dividiendo por 1000.
Moles = Masa de la sustancia (en gramos) / Masa Molar de la sustancia (en g/mol)
La unidad resultante de la concentración molar es mol/L, que a menudo se abrevia simplemente como 'M' (mayúscula), lo que se lee como "molar". Por ejemplo, una solución 0.5 M de NaCl significa que hay 0.5 moles de cloruro de sodio disueltos en cada litro de disolución.
¿Por Qué la Molaridad es Tan Importante?
La molaridad es la unidad de concentración preferida en la mayoría de los trabajos de laboratorio y en la investigación química por varias razones clave:
- Relación Directa con las Reacciones: Las ecuaciones químicas balanceadas representan las proporciones molares en las que los reactivos se combinan y los productos se forman. Al conocer la concentración molar de las soluciones, es fácil determinar la cantidad de moles de cada reactivo disponible y predecir la cantidad de producto que se formará.
- Facilidad de Medición: Aunque la masa se mide con balanzas y el volumen con material volumétrico, la molaridad combina ambos para proporcionar una medida de concentración que es directamente útil para la estequiometría. Medir el volumen de una solución es a menudo más práctico que medir la masa de un soluto disuelto.
- Aplicaciones Amplias: Desde la preparación de soluciones para titulaciones en un laboratorio de química analítica hasta la formulación de medicamentos en la industria farmacéutica o la creación de fertilizantes en la agricultura, la molaridad es una herramienta indispensable.
Ejemplos Prácticos de Cálculo
Ejemplo 1: Calcular la Molaridad Directamente
Problema: Se disuelven 0.25 moles de glucosa (C6H12O6) en agua para formar 500 mL de disolución. ¿Cuál es la concentración molar de la glucosa?
Solución:
- Convertir el volumen a litros:
Volumen = 500 mL / 1000 mL/L = 0.50 L
- Aplicar la fórmula de la molaridad:
Molaridad (M) = Moles de Soluto / Volumen de Disolución (L)
M = 0.25 mol / 0.50 L
M = 0.50 mol/L o 0.50 M
La concentración molar de la disolución de glucosa es 0.50 M.
Ejemplo 2: Calcular la Molaridad a partir de la Masa
Problema: Se disuelven 58.44 gramos de cloruro de sodio (NaCl) en suficiente agua para obtener un volumen final de 1.00 L de disolución. ¿Cuál es la concentración molar de la disolución?
Solución:
- Calcular la masa molar de NaCl:
Na: 22.99 g/mol
Cl: 35.45 g/mol
Masa Molar de NaCl = 22.99 + 35.45 = 58.44 g/mol
- Calcular los moles de NaCl:
Moles = Masa / Masa Molar
Moles = 58.44 g / 58.44 g/mol = 1.00 mol
- Aplicar la fórmula de la molaridad:
Molaridad (M) = Moles de Soluto / Volumen de Disolución (L)
M = 1.00 mol / 1.00 L
M = 1.00 mol/L o 1.00 M
La concentración molar de la disolución de cloruro de sodio es 1.00 M.
Conceptos Relacionados y Consideraciones Adicionales
Dilución de Soluciones
Un concepto estrechamente relacionado con la molaridad es la dilución. Cuando se añade más disolvente a una solución concentrada, el número de moles de soluto permanece constante, pero el volumen de la disolución aumenta, lo que disminuye la concentración. La fórmula para la dilución es:
M₁V₁ = M₂V₂
Donde:
- M₁ = Concentración molar inicial
- V₁ = Volumen inicial
- M₂ = Concentración molar final
- V₂ = Volumen final
Esta ecuación es vital para preparar soluciones de menor concentración a partir de soluciones madre más concentradas, una práctica común en cualquier laboratorio.
Otras Unidades de Concentración
Aunque la molaridad es la más utilizada en química, existen otras formas de expresar la concentración, cada una con sus propias ventajas y aplicaciones específicas. Es importante conocerlas para elegir la más adecuada según el contexto:
- Porcentaje en masa (% m/m): (Masa de soluto / Masa total de disolución) x 100. Útil cuando se trabaja con sólidos.
- Porcentaje en volumen (% v/v): (Volumen de soluto / Volumen total de disolución) x 100. Común para mezclas de líquidos.
- Partes por millón (ppm): (Masa de soluto / Masa total de disolución) x 106. Usado para concentraciones muy bajas, por ejemplo, contaminantes en agua.
- Molalidad (m): Moles de soluto / Kilogramos de disolvente. A diferencia de la molaridad, la molalidad es independiente de la temperatura porque se basa en la masa del disolvente, no en el volumen de la disolución. Esto la hace útil en estudios de propiedades coligativas.
Tabla Comparativa de Unidades de Concentración
| Unidad de Concentración | Definición | Unidades | Ventajas | Desventajas |
|---|---|---|---|---|
| Molaridad (M) | Moles de soluto por litro de disolución | mol/L o M | Directamente relacionada con la estequiometría; fácil de usar en reacciones. | Dependiente de la temperatura (el volumen cambia). |
| Molalidad (m) | Moles de soluto por kilogramo de disolvente | mol/kg o m | Independiente de la temperatura; útil para propiedades coligativas. | No tan directa para cálculos volumétricos. |
| Porcentaje en masa (% m/m) | Masa de soluto por 100 unidades de masa de disolución | % | Fácil de preparar; independiente de la temperatura. | No directamente estequiométrica; requiere densidad para convertir a molaridad. |
| Partes por millón (ppm) | Masa de soluto por millón de unidades de masa de disolución | ppm | Ideal para concentraciones muy bajas. | No directamente estequiométrica. |
Consejos Clave y Errores Comunes a Evitar
- Unidades del Volumen: ¡Siempre asegúrate de que el volumen esté en litros! Este es el error más común. Si trabajas con mL, divide por 1000.
- Masa Molar Precisa: Calcula la masa molar del soluto con la mayor precisión posible, utilizando los pesos atómicos correctos de la tabla periódica.
- Soluto vs. Disolución: Recuerda que la molaridad se refiere al volumen total de la disolución, no solo al volumen del disolvente. Al preparar una solución, se añade el soluto y luego se añade disolvente hasta alcanzar el volumen final deseado en un matraz aforado.
- Temperatura: Ten en cuenta que la molaridad es sensible a los cambios de temperatura, ya que el volumen de la disolución puede expandirse o contraerse. Para aplicaciones de alta precisión, la molalidad puede ser una alternativa mejor.
- Pureza del Soluto: Si el soluto no es 100% puro, debes tener en cuenta su pureza al calcular la cantidad de soluto real presente.
Preguntas Frecuentes (FAQ)
¿Es lo mismo concentración molar que molaridad?
Sí, son términos sinónimos y se usan indistintamente para referirse a la misma unidad de concentración: moles de soluto por litro de disolución.
¿Por qué el volumen debe estar en litros?
La unidad estándar del Sistema Internacional (SI) para la concentración molar es moles por litro (mol/L). Utilizar litros asegura la coherencia con esta unidad estándar y simplifica los cálculos en química.
¿La molaridad de una solución cambia con la temperatura?
Sí, la molaridad es dependiente de la temperatura. Esto se debe a que el volumen de una disolución (y del disolvente) puede expandirse o contraerse ligeramente con los cambios de temperatura, mientras que la cantidad de moles de soluto permanece constante. Por lo tanto, un cambio en el volumen afectará la relación moles/volumen.
¿Cómo se prepara una solución de una molaridad específica en el laboratorio?
Para preparar una solución con una molaridad específica, primero se calcula la masa de soluto necesaria utilizando la molaridad deseada y el volumen final. Luego, se pesa esa cantidad de soluto y se transfiere a un matraz aforado (un recipiente de vidrio volumétrico preciso). Se añade disolvente (generalmente agua) hasta disolver el soluto, y finalmente se añade más disolvente hasta que el nivel del líquido coincida exactamente con la marca de aforo del matraz. Es crucial asegurar que el soluto esté completamente disuelto antes de aforar.
¿Cuándo debería usar molalidad en lugar de molaridad?
La molalidad es preferible cuando se necesita una medida de concentración que sea independiente de la temperatura, como en el estudio de propiedades coligativas (descenso crioscópico, aumento ebulloscópico, presión osmótica) o en situaciones donde se esperan grandes cambios de temperatura. También es útil cuando se trabaja con disolventes no acuosos o cuando la densidad de la solución cambia significativamente con la concentración.
En resumen, la fórmula para la concentración en moles, o molaridad, es una herramienta indispensable en el ámbito de la química. Nos permite cuantificar de manera precisa la cantidad de una sustancia disuelta en una solución, lo cual es fundamental para el éxito de innumerables experimentos, procesos industriales y aplicaciones médicas. Dominar esta fórmula y sus implicaciones no solo te permitirá resolver problemas químicos con confianza, sino que también te abrirá las puertas a una comprensión más profunda de cómo las sustancias interactúan a nivel molecular.
Si quieres conocer otros artículos parecidos a Concentración en Moles: La Fórmula Esencial puedes visitar la categoría Química.