22/02/2025
En el vasto y fascinante mundo de la química, la biología y la farmacia, la capacidad de determinar la concentración de una sustancia en una solución es fundamental. Ya sea para monitorear una reacción, analizar la pureza de un compuesto o cuantificar un principio activo en un medicamento, la medición precisa es clave. Una de las herramientas más potentes y ampliamente utilizadas para este propósito es la espectrofotometría, una técnica que se basa en la interacción de la luz con la materia. A través de la medición de la absorbancia de una solución, podemos desentrañar el misterio de cuánta sustancia hay presente. Pero, ¿cómo se pasa exactamente de un valor de absorbancia, que es una medida de cuánto absorbe la luz una muestra, a una concentración tangible? La respuesta reside en principios fundamentales y métodos prácticos que exploraremos en profundidad a continuación.
La relación entre la absorbancia y la concentración no es una conjetura, sino que está respaldada por una ley física bien establecida: la Ley de Beer-Lambert. Comprender esta ley es el primer paso para dominar la conversión de absorbancia a concentración y aplicarla eficazmente en diversos escenarios científicos e industriales. Acompáñanos en este viaje para desglosar sus componentes, explorar sus aplicaciones y aprender a calcular con precisión la concentración de cualquier analito.
- La Ley de Beer-Lambert: El Corazón de la Espectrofotometría
- Curvas de Calibración: La Herramienta Práctica para la Cuantificación
- Cálculo de la Concentración de Equilibrio a Partir de la Absorbancia
- Cálculo del Contenido de un Fármaco a Partir de la Absorbancia
- Comparación de Métodos de Cuantificación por Espectrofotometría
- Preguntas Frecuentes sobre Absorbancia y Concentración
- ¿Cuáles son las unidades de la absortividad molar (ε)?
- ¿Qué es el 'blanco' en espectrofotometría y por qué es importante?
- ¿Cuáles son las limitaciones o desviaciones de la Ley de Beer-Lambert?
- ¿Cómo sé si mi solución cumple con la Ley de Beer-Lambert?
- ¿Qué instrumentos se utilizan para medir la absorbancia?
- Conclusión
La Ley de Beer-Lambert: El Corazón de la Espectrofotometría
La Ley de Beer-Lambert es el principio fundamental que rige la relación entre la cantidad de luz absorbida por una solución y la concentración de la sustancia disuelta en ella. Es una ley empírica que establece que la absorbancia (A) de una solución es directamente proporcional a la concentración (c) del analito y a la longitud del camino óptico (l) que la luz atraviesa a través de la solución. Su expresión matemática es sencilla pero poderosa:
A = εlc
Desglosemos cada uno de los términos de esta ecuación:
- A (Absorbancia): Es una medida adimensional de la cantidad de luz que ha sido absorbida por la muestra. Se calcula como el logaritmo de la relación entre la intensidad de la luz incidente (I₀) y la intensidad de la luz transmitida (I): A = log(I₀/I). Cuanto mayor es la absorbancia, menos luz ha pasado a través de la muestra, indicando una mayor concentración del analito.
- ε (Absortividad Molar o Coeficiente de Extinción Molar): Esta es una constante característica de cada sustancia a una longitud de onda y temperatura dadas. Nos indica cuán eficientemente una sustancia absorbe la luz a una longitud de onda específica. Sus unidades suelen ser L·mol⁻¹·cm⁻¹. Un valor de ε alto significa que la sustancia absorbe mucha luz incluso a bajas concentraciones. La absortividad molar es crucial porque es única para cada cromóforo (parte de la molécula que absorbe la luz) y permite identificar y cuantificar sustancias.
- l (Longitud del Camino Óptico): Es la distancia que la luz recorre a través de la muestra, medida generalmente en centímetros (cm). En la práctica de laboratorio, esta longitud suele ser la anchura de la cubeta utilizada para contener la muestra, que comúnmente es de 1 cm.
- c (Concentración): Es la cantidad de la sustancia disuelta en la solución, expresada típicamente en moles por litro (mol/L) o molaridad (M). Este es el valor que buscamos determinar.
De la Absorbancia a la Concentración: Reorganizando la Fórmula
Si conocemos la absortividad molar (ε) de la sustancia en cuestión y la longitud del camino óptico (l) de la cubeta, podemos reorganizar la Ley de Beer-Lambert para despejar la concentración (c):
c = A / (εl)
Este cálculo directo es posible cuando se dispone de los valores precisos de ε y l. Sin embargo, en muchas ocasiones, ε no se conoce con exactitud o la relación lineal de la Ley de Beer-Lambert puede desviarse a altas concentraciones o por otros factores. Es aquí donde las curvas de calibración se vuelven indispensables.
Curvas de Calibración: La Herramienta Práctica para la Cuantificación
Cuando la absortividad molar no se conoce con precisión o cuando queremos validar la linealidad de la Ley de Beer-Lambert en un rango de concentración específico, recurrimos a las curvas de calibración (también conocidas como curvas estándar). Este método es el pilar de la cuantificación en muchos laboratorios.
Creando una Curva de Calibración
El proceso implica los siguientes pasos:
- Preparación de Soluciones Estándar: Se preparan una serie de soluciones de la sustancia de interés con concentraciones conocidas y precisas. Estas concentraciones deben abarcar el rango en el que se espera que caiga la concentración de la muestra desconocida.
- Medición de la Absorbancia: Se mide la absorbancia de cada una de estas soluciones estándar a la longitud de onda de máxima absorbancia (λmax) del analito, utilizando el mismo espectrofotómetro y las mismas cubetas que se usarán para la muestra desconocida.
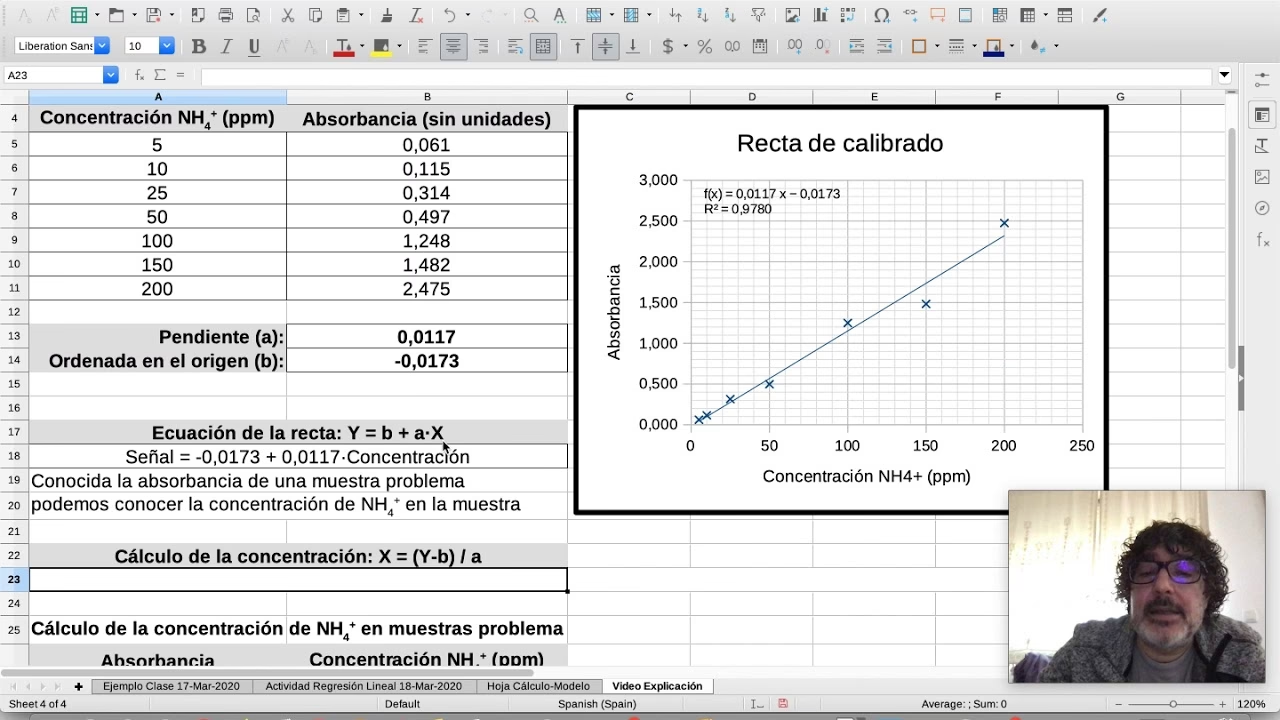
- Construcción de la Gráfica: Se grafica la absorbancia (en el eje Y) frente a la concentración (en el eje X) de las soluciones estándar.
- Ajuste de la Recta de Calibración: Si la Ley de Beer-Lambert se cumple, los puntos deberían formar una línea recta que pasa por el origen (0,0) o muy cerca de él. Se realiza un ajuste por mínimos cuadrados para obtener la ecuación de esta línea recta. La ecuación de una línea recta general es
y = mx + b, donde en nuestro caso:Yes la absorbancia (A)Xes la concentración (c)mes la pendiente de la recta, que es equivalente a (εl) de la Ley de Beer-Lambert.bes la intersección con el eje Y. Idealmente, para la Ley de Beer-Lambert, b debería ser cero, pero en la práctica puede haber un pequeño valor debido a la absorbancia del disolvente o al ruido instrumental.
Cálculo de la Concentración de una Muestra Desconocida
Una vez que se tiene la ecuación de la recta de calibración (A = mc + b), se mide la absorbancia de la muestra desconocida. Luego, se utiliza la ecuación para despejar la concentración (c) de la muestra:
c = (A - b) / m
Este método es robusto y compensa pequeñas desviaciones o la falta de un valor exacto de ε, ya que la pendiente 'm' ya incorpora la respuesta específica del sistema (analito, disolvente, instrumento, cubeta) bajo las condiciones de medición.
Cálculo de la Concentración de Equilibrio a Partir de la Absorbancia
La espectrofotometría es una herramienta invaluable para estudiar reacciones químicas, incluyendo aquellas que alcanzan un estado de equilibrio. En una reacción en equilibrio, las concentraciones de reactivos y productos permanecen constantes, aunque la reacción sigue ocurriendo en ambas direcciones. Si uno de los reactivos o productos es cromofórico (es decir, absorbe luz en el rango visible o UV), podemos monitorear su concentración a lo largo del tiempo hasta que el sistema alcance el equilibrio.

Para calcular la concentración de equilibrio a partir de la absorbancia, el enfoque es similar al de cualquier otra determinación de concentración desconocida:
- Identificar el Especie Cromofórica: Determinar cuál de las especies en equilibrio absorbe luz y a qué longitud de onda.
- Establecer la Curva de Calibración: Preparar una curva de calibración para la especie cromofórica, como se describió anteriormente. Esto es crucial para relacionar la absorbancia con la concentración.
- Medir la Absorbancia de Equilibrio: Una vez que la reacción ha alcanzado el equilibrio (lo que se puede verificar si la absorbancia deja de cambiar con el tiempo), se mide la absorbancia de la solución en equilibrio.
- Calcular la Concentración de Equilibrio: Usando la ecuación de la recta de calibración (
A = mc + b), donde A es la absorbancia medida en el equilibrio, se despeja la concentración (c). Si la intersección 'b' es significativa, debe restarse de la absorbancia antes de dividir por la pendiente 'm':c_equilibrio = (A_equilibrio - b) / m.
Este método permite cuantificar las especies presentes en el equilibrio y, a partir de ahí, calcular constantes de equilibrio (Keq) u otros parámetros termodinámicos.
Cálculo del Contenido de un Fármaco a Partir de la Absorbancia
En la industria farmacéutica, la cuantificación precisa de los principios activos es de suma importancia para el control de calidad, el desarrollo de formulaciones y los estudios de estabilidad. La espectrofotometría UV-Vis es una técnica común y rentable para determinar el contenido de fármacos en diversas matrices.
El procedimiento para calcular la concentración de un fármaco a partir de su absorbancia sigue los mismos principios que los discutidos anteriormente:
- Selección de la Longitud de Onda: Identificar la longitud de onda de máxima absorbancia (λmax) del fármaco en el solvente utilizado.
- Preparación de Estándares del Fármaco: Se preparan soluciones estándar del fármaco puro con concentraciones conocidas.
- Construcción de la Curva de Calibración: Se mide la absorbancia de los estándares y se grafica la absorbancia vs. la concentración para obtener la ecuación
Y = mX + C, dondeYes la absorbancia,Xes la concentración del fármaco,mes la pendiente yCes el origen (intersección con el eje Y). - Medición de Muestras del Fármaco: Las muestras que contienen el fármaco (por ejemplo, tabletas disueltas, soluciones inyectables) se preparan adecuadamente (dilución si es necesario) y se mide su absorbancia a la misma λmax.
- Determinación de la Concentración: Se sustituye la absorbancia de la muestra (Y) en la ecuación de la recta de calibración y se despeja
X(la concentración del fármaco):X = (Y - C) / m.
Es crucial que las muestras del fármaco se preparen de manera que la absorbancia medida caiga dentro del rango lineal de la curva de calibración. Además, cualquier excipiente o componente de la matriz que pueda absorber luz a la misma longitud de onda debe ser tenido en cuenta, a menudo mediante el uso de blancos apropiados o métodos más sofisticados.
Comparación de Métodos de Cuantificación por Espectrofotometría
Aunque todos los métodos se basan en la Ley de Beer-Lambert, existen diferencias en su aplicación y las condiciones bajo las cuales son más adecuados.
| Método | Descripción | Ventajas | Limitaciones / Consideraciones |
|---|---|---|---|
| Cálculo Directo (A = εlc) | Uso de la Ley de Beer-Lambert con absortividad molar (ε) y longitud de camino (l) conocidas. | Rápido, no requiere preparación de múltiples estándares. | Requiere un valor de ε muy preciso. Sensible a desviaciones de la linealidad. |
| Curva de Calibración (A = mc + b) | Preparación de estándares de concentración conocida, graficar A vs. c y obtener la ecuación de la recta. | Más robusto, compensa pequeñas desviaciones instrumentales/matriciales. Permite verificar la linealidad. | Requiere más tiempo y materiales (preparación de estándares). Necesita un rango lineal claro. |
| Aplicación a Equilibrio/Fármacos | Uso de la curva de calibración o cálculo directo para determinar concentraciones en estados específicos (equilibrio, productos farmacéuticos). | Permite cuantificar especies específicas en sistemas complejos. Esencial para control de calidad farmacéutico. | Requiere validación del método, consideración de interferencias de matriz. |
Preguntas Frecuentes sobre Absorbancia y Concentración
A continuación, abordamos algunas de las preguntas más comunes relacionadas con la conversión de absorbancia a concentración:
¿Cuáles son las unidades de la absortividad molar (ε)?
La absortividad molar (ε) generalmente se expresa en L·mol⁻¹·cm⁻¹ (litros por mol por centímetro). Esto se deriva de la ecuación A = εlc, donde A es adimensional, l está en cm y c en mol/L. Para que la ecuación sea dimensionalmente consistente, ε debe tener estas unidades.

¿Qué es el 'blanco' en espectrofotometría y por qué es importante?
El blanco es una solución que contiene todos los componentes de la muestra excepto el analito de interés. Se mide su absorbancia y se resta de la absorbancia de las muestras. Esto compensa la absorción de luz por el disolvente, las cubetas o cualquier otro componente de la matriz que no sea el analito. Es fundamental para asegurar que la absorbancia medida se deba únicamente a la sustancia que se desea cuantificar.
¿Cuáles son las limitaciones o desviaciones de la Ley de Beer-Lambert?
La Ley de Beer-Lambert es una ley ideal y tiene varias limitaciones:
- Altas Concentraciones: A concentraciones muy altas, las moléculas del analito pueden interactuar entre sí, alterando su capacidad de absorción y causando desviaciones negativas de la linealidad.
- Interacciones Químicas: Si el analito reacciona o se disocia en la solución, su absortividad molar efectiva puede cambiar, lo que lleva a desviaciones.
- Luz No Monocromática: La ley asume que la luz utilizada es estrictamente monocromática. Los espectrofotómetros reales usan un rango estrecho de longitudes de onda, lo que puede causar pequeñas desviaciones.
- Dispersión de la Luz (Turbidez): Las soluciones turbias o con partículas en suspensión dispersarán la luz, lo que se interpretará como una absorbancia mayor, llevando a resultados erróneos.
- Fluorescencia o Fosforescencia: Si el analito emite luz a la misma longitud de onda a la que absorbe, puede afectar la medición de la luz transmitida.
¿Cómo sé si mi solución cumple con la Ley de Beer-Lambert?
La mejor manera de verificar el cumplimiento es construir una curva de calibración. Si los puntos de datos forman una línea recta con un buen coeficiente de correlación (R² cercano a 1) en el rango de concentraciones de interés, entonces la ley se cumple para ese sistema.
¿Qué instrumentos se utilizan para medir la absorbancia?
Los instrumentos utilizados son los espectrofotómetros, comúnmente espectrofotómetros UV-Vis (ultravioleta-visible). Estos dispositivos emiten luz a una longitud de onda seleccionada, la hacen pasar a través de la muestra y miden la cantidad de luz transmitida para calcular la absorbancia.
Conclusión
La capacidad de convertir la absorbancia a concentración es una habilidad esencial en cualquier laboratorio que trabaje con análisis cuantitativos. Desde los principios fundamentales de la Ley de Beer-Lambert hasta la aplicación práctica de las curvas de calibración, hemos desglosado los métodos y consideraciones clave. Ya sea que esté determinando la concentración de un reactivo en una síntesis química, monitoreando la formación de un producto en una reacción en equilibrio o cuantificando la dosis de un fármaco en una formulación, la espectrofotometría ofrece una vía confiable y eficiente. Recordar las limitaciones de la ley y aplicar las mejores prácticas de laboratorio, como el uso de blancos y la validación de curvas de calibración, garantizará resultados precisos y confiables, pilares de la investigación y el control de calidad en la ciencia moderna.
Si quieres conocer otros artículos parecidos a De Absorbancia a Concentración: Guía Esencial puedes visitar la categoría Química.

