22/12/2025
En el vasto universo de la química, las soluciones son omnipresentes. Desde el café que bebemos por la mañana hasta los medicamentos que tomamos, pasando por los productos de limpieza y los procesos industriales, las soluciones juegan un papel fundamental. Comprender cómo están compuestas es el primer paso para dominar su comportamiento y aplicación. Pero, ¿cómo sabemos exactamente cuánto de cada componente hay en una solución? La clave reside en identificar y cuantificar el soluto y el solvente.
Una solución química es una mezcla homogénea de dos o más sustancias. Esto significa que sus componentes están distribuidos de manera uniforme, lo que da como resultado una apariencia y propiedades consistentes en toda la mezcla. Para entenderla a fondo, es crucial diferenciar entre sus dos componentes principales: el soluto y el solvente.
- ¿Qué es una Solución? Desentrañando el Concepto Básico
- El Corazón del Cálculo: Determinando Cantidades por Porcentaje
- Más Allá del Porcentaje: Otras Formas de Expresar la Concentración
- Aplicaciones Cotidianas: ¿Dónde Usamos Esto?
- Tabla Comparativa: Tipos de Soluciones Comunes (Basadas en el estado de la materia)
- Preguntas Frecuentes (FAQs)
- ¿Cómo se calcula la cantidad de soluto y solvente en una solución?
- ¿Cuánto soluto y disolvente hay en 200 ml de una disolución al 12%?
- ¿Cómo saber cuál es el soluto y el solvente en una solución?
- ¿Qué pasa si el soluto es un gas o un sólido?
- ¿Siempre el agua es el solvente?
- ¿Qué significa una solución "concentrada" o "diluida"?
- Conclusión
¿Qué es una Solución? Desentrañando el Concepto Básico
Antes de sumergirnos en los cálculos, es vital tener claridad sobre los términos. Una solución es una mezcla homogénea, es decir, que presenta una sola fase y sus componentes no pueden distinguirse a simple vista ni con métodos ópticos. Se compone de:
- Soluto: Es la sustancia que se disuelve en otra. Generalmente, está presente en menor cantidad. Puede ser un sólido, un líquido o un gas. Por ejemplo, la sal en agua o el azúcar en el café.
- Solvente (o Disolvente): Es la sustancia en la que se disuelve el soluto. Generalmente, está presente en mayor cantidad. Es el medio que facilita la disolución. El solvente más común y versátil es el agua, por lo que las soluciones que utilizan agua como solvente se conocen como soluciones acuosas.
Imaginemos un vaso de agua con azúcar. El azúcar es el soluto, y el agua es el solvente. Al mezclarse, forman una solución de agua azucarada.
Identificando al Soluto y al Solvente: La Clave Principal
A menudo, la identificación del soluto y el solvente es intuitiva, especialmente cuando uno de los componentes es el agua. Sin embargo, en otros casos, puede ser un poco más complejo. Aquí hay algunas pautas generales:
- Cantidad: En la mayoría de los casos, la sustancia presente en menor cantidad es el soluto, y la presente en mayor cantidad es el solvente.
- Estado Físico: Si una sustancia cambia de estado físico al formar la solución (por ejemplo, un sólido que se disuelve en un líquido para formar una solución líquida), la sustancia que mantiene su estado físico original suele ser el solvente. Por ejemplo, cuando la sal (sólido) se disuelve en agua (líquido), la solución resultante es líquida, por lo que el agua es el solvente.
- Naturaleza de la Sustancia: El agua es casi siempre considerada el solvente universal debido a su capacidad para disolver una gran variedad de sustancias polares e iónicas.
Por ejemplo, en una aleación de bronce (una mezcla de cobre y estaño), el cobre es el solvente porque es el componente principal, mientras que el estaño es el soluto.
El Corazón del Cálculo: Determinando Cantidades por Porcentaje
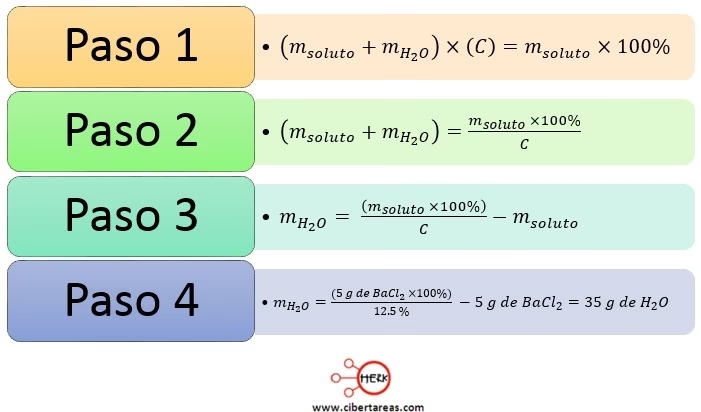
Una de las formas más comunes y sencillas de expresar la concentración de una solución es mediante porcentajes. Estos porcentajes pueden basarse en masa, volumen o una combinación de ambos. La fórmula general para calcular la concentración porcentual es:
Porcentaje (%) = (Cantidad de Soluto / Cantidad Total de Solución) * 100
Es crucial recordar que la "Cantidad Total de Solución" es la suma de la cantidad de soluto y la cantidad de solvente.
Ejemplo Práctico: Calculando Cantidades en una Disolución al 12%
Tomemos el ejemplo proporcionado: ¿Cuánto soluto y disolvente hay en 200 ml de una disolución al 12%?
Para resolver este problema, seguimos dos pasos claros:
Calcular la cantidad de soluto:
El porcentaje indica la proporción del soluto en la solución total. Si la disolución está al 12%, significa que el 12% del volumen total (200 ml) es soluto.

La solubilidad de un soluto se mide como la masa en gramos que puede disolverse en 100 g de disolvente a cualquier temperatura. Por ejemplo, la solubilidad del cloruro de aluminio en agua es de 45,8 g por 100 g de agua a 20 ° C. Cantidad de soluto = Porcentaje de la disolución * Volumen total de la disolución
Cantidad de soluto = (12 / 100) * 200 ml
Cantidad de soluto = 0.12 * 200 ml
Cantidad de soluto = 24 ml
Calcular la cantidad de disolvente:
Una vez que conocemos la cantidad de soluto, podemos encontrar la cantidad de disolvente restando la cantidad de soluto del volumen total de la disolución.
Cantidad de disolvente = Volumen total de la disolución - Cantidad de soluto
Cantidad de disolvente = 200 ml - 24 ml
Cantidad de disolvente = 176 ml
Por lo tanto, en 200 ml de una disolución al 12%, hay 24 ml de soluto y 176 ml de disolvente.
Otro Ejemplo: Concentración por Masa
Supongamos que tenemos una solución de 500 gramos de azúcar en agua, y la concentración es del 20% en masa. ¿Cuántos gramos de azúcar y agua hay?
Calcular la masa de soluto (azúcar):
Masa de soluto = (20 / 100) * 500 g
Masa de soluto = 0.20 * 500 g
Masa de soluto = 100 g de azúcar
Calcular la masa de disolvente (agua):
Masa de disolvente = Masa total de la disolución - Masa de soluto
Masa de disolvente = 500 g - 100 g
Masa de disolvente = 400 g de agua
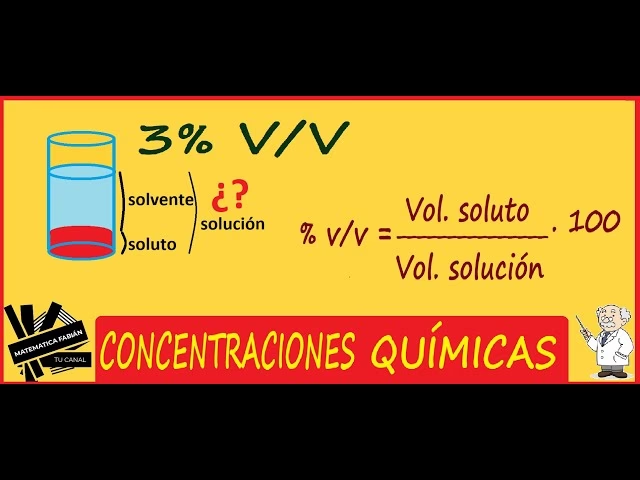
Más Allá del Porcentaje: Otras Formas de Expresar la Concentración
Aunque el porcentaje es muy útil, existen otras formas más precisas o adecuadas para expresar la concentración de una solución, especialmente en contextos científicos o industriales. Algunas de ellas incluyen:
- Molaridad (M): Moles de soluto por litro de solución. Es muy común en química para reacciones.
- Molalidad (m): Moles de soluto por kilogramo de solvente. Útil cuando la temperatura cambia, ya que la masa no varía con la temperatura a diferencia del volumen.
- Partes por millón (ppm) y Partes por billón (ppb): Se utilizan para concentraciones muy bajas, comunes en análisis de contaminantes o trazas.
- Fracción molar (X): Relación de moles de un componente respecto a los moles totales de la solución.
Cada una de estas unidades tiene su propósito y es elegida según la aplicación específica, pero el concepto fundamental de soluto y solvente permanece inalterable.
Aplicaciones Cotidianas: ¿Dónde Usamos Esto?
La capacidad de calcular las cantidades de soluto y solvente es fundamental en diversas áreas:
- Medicina y Farmacología: Para preparar sueros, medicamentos con dosis exactas, desinfectantes y soluciones intravenosas. La precisión es vital para la seguridad del paciente.
- Industria Alimentaria: En la preparación de bebidas (concentrados de jugos, refrescos), conservantes (salmueras, jarabes) y productos saborizados. Asegura la calidad y el sabor consistentes.
- Química Analítica e Investigación: Para preparar reactivos con concentraciones específicas para experimentos, calibración de instrumentos y análisis de muestras.
- Productos de Limpieza y Cosméticos: La formulación de detergentes, blanqueadores, perfumes y cremas requiere un control estricto de las concentraciones de sus ingredientes activos.
- Agricultura: Preparación de fertilizantes líquidos y pesticidas, donde la concentración adecuada es crucial para la eficacia y para evitar daños a los cultivos o al medio ambiente.
Tabla Comparativa: Tipos de Soluciones Comunes (Basadas en el estado de la materia)
Las soluciones no se limitan solo a líquidos. Aquí hay una tabla que ilustra diferentes tipos:
| Estado del Soluto | Estado del Solvente | Ejemplo |
|---|---|---|
| Gas | Gas | Aire (Nitrógeno como solvente, Oxígeno, Argón, CO2 como solutos) |
| Gas | Líquido | Bebidas carbonatadas (CO2 en agua) |
| Líquido | Líquido | Alcohol en agua (bebidas alcohólicas) |
| Sólido | Líquido | Sal en agua, azúcar en café |
| Gas | Sólido | Hidrógeno en paladio (almacenamiento de hidrógeno) |
| Líquido | Sólido | Amalgama dental (Mercurio en Plata) |
| Sólido | Sólido | Bronce (Estaño en Cobre), Acero (Carbono en Hierro) |
Preguntas Frecuentes (FAQs)
¿Cómo se calcula la cantidad de soluto y solvente en una solución?
Se calcula utilizando la concentración conocida de la solución. Si la concentración se expresa como porcentaje (la forma más común para soluciones simples), puedes usar la fórmula: Cantidad de Soluto = (Porcentaje de la Solución / 100) * Cantidad Total de Solución. Una vez que tienes la cantidad de soluto, la cantidad de solvente se obtiene restando la cantidad de soluto de la cantidad total de la solución: Cantidad de Solvente = Cantidad Total de Solución - Cantidad de Soluto.
¿Cuánto soluto y disolvente hay en 200 ml de una disolución al 12%?
Para una disolución de 200 ml al 12%:
- Cantidad de soluto: 0.12 * 200 ml = 24 ml
- Cantidad de disolvente: 200 ml - 24 ml = 176 ml
¿Cómo saber cuál es el soluto y el solvente en una solución?
Generalmente, el soluto es la sustancia que se disuelve y está presente en menor cantidad. El solvente es la sustancia que disuelve y está presente en mayor cantidad. Si una sustancia cambia de estado físico al formar la solución, la que mantiene su estado original suele ser el solvente. El agua es casi siempre el solvente cuando está presente.
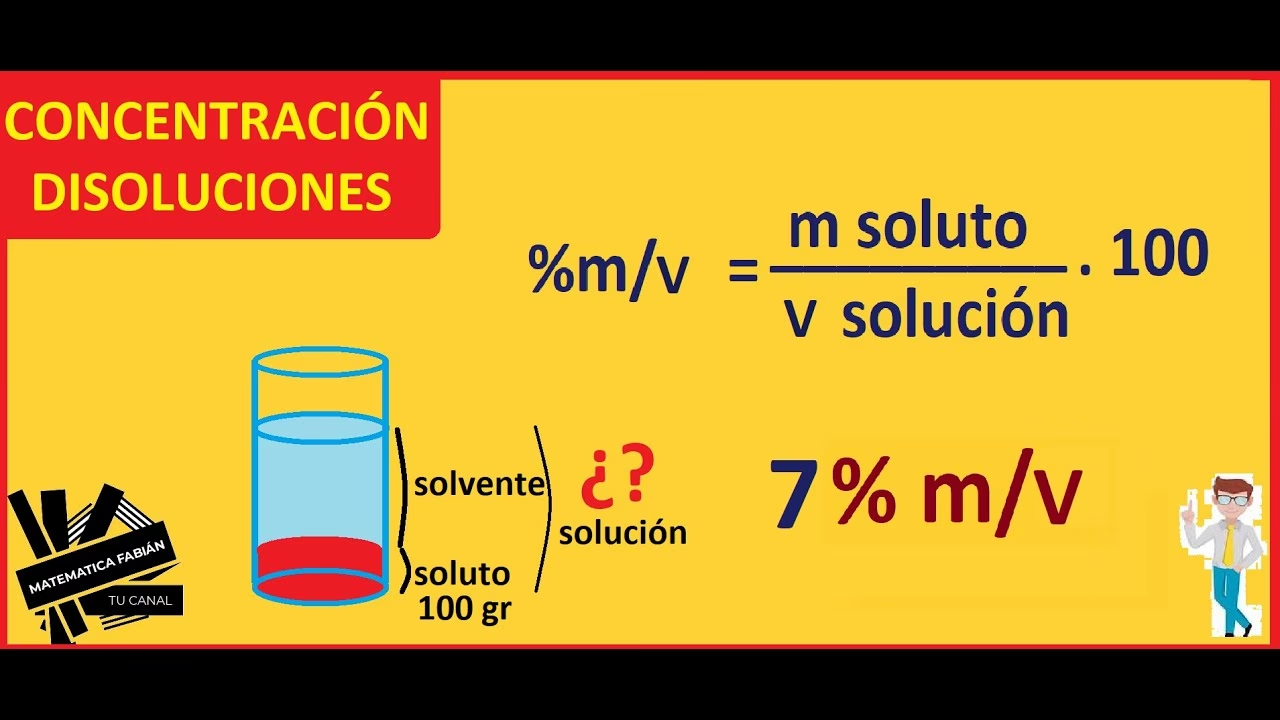
¿Qué pasa si el soluto es un gas o un sólido?
El principio es el mismo. Si el soluto es un gas (como el oxígeno disuelto en agua), se calcula su volumen o masa disuelta. Si es un sólido (como la sal), se calcula su masa disuelta. La concentración se expresará a menudo como porcentaje en masa (% m/m) o porcentaje masa/volumen (% m/v) en estos casos.
¿Siempre el agua es el solvente?
No, el agua no es siempre el solvente, aunque es el solvente más común y se conoce como el "solvente universal" por su capacidad para disolver muchas sustancias. Existen numerosos solventes orgánicos (como el alcohol, la acetona, el benceno) y otros solventes inorgánicos que se utilizan según la naturaleza del soluto y la aplicación deseada.
¿Qué significa una solución "concentrada" o "diluida"?
Una solución concentrada contiene una gran cantidad de soluto en relación con la cantidad de solvente. Por el contrario, una solución diluida contiene una pequeña cantidad de soluto en relación con la cantidad de solvente. Estos términos son relativos y no indican una concentración exacta, sino una comparación cualitativa.
Conclusión
La habilidad para calcular la cantidad de soluto y solvente en una solución es una destreza fundamental en química y en numerosas disciplinas aplicadas. Dominar estos cálculos, especialmente los basados en porcentajes, no solo nos permite comprender mejor la composición de las mezclas que nos rodean, sino que también es crucial para la seguridad, la eficiencia y la calidad en campos que van desde la medicina hasta la industria. Con las herramientas y ejemplos presentados, esperamos que ahora te sientas más seguro al abordar cualquier problema de concentración y disolución que se te presente.
Si quieres conocer otros artículos parecidos a Calculando Soluto y Solvente en Soluciones Químicas puedes visitar la categoría Química.