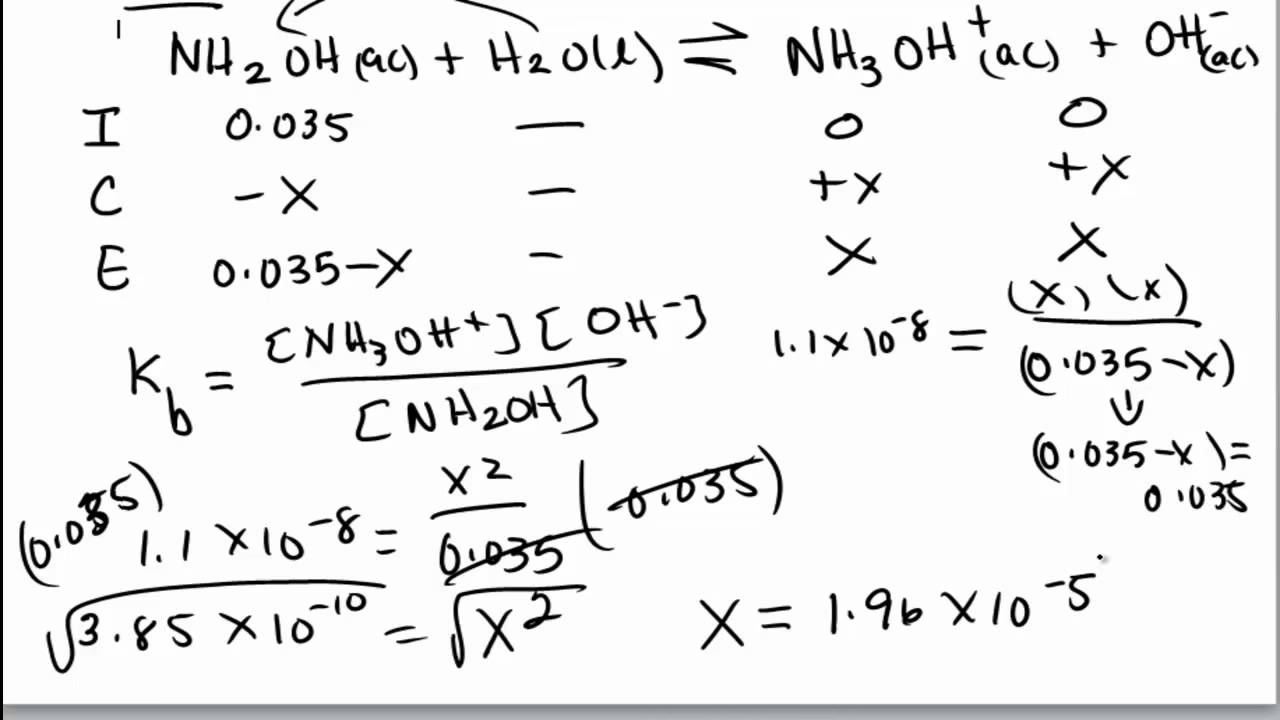26/09/2023
En el fascinante mundo de la química, las bases juegan un papel crucial en innumerables procesos, desde reacciones industriales hasta funciones biológicas vitales en nuestro propio cuerpo. Al igual que los ácidos, las bases pueden ser fuertes o débiles, dependiendo de su capacidad para disociarse en solución acuosa. Para cuantificar la fuerza de una base débil, los químicos utilizan una herramienta fundamental: la Constante de Disociación de Base (Kb). Entender Kb no solo nos permite predecir cómo se comportará una base en una solución, sino que también nos abre la puerta a comprender mejor el delicado equilibrio químico de los sistemas acuosos.

Este artículo te guiará a través de la definición de Kb, te enseñará cómo calcularla a partir de mediciones de pH, y explorará su profunda relación con la constante de disociación de ácido (Ka). Prepárate para sumergirte en los principios que rigen la fuerza de las bases y cómo estos conceptos son aplicados en la química analítica y más allá.
¿Qué es la Constante de Disociación de Base (Kb)?
La constante de disociación de base, denotada como Kb, es una medida cuantitativa de la fuerza de una base. Cuando una base débil (B) se disocia en agua, reacciona parcialmente con las moléculas de agua para producir su ácido conjugado (BH+) y iones hidróxido (OH-). Esta reacción es un equilibrio químico que se puede representar de la siguiente manera:
B(aq) + H2O(l) ⇴ BH+(aq) + OH-(aq)
La expresión para la constante de equilibrio de esta reacción es Kb, que se define como:
Kb = [BH+][OH-] / [B]
Donde:
- [BH+] es la concentración molar del ácido conjugado de la base en el equilibrio.
- [OH-] es la concentración molar de iones hidróxido en el equilibrio.
- [B] es la concentración molar de la base no disociada en el equilibrio.
Un valor de Kb grande indica que la base se disocia en mayor medida, lo que significa que es una base más fuerte. Por el contrario, un valor de Kb pequeño sugiere que la base se disocia en menor medida, indicando que es una base más débil. Es importante recordar que Kb es específica para una base dada y su valor depende de la temperatura.
Calculando Kb a Partir del pH: Un Enfoque Paso a Paso
Calcular la constante de disociación de base (Kb) a partir de una medición de pH puede parecer una tarea compleja, pero se vuelve sencilla si se siguen una serie de pasos lógicos. Este método es aplicable para bases débiles, ya que las bases fuertes se disocian completamente y sus Kb son tan grandes que no suelen tabularse o calcularse de esta manera.
Paso 1: Determinar el pOH a Partir del pH
El primer paso es convertir el valor de pH dado a pOH. El pH y el pOH están intrínsecamente relacionados en soluciones acuosas a una temperatura constante (típicamente 25°C) por la siguiente ecuación:
pH + pOH = 14.00 (a 25°C)
Por lo tanto, para encontrar el pOH, simplemente reordenamos la fórmula:
pOH = 14.00 - pH
Este paso es crucial porque la disociación de una base débil produce iones OH-, y el pOH es una medida directa de la concentración de estos iones.

Paso 2: Calcular la Concentración de Iones Hidróxido ([OH-])
Una vez que tenemos el valor de pOH, podemos calcular la concentración molar de iones hidróxido ([OH-]) utilizando la siguiente relación logarítmica:
[OH-] = 10-pOH
Esta concentración de OH- en el equilibrio es un componente clave para el cálculo de Kb.
Paso 3: Determinar las Concentraciones de Equilibrio de la Base y su Ácido Conjugado
Este es el paso que a menudo requiere el conocimiento de la concentración inicial de la base y la estequiometría de la reacción. Para una base débil genérica B que reacciona con agua:
B(aq) + H2O(l) ⇴ BH+(aq) + OH-(aq)
Si la concentración inicial de la base es [B]inicial y la concentración de OH- en el equilibrio es la que calculamos en el Paso 2, entonces:
- La concentración de BH+ en el equilibrio será igual a la concentración de OH- en el equilibrio (asumiendo que la única fuente de OH- es la disociación de la base). Es decir, [BH+] = [OH-].
- La concentración de la base no disociada [B] en el equilibrio será aproximadamente [B]inicial - [OH-]. En muchos casos, si la base es muy débil y la concentración inicial es suficientemente alta, la cantidad de base que se disocia ([OH-]) es insignificante en comparación con la concentración inicial, permitiendo la aproximación [B] ≈ [B]inicial. Sin embargo, para mayor precisión, se debe usar [B] = [B]inicial - [OH-].
Este paso a menudo implica el uso de un cuadro ICE (Inicial, Cambio, Equilibrio) para organizar las concentraciones, aunque no es necesario dibujar el cuadro explícitamente si se entienden los cambios.
Paso 4: Calcular Kb Usando la Ecuación de Equilibrio
Finalmente, con todas las concentraciones de equilibrio determinadas, podemos sustituirlas en la fórmula de Kb:
Kb = [BH+][OH-] / [B]
Al realizar estos cálculos, es fundamental asegurarse de que todas las concentraciones estén expresadas en molaridad (moles/litro).
La Interconexión entre Ka, Kb y Kw
Existe una relación fundamental entre la constante de disociación de un ácido (Ka) y la constante de disociación de su base conjugada (Kb). Para cualquier par conjugado ácido-base, el producto de sus constantes de disociación es igual a la constante del producto iónico del agua (Kw).
Consideremos un ácido débil genérico HA y su base conjugada A-:
HA(aq) + H2O(l) ⇴ H3O+(aq) + A-(aq) (Ka)
A-(aq) + H2O(l) ⇴ HA(aq) + OH-(aq) (Kb)
Si sumamos estas dos reacciones, obtenemos la autoionización del agua:
2H2O(l) ⇴ H3O+(aq) + OH-(aq) (Kw)
La relación entre las constantes de equilibrio es:
Ka × Kb = Kw
A 25°C, Kw tiene un valor de 1.0 × 10-14. Esto significa que si conocemos la Ka de un ácido, podemos calcular fácilmente la Kb de su base conjugada, y viceversa. Esta relación es increíblemente útil en química.

De manera análoga, podemos expresar esta relación en términos de pKa y pKb, utilizando la función logarítmica negativa:
- pKa = -log10Ka
- pKb = -log10Kb
- pKw = -log10Kw
Así, la relación logarítmica es:
pKa + pKb = pKw
Y a 25°C:
pKa + pKb = 14.00
Esta ecuación nos dice que cuanto más fuerte es un ácido (menor pKa), más débil es su base conjugada (mayor pKb), y viceversa. Esta relación inversa es fundamental para comprender la fuerza relativa de los pares ácido-base conjugados.
Tabla Comparativa de Pares Ácido-Base Conjugados Seleccionados
Para ilustrar la relación entre Ka, pKa, Kb y pKb, consideremos algunos ejemplos comunes a 25°C:
| Ácido (HA) | Ka | pKa | Base Conjugada (A-) | Kb | pKb |
|---|---|---|---|---|---|
| Ácido Acético (CH3COOH) | 1.7 × 10-5 | 4.76 | Acetato (CH3COO-) | 5.8 × 10-10 | 9.24 |
| Ión Amonio (NH4+) | 5.6 × 10-10 | 9.25 | Amoníaco (NH3) | 1.8 × 10-5 | 4.75 |
| Ácido Cianhídrico (HCN) | 6.2 × 10-10 | 9.21 | Cianuro (CN-) | 1.6 × 10-5 | 4.79 |
| Agua (H2O) | 1.0 × 10-14 | 14.00 | Hidróxido (OH-) | 1.0 | 0.00 |
Observa cómo la fuerza de un ácido se relaciona inversamente con la fuerza de su base conjugada. Por ejemplo, el ácido acético es un ácido débil (pKa = 4.76), y su base conjugada, el ion acetato, es una base débil (pKb = 9.24). En contraste, el ion amonio es un ácido muy débil (pKa = 9.25), pero su base conjugada, el amoníaco, es una base más fuerte (pKb = 4.75) en comparación con el ion acetato.
El Efecto de Nivelación en Soluciones Acuosas
Un concepto importante relacionado con la fuerza de ácidos y bases en solución acuosa es el Efecto de Nivelación. En agua, el ion hidronio (H3O+) es el ácido más fuerte que puede existir en equilibrio, y el ion hidróxido (OH-) es la base más fuerte que puede existir en equilibrio. Esto significa que cualquier ácido más fuerte que H3O+ (como HCl, H2SO4, HNO3) reaccionará completamente con el agua para formar H3O+. Del mismo modo, cualquier base más fuerte que OH- (como O2-, NH2-) reaccionará completamente con el agua para formar OH-.
Este efecto significa que no podemos distinguir la fuerza relativa de ácidos muy fuertes entre sí en agua, ya que todos se nivelan a la fuerza del H3O+. Lo mismo ocurre con las bases muy fuertes. Para comparar la fuerza de ácidos o bases que son más fuertes que H3O+ o OH-, respectivamente, se deben utilizar solventes no acuosos que sean menos básicos o menos ácidos que el agua.

Preguntas Frecuentes sobre Kb
¿Cuál es la fórmula para calcular Kb?
La fórmula general para calcular la constante de disociación de base (Kb) para una base débil B que se disocia en agua es: Kb = [BH+][OH-] / [B]. Donde [BH+], [OH-] y [B] son las concentraciones molares en el equilibrio del ácido conjugado, el ion hidróxido y la base no disociada, respectivamente.
¿Cómo se calcula Kb cuando se da el pH?
Para calcular Kb a partir del pH, siga estos pasos:
- Calcule el pOH utilizando la relación: pOH = 14.00 - pH (a 25°C).
- Determine la concentración de iones hidróxido ([OH-]) a partir del pOH: [OH-] = 10-pOH.
- Utilice la estequiometría de la reacción de disociación de la base para encontrar las concentraciones de equilibrio del ácido conjugado ([BH+]) y la base no disociada ([B]). Generalmente, [BH+] = [OH-], y [B] = [B]inicial - [OH-].
- Sustituya estas concentraciones en la fórmula de Kb: Kb = [BH+][OH-] / [B].
¿Cuál es el Kb de un ácido débil?
Un ácido débil no tiene un valor de Kb. Los ácidos tienen una constante de disociación de ácido (Ka), que mide su fuerza como donadores de protones. Sin embargo, un ácido débil sí tiene una base conjugada. La Kb de esta base conjugada se puede calcular a partir de la Ka del ácido débil usando la relación Ka × Kb = Kw. Por ejemplo, el ácido acético (un ácido débil) tiene una Ka, y su base conjugada, el ion acetato, tiene una Kb.
¿Por qué es importante conocer Kb?
Conocer Kb es fundamental para predecir el comportamiento de las bases débiles en solución, incluyendo su grado de ionización y el pH de la solución resultante. Es crucial en áreas como la química analítica (por ejemplo, en titulaciones ácido-base), la bioquímica (para entender sistemas amortiguadores biológicos) y la química ambiental (en el estudio de la acidez y basicidad de cuerpos de agua).
Conclusión
La constante de disociación de base (Kb) es un pilar fundamental en la química ácido-base, proporcionándonos una medida cuantitativa de la fuerza de una base débil. Su cálculo, a menudo derivado de mediciones de pH y pOH, es un proceso metódico que revela la concentración de iones hidróxido en el equilibrio y, por ende, el grado de ionización de la base. Hemos explorado cómo Kb se entrelaza con Ka a través de la constante de autoionización del agua (Kw), destacando la relación inversa entre la fuerza de un ácido y la de su base conjugada. Además, el concepto del Efecto de Nivelación nos recuerda las limitaciones del agua como solvente para discernir entre las fuerzas de ácidos y bases extremadamente fuertes. Dominar Kb no solo es esencial para la comprensión teórica de la química, sino que también es una habilidad práctica invaluable para la resolución de problemas y la aplicación en diversos campos científicos. La comprensión de estos equilibrios es la base para entender sistemas químicos más complejos y su comportamiento en el mundo real.
Si quieres conocer otros artículos parecidos a Calculando Kb: La Clave para Entender las Bases Débiles puedes visitar la categoría Química.