06/04/2024
La ebullición es un fenómeno cotidiano que observamos al calentar agua, pero detrás de esta simple acción se esconde un concepto fundamental en la química y la física: el punto de ebullición. Comprenderlo es esencial para campos que van desde la ingeniería petrolera hasta la síntesis de fármacos. Este artículo explorará en profundidad el punto de ebullición normal, cómo se define, qué factores lo influencian, y las metodologías tanto teóricas como prácticas para su cálculo y determinación.
- ¿Qué es el Punto de Ebullición Normal?
- Factores que Influyen en el Punto de Ebullición
- Cálculo del Punto de Ebullición Normal
- Determinación Experimental del Punto de Ebullición
- Preguntas Frecuentes
- ¿Cuál es la diferencia entre el punto de ebullición y el punto de ebullición normal?
- ¿Por qué los compuestos ramificados tienen puntos de ebullición más bajos que sus isómeros de cadena lineal?
- ¿Cómo afecta el peso molecular al punto de ebullición?
- ¿Es lo mismo calcular que determinar experimentalmente el punto de ebullición?
- ¿Qué son las fuerzas de dispersión de London?
- Conclusión
¿Qué es el Punto de Ebullición Normal?
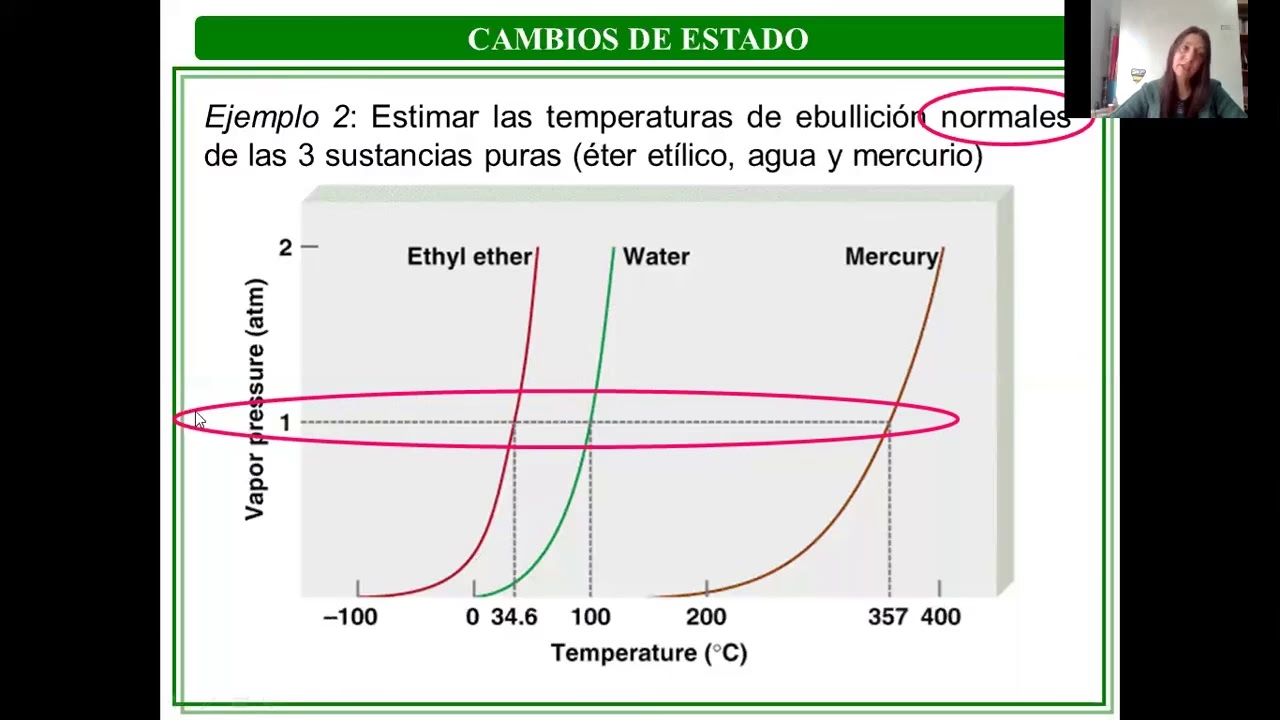
El punto de ebullición de un compuesto orgánico es la temperatura a la cual la presión de vapor del líquido iguala la presión ambiental que rodea al líquido. En otras palabras, es el momento en que las moléculas de un líquido tienen suficiente energía cinética para escapar de la superficie y convertirse en gas. Cuando hablamos del punto de ebullición normal, nos referimos específicamente a la temperatura a la cual una sustancia pura cambia de estado líquido a vapor a una presión de 1 atmósfera (1 atm o 14.7 psi). Esta es una propiedad característica y tabulada para la mayoría de los componentes puros, con la excepción de sustancias de muy alto punto de ebullición que no alcanzan este estado a presión atmosférica.
La presión de vapor es el resultado del equilibrio dinámico entre las moléculas en estado gaseoso y las moléculas en estado líquido. Las moléculas en estado líquido que poseen una energía cinética suficiente pueden vencer las fuerzas de atracción que las mantienen unidas y escapar a la fase gaseosa. La energía cinética, a su vez, está directamente relacionada con la temperatura, así como con la masa y la velocidad de las moléculas (K.E. = 1/2 mv²). Por lo tanto, a medida que la temperatura aumenta, la energía cinética promedio de las partículas líquidas se incrementa, permitiendo que más moléculas escapen y, consecuentemente, aumentando la presión de vapor. Cuando esta presión de vapor alcanza la presión externa (atmosférica), el líquido hierve.
Factores que Influyen en el Punto de Ebullición
El punto de ebullición de un compuesto no es una constante arbitraria; está influenciado por varias características moleculares. Comprender estos factores nos permite predecir y explicar las variaciones observadas en diferentes sustancias.
Peso Molecular y Estructura
Una de las reglas más generales es que los puntos de ebullición aumentan con el peso molecular dentro de una serie homóloga de derivados de hidrocarburos. Esto se debe a que las moléculas más grandes tienen más electrones, lo que conduce a fuerzas intermoleculares más fuertes. Como regla general, el punto de ebullición aumenta entre 20 y 30°C por cada carbono adicional en la cadena, una tendencia que se aplica a otras series homólogas.
La estructura molecular también tiene una influencia notable. Los isómeros de parafinas ramificadas suelen tener puntos de ebullición más bajos que los n-alcanos correspondientes. Esto se debe a que las ramificaciones reducen el área de superficie de contacto entre las moléculas, disminuyendo la efectividad de las fuerzas de Van der Waals. Por ejemplo, el isobutano (2-metilpropano) hierve a -12°C, mientras que el n-butano hierve a 0°C. Del mismo modo, el 2,2-dimetilbutano hierve a 50°C, mientras que el 2,3-dimetilbutano hierve a 58°C, ya que la forma del 2,3-dimetilbutano permite una mejor asociación intermolecular.

Los derivados de cicloalcanos, por otro lado, tienden a tener puntos de ebullición más altos que sus contrapartes lineales. Esto se atribuye a las conformaciones 'bloqueadas' de las moléculas anulares, que permiten una mayor área de contacto intermolecular y, por lo tanto, fuerzas de London más fuertes.
Fuerzas Intermoleculares
Las fuerzas de Van der Waals son determinantes clave de la fuerza de atracción intermolecular. Estas fuerzas dependen de dos factores principales:
- El número de electrones que rodean la molécula, que aumenta con el peso molecular.
- El área de superficie de la molécula.
Las fuerzas de dispersión de London son las fuerzas intermoleculares más débiles. Son fuerzas atractivas temporales que resultan cuando los electrones en dos átomos adyacentes ocupan posiciones que hacen que los átomos formen dipolos temporales. Una distribución asimétrica de electrones crea un dipolo instantáneo que puede inducir un dipolo en una molécula vecina, llevando a una atracción electrostática. Sustancias no polares condensan a líquidos y se congelan a sólidos debido a estas fuerzas cuando la temperatura disminuye lo suficiente.
Comparación entre Series Homólogas
Los derivados de alcanos, desde el metano (CH₄) hasta el butano (C₄H₁₀), son gaseosos en condiciones estándar (STP); desde el pentano (C₅H₁₂) hasta el C₁₇H₃₆ son líquidos; y a partir del C₁₈H₃₈ son sólidos. La siguiente tabla ilustra los puntos de ebullición de algunos alcanos:
| Nombre | Fórmula Molecular | Fórmula Estructural | Punto de Ebullición (°C) | Punto de Fusión (°C) | Densidad (g/ml, 20°C) |
|---|---|---|---|---|---|
| Metano | CH₄ | CH₄ | −161.5 | −182.5 | |
| Etano | C₂H₆ | CH₃CH₃ | −88.6 | −183.3 | |
| Propano | C₃H₈ | CH₃CH₂CH₃ | −42.1 | −189.7 | |
| Butano | C₄H₁₀ | CH₃(CH₂)₂CH₃ | −0.5 | −138.4 | |
| Pentano | C₅H₁₂ | CH₃(CH₂)₃CH₃ | 36.1 | −129.7 | 0.626 |
| Hexano | C₆H₁₄ | CH₃(CH₂)₄CH₃ | 68.7 | −95.3 | 0.659 |
| Heptano | C₇H₁₆ | CH₃(CH₂)₅CH₃ | 98.4 | −90.6 | 0.684 |
| Octano | C₈H₁₈ | CH₃(CH₂)₆CH₃ | 125.7 | −56.8 | 0.703 |
| Nonano | C₉H₂₀ | CH₃(CH₂)₇CH₃ | 150.8 | −53.5 | 0.718 |
| Decano | C₁₀H₂₂ | CH₃(CH₂)₈CH₃ | 174.1 | −29.7 | 0.730 |
Los puntos de ebullición de los derivados de alquenos, al igual que los de los alcanos, aumentan con el peso molecular. Sin embargo, el punto de ebullición de cada alqueno es muy similar al del alcano con el mismo número de átomos de carbono, aunque ligeramente inferior. Esto se debe a que los alquenos tienen dos electrones menos que el alcano correspondiente, lo que resulta en fuerzas de dispersión de Van der Waals ligeramente más débiles. Etileno, propileno y los diversos butenos son gases a temperatura ambiente, mientras que los alquenos de mayor punto de ebullición son líquidos.
| Alqueno | Punto de Ebullición (°C) |
|---|---|
| Etileno | −104 |
| Propileno | −47 |
| Trans-2-buteno | 0.9 |
| Cis-2-buteno | 3.7 |
| 1-Penteno | 30 |
| Trans-2-penteno | 36 |
| Cis-2-penteno | 37 |
| 1-Hepteno | 115 |
| 3-Octeno | 122 |
| 3-Noneno | 147 |
| 5-Deceno | 170 |
En cuanto a los alquinos, sus puntos de ebullición son generalmente más altos que los de los alcanos o alquenos con el mismo número de carbonos. Esto se atribuye al mayor número de electrones pi débilmente retenidos debido al triple enlace. Estos electrones son más fáciles de distorsionar, produciendo fuerzas atractivas más fuertes entre las moléculas, lo que las mantiene unidas a temperaturas más elevadas y evita la vaporización. La siguiente tabla muestra las propiedades de algunos alquinos:
| Nombre | Fórmula | Punto de Fusión (°C) | Punto de Ebullición (°C) | Densidad (20°C) |
|---|---|---|---|---|
| Acetileno | HC CH | −82 | −75 | |
| Propino | HC CCH₃ | −101.5 | −23 | |
| 1-Butino | HC CCH₂CH₃ | −122 | 91 | |
| 2-Butino | CH₃C CCH₃ | −24 | 27 | 0.694 |
| 1-Pentino | HC C(CH₂)₂CH₃ | −98 | 40 | 0.695 |
| 2-Pentino | CH₃C CCH₂CH₃ | −101 | 55 | 0.714 |
| 1-Hexino | HC C(CH₂)₃CH₃ | −124 | 72 | 0.719 |
| 1-Heptino | HC C(CH₂)₄CH₃ | −80 | 100 | 0.733 |
| 1-Octino | HC C(CH₂)₅CH₃ | −70 | 126 | 0.747 |
| 1-Nonino | HC C(CH₂)₆CH₃ | −65 | 151 | 0.763 |
| 1-Decino | HC C(CH₂)₇CH₃ | −35 | 182 | 0.770 |
Además de las series de hidrocarburos, es útil conocer los grupos alquilo comunes, que influyen en las propiedades de muchos compuestos orgánicos:
| Grupo | Átomos de Carbono | Fórmula |
|---|---|---|
| Metil | 1 | CH₃− |
| Etil | 2 | CH₃CH₂− |
| Propil | 3 | CH₃CH₂CH₂− |
| Butil | 4 | CH₃CH₂CH₂CH₂− |
| Pentil | 5 | CH₃CH₂CH₂CH₂CH₂− |
| Hexil | 6 | CH₃CH₂CH₂CH₂CH₂CH₂− |
| Heptil | 7 | CH₃CH₂CH₂CH₂CH₂CH₂CH₂− |
| Octil | 8 | CH₃CH₂CH₂CH₂CH₂CH₂CH₂CH₂− |
| Nonil | 9 | CH₃CH₂CH₂CH₂CHCH₂CH₂CH₂CH₂− |
| Decil | 10 | CH₃CH₂CH₂CH₂CH₂CH₂CH₂CH₂CH₂CH₂− |
Cálculo del Punto de Ebullición Normal
El punto de ebullición normal puede ser determinado teóricamente a partir del calor de vaporización utilizando la ecuación de Clausius-Clapeyron. Esta ecuación fundamental en la termodinámica relaciona la presión de vapor de una sustancia a una temperatura con su presión de vapor a otra temperatura, dado el calor de vaporización. Para encontrar el punto de ebullición normal, se debe resolver esta ecuación para la temperatura en la que la presión de vapor es igual a 1 atmósfera. Si bien la ecuación en sí misma implica logaritmos y constantes, conceptualmente permite predecir el punto de ebullición en condiciones estándar si se conocen otras propiedades termodinámicas de la sustancia.
Determinación Experimental del Punto de Ebullición
Existen diversos métodos para determinar el punto de ebullición de una muestra en el laboratorio, cada uno con sus ventajas y consideraciones. Los más comunes incluyen la destilación, el método de reflujo y el uso del tubo de Thiele.

Método de Destilación Simple
Para la mayoría de las situaciones, una destilación simple es suficiente para determinar el punto de ebullición. Se recomienda usar al menos 5 mL de muestra en el matraz de destilación junto con algunas piedras de ebullición o una barra de agitación. A medida que la mayor parte del material se destila, la temperatura más alta registrada en el termómetro corresponde al punto de ebullición. Una fuente importante de error en este método es registrar una temperatura demasiado baja antes de que los vapores calientes sumerjan completamente el bulbo del termómetro. Es crucial monitorear el termómetro periódicamente, especialmente cuando la destilación está activa. Se debe registrar la presión barométrica junto con el punto de ebullición, ya que este valor influye directamente en el punto de ebullición observado.
Método de Reflujo
Una configuración de reflujo también puede utilizarse para determinar el punto de ebullición de un compuesto. El reflujo ocurre cuando un líquido está hirviendo y condensándose activamente, con el líquido condensado regresando al matraz original. Es análogo a una configuración de destilación, con la principal diferencia en la colocación vertical del condensador. Se utiliza un condensador a microescala y un termómetro digital, con aproximadamente 5 mL de líquido y algunas piedras de ebullición. El termómetro se coloca bajo en el aparato, de modo que la parte inferior esté entre el líquido hirviendo y la parte inferior del condensador. En esta posición, el termómetro puede medir con precisión los vapores calientes y la temperatura se estabilizará en el punto de ebullición del compuesto. Es importante no sumergir el termómetro directamente en el líquido hirviendo, ya que el líquido podría estar sobrecalentado, es decir, más caliente que su punto de ebullición real. También existe un método de reflujo alternativo utilizando un tubo de ensayo, aunque puede tener errores significativos para compuestos con puntos de ebullición muy bajos (< 70°C) o muy altos (> 150°C).
Método del Tubo de Thiele
Este es el método más sencillo y tiene la ventaja de usar menos de 0.5 mL de material, lo que lo hace ideal para muestras pequeñas. El tubo de Thiele se calienta con un mechero, creando una corriente de convección de aceite que calienta uniformemente una pequeña muestra. Se introduce un capilar invertido con la muestra líquida, y el punto de ebullición se determina observando la temperatura a la que el líquido comienza a ascender por el capilar y luego desciende a medida que los vapores se condensan, indicando que la presión de vapor iguala la presión atmosférica.
Preguntas Frecuentes
¿Cuál es la diferencia entre el punto de ebullición y el punto de ebullición normal?
El punto de ebullición es la temperatura a la que un líquido hierve a una presión ambiental determinada, que puede variar. El punto de ebullición normal es un punto de referencia estandarizado, que ocurre específicamente cuando la presión de vapor del líquido iguala 1 atmósfera (presión atmosférica estándar).
¿Por qué los compuestos ramificados tienen puntos de ebullición más bajos que sus isómeros de cadena lineal?
Los compuestos ramificados tienen una forma más compacta y esférica, lo que reduce el área de superficie de contacto entre las moléculas adyacentes. Esto disminuye la fuerza de las interacciones de Van der Waals (fuerzas de dispersión de London), requiriendo menos energía (temperatura) para que las moléculas escapen a la fase gaseosa.

¿Cómo afecta el peso molecular al punto de ebullición?
En general, a mayor peso molecular dentro de una serie homóloga, mayor es el punto de ebullición. Esto se debe a que las moléculas más grandes tienen más electrones, lo que resulta en fuerzas de dispersión de London más fuertes y temporales entre las moléculas, que requieren más energía para ser superadas.
¿Es lo mismo calcular que determinar experimentalmente el punto de ebullición?
No, no es lo mismo. Calcular el punto de ebullición implica el uso de ecuaciones termodinámicas, como la de Clausius-Clapeyron, para predecir el valor basándose en otras propiedades físicas (como el calor de vaporización). Determinar experimentalmente implica realizar mediciones en el laboratorio utilizando técnicas como la destilación o el reflujo, observando directamente la temperatura a la que ocurre la ebullición.
¿Qué son las fuerzas de dispersión de London?
Son las fuerzas intermoleculares más débiles y ocurren entre todas las moléculas. Son atracciones temporales que surgen de la formación de dipolos instantáneos debido al movimiento aleatorio de los electrones. Estos dipolos pueden inducir dipolos en moléculas vecinas, creando una atracción momentánea.
Conclusión
El punto de ebullición normal es una propiedad física crucial que nos proporciona valiosa información sobre las características estructurales y las propiedades intermoleculares de una sustancia. Ya sea a través de cálculos teóricos basados en la ecuación de Clausius-Clapeyron o mediante métodos experimentales rigurosos como la destilación y el reflujo, la capacidad de definir y determinar este punto es fundamental en numerosos campos científicos e industriales. Comprender cómo factores como el peso molecular, la ramificación y las fuerzas intermoleculares influyen en el punto de ebullición no solo enriquece nuestro conocimiento de la materia, sino que también nos permite predecir el comportamiento de las sustancias en diversas condiciones.
Si quieres conocer otros artículos parecidos a Punto de Ebullición Normal: Definición y Cálculo puedes visitar la categoría Química.
