28/01/2024
Cuando hablamos de soluciones en química, nos referimos a mezclas homogéneas donde una sustancia, el soluto, se disuelve en otra, el disolvente. Pero, ¿existe un límite para la cantidad de soluto que puede disolverse? La respuesta es sí, y es precisamente en este límite donde encontramos el concepto crucial de solución saturada. Una solución se considera saturada cuando el disolvente ha logrado disolver la máxima cantidad de soluto posible a una temperatura y presión dadas, estableciéndose un equilibrio dinámico entre el soluto disuelto y el soluto no disuelto.

Imaginemos que estamos preparando una bebida azucarada. Añadimos una cucharada de azúcar y se disuelve completamente. Añadimos otra y también se disuelve. Pero si seguimos añadiendo azúcar, llegará un punto en que, por mucho que agitemos, el azúcar ya no se disolverá y permanecerá en el fondo del recipiente. En ese instante, nuestra bebida ha alcanzado la saturación.
- ¿Qué Define una Solución Saturada?
- Factores Clave que Afectan la Solubilidad y la Saturación
- Soluciones Insaturadas y Sobresaturadas: Un Espectro de Posibilidades
- El Caso del Nitrato de Potasio: Un Ejemplo Ilustrativo
- Curvas de Solubilidad: Una Herramienta Visual
- Aplicaciones Prácticas de las Soluciones Saturadas
- ¿Cómo Preparar una Solución Saturada?
- Preguntas Frecuentes (FAQ)
¿Qué Define una Solución Saturada?
Una solución saturada es aquella en la que se ha disuelto la cantidad máxima de soluto que un disolvente puede contener a una temperatura y presión específicas. En este estado, la velocidad a la que el soluto se disuelve es igual a la velocidad a la que el soluto disuelto cristaliza o precipita fuera de la solución. Esto significa que, aunque parezca que no hay más disolución, las partículas de soluto siguen entrando y saliendo de la solución en un proceso de equilibrio dinámico. Si se añade más soluto a una solución ya saturada, este soluto adicional simplemente se acumulará en el fondo del recipiente sin disolverse.
Es fundamental comprender que la capacidad de un disolvente para disolver un soluto no es ilimitada y varía significativamente según diversos factores. La solubilidad es una propiedad intensiva de la materia que nos indica la cantidad máxima de soluto que se puede disolver en una cantidad específica de disolvente a una temperatura determinada.
Factores Clave que Afectan la Solubilidad y la Saturación
La formación de una solución saturada está directamente influenciada por varios factores:
1. La Temperatura
La temperatura es, sin duda, el factor más influyente en la solubilidad de la mayoría de los sólidos en líquidos. Generalmente, a medida que la temperatura aumenta, la solubilidad de los sólidos en líquidos también lo hace. Esto se debe a que un incremento de la temperatura proporciona más energía cinética a las moléculas del disolvente, permitiéndoles interactuar más eficazmente con las partículas del soluto y romper sus enlaces intermoleculares. El ejemplo proporcionado sobre el nitrato de potasio ilustra esto perfectamente: un litro de agua a 40°C puede disolver hasta 639 gramos de nitrato de potasio. Si la temperatura fuera menor, la cantidad disuelta sería significativamente menor.
Por otro lado, la solubilidad de los gases en líquidos suele disminuir a medida que aumenta la temperatura. Piense en una bebida carbonatada: cuando está fría, retiene mejor el dióxido de carbono disuelto, pero al calentarse, el gas escapa rápidamente.
2. La Naturaleza del Soluto y del Disolvente
El principio de "lo similar disuelve lo similar" es fundamental aquí. Los solutos polares tienden a disolverse mejor en disolventes polares (como el agua), mientras que los solutos no polares se disuelven mejor en disolventes no polares (como el hexano). La estructura química y la polaridad de ambas sustancias determinan la fuerza de las interacciones intermoleculares que pueden formarse entre ellas, lo cual es crucial para la disolución. Por ejemplo, la sal de mesa (cloruro de sodio, un compuesto iónico y polar) se disuelve muy bien en agua (polar), pero no en aceite (no polar).
3. La Presión
La presión tiene un efecto mínimo en la solubilidad de sólidos y líquidos en disolventes líquidos. Sin embargo, es un factor muy importante para la solubilidad de los gases en líquidos. A mayor presión parcial de un gas sobre la superficie de un líquido, mayor será la cantidad de gas que se disolverá en ese líquido. Esto es lo que ocurre en las bebidas carbonatadas, donde el CO2 se disuelve a alta presión y burbujea al abrir el envase y liberar esa presión.
4. El Tamaño de Partícula del Soluto
Aunque no afecta la solubilidad máxima (la cantidad total que se puede disolver), el tamaño de partícula influye en la velocidad a la que el soluto se disuelve. Las partículas más pequeñas tienen una mayor superficie de contacto con el disolvente, lo que acelera el proceso de disolución y permite alcanzar la saturación más rápidamente. Por eso, el azúcar en polvo se disuelve más rápido que el azúcar granulado.
Soluciones Insaturadas y Sobresaturadas: Un Espectro de Posibilidades
Además de las soluciones saturadas, existen otras dos categorías importantes:
Soluciones Insaturadas
Una solución insaturada contiene menos soluto del que el disolvente puede disolver a una temperatura y presión dadas. En este tipo de solución, es posible añadir más soluto y que este se disuelva completamente. Es el estado inicial de muchas mezclas antes de alcanzar su límite.
Soluciones Sobresaturadas
Las soluciones sobresaturadas son un caso especial y fascinante. Contienen más soluto disuelto del que normalmente sería posible a una temperatura y presión dadas. Estas soluciones son intrínsecamente inestables y se preparan enfriando lentamente una solución saturada que inicialmente estaba caliente, sin que el soluto excedente precipite. Cualquier pequeña perturbación, como la adición de un cristal semilla o una agitación, puede provocar la cristalización súbita del exceso de soluto, volviendo la solución a un estado saturado estable. Un ejemplo clásico es el tiosulfato de sodio o el acetato de sodio, utilizados en las bolsas de calor reutilizables.
| Tipo de Solución | Cantidad de Soluto | Estabilidad | Comportamiento al Añadir Más Soluto |
|---|---|---|---|
| Insaturada | Menos del máximo | Estable | Se disuelve |
| Saturada | Máximo disuelto | Estable (equilibrio dinámico) | No se disuelve, se acumula |
| Sobresaturada | Más del máximo (inestable) | Inestable | Provoca cristalización masiva |
El Caso del Nitrato de Potasio: Un Ejemplo Ilustrativo
Volvamos al ejemplo proporcionado: un litro de agua a 40°C puede disolver hasta 639 gramos de nitrato de potasio (KNO3). Esto significa que, si usted tiene un litro de agua a esa temperatura y añade 639 gramos de KNO3, y agita, obtendrá una solución saturada. Si añade un gramo más, ese gramo no se disolverá y permanecerá como sólido en el fondo. Si, por el contrario, añade solo 500 gramos, la solución será insaturada y aún podría disolver 139 gramos adicionales de KNO3.
Este comportamiento es típico de muchos compuestos iónicos. La solubilidad del nitrato de potasio en agua es particularmente sensible a la temperatura. A 0°C, solo se disuelven aproximadamente 13.3 gramos de KNO3 en 100 mL de agua, mientras que a 100°C, la solubilidad se dispara a unos 247 gramos por 100 mL. Esto hace del nitrato de potasio un excelente ejemplo para demostrar cómo la temperatura afecta drásticamente la capacidad de disolución y la formación de soluciones saturadas y sobresaturadas.
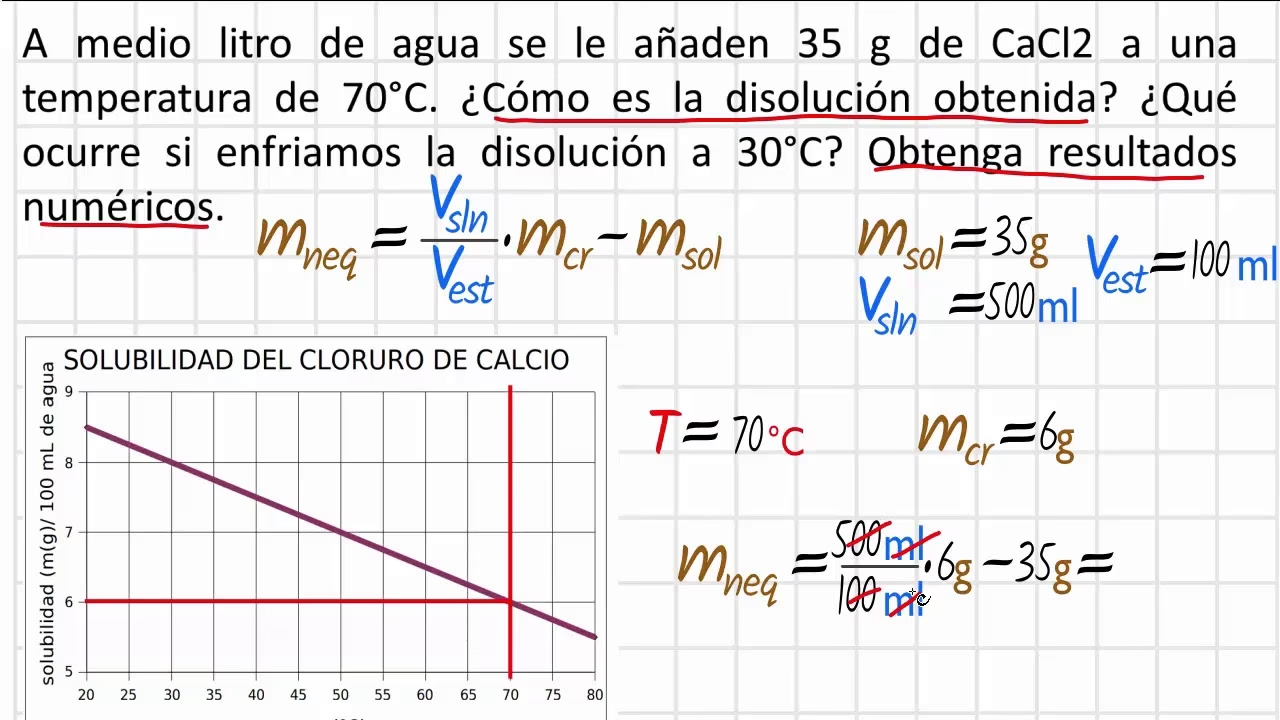
Curvas de Solubilidad: Una Herramienta Visual
En química, las curvas de solubilidad son gráficos que muestran la cantidad máxima de un soluto que puede disolverse en 100 gramos (o 100 mL) de un disolvente a diferentes temperaturas. Estas curvas son invaluablemente útiles para predecir si una solución será insaturada, saturada o sobresaturada a una temperatura específica. Cada punto en la curva representa una solución saturada a esa temperatura. Los puntos por debajo de la curva indican soluciones insaturadas, mientras que los puntos por encima de la curva (si se logran) representarían soluciones sobresaturadas, que son inestables.
Observar una curva de solubilidad para el nitrato de potasio mostraría una pendiente ascendente muy pronunciada, confirmando su alta dependencia de la temperatura. Otras sales como el cloruro de sodio (NaCl) tienen una curva de solubilidad mucho más plana, indicando que su solubilidad no cambia drásticamente con la temperatura.
Aplicaciones Prácticas de las Soluciones Saturadas
El concepto de soluciones saturadas no es meramente teórico; tiene numerosas aplicaciones prácticas en diversas industrias y procesos:
- Cristalización: Es uno de los métodos más importantes para purificar sustancias. Al enfriar lentamente una solución caliente saturada o evaporar el disolvente, el soluto excedente precipita en forma de cristales puros. Este proceso se utiliza para obtener azúcar, sal, fármacos y muchos otros productos químicos.
- Preparación de Soluciones Estándar: En laboratorios, las soluciones saturadas se utilizan a veces como punto de partida para preparar soluciones de concentraciones conocidas, aunque es más común usar soluciones patrón con concentraciones exactas y predefinidas.
- Industria Alimentaria: La saturación es clave en la producción de dulces, mermeladas y bebidas concentradas, donde se busca disolver la máxima cantidad de azúcar para lograr la textura y dulzura deseadas.
- Farmacología: La solubilidad de los fármacos es un factor crítico para su absorción y eficacia en el cuerpo. Comprender los límites de solubilidad ayuda en la formulación de medicamentos.
- Geología: La formación de minerales y rocas a menudo implica la precipitación de sustancias de soluciones sobresaturadas en la naturaleza, como la formación de estalactitas y estalagmitas en cuevas.
¿Cómo Preparar una Solución Saturada?
Para preparar una solución saturada de un sólido en un líquido, sigue estos pasos:
- Mide una cantidad específica del disolvente (por ejemplo, 100 mL de agua) a una temperatura constante y controlada.
- Añade pequeñas cantidades del soluto al disolvente, agitando vigorosamente después de cada adición.
- Continúa añadiendo soluto hasta que observes que una pequeña cantidad de soluto ya no se disuelve y permanece como sólido en el fondo del recipiente, incluso después de una agitación prolongada y vigorosa.
- En este punto, la solución líquida que tienes es una solución saturada. El sólido que no se disolvió es el exceso de soluto.
- Para mayor precisión, puedes dejar que la solución se asiente para que el exceso de sólido se asiente en el fondo, y luego decantar cuidadosamente la solución saturada.
Es importante recordar que la temperatura debe mantenerse constante durante todo el proceso, ya que cualquier fluctuación afectará la cantidad de soluto que puede disolverse.
Preguntas Frecuentes (FAQ)
¿Se puede disolver más soluto en una solución saturada?
No, a una temperatura y presión dadas, una solución saturada ya contiene la máxima cantidad de soluto que puede disolver. Cualquier soluto adicional que se añada no se disolverá y permanecerá como sólido en el fondo del recipiente.
¿Es lo mismo una solución saturada que una solución concentrada?
No necesariamente. Una solución concentrada simplemente tiene una gran cantidad de soluto disuelto en relación con el disolvente. Puede ser concentrada y aún así ser insaturada si aún puede disolver más soluto. Una solución saturada es siempre concentrada hasta su límite de solubilidad, pero no todas las soluciones concentradas son saturadas.
¿Cómo puedo saber si una solución está saturada?
La forma más sencilla de saber si una solución está saturada es intentar añadir un poco más de soluto. Si el soluto adicional no se disuelve y se asienta en el fondo (o flota, dependiendo de su densidad), entonces la solución está saturada. Otra forma es comparar la concentración de la solución con la solubilidad conocida del soluto a esa temperatura.
¿Qué sucede si caliento una solución saturada?
Si calientas una solución saturada de un sólido en un líquido (donde la solubilidad aumenta con la temperatura), la solución se volverá insaturada, ya que la capacidad del disolvente para disolver el soluto aumentará. Esto significa que podrás disolver más soluto a la nueva temperatura más alta.
¿Qué sucede si enfrío una solución saturada?
Si enfrías una solución saturada de un sólido en un líquido (donde la solubilidad disminuye con la temperatura), el soluto excedente precipitará fuera de la solución en forma de sólido, ya que el disolvente ya no podrá mantener la misma cantidad de soluto disuelto a la temperatura más baja. Este es el principio de la cristalización.
En resumen, el concepto de solución saturada es fundamental para comprender cómo interactúan las sustancias y cuáles son los límites de la disolución. Es un equilibrio delicado influenciado principalmente por la temperatura y la naturaleza de las sustancias involucradas, con implicaciones que van desde la química básica hasta procesos industriales complejos y fenómenos naturales.
Si quieres conocer otros artículos parecidos a Soluciones Saturadas: El Límite de la Disolución puedes visitar la categoría Química.