11/11/2025
En el vasto universo de la química, las reacciones son el motor que impulsa la transformación de la materia. Desde la combustión que enciende un motor hasta los complejos procesos biológicos que sustentan la vida, cada cambio implica la interacción de sustancias. Para comprender, predecir y controlar estas transformaciones, es fundamental saber exactamente cuánta de cada sustancia se necesita y cuánta se producirá. Aquí es donde entra en juego la estequiometría, la rama de la química que nos permite cuantificar con precisión las relaciones entre reactivos y productos.

Este artículo te guiará a través de los principios esenciales para calcular las cantidades involucradas en cualquier reacción química, desvelando el misterio detrás de las fórmulas y las flechas que vemos en las ecuaciones. Prepárate para dominar el arte de la cuantificación química, una habilidad indispensable para científicos, ingenieros y cualquier persona interesada en comprender cómo funciona el mundo a nivel molecular.
- ¿Qué son Reactivos y Productos en una Reacción Química?
- La Ecuación Química: El Mapa Detallado de la Transformación
- Balanceo de Ecuaciones Químicas: La Clave de la Conservación
- Estequiometría: El Arte de Cuantificar la Materia
- El Reactivo Limitante: El Factor Determinante de la Reacción
- Rendimiento Teórico vs. Rendimiento Real
- Aplicaciones Prácticas de la Estequiometría
- Tabla Comparativa: Reactivos vs. Productos
- Preguntas Frecuentes (FAQ)
- ¿Por qué es tan importante balancear una ecuación química antes de hacer cálculos?
- ¿Qué es un mol y por qué se usa en estequiometría?
- ¿Pueden los reactivos y productos ser lo mismo?
- ¿Cómo se manejan los gases en los cálculos estequiométricos?
- ¿Qué debo hacer si mis cantidades iniciales no están en moles?
- ¿La estequiometría siempre predice el resultado exacto en el laboratorio?
- Conclusión
¿Qué son Reactivos y Productos en una Reacción Química?
Antes de sumergirnos en los cálculos, es crucial entender los actores principales de cualquier transformación química: los reactivos y los productos. Piensa en ellos como un par inseparable, como el concepto de 'arriba' y 'abajo'; uno no puede existir sin el otro en el contexto de una reacción. Cuando átomos o moléculas se juntan bajo las condiciones adecuadas, las energías que rigen el comportamiento de los electrones en los enlaces químicos permiten que se formen nuevos enlaces y que los existentes cambien de maneras específicas, dando lugar a una reacción química.
Los reactivos son las sustancias iniciales, las 'materias primas', que se consumen o transforman durante la reacción. Son los ingredientes que pones al principio. Una vez que la reacción ocurre, sus identidades químicas cambian. Dejan de ser los elementos o compuestos que eran antes de la interacción y se convierten en nuevos compuestos como resultado de los diversos cambios que han experimentado. En otras palabras, se transforman de reactivos en productos.
Los productos, por su parte, son las nuevas sustancias que se forman como resultado de la reacción química. Son el resultado final, lo que obtienes después de que los ingredientes iniciales han reaccionado. La relación entre reactivos y productos se indica en una ecuación química general de la siguiente manera:
A + B → C + D
Esta representación particular muestra que dos compuestos, A y B, reaccionan para producir dos productos, C y D. Por convención, los materiales de partida (los reactivos) se presentan a la izquierda de la flecha, y los productos a la derecha. La flecha siempre apunta desde los reactivos hacia los productos, indicando la dirección de la reacción.
Es importante destacar que la designación de qué compuestos o elementos son reactivos y cuáles son productos es relativa y depende de la dirección deseada de la reacción. Prácticamente todas las reacciones que proceden en una dirección también pueden hacerse proceder en la dirección opuesta. Esto significa que la ecuación A + B → C + D, que indica que A y B reaccionan para producir C y D, usualmente también puede escribirse como C + D → A + B, indicando que C y D reaccionan para producir A y B. Lo que eran reactivos en la primera reacción son productos en la segunda.
Muchos sistemas de reacción alcanzan una condición llamada equilibrio. En estos casos, la reacción directa, en la que los reactivos forman los productos, ocurre al mismo tiempo que la reacción inversa, en la que los productos vuelven a formar los reactivos. En el equilibrio, estos dos procesos de reacción opuestos tienen lugar exactamente a la misma velocidad, lo que se indica en la ecuación de reacción reemplazando la flecha unidireccional por una doble media flecha que apunta en ambas direcciones:
A + B ⇌ C + D
La Ecuación Química: El Mapa Detallado de la Transformación
Para proporcionar la información precisa y utilizable que una ecuación de reacción debe transmitir, como las identidades químicas de los reactivos y productos, se requiere una fórmula química que identifique de manera única e inequívoca cada reactivo y producto. La fórmula química también utiliza subíndices y coeficientes numéricos para identificar todos los átomos o moléculas presentes y cuántos de cada uno.
Por ejemplo, la ecuación:
2Al + Fe₂O₃ → 2Fe + Al₂O₃
establece claramente que dos átomos de aluminio reaccionan con una molécula de óxido de hierro para producir dos átomos de hierro y una molécula de óxido de aluminio. También indica que cada molécula de óxido de hierro se compone de dos átomos de hierro y tres de oxígeno, mientras que cada molécula de óxido de aluminio se compone de dos átomos de aluminio y tres de oxígeno. Para la mayoría de los compuestos orgánicos, la ecuación de reacción se escribe utilizando una representación pictórica de la estructura molecular tridimensional de cada reactivo y producto en lugar de solo sus fórmulas químicas.
Balanceo de Ecuaciones Químicas: La Clave de la Conservación
El primer paso y el más crucial para calcular las cantidades de reactivos y productos es asegurar que la ecuación química esté balanceada. Una ecuación balanceada obedece la Ley de Conservación de la Masa, que establece que la masa no se crea ni se destruye en una reacción química. Esto significa que el número de átomos de cada elemento debe ser el mismo en ambos lados de la ecuación (tanto en los reactivos como en los productos).
Balancear una ecuación implica ajustar los coeficientes (los números grandes delante de las fórmulas) para que el número de átomos de cada tipo sea igual en ambos lados de la flecha. Nunca se deben cambiar los subíndices dentro de las fórmulas, ya que esto alteraría la identidad de la sustancia.
Consideremos un ejemplo simple, la formación de agua:
H₂ + O₂ → H₂O
En el lado de los reactivos, tenemos 2 átomos de H y 2 átomos de O. En el lado de los productos, tenemos 2 átomos de H y 1 átomo de O. La ecuación no está balanceada para el oxígeno. Para balancearla, colocamos un coeficiente de '2' delante del H₂O:
H₂ + O₂ → 2H₂O
Ahora, en los productos tenemos 4 átomos de H (2x2) y 2 átomos de O (2x1). El oxígeno está balanceado, pero el hidrógeno no. Para balancear el hidrógeno en los reactivos, colocamos un '2' delante del H₂:
2H₂ + O₂ → 2H₂O
Ahora, ambos lados tienen 4 átomos de H y 2 átomos de O. La ecuación está balanceada. Este proceso de ajuste de coeficientes es fundamental porque las proporciones de los coeficientes en una ecuación balanceada son las proporciones molares en las que las sustancias reaccionan y se producen.
Estequiometría: El Arte de Cuantificar la Materia
La estequiometría es el pilar de la química cuantitativa. Se basa en las relaciones numéricas entre las cantidades de reactivos y productos en una reacción química. Estas relaciones se derivan directamente de los coeficientes de la ecuación química balanceada. Estos coeficientes representan las proporciones de moles de cada sustancia involucrada.
Para realizar cálculos estequiométricos, necesitamos comprender el concepto de mol. Un mol es una unidad de cantidad de sustancia que contiene aproximadamente 6.022 x 1023 partículas (átomos, moléculas, iones, etc.), conocido como el Número de Avogadro. La importancia del mol radica en que la masa molar de una sustancia (su masa en gramos por mol) es numéricamente igual a su peso atómico o molecular expresado en unidades de masa atómica.
Por ejemplo, el oxígeno molecular (O₂) tiene una masa molecular de aproximadamente 32 g/mol (16 g/mol por cada átomo de oxígeno). Esto significa que 1 mol de O₂ pesa 32 gramos. Esta conversión entre masa y moles es esencial para los cálculos, ya que la balanza de laboratorio mide masa, no moles.
Pasos para Calcular Cantidades de Reactivos y Productos:
- Escribir la ecuación química no balanceada: Asegúrate de que todas las fórmulas de los reactivos y productos sean correctas.
- Balancear la ecuación: Ajusta los coeficientes para que el número de átomos de cada elemento sea el mismo en ambos lados de la ecuación. Este es el paso más crítico.
- Identificar la cantidad conocida: Determina la cantidad de la sustancia de partida. Puede estar en gramos, litros (para gases a condiciones estándar), o moles.
- Convertir la cantidad conocida a moles: Si la cantidad conocida no está en moles, usa la masa molar (para sólidos/líquidos) o el volumen molar (para gases ideales a C.N.T.P.) para convertirla a moles.
- Usar la relación molar (factor estequiométrico): Utiliza los coeficientes de la ecuación balanceada para establecer una proporción entre los moles de la sustancia conocida y los moles de la sustancia deseada (ya sea otro reactivo o un producto).
- Convertir los moles de la sustancia deseada a la unidad requerida: Si la respuesta se necesita en gramos, litros o cualquier otra unidad, usa la masa molar o el volumen molar para realizar la conversión final.
Ejemplo de Cálculo Masa-Masa:
¿Cuántos gramos de agua (H₂O) se producen cuando 10 gramos de hidrógeno (H₂) reaccionan completamente con oxígeno (O₂)?
- Ecuación no balanceada:
H₂ + O₂ → H₂O - Ecuación balanceada:
2H₂ + O₂ → 2H₂O - Cantidad conocida: 10 g de H₂.
- Convertir H₂ a moles: La masa molar de H₂ es 2 g/mol.
Moles de H₂ = 10 g H₂ * (1 mol H₂ / 2 g H₂) = 5 moles H₂ - Usar relación molar (H₂ a H₂O): De la ecuación balanceada, 2 moles de H₂ producen 2 moles de H₂O, lo que es una relación de 1:1.
Moles de H₂O = 5 moles H₂ * (2 moles H₂O / 2 moles H₂) = 5 moles H₂O - Convertir H₂O a gramos: La masa molar de H₂O es 18 g/mol.
Gramos de H₂O = 5 moles H₂O * (18 g H₂O / 1 mol H₂O) = 90 g H₂O
Así, 10 gramos de hidrógeno producirán 90 gramos de agua.
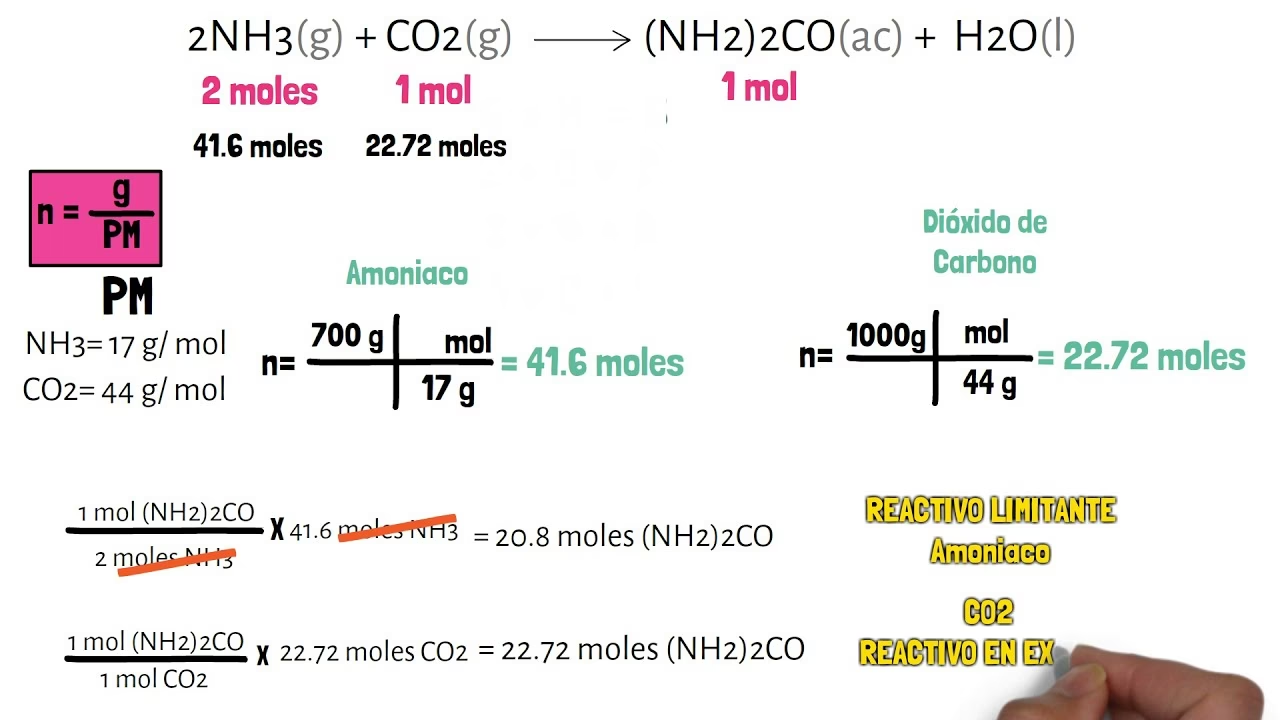
El Reactivo Limitante: El Factor Determinante de la Reacción
En muchas reacciones, los reactivos no están presentes en las proporciones estequiométricas exactas. Cuando esto sucede, uno de los reactivos se agotará primero, deteniendo la reacción y limitando la cantidad de producto que se puede formar. Este reactivo se conoce como el reactivo limitante. El otro reactivo, que queda en exceso después de que la reacción ha terminado, es el reactivo en exceso.
Identificar el reactivo limitante es crucial porque determina el rendimiento máximo posible de la reacción. Para encontrarlo, se calcula la cantidad de producto que cada reactivo podría formar si fuera el único en agotarse. El reactivo que produce la menor cantidad de producto es el limitante.
Ejemplo de Cálculo con Reactivo Limitante:
Si reaccionan 50 g de N₂ con 10 g de H₂ para producir amoníaco (NH₃), ¿cuántos gramos de NH₃ se formarán?
Ecuación balanceada:N₂(g) + 3H₂(g) → 2NH₃(g)
1. Moles de N₂: Masa molar de N₂ = 28 g/mol. Moles de N₂ = 50 g N₂ * (1 mol N₂ / 28 g N₂) ≈ 1.786 moles N₂ 2. Moles de H₂: Masa molar de H₂ = 2 g/mol. Moles de H₂ = 10 g H₂ * (1 mol H₂ / 2 g H₂) = 5.000 moles H₂ 3. Calcular el producto que cada reactivo podría formar: * Si N₂ es el limitante: Moles de NH₃ = 1.786 moles N₂ * (2 moles NH₃ / 1 mol N₂) = 3.572 moles NH₃ * Si H₂ es el limitante: Moles de NH₃ = 5.000 moles H₂ * (2 moles NH₃ / 3 moles H₂) = 3.333 moles NH₃ 4. Identificar el reactivo limitante: H₂ produce la menor cantidad de NH₃ (3.333 moles), por lo tanto, el H₂ es el reactivo limitante. 5. Calcular los gramos de NH₃ formados: Masa molar de NH₃ = 17 g/mol. Gramos de NH₃ = 3.333 moles NH₃ * (17 g NH₃ / 1 mol NH₃) ≈ 56.66 g NH₃
Por lo tanto, se formarán aproximadamente 56.66 gramos de amoníaco.
Rendimiento Teórico vs. Rendimiento Real
El cálculo estequiométrico que acabamos de realizar nos da el rendimiento teórico: la cantidad máxima de producto que se podría obtener si la reacción fuera 100% eficiente y no hubiera pérdidas. Sin embargo, en la práctica, el rendimiento real (la cantidad de producto realmente obtenida en el laboratorio o la industria) casi siempre es menor que el rendimiento teórico. Esto se debe a varios factores, como impurezas en los reactivos, reacciones secundarias no deseadas, pérdidas durante la purificación del producto, o que la reacción no llega a completarse.
El porcentaje de rendimiento se calcula como:
Porcentaje de Rendimiento = (Rendimiento Real / Rendimiento Teórico) * 100%
Comprender la diferencia entre el rendimiento teórico y el real es fundamental para optimizar los procesos químicos y evaluar la eficiencia de una síntesis.
Aplicaciones Prácticas de la Estequiometría
La capacidad de cuantificar reactivos y productos no es solo un ejercicio académico; es una habilidad fundamental con vastas aplicaciones en el mundo real:
- Industria Química: Para determinar la cantidad de materias primas necesarias para producir una cantidad específica de un producto, minimizando residuos y optimizando costos.
- Farmacología: En la síntesis de medicamentos, para calcular las dosis exactas de los ingredientes y asegurar la pureza del producto final.
- Medio Ambiente: Para analizar contaminantes, determinar la cantidad de sustancias tóxicas en una muestra o calcular la eficiencia de procesos de tratamiento de aguas.
- Alimentos y Bebidas: En la formulación de productos, para asegurar que los ingredientes estén en las proporciones correctas y que los procesos de fermentación o cocción sean eficientes.
- Metalurgia: Para calcular las proporciones de minerales y agentes reductores necesarios en la extracción de metales.
En esencia, la estequiometría es el lenguaje cuantitativo de la química, permitiendo a los profesionales de diversas disciplinas predecir y controlar las transformaciones de la materia.
Tabla Comparativa: Reactivos vs. Productos
| Característica | Reactivos | Productos |
|---|---|---|
| Definición | Sustancias iniciales que se transforman. | Nuevas sustancias formadas por la reacción. |
| Posición en la ecuación (convención) | Lado izquierdo de la flecha (→). | Lado derecho de la flecha (→). |
| Identidad Química | Cambia durante la reacción. | Diferente a la de los reactivos. |
| Transformación | Se consumen o disminuyen durante la reacción. | Se forman o aumentan durante la reacción. |
| Relación | Son las 'entradas' al proceso químico. | Son las 'salidas' o resultados del proceso químico. |
Preguntas Frecuentes (FAQ)
¿Por qué es tan importante balancear una ecuación química antes de hacer cálculos?
Balancear una ecuación química es crucial porque asegura que se cumpla la Ley de Conservación de la Masa. Sin una ecuación balanceada, las proporciones molares entre reactivos y productos serían incorrectas, lo que llevaría a cálculos estequiométricos erróneos y, en última instancia, a predicciones incorrectas sobre las cantidades de sustancias involucradas.
¿Qué es un mol y por qué se usa en estequiometría?
Un mol es una unidad fundamental en química que representa una cantidad específica de partículas (6.022 x 1023, el Número de Avogadro). Se utiliza en estequiometría porque las reacciones químicas ocurren a nivel atómico y molecular, y los coeficientes en una ecuación balanceada representan las proporciones de moles de las sustancias. El mol permite relacionar la masa (que podemos medir) con el número de partículas y las proporciones estequiométricas.
¿Pueden los reactivos y productos ser lo mismo?
No, por definición, los reactivos son las sustancias que se consumen para formar nuevas sustancias (los productos). Las identidades químicas de los productos son diferentes a las de los reactivos. Sin embargo, en reacciones reversibles que alcanzan el equilibrio, los productos de la reacción directa pueden actuar como reactivos para la reacción inversa, reformando las sustancias originales.
¿Cómo se manejan los gases en los cálculos estequiométricos?
Para los gases, los cálculos estequiométricos pueden involucrar volúmenes. A condiciones normales de temperatura y presión (0°C y 1 atm), un mol de cualquier gas ideal ocupa 22.4 litros (volumen molar). Si las condiciones no son estándar, se puede usar la Ley de los Gases Ideales (PV=nRT) para convertir el volumen a moles o viceversa.
¿Qué debo hacer si mis cantidades iniciales no están en moles?
Si las cantidades iniciales están en gramos, debes convertirlas a moles usando la masa molar de la sustancia (masa molar = gramos/mol). Si están en volumen y se trata de un líquido con una densidad conocida, puedes usar la densidad para convertir el volumen a masa, y luego la masa a moles. Para gases, como se mencionó, se usa el volumen molar o la Ley de los Gases Ideales.
¿La estequiometría siempre predice el resultado exacto en el laboratorio?
La estequiometría predice el rendimiento teórico, que es la cantidad máxima de producto que se podría obtener bajo condiciones ideales. En el laboratorio, el rendimiento real casi siempre es menor debido a factores como impurezas, reacciones secundarias, pérdidas durante la manipulación y purificación, o que la reacción no se completa al 100%. Por eso se calcula el porcentaje de rendimiento para evaluar la eficiencia de una reacción experimental.
Conclusión
La capacidad de calcular las cantidades de reactivos y productos en una reacción química es una habilidad fundamental en la química. A través de la estequiometría, y apoyándose en el balanceo de ecuaciones, el concepto de mol y la identificación del reactivo limitante, podemos predecir con precisión los resultados de las transformaciones químicas. Esta comprensión no solo es vital para el avance científico, sino que también tiene implicaciones prácticas profundas en industrias que van desde la farmacéutica hasta la energética, permitiéndonos diseñar procesos más eficientes, seguros y sostenibles. Dominar la estequiometría es, en esencia, dominar el lenguaje cuantitativo del cambio químico, una herramienta poderosa para cualquier explorador del mundo molecular.
Si quieres conocer otros artículos parecidos a Estequiometría: Cuantificando Reactivos y Productos puedes visitar la categoría Química.

