28/01/2026
En el vasto universo de la química, existen procesos fundamentales que rigen cómo los elementos interactúan entre sí. Entre ellos, las reacciones de oxidación y reducción, comúnmente conocidas como reacciones redox, son protagonistas silenciosos pero omnipresentes. Desde la corrosión de un metal hasta la respiración que nos mantiene vivos, estos fenómenos son clave para entender el mundo que nos rodea. Pero, ¿cómo podemos identificar cuándo un elemento se oxida o se reduce? ¿Y cómo logramos balancear estas complejas transformaciones? Acompáñenos en este viaje para desentrañar los misterios de la oxidación y la reducción, sus principios, métodos de cuantificación y su impacto en nuestra vida diaria.
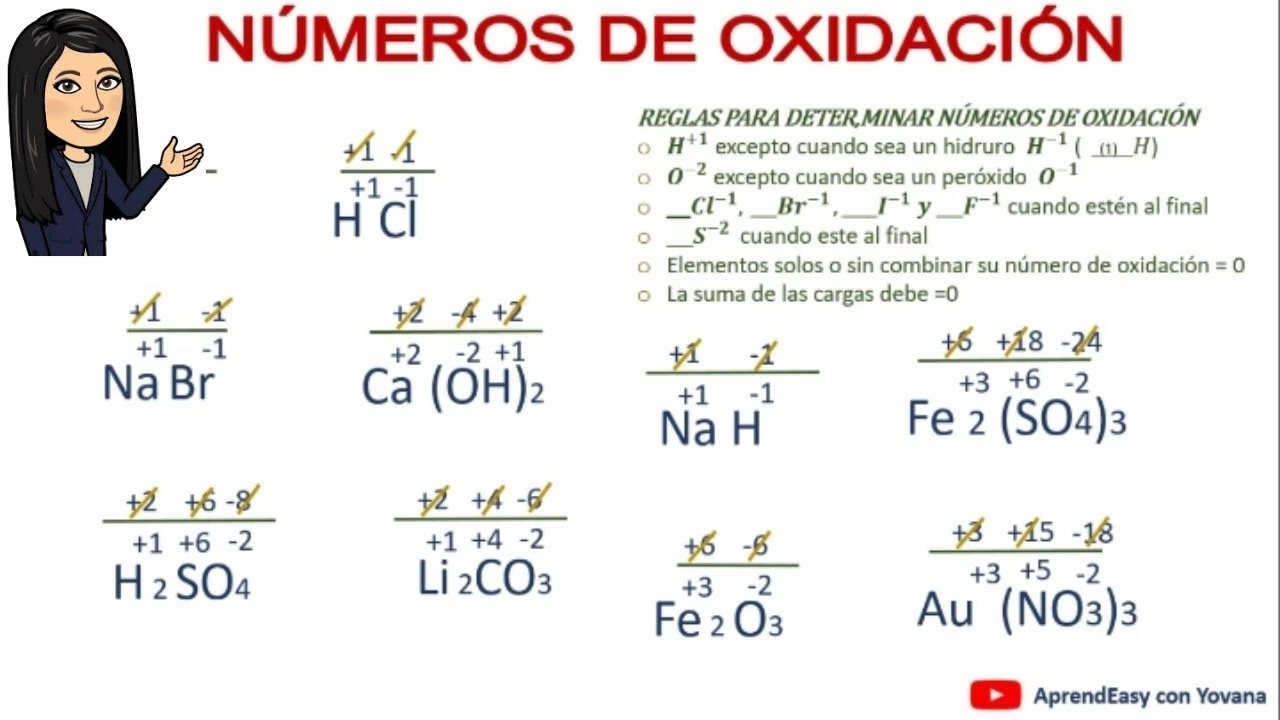
¿Qué son la Oxidación y la Reducción?
Las reacciones redox son procesos químicos en los que hay una transferencia de electrones entre dos especies químicas. Estos procesos siempre ocurren de forma simultánea: no puede haber oxidación sin reducción y viceversa. Son dos caras de la misma moneda.
Oxidación: Perder para Ganar
La oxidación es un proceso químico en el que una sustancia pierde electrones. Históricamente, se definía como la ganancia de oxígeno por parte de un elemento. Sin embargo, la definición moderna y más amplia se centra en la pérdida de electrones. Cuando un elemento se oxida, su número de oxidación (o estado de oxidación) aumenta. La especie que se oxida se conoce como agente reductor, porque al oxidarse a sí misma, causa la reducción de otra sustancia.
Reducción: Ganar para Disminuir
Por otro lado, la reducción es el proceso químico opuesto, donde una sustancia gana electrones. Tradicionalmente, se entendía como la pérdida de oxígeno. En la concepción actual, la reducción implica la ganancia de electrones, lo que resulta en una disminución del número de oxidación del elemento. La especie que se reduce se llama agente oxidante, ya que al reducirse a sí misma, provoca la oxidación de otra sustancia.
El Número de Oxidación: La Clave para Cuantificar
Para cuantificar y comprender los cambios que ocurren en una reacción redox, utilizamos el concepto de número de oxidación. Este es un número entero que representa el número de electrones que un átomo pone en juego cuando forma un enlace determinado, indicando el grado de oxidación de un átomo en un compuesto químico.
Reglas Fundamentales para Asignar el Número de Oxidación
Asignar correctamente el número de oxidación es fundamental para identificar qué se oxida y qué se reduce. Aquí están las reglas clave:
- Elementos sin combinar: El número de oxidación de cualquier elemento en su estado elemental (sin combinar con otros átomos) es siempre cero. Esto incluye moléculas diatómicas como O2, H2, N2, Cl2, o metales como Fe, Cu, Al.
- Iones monoatómicos: El número de oxidación de una especie iónica monoatómica (un solo átomo con carga) coincide con la carga del ion. Por ejemplo, en Na+ es +1, en Cl− es −1, y en Fe3+ es +3.
- Hidrógeno (H): En la mayoría de los compuestos, el hidrógeno tiene un número de oxidación de +1. La única excepción son los hidruros metálicos (compuestos de hidrógeno con metales más electropositivos), donde su número de oxidación es −1 (ej: AlH3, LiH).
- Oxígeno (O): Generalmente, el oxígeno tiene un número de oxidación de −2. Las excepciones notables son los peróxidos (como H2O2 o Na2O2), donde su número de oxidación es −1.
- Metales combinados: En los compuestos, los elementos metálicos siempre tienen un número de oxidación positivo, y su valor numérico es igual a la carga de su ion.
- Halógenos y Azufre: Los halógenos (F, Cl, Br, I) en hidrácidos (como HCl, HBr) y sus sales tienen un número de oxidación de −1. El azufre (S) en su hidrácido (H2S) y sus sales tiene un número de oxidación de −2.
- Moléculas neutras: La suma algebraica de los números de oxidación de todos los átomos en una molécula neutra es cero.
- Iones poliatómicos: La suma algebraica de los números de oxidación de todos los átomos que constituyen un ion poliatómico (no neutro) es igual a la carga total del ion. Por ejemplo, en MnO4−, si el oxígeno es −2, y hay 4 oxígenos (4 * −2 = −8), para que la carga total sea −1, el manganeso (Mn) debe tener un número de oxidación de +7 (+7 − 8 = −1).
Balanceando Ecuaciones Redox: Un Arte Preciso
El balanceo de ecuaciones redox es un paso crucial para asegurar que la cantidad de átomos y la carga eléctrica sean iguales en ambos lados de la ecuación. Esto se logra mediante el método del ion-electrón, que se adapta según el medio en el que ocurre la reacción (ácido o básico).
Ajuste en Medio Ácido: El Poder del Hidronio
En medio ácido, se utilizan iones hidrógeno (H+) y moléculas de agua (H2O) para balancear las semirreacciones. El proceso general es el siguiente:
- Separar en semirreacciones: Identificar las especies que se oxidan y las que se reducen, y escribir sus respectivas semirreacciones.
- Balancear átomos diferentes de O y H: Asegurar que la cantidad de cada elemento (excepto oxígeno e hidrógeno) sea la misma en ambos lados.
- Balancear oxígeno (O): Añadir moléculas de agua (H2O) al lado donde falte oxígeno.
- Balancear hidrógeno (H): Añadir iones H+ al lado donde falte hidrógeno.
- Balancear carga: Añadir electrones (e−) al lado con mayor carga positiva para igualar la carga neta en ambos lados de cada semirreacción.
- Igualar electrones: Multiplicar cada semirreacción por el coeficiente necesario para que el número de electrones transferidos sea el mismo en ambas.
- Sumar semirreacciones: Combinar las dos semirreacciones y simplificar cualquier especie que aparezca en ambos lados (H2O, H+, e−).
Ejemplo en Medio Ácido: Reacción entre Manganeso (II) y Bismutato de Sodio
Ecuación sin balancear: Mn2+(aq) + BiO3−(s) → Bi3+(aq) + MnO4−(aq)
1. Separar semirreacciones:
Oxidación: Mn2+(aq) → MnO4−(aq)
Reducción: BiO3−(s) → Bi3+(aq)
2. Balancear átomos (Mn y Bi ya están balanceados).
3. Balancear oxígeno con H2O:
Oxidación: 4 H2O + Mn2+(aq) → MnO4−(aq)
Reducción: BiO3−(s) → Bi3+(aq) + 3 H2O
4. Balancear hidrógeno con H+:
Oxidación: 4 H2O + Mn2+(aq) → MnO4−(aq) + 8 H+(aq)
Reducción: 6 H+(aq) + BiO3−(s) → Bi3+(aq) + 3 H2O
5. Balancear carga con electrones:
Oxidación: 4 H2O + Mn2+(aq) → MnO4−(aq) + 8 H+(aq) + 5 e− (Carga neta: +2 → +7 -5 = +2)
Reducción: 2 e− + 6 H+(aq) + BiO3−(s) → Bi3+(aq) + 3 H2O (Carga neta: −1 +6 -2 = +3 → +3)
6. Igualar electrones (mcm de 5 y 2 es 10):
Oxidación: (4 H2O + Mn2+(aq) → MnO4−(aq) + 8 H+(aq) + 5 e−) × 2
Reducción: (2 e− + 6 H+(aq) + BiO3−(s) → Bi3+(aq) + 3 H2O) × 5
Resulta en:
Oxidación: 8 H2O + 2 Mn2+(aq) → 2 MnO4−(aq) + 16 H+(aq) + 10 e−
Reducción: 10 e− + 30 H+(aq) + 5 BiO3−(s) → 5 Bi3+(aq) + 15 H2O
7. Sumar semirreacciones y simplificar:
8 H2O + 2 Mn2+(aq) + 10 e− + 30 H+(aq) + 5 BiO3−(s) → 2 MnO4−(aq) + 16 H+(aq) + 10 e− + 5 Bi3+(aq) + 15 H2O
Simplificando (restar 10 e−, 16 H+ y 8 H2O de ambos lados):
14 H+(aq) + 2 Mn2+(aq) + 5 BiO3−(s) → 7 H2O + 2 MnO4−(aq) + 5 Bi3+(aq)
Si consideramos que el BiO3− proviene de NaBiO3, y los iones Na+ son espectadores, la ecuación completa sería:
14 H+(aq) + 2 Mn2+(aq) + 5 NaBiO3(s) → 7 H2O + 2 MnO4−(aq) + 5 Bi3+(aq) + 5 Na+(aq)
Ajuste en Medio Básico: La Influencia del Hidróxido
En medio básico, se utilizan iones hidróxido (OH−) y moléculas de agua (H2O) para balancear las semirreacciones. El procedimiento es similar al medio ácido, con una pequeña variación en el balanceo de oxígeno e hidrógeno:
- Separar en semirreacciones.
- Balancear átomos diferentes de O y H.
- Balancear oxígeno (O): Añadir moléculas de agua (H2O) al lado donde falte oxígeno. Luego, añadir el doble de iones OH− en el lado opuesto para balancear el H de las moléculas de agua.
- Balancear hidrógeno (H): Si aún falta hidrógeno, añadir H2O al lado con menos H, y OH− al otro lado para balancear. (Una forma alternativa es balancear como en medio ácido y luego añadir OH− a ambos lados para neutralizar H+).
- Balancear carga con electrones.
- Igualar electrones.
- Sumar semirreacciones y simplificar.
Ejemplo en Medio Básico: Permanganato de Potasio y Sulfito de Sodio
Ecuación sin balancear: KMnO4 + Na2SO3 + H2O → MnO2 + Na2SO4 + KOH
1. Separar semirreacciones (ignorando iones espectadores K+ y Na+):
Oxidación: SO32− → SO42−
Reducción: MnO4− → MnO2
2. Balancear átomos (S y Mn ya están balanceados).
3. Balancear oxígeno con H2O y OH−:
Oxidación: SO32− + 2 OH− → SO42− + H2O (Se necesita 1 O en izquierda, se añade H2O a la derecha y 2 OH− a la izquierda)
Reducción: MnO4− + 2 H2O → MnO2 + 4 OH− (Se necesitan 2 O en derecha, se añaden 2 H2O a la izquierda y 4 OH− a la derecha)
4. Balancear hidrógeno (ya balanceado por el paso anterior).
5. Balancear carga con electrones:
Oxidación: SO32− + 2 OH− → SO42− + H2O + 2 e− (Carga neta: −2 −2 = −4 → −2 −2 = −4)
Reducción: MnO4− + 2 H2O + 3 e− → MnO2 + 4 OH− (Carga neta: −1 −3 = −4 → −4)
6. Igualar electrones (mcm de 2 y 3 es 6):
Oxidación: (SO32− + 2 OH− → SO42− + H2O + 2 e−) × 3
Reducción: (MnO4− + 2 H2O + 3 e− → MnO2 + 4 OH−) × 2
Resulta en:
Oxidación: 3 SO32− + 6 OH− → 3 SO42− + 3 H2O + 6 e−
Reducción: 2 MnO4− + 4 H2O + 6 e− → 2 MnO2 + 8 OH−
7. Sumar semirreacciones y simplificar:
3 SO32− + 6 OH− + 2 MnO4− + 4 H2O + 6 e− → 3 SO42− + 3 H2O + 6 e− + 2 MnO2 + 8 OH−
Simplificando (restar 6 e−, 6 OH− y 3 H2O de ambos lados):
3 SO32− + 2 MnO4− + H2O → 3 SO42− + 2 MnO2 + 2 OH−
Reincorporando los iones espectadores para la ecuación molecular original:
2 KMnO4 + 3 Na2SO3 + H2O → 2 MnO2 + 3 Na2SO4 + 2 KOH
Aplicaciones Cotidianas e Industriales de las Reacciones Redox
Las reacciones redox no son solo un concepto de laboratorio; tienen una vasta gama de aplicaciones en la industria, la biología y nuestra vida diaria.
La Corrosión: El Lado Oscuro de la Oxidación
Una de las consecuencias más visibles de la oxidación es la corrosión, un fenómeno electroquímico en el que los metales se degradan al reaccionar con su entorno, generalmente oxígeno y agua. La formación de óxido en el hierro es un ejemplo clásico de oxidación, que genera un impacto estructural muy negativo en infraestructuras y materiales. Comprender los procesos redox es crucial para desarrollar métodos de prevención, como el recubrimiento de metales o el uso de ánodos de sacrificio.
Las Pilas Electroquímicas: Energía a Través de Redox
Las baterías y pilas que usamos a diario son dispositivos que aprovechan las reacciones redox para generar corriente eléctrica continua. En una celda galvánica, la transferencia espontánea de electrones de una sustancia que se oxida a otra que se reduce se canaliza a través de un circuito externo, produciendo energía eléctrica. La reacción inversa, la electrólisis, utiliza energía eléctrica para forzar una reacción redox no espontánea, como la obtención de aluminio a partir de su mineral.

El Metabolismo: La Química de la Vida
En el corazón de todos los seres vivos, los procesos redox son de una importancia capital. Son la base de la fotosíntesis en plantas y algas, donde la energía solar se utiliza para reducir el dióxido de carbono en azúcares, y de la respiración aeróbica en animales y muchos otros organismos, donde los azúcares se oxidan para liberar energía en forma de ATP. En estas reacciones, una cadena transportadora de electrones, compuesta por complejos enzimáticos como los citocromos, acepta (se reduce) y cede (se oxida) pares de electrones de manera secuencial. Durante este viaje, los electrones liberan energía que se aprovecha para sintetizar enlaces de alta energía.
Otro tipo de reacción redox fundamental en el metabolismo son las deshidrogenaciones. Aquí, enzimas llamadas deshidrogenasas eliminan pares de átomos de hidrógeno (un protón y un electrón) de un sustrato, oxidándolo. Estos electrones son captados por coenzimas especializadas como NAD+, NADP+ y FAD, que se reducen y transportan los electrones a las cadenas transportadoras. El catabolismo (procesos de degradación) implica la oxidación de sustratos y la reducción de coenzimas, mientras que el anabolismo (procesos de síntesis) implica la reducción de sustratos y la oxidación de coenzimas. En conjunto, catabolismo y anabolismo forman el metabolismo, un intrincado ballet de reacciones redox.
La Combustión: Energía y Transformación
La combustión es un ejemplo cotidiano y potente de una reacción de oxidación rápida y exotérmica. Cuando quemamos madera, gas natural o cualquier combustible, estos reaccionan con el oxígeno del aire, liberando una gran cantidad de energía en forma de calor y luz. Esencialmente, el combustible se oxida mientras el oxígeno se reduce, produciendo óxidos como dióxido de carbono y agua.
Tabla Comparativa: Oxidación vs. Reducción
Para resumir las diferencias clave, observemos la siguiente tabla:
| Característica | Oxidación | Reducción |
|---|---|---|
| Definición Básica | Pérdida de electrones | Ganancia de electrones |
| Oxígeno (histórico) | Ganancia de oxígeno | Pérdida de oxígeno |
| Número de Oxidación | Aumenta | Disminuye |
| Rol en la Reacción | Se oxida (es el agente reductor) | Se reduce (es el agente oxidante) |
| Ejemplo Visual | Metal oxidándose (corrosión) | Mineral convirtiéndose en metal puro |
Preguntas Frecuentes sobre Reacciones Redox
¿Por qué la oxidación y la reducción siempre ocurren juntas?
Porque los electrones no pueden simplemente desaparecer o aparecer de la nada. Si una sustancia pierde electrones (se oxida), otra sustancia debe ganar esos mismos electrones (se reduce). Es una transferencia, no una creación o destrucción de electrones.
¿Qué es un agente oxidante y un agente reductor?
Un agente oxidante es la sustancia que provoca la oxidación de otra. Para hacerlo, ella misma debe ganar electrones, es decir, se reduce. Un agente reductor es la sustancia que provoca la reducción de otra. Para hacerlo, ella misma debe perder electrones, es decir, se oxida. Son términos recíprocos.
¿Cómo se aplica esto en la vida cotidiana?
Las reacciones redox están presentes en muchos aspectos de nuestra vida: desde la digestión de alimentos (donde las moléculas se oxidan para liberar energía) y la respiración, hasta el blanqueado de ropa con lejía (un agente oxidante), la desinfección con cloro, la fotografía (reacciones de oxidación y reducción en los químicos fotográficos) y la purificación de metales.
¿Es la corrosión siempre mala?
Aunque la corrosión suele ser vista como un proceso perjudicial que degrada materiales, en algunos casos puede ser beneficiosa o controlada. Por ejemplo, en el aluminio, la oxidación forma una capa delgada y protectora de óxido de aluminio que previene una mayor corrosión. Este proceso se llama pasivación y es deseable.
Si quieres conocer otros artículos parecidos a Oxidación y Reducción: Guía Completa de Reacciones Redox puedes visitar la categoría Química.
