12/01/2026
En el vasto y fascinante mundo de la química, la concentración de una solución es un parámetro fundamental que define la cantidad de soluto presente en una determinada cantidad de disolvente o de solución. Comprender y calcular estas concentraciones es crucial para experimentos de laboratorio, procesos industriales y la vida cotidiana. Sin embargo, no todas las concentraciones se expresan de la misma manera. Mientras que algunas se presentan como porcentajes (masa/volumen, masa/masa, o volumen/volumen), otras, especialmente en química analítica y de reacciones, requieren la expresión en molaridad. La transición de una unidad a otra puede parecer un desafío, pero con una guía clara y estructurada, es un cálculo perfectamente abordable. Este artículo tiene como objetivo desmitificar el proceso de cómo calcular la molaridad de una solución cuando se parte de una concentración expresada en porcentaje masa/volumen (m/v), proporcionando las herramientas y el conocimiento necesarios para que domines este importante concepto.
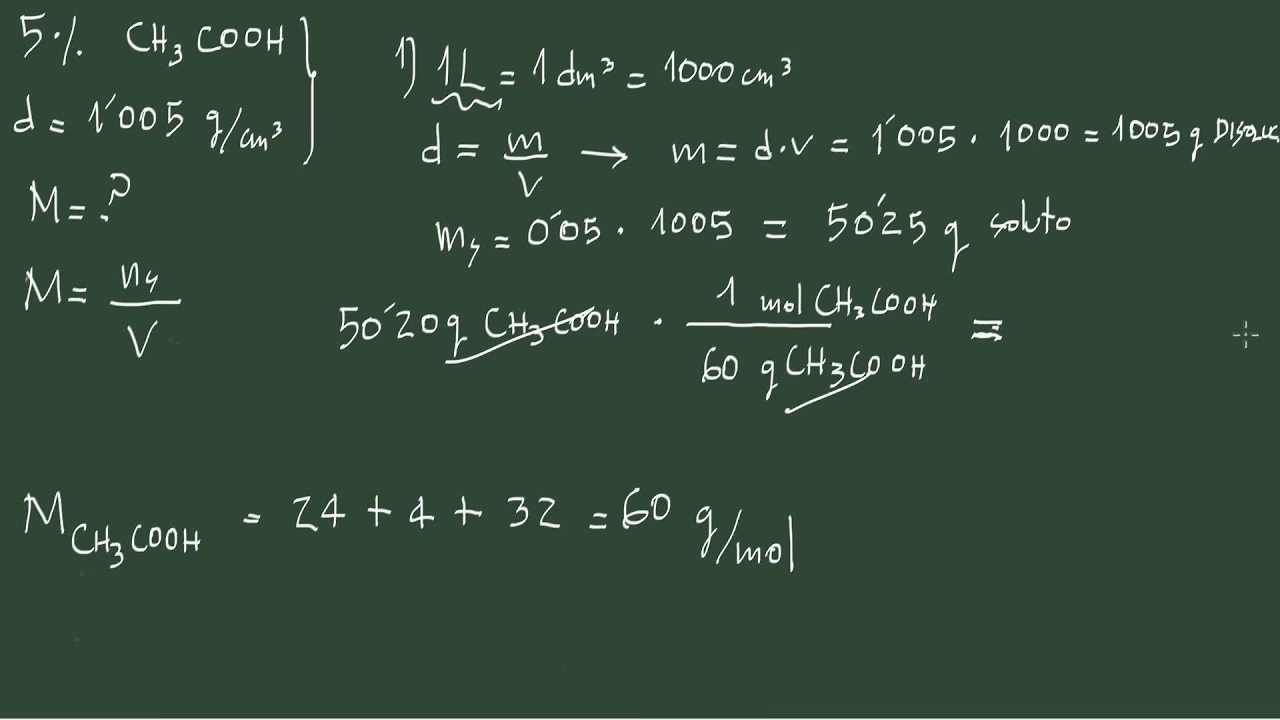
La capacidad de convertir entre diferentes unidades de concentración no solo demuestra un entendimiento profundo de la química de las soluciones, sino que también es una habilidad práctica invaluable. A menudo, las etiquetas de los reactivos químicos o las especificaciones de los productos comerciales se presentan en porcentajes, mientras que las ecuaciones químicas y los cálculos estequiométricos requieren la molaridad. Por ello, dominar esta conversión es un paso esencial para cualquier estudiante o profesional que trabaje con soluciones químicas.
- Entendiendo las Unidades de Concentración: Porcentaje (m/v) vs. Molaridad
- Guía Paso a Paso: Calculando Molaridad a partir de Porcentaje (m/v)
- Fórmula Consolidada y Un Atajo Útil para % m/v
- Ejemplos Prácticos
- Consideraciones Importantes y Errores Comunes
- Tabla Comparativa de Unidades de Concentración
- Preguntas Frecuentes (FAQ)
- ¿Qué es la masa molar y cómo se calcula?
- ¿Cuál es la diferencia principal entre porcentaje masa/volumen y porcentaje masa/masa?
- ¿Por qué es importante el volumen de la solución y no solo del solvente para la molaridad?
- ¿Se ve afectada la molaridad por la temperatura?
- ¿Es el atajo (Porcentaje * 10) / Masa Molar siempre válido?
Entendiendo las Unidades de Concentración: Porcentaje (m/v) vs. Molaridad
Antes de sumergirnos en los cálculos, es vital comprender qué representa cada unidad de concentración y por qué son diferentes. Esta comprensión es la base para una conversión exitosa y sin errores.
¿Qué es el Porcentaje Masa/Volumen (% m/v)?
El porcentaje masa/volumen, abreviado como % m/v, es una unidad de concentración que expresa la masa de soluto (en gramos) disuelta en 100 mililitros (mL) de solución. Es una forma sencilla y común de expresar la concentración, especialmente en campos como la farmacia o la medicina, donde las dosis suelen estar relacionadas con volúmenes específicos. Por ejemplo, una solución de suero fisiológico al 0.9% m/v significa que hay 0.9 gramos de cloruro de sodio (NaCl) en cada 100 mL de solución.
¿Qué es la Molaridad (M)?
La molaridad, representada por la letra 'M', es quizás la unidad de concentración más utilizada en química. Se define como el número de moles de soluto disueltos por cada litro de solución. Su fórmula es:
Molaridad (M) = moles de soluto / litros de solución
La molaridad es particularmente útil porque relaciona directamente la cantidad de sustancia (moles) con el volumen de la solución, lo que facilita los cálculos estequiométricos en reacciones químicas. Una solución 1 M de ácido clorhídrico (HCl) contiene 1 mol de HCl en cada litro de solución.
La principal diferencia, y la razón por la que necesitamos una conversión, radica en que el porcentaje m/v usa gramos y mililitros, mientras que la molaridad usa moles y litros. Para pasar de gramos a moles, necesitamos la masa molar del soluto, y para pasar de mililitros a litros, una simple conversión de unidades de volumen.
Guía Paso a Paso: Calculando Molaridad a partir de Porcentaje (m/v)
El proceso para convertir una concentración de porcentaje masa/volumen a molaridad implica una serie de pasos lógicos y secuenciales. Aquí te los presentamos detalladamente:
Paso 1: Interpretar el Porcentaje Masa/Volumen (% m/v)
El primer paso es entender exactamente qué significa el porcentaje que se te ha dado. Si tienes una solución al X% m/v, esto implica que hay X gramos de soluto por cada 100 mililitros (mL) de solución. Este es tu punto de partida para determinar la masa de soluto en un volumen conocido. Es crucial recordar que la base es siempre 100 mL para este tipo de porcentaje. Si, por ejemplo, te dicen que tienes una solución de glucosa al 5% m/v, esto significa que hay 5 gramos de glucosa disueltos en 100 mL de la solución total. Esta interpretación inicial es la clave para desglosar el problema.
Paso 2: Determinar la Masa del Soluto en un Volumen Conveniente
Aunque el porcentaje se basa en 100 mL, para calcular la molaridad, es más práctico pensar en un volumen de 1 litro (1000 mL) de solución, ya que la molaridad se define por litro. Si una solución contiene X gramos de soluto por cada 100 mL, entonces en 1000 mL (que es 10 veces 100 mL), habrá 10 veces la cantidad de soluto. Por lo tanto, la masa de soluto en 1 litro de solución será: Masa de soluto (g) = Porcentaje (X) * 10. Por ejemplo, si tienes una solución al 5% m/v, en 1 litro de solución tendrás 5 g/100 mL * (1000 mL / 1 L) = 50 gramos de soluto por litro.
Paso 3: Calcular la Masa Molar del Soluto
La masa molar (o peso molecular) es la masa de un mol de una sustancia y se expresa en gramos por mol (g/mol). Para calcularla, necesitas la fórmula química del soluto y las masas atómicas de cada elemento que lo compone, las cuales se encuentran en la tabla periódica. Suma las masas atómicas de todos los átomos presentes en la fórmula. Por ejemplo, si tu soluto es NaCl (cloruro de sodio):
- Masa atómica de Na (Sodio) ≈ 22.99 g/mol
- Masa atómica de Cl (Cloro) ≈ 35.45 g/mol
- Masa molar de NaCl = 22.99 + 35.45 = 58.44 g/mol
Este valor es fundamental para convertir la masa del soluto (obtenida en el Paso 2) a moles.
Paso 4: Convertir la Masa del Soluto a Moles
Una vez que tienes la masa del soluto (en gramos) y su masa molar (en g/mol), puedes calcular el número de moles de soluto utilizando la siguiente fórmula:
Moles de soluto = Masa del soluto (g) / Masa molar del soluto (g/mol)
Este paso te proporciona la cantidad de sustancia en términos de moles, que es el numerador en la definición de molaridad.
Paso 5: Ajustar el Volumen de la Solución a Litros
La molaridad se define como moles de soluto por litro de solución. Si en el Paso 2 asumiste un volumen de 100 mL, o si el problema te dio un volumen en mililitros, debes convertirlo a litros. Recuerda que 1 litro (L) equivale a 1000 mililitros (mL).
Volumen de solución (L) = Volumen de solución (mL) / 1000
Si, como se sugirió en el Paso 2, ya trabajaste con 1 litro de solución, este paso ya está cubierto, y tu volumen para la molaridad será simplemente 1 L.
Paso 6: Calcular la Molaridad Final
Con el número de moles de soluto (del Paso 4) y el volumen de la solución en litros (del Paso 5), ya tienes todos los componentes para calcular la molaridad:
Molaridad (M) = Moles de soluto / Volumen de solución (L)
Este es el resultado final de tu conversión de porcentaje a molaridad.
Fórmula Consolidada y Un Atajo Útil para % m/v
Aunque los pasos individuales son importantes para la comprensión, es posible consolidarlos en una única expresión. Si el porcentaje es m/v (gramos de soluto por 100 mL de solución) y queremos la molaridad (moles de soluto por litro de solución), podemos usar un atajo muy práctico:
Molaridad (M) = (Porcentaje % m/v * 10) / Masa Molar del Soluto (g/mol)
Este atajo funciona porque multiplicar el porcentaje por 10 convierte los gramos por 100 mL en gramos por 1000 mL (es decir, gramos por litro), y luego dividir por la masa molar transforma esos gramos por litro en moles por litro. Este es un método rápido una vez que se comprende la lógica subyacente de los pasos individuales.
Ejemplos Prácticos
Ejemplo 1: Calcular la molaridad de una solución de NaCl al 0.9% (m/v)
Este es el ejemplo del suero fisiológico, muy común.
Datos:
- Concentración: 0.9% m/v de NaCl
- Soluto: NaCl (Cloruro de Sodio)
Pasos:
- Interpretar el porcentaje: 0.9% m/v significa 0.9 gramos de NaCl por cada 100 mL de solución.
- Masa de soluto en 1 L: En 1 litro (1000 mL) de solución, tendremos 0.9 g/100 mL * 10 = 9 gramos de NaCl.
- Calcular la masa molar de NaCl:
- Na: 22.99 g/mol
- Cl: 35.45 g/mol
- Masa molar de NaCl = 22.99 + 35.45 = 58.44 g/mol
- Convertir masa a moles:
- Moles de NaCl = 9 g / 58.44 g/mol = 0.1540 moles
- Volumen en litros: Ya trabajamos con 1 L de solución.
- Calcular la molaridad:
- Molaridad = 0.1540 moles / 1 L = 0.1540 M
Resultado: Una solución de NaCl al 0.9% (m/v) tiene una molaridad de aproximadamente 0.154 M.
Ejemplo 2: Calcular la molaridad de una solución de H₂SO₄ al 20% (m/v)
Datos:
- Concentración: 20% m/v de H₂SO₄
- Soluto: H₂SO₄ (Ácido Sulfúrico)
Pasos:
- Interpretar el porcentaje: 20% m/v significa 20 gramos de H₂SO₄ por cada 100 mL de solución.
- Masa de soluto en 1 L: En 1 litro (1000 mL) de solución, tendremos 20 g/100 mL * 10 = 200 gramos de H₂SO₄.
- Calcular la masa molar de H₂SO₄:
- H: 1.008 g/mol (x2) = 2.016 g/mol
- S: 32.07 g/mol (x1) = 32.07 g/mol
- O: 16.00 g/mol (x4) = 64.00 g/mol
- Masa molar de H₂SO₄ = 2.016 + 32.07 + 64.00 = 98.086 g/mol
- Convertir masa a moles:
- Moles de H₂SO₄ = 200 g / 98.086 g/mol = 2.039 moles
- Volumen en litros: Ya trabajamos con 1 L de solución.
- Calcular la molaridad:
- Molaridad = 2.039 moles / 1 L = 2.039 M
Resultado: Una solución de H₂SO₄ al 20% (m/v) tiene una molaridad de aproximadamente 2.039 M.
Consideraciones Importantes y Errores Comunes
Aunque el cálculo es directo, hay varios puntos importantes a tener en cuenta para evitar errores y asegurar la precisión:
- Tipo de Porcentaje: Siempre verifica si el porcentaje es masa/volumen (m/v), masa/masa (m/m) o volumen/volumen (v/v). El método descrito aquí es específicamente para % m/v. Si tienes % m/m, necesitarás la densidad de la solución para convertir la masa de la solución a volumen. Si es % v/v, necesitarás la densidad del soluto y la masa molar para convertir el volumen del soluto a moles.
- Unidades Consistentes: Asegúrate de que todas tus unidades sean consistentes. La masa del soluto debe estar en gramos, la masa molar en g/mol, y el volumen de la solución en litros. Un error común es olvidar convertir mililitros a litros.
- Masa Molar Correcta: Un error en el cálculo de la masa molar del soluto afectará directamente el resultado final de la molaridad. Revisa cuidadosamente la fórmula química y las masas atómicas.
- Volumen de la Solución vs. Volumen del Disolvente: La molaridad se basa en el volumen total de la solución (soluto + disolvente), no solo en el volumen del disolvente. Esto es importante, ya que el volumen de la solución puede no ser simplemente la suma del volumen del soluto y el volumen del disolvente, especialmente en soluciones concentradas.
- Temperatura: La molaridad es sensible a los cambios de temperatura porque el volumen de la solución puede expandirse o contraerse con la temperatura. Si la temperatura de la solución cambia significativamente, su volumen cambiará, y por lo tanto, su molaridad.
Tabla Comparativa de Unidades de Concentración
Para contextualizar la molaridad y el porcentaje m/v, es útil compararlos con otras unidades de concentración comunes. Cada una tiene sus ventajas y aplicaciones específicas.
| Unidad de Concentración | Definición | Uso Principal | Ventajas | Desventajas |
|---|---|---|---|---|
| Molaridad (M) | Moles de soluto por litro de solución | Química analítica, estequiometría, reacciones | Relaciona directamente con moles (cantidad de sustancia), útil para reacciones | Depende de la temperatura (el volumen cambia) |
| Porcentaje Masa/Volumen (% m/v) | Gramos de soluto por 100 mL de solución | Farmacia, medicina, concentraciones rápidas | Fácil de preparar y entender en laboratorio, útil para líquidos | No relaciona directamente con moles, depende de la temperatura |
| Porcentaje Masa/Masa (% m/m) | Gramos de soluto por 100 gramos de solución | Industria alimentaria, química, preparaciones en masa | Independiente de la temperatura, fácil de medir por peso | No relaciona directamente con volumen ni moles, requiere densidad para volumen |
| Porcentaje Volumen/Volumen (% v/v) | Mililitros de soluto por 100 mL de solución | Alcoholes, mezclas de líquidos | Fácil de preparar con líquidos, útil para mezclas simples | No relaciona con moles, suma de volúmenes no siempre aditiva, depende de temperatura |
| Partes Por Millón (ppm) | Miligramos de soluto por litro de solución (o gramos de soluto por millón de gramos de solución) | Contaminación ambiental, trazas de sustancias | Útil para concentraciones muy bajas | No relaciona con moles, puede ser ambiguo (m/m, m/v, v/v) |
Preguntas Frecuentes (FAQ)
¿Qué es la masa molar y cómo se calcula?
La masa molar es la masa de un mol de cualquier sustancia (átomo, molécula, ion) expresada en gramos por mol (g/mol). Se calcula sumando las masas atómicas de todos los átomos presentes en la fórmula química de la sustancia. Por ejemplo, para el agua (H₂O), se suman dos veces la masa atómica del hidrógeno (H) y una vez la masa atómica del oxígeno (O).
¿Cuál es la diferencia principal entre porcentaje masa/volumen y porcentaje masa/masa?
La diferencia clave radica en el denominador. El porcentaje masa/volumen (% m/v) se refiere a la masa de soluto por cada 100 mL de solución, mientras que el porcentaje masa/masa (% m/m) se refiere a la masa de soluto por cada 100 gramos de solución. Para convertir de % m/m a molaridad, generalmente se necesita la densidad de la solución para transformar la masa de la solución en un volumen.
¿Por qué es importante el volumen de la solución y no solo del solvente para la molaridad?
La molaridad, por definición, es una medida de la concentración de soluto en el volumen total de la solución. El volumen del soluto contribuye al volumen total, y en muchos casos, el volumen final de la solución no es simplemente la suma del volumen del soluto y el volumen del disolvente debido a interacciones intermoleculares. Por lo tanto, para una medida precisa de la concentración molar, siempre se debe considerar el volumen total de la solución.
¿Se ve afectada la molaridad por la temperatura?
Sí, la molaridad se ve afectada por la temperatura. Esto se debe a que el volumen de la solución puede expandirse o contraerse ligeramente con los cambios de temperatura. Dado que la molaridad se define como moles de soluto por volumen de solución, una variación en el volumen (por cambio de temperatura) resultará en una variación en la molaridad. Por esta razón, en aplicaciones de alta precisión, a menudo se especifica la temperatura a la que se mide la molaridad.
¿Es el atajo (Porcentaje * 10) / Masa Molar siempre válido?
El atajo Molaridad (M) = (Porcentaje % m/v * 10) / Masa Molar del Soluto (g/mol) es válido y muy útil SIEMPRE Y CUANDO el porcentaje se exprese en masa/volumen (gramos de soluto por 100 mL de solución). Si el porcentaje es masa/masa o volumen/volumen, este atajo no es aplicable directamente y requerirá pasos adicionales, como el uso de la densidad.
Dominar la conversión entre diferentes unidades de concentración es una habilidad fundamental en química. Al seguir los pasos detallados en este artículo, o al aplicar el atajo cuando sea apropiado, puedes transformar de manera eficiente una concentración porcentual de masa/volumen a molaridad. Recuerda siempre verificar tus unidades, calcular correctamente la masa molar del soluto y considerar el volumen total de la solución. Con práctica, estos cálculos se convertirán en una segunda naturaleza, abriendo la puerta a un entendimiento más profundo de las reacciones químicas y la composición de las soluciones. ¡Continúa practicando y explorando el fascinante mundo de la química!
Si quieres conocer otros artículos parecidos a Dominando la Molaridad: De Porcentaje a Concentración Molar puedes visitar la categoría Química.

