29/08/2024
La comprensión de la velocidad de las reacciones químicas es fundamental en diversas disciplinas científicas, desde la química y la biología hasta la ingeniería. Una herramienta esencial para desentrañar los misterios de la cinética química es la ecuación de Arrhenius, propuesta por Svante Arrhenius en 1889. Esta ecuación no solo nos permite relacionar la constante de velocidad de una reacción con la temperatura, sino que también nos introduce a dos parámetros cruciales: la energía de activación y el factor preexponencial. Este último, a menudo denotado como 'A', es una pieza clave para entender la frecuencia y la orientación de las colisiones moleculares que conducen a una reacción. Aunque su cálculo directo puede parecer complejo, la genialidad de la gráfica de Arrhenius radica en ofrecer una metodología visual y sencilla para determinar este importante factor. En este artículo, exploraremos en detalle cómo la manipulación de la ecuación de Arrhenius y la construcción de su gráfica asociada nos permiten desvelar el valor del factor preexponencial, proporcionando una visión profunda de la dinámica molecular de las reacciones.

- La Ecuación de Arrhenius: Una Mirada Profunda
- Linealizando la Ecuación de Arrhenius para el Trazado
- Construcción de la Gráfica de Arrhenius
- Cómo Calcular el Factor Preexponencial (A) desde la Gráfica
- Unidades del Factor Preexponencial (A)
- Significado Físico y Teórico del Factor Preexponencial
- Variaciones de la Ecuación de Arrhenius
- Consideraciones Importantes y Limitaciones
- Componentes Clave de la Gráfica de Arrhenius
- Preguntas Frecuentes sobre el Factor Preexponencial
- Conclusión
La Ecuación de Arrhenius: Una Mirada Profunda
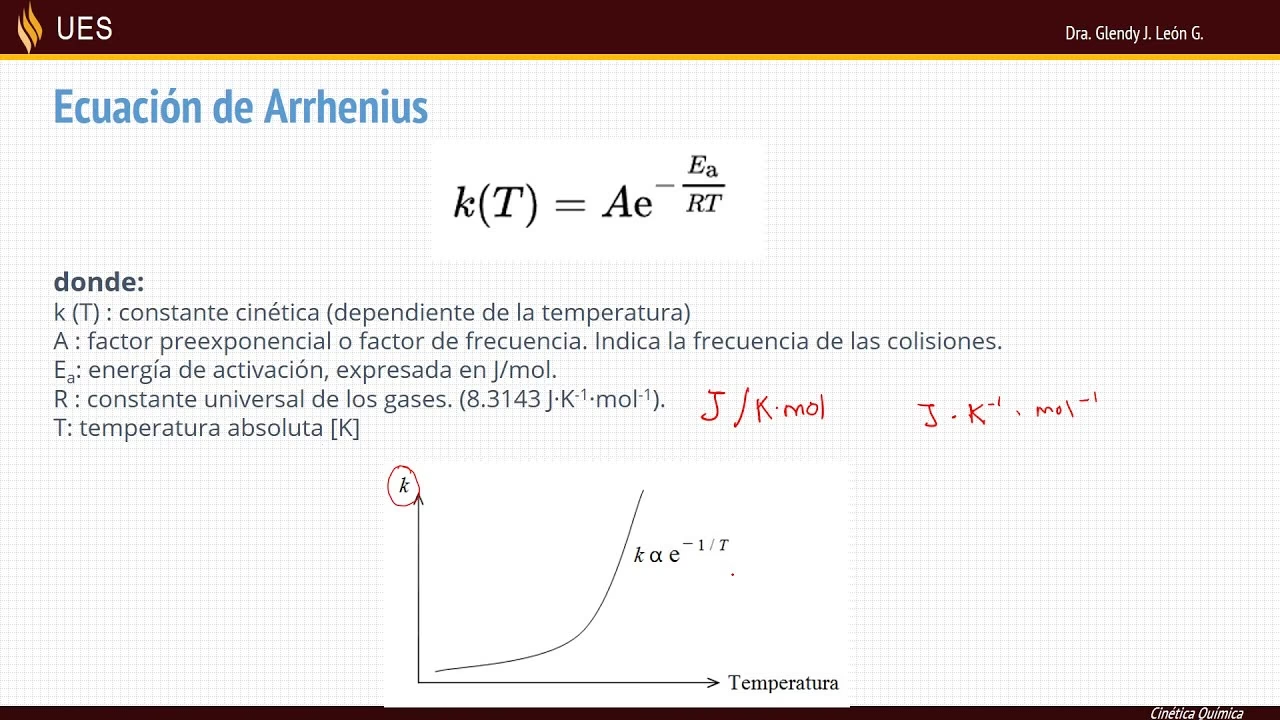
En 1889, Svante Arrhenius propuso una relación empírica que describe la dependencia de la constante de velocidad de una reacción (k) con la temperatura (T). Esta ecuación, conocida como la ecuación de Arrhenius, se expresa de la siguiente forma:
k = Ae-Ea/RT
Donde:
kes la constante de velocidad de la reacción.Aes el factor preexponencial, también conocido como factor de frecuencia o factor de Arrhenius.Eaes la energía de activación, la energía mínima que deben poseer las moléculas para reaccionar y formar productos.Res la constante de los gases ideales (8.314 J·mol-1·K-1).Tes la temperatura absoluta en Kelvin.
El factor preexponencial, A, es de gran significado. Según la teoría de colisiones, A puede interpretarse como el producto de un factor estérico (p) y la frecuencia de colisión (Z). El factor estérico (p) representa la probabilidad de que las moléculas colisionen con la orientación adecuada para que la reacción ocurra. La frecuencia de colisión (Z) se refiere al número total de colisiones entre las moléculas reaccionantes por unidad de tiempo. Por lo tanto, A está directamente relacionado con la cantidad de veces que las moléculas colisionarán con la orientación necesaria para que se produzca una reacción efectiva. Es importante destacar que la ecuación de Arrhenius se fundamenta en la teoría de colisiones, la cual postula que las partículas deben colisionar con la orientación y energía suficientes para reaccionar.
Linealizando la Ecuación de Arrhenius para el Trazado
La ecuación de Arrhenius en su forma original es exponencial, lo que dificulta su representación gráfica para la determinación de los parámetros A y Ea. Sin embargo, puede ser linealizada tomando el logaritmo natural (ln) en ambos lados de la ecuación:
ln k = ln(Ae-Ea/RT)
Aplicando las propiedades de los logaritmos (ln(xy) = ln x + ln y y ln(ex) = x), obtenemos:
ln k = ln A + ln(e-Ea/RT)
ln k = ln A - (Ea/RT)
Reorganizando los términos para que se asemeje a la ecuación de una línea recta (y = mx + b):
ln k = (-Ea/R)(1/T) + ln A
En esta forma linealizada, podemos identificar claramente los componentes de una línea recta:
y = ln k(el valor que se graficará en el eje Y)m = -Ea/R(la pendiente de la línea)x = 1/T(el valor que se graficará en el eje X)b = ln A(la intersección en el eje Y)
Esta transformación es crucial porque nos permite utilizar un método gráfico sencillo para determinar tanto la energía de activación como el factor preexponencial a partir de datos experimentales de constantes de velocidad a diferentes temperaturas.
Construcción de la Gráfica de Arrhenius
Una vez que hemos linealizado la ecuación de Arrhenius, el siguiente paso es construir la gráfica de Arrhenius. Para ello, se requiere tener datos experimentales de la constante de velocidad (k) a varias temperaturas (T). Los pasos son los siguientes:
- Recopilar datos: Obtenga pares de datos (k, T) de su experimento.
- Convertir temperaturas: Asegúrese de que todas las temperaturas estén en Kelvin (K). Si tiene temperaturas en grados Celsius, sume 273.15 a cada valor.
- Calcular inversos de temperatura: Calcule
1/Tpara cada temperatura en Kelvin. - Calcular logaritmos naturales de k: Calcule
ln kpara cada constante de velocidad. - Graficar: Trace
ln ken el eje Y contra1/Ten el eje X.
La gráfica resultante será una línea recta con una pendiente negativa. Esta línea es increíblemente útil para desentrañar los componentes desconocidos de la ecuación de Arrhenius.
Cómo Calcular el Factor Preexponencial (A) desde la Gráfica
Aquí es donde la gráfica de Arrhenius revela su poder para determinar el factor preexponencial. Como se mencionó en la sección de linealización, la ecuación de la línea recta es ln k = (-Ea/R)(1/T) + ln A. La intersección en el eje Y (el punto donde la línea cruza el eje Y, es decir, cuando 1/T = 0) corresponde a ln A.
Para calcular el factor preexponencial (A) a partir de la gráfica, siga estos pasos:
- Extrapolar la línea: Una vez que haya trazado sus puntos y ajustado una línea recta (usando regresión lineal si es posible, lo que es lo ideal para mayor precisión), extienda esta línea hasta que intercepte el eje Y (donde 1/T es cero).
- Leer el valor de la intersección en Y: El valor en el eje Y en el punto de intersección es
ln A. - Calcular A: Para obtener A, debe tomar el antilogaritmo natural (exponencial) de este valor. Es decir,
A = e(valor de la intersección en Y).
Por ejemplo, si la intersección en el eje Y de su gráfica de Arrhenius es 25, entonces:
ln A = 25
A = e25
A ≈ 7.2 x 1010
Este método gráfico es una forma práctica y visual de obtener el factor preexponencial y la energía de activación (que se obtiene de la pendiente, -Ea/R).
Unidades del Factor Preexponencial (A)
Las unidades del factor preexponencial (A) son idénticas a las de la constante de velocidad (k), y por lo tanto, varían según el orden de la reacción. Es crucial que las unidades en el exponente de la ecuación de Arrhenius (-Ea/RT) se cancelen para que el término exponencial sea adimensional. Esto asegura que A tenga las mismas unidades que k.
- Para una reacción de primer orden: Las unidades de k son s-1 (o min-1, etc.). Por lo tanto, A también tendrá unidades de s-1. Por esta razón, A a menudo se denomina factor de frecuencia.
- Para una reacción de segundo orden: Las unidades de k son L·mol-1·s-1 (o M-1·s-1). En este caso, A también tendrá estas unidades.
- Para una reacción de orden cero: Las unidades de k son mol·L-1·s-1. A tendrá las mismas unidades.
Es importante no confundir las unidades de A con las de Ea o RT. Ea se expresa típicamente en Joules por mol (J/mol) o kilojoules por mol (kJ/mol), y RT también tiene unidades de energía por mol (J/mol). La cancelación de unidades dentro del exponente es lo que permite que A adquiera las unidades de la constante de velocidad.
Significado Físico y Teórico del Factor Preexponencial
El factor preexponencial, A, ofrece una visión más profunda sobre la naturaleza microscópica de las reacciones. Su significado se interpreta principalmente a través de dos teorías:
Teoría de Colisiones
Según la teoría de colisiones, el factor preexponencial (A) está directamente relacionado con la frecuencia con la que las moléculas reaccionantes colisionan y la probabilidad de que estas colisiones sean efectivas. Se expresa como:
A = pZ
pes el factor estérico (o factor de probabilidad), que representa la fracción de colisiones que tienen la orientación molecular adecuada para que la reacción ocurra. Su valor suele ser menor o igual a 1.Zes la frecuencia de colisión, que es el número de colisiones por unidad de tiempo y volumen cuando las concentraciones de los reactivos son unitarias (por ejemplo, 1 M).
Un valor alto de A sugiere que las moléculas colisionan con mucha frecuencia y/o que la orientación requerida para la reacción no es muy restrictiva. Por el contrario, un valor bajo de A podría indicar que las moléculas tienen una orientación muy específica para reaccionar o que las colisiones son menos frecuentes.
Teoría del Estado de Transición
Desde la perspectiva de la teoría del estado de transición (o teoría del complejo activado), A puede expresarse en términos de la entropía de activación (ΔS‡). Esta teoría postula que los reactivos forman un complejo activado (o estado de transición) antes de convertirse en productos. La expresión para A en este contexto es más compleja y depende de las funciones de partición de los reactivos y del estado de transición:
A = (kBT/h)eΔS‡/R
Donde kB es la constante de Boltzmann, h es la constante de Planck, y ΔS‡ es la entropía de activación. La entropía de activación proporciona información sobre el grado de desorden o libertad de movimiento en el estado de transición en comparación con los reactivos. Un valor positivo de ΔS‡ (y por lo tanto un A alto) sugiere que el estado de transición es más desordenado que los reactivos, mientras que un valor negativo (y un A bajo) indica un estado de transición más ordenado.
Variaciones de la Ecuación de Arrhenius
La ecuación de Arrhenius también puede presentarse en formas adaptadas para situaciones específicas:
Ecuación de Arrhenius Integrada
Cuando se tienen dos puntos de datos (k1 a T1 y k2 a T2), se puede utilizar la forma integrada de la ecuación de Arrhenius para calcular la energía de activación sin necesidad de una gráfica completa:
ln(k2/k1) = (Ea/R)(1/T1 - 1/T2)
Esta forma es particularmente útil cuando solo se dispone de datos de constante de velocidad a dos temperaturas diferentes. Permite una inferencia directa de la sensibilidad de la constante de velocidad a los cambios de temperatura y energía de activación. Si la energía de activación es alta para un rango de temperatura dado, la constante de velocidad es altamente sensible, lo que significa que pequeños cambios en la temperatura tienen un efecto significativo en la velocidad de reacción. Por el contrario, si la energía de activación es baja, la constante de velocidad es menos sensible a los cambios de temperatura.
Constante de los Gases (R) vs. Constante de Boltzmann (kB)
Es fundamental elegir la constante adecuada (R o kB) en el denominador de la función exponencial de la ecuación de Arrhenius, dependiendo de las unidades de la energía de activación. La clave es que el exponente -Ea/RT o -Ea/kBT debe ser adimensional (sin unidades).

- Si la energía de activación (Ea) se expresa en términos de Joules por mol (J/mol), entonces se debe usar la constante de los gases (R), que tiene unidades de J/mol·K. Las unidades de mol se cancelan.
- Si la energía de activación (Ea) se expresa en términos de Joules por molécula (J/molécula), entonces se debe usar la constante de Boltzmann (kB), que tiene unidades de J/K. Las unidades de molécula se entienden como implícitas en Ea y se cancelan.
La elección de la constante se basa puramente en la cancelación de unidades para asegurar la validez matemática de la expresión exponencial.
Consideraciones Importantes y Limitaciones
Aunque la ecuación de Arrhenius y su representación gráfica son herramientas poderosas, es importante tener en cuenta algunas consideraciones y limitaciones:
- No linealidad: En algunos casos, especialmente en sistemas biológicos o reacciones complejas, la gráfica de Arrhenius puede volverse no lineal. Esto puede ocurrir si los pasos determinantes de la velocidad cambian a diferentes temperaturas, si hay cambios en la composición de membranas celulares (como en el transporte de beta-glicósidos en E. coli estudiado por Fox y colaboradores en 1972) o si ocurre desnaturalización de proteínas a altas temperaturas. Una caída repentina en la gráfica a bajas 1/T (altas temperaturas) puede ser un indicio de desnaturalización.
- Dependencia de la temperatura de A y Ea: Si bien se asume que A y Ea son constantes, en realidad pueden tener una ligera dependencia de la temperatura. Sin embargo, para la mayoría de los rangos de temperatura estudiados, y cuando Ea >> RT, esta dependencia es lo suficientemente pequeña como para ser despreciable, a menos que se estudie un rango de temperatura muy amplio. Los valores obtenidos de A y Ea suelen ser un promedio o un valor "aparente" para el rango experimental.
- Reacciones complejas: La ecuación de Arrhenius se ajusta muy bien para una gran cantidad de reacciones homogéneas elementales. Para reacciones complejas (múltiples pasos), los valores de A y Ea obtenidos son a menudo "aparentes" y representan un promedio de los pasos individuales.
Componentes Clave de la Gráfica de Arrhenius
Para resumir los elementos esenciales de la gráfica de Arrhenius, podemos presentar una tabla comparativa de sus componentes principales:
| Componente de la Ecuación Linealizada | Representación en la Gráfica de Arrhenius | Significado o Derivación |
|---|---|---|
y = ln k | Eje Y | Logaritmo natural de la constante de velocidad de la reacción. |
x = 1/T | Eje X | Inverso de la temperatura absoluta (en Kelvin). |
m = -Ea/R | Pendiente de la línea recta | Relacionada directamente con la energía de activación (Ea). Permite calcular Ea (Ea = -mR). |
b = ln A | Intersección en el eje Y | Logaritmo natural del factor preexponencial (A). Permite calcular A (A = eb). |
Preguntas Frecuentes sobre el Factor Preexponencial
¿Es el factor preexponencial (A) una constante exacta?
No, el factor preexponencial (A) y la energía de activación (Ea) obtenidos de la ecuación de Arrhenius son generalmente valores "aparentes" o promedios. Aunque se asume que son constantes para un rango de temperatura dado, en realidad pueden tener una ligera dependencia de la temperatura. Sin embargo, para la mayoría de las reacciones y rangos de temperatura estudiados, esta dependencia es lo suficientemente pequeña como para que la aproximación de que son constantes sea válida y muy útil.
¿Qué indica un valor alto o bajo del factor preexponencial (A)?
Un valor alto de A sugiere que la reacción tiene una alta frecuencia de colisiones entre las moléculas y/o que la orientación molecular requerida para que la reacción ocurra no es muy restrictiva. Esto significa que una gran proporción de las colisiones tiene la orientación adecuada para ser efectiva. Por el contrario, un valor bajo de A podría indicar que las moléculas tienen una orientación muy específica y rara vez se alinean correctamente para reaccionar, o que la frecuencia de colisiones es intrínsecamente baja.
¿Por qué es importante calcular el factor preexponencial?
Calcular el factor preexponencial es importante por varias razones:
- Predicción de la constante de velocidad: Una vez que se conocen A y Ea, se puede predecir la constante de velocidad de la reacción a cualquier temperatura.
- Comprensión del mecanismo de reacción: A proporciona información sobre la naturaleza microscópica de la reacción, como la frecuencia de colisiones y los requisitos estéricos. Esto ayuda a comprender cómo se comportan las moléculas durante la reacción.
- Diseño de procesos: En química industrial y biotecnología, conocer A y Ea es crucial para optimizar las condiciones de reacción, como la temperatura, para maximizar la eficiencia y el rendimiento.
¿Cuándo debo usar la constante de los gases (R) o la constante de Boltzmann (kB) en la ecuación de Arrhenius?
La elección entre la constante de los gases (R) y la constante de Boltzmann (kB) depende de las unidades en las que se exprese la energía de activación (Ea). El objetivo es que el exponente de la ecuación de Arrhenius sea adimensional:
- Use la constante de los gases (R = 8.314 J·mol-1·K-1) cuando la energía de activación (Ea) esté en unidades de Joules por mol (J/mol) o kilojoules por mol (kJ/mol). Las unidades de 'mol' se cancelarán.
- Use la constante de Boltzmann (kB = 1.381 × 10-23 J·K-1) cuando la energía de activación (Ea) esté en unidades de Joules por molécula (J/molécula). Las unidades de 'molécula' se cancelarán implícitamente, dejando el exponente adimensional.
La decisión se basa puramente en la consistencia y cancelación de unidades para que el cálculo sea correcto.
Conclusión
La gráfica de Arrhenius es una herramienta poderosa y elegante en la cinética química que permite la visualización y cuantificación de parámetros fundamentales de la reacción. Al linealizar la ecuación de Arrhenius y trazar el logaritmo natural de la constante de velocidad contra el inverso de la temperatura, no solo podemos determinar la crucial energía de activación a partir de la pendiente, sino que también podemos calcular el escurridizo factor preexponencial 'A' a partir de la intersección en el eje Y. Este factor 'A' no es meramente un número; es un reflejo de la frecuencia de colisiones y de la orientación molecular necesaria para que una reacción ocurra, ofreciéndonos una ventana al mundo microscópico de las interacciones moleculares. Dominar la construcción e interpretación de la gráfica de Arrhenius es, por tanto, fundamental para cualquier persona que busque comprender y predecir el comportamiento de las reacciones químicas.
Si quieres conocer otros artículos parecidos a Calculando el Factor Preexponencial de Arrhenius puedes visitar la categoría Química.
