26/04/2025
En nuestro día a día, escuchamos hablar del pH en diversos contextos: desde productos de limpieza hasta cosméticos, pasando por la calidad del agua que bebemos o la salud de nuestro suelo. Pero, ¿qué es exactamente el pH y por qué es tan importante medirlo? El pH no es más que el indicador del potencial de hidrógenos, una medida fundamental que nos permite entender el grado de acidez o alcalinidad de una disolución. Su comprensión es clave en campos tan diversos como la química, la biología, la agricultura e incluso la medicina.
Esta guía exhaustiva te llevará de la mano a través de los conceptos esenciales del pH, cómo se define, cómo se relaciona con la acidez y la basicidad, y lo más importante, cómo se mide utilizando diversas herramientas y técnicas. Prepárate para descubrir el fascinante equilibrio que rige la naturaleza de las sustancias que nos rodean.
¿Qué es el pH y por qué es crucial?
El término pH se deriva de “potencial de hidrógeno” y es una medida logarítmica que nos indica la concentración de iones de hidrógeno (H+) en una disolución. En términos más técnicos, se define como el logaritmo negativo de base 10 de la concentración de iones de hidrógeno. Matemáticamente, esto se expresa como pH = -log[H+]. Cuanto mayor sea la concentración de iones H+, menor será el valor del pH y, por lo tanto, más ácida será la disolución.
Por otro lado, existe una medida complementaria llamada pOH, que representa la concentración de iones hidroxilo (OH-) en una disolución, expresada de manera similar como pOH = -log[OH-]. A diferencia del pH, el pOH se utiliza para medir el nivel de alcalinidad o basicidad. Un dato fundamental es que, en disoluciones acuosas a 25 °C, la suma del pH y el pOH siempre es igual a 14 (pH + pOH = 14). Esta relación es vital para comprender el equilibrio ácido-base.
La importancia de medir el pH radica en que la mayoría de los procesos químicos y biológicos son extremadamente sensibles a los cambios en la acidez o alcalinidad del medio. Pequeñas variaciones pueden alterar drásticamente reacciones, el crecimiento de organismos o la estabilidad de materiales. Por ejemplo, el pH de la sangre humana debe mantenerse en un rango muy estrecho (aproximadamente 7.35 a 7.45) para que las funciones vitales se desarrollen correctamente. Fuera de este rango, pueden ocurrir condiciones médicas graves.
La Relación entre Acidez y pH: Un Vínculo Inseparable
La relación entre el nivel de acidez y el pH es inversa pero directa en su efecto. Las disoluciones consideradas ácidas se caracterizan por tener una alta concentración de iones hidrógeno (H+). Según la definición del pH (pH = -log[H+]), esto se traduce en valores de pH bajos. Por lo tanto, cuanto menor sea el valor de pH, mayor será el nivel de acidez de una disolución. Un ácido fuerte, como el ácido clorhídrico, tendrá un pH cercano a 0 o 1, lo que indica una abundancia extrema de iones H+.
En contraste, las disoluciones básicas o alcalinas se distinguen por tener una baja concentración de iones hidrógeno. Esto implica que la concentración de iones hidroxilo (OH-) es relativamente alta. Consecuentemente, estas disoluciones presentan valores de pH elevados, acercándose al 14. Así, una sustancia con un pH de 13 o 14, como la lejía, es altamente básica y tiene una concentración muy baja de iones H+.
Es importante destacar que una disolución neutra, como el agua pura a 25 °C, tiene un pH de 7. En este punto, la concentración de iones H+ es igual a la concentración de iones OH-, lo que representa un equilibrio perfecto entre la acidez y la basicidad.
La Escala de Medida del pH: Un Rango de Posibilidades
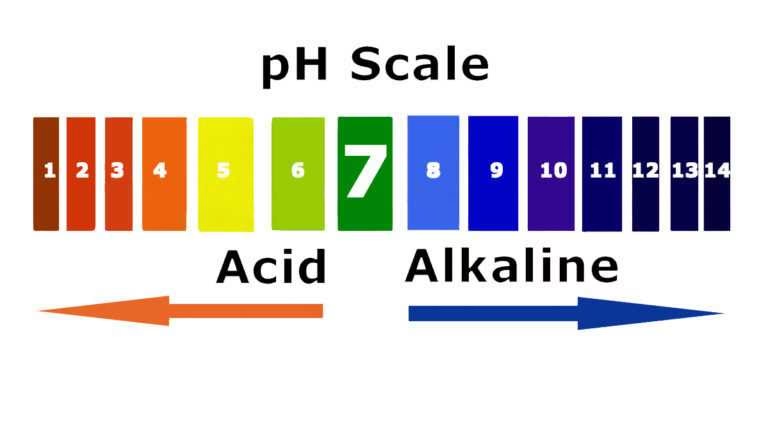
La escala de pH es la herramienta universalmente aceptada para cuantificar el grado de acidez o basicidad de una disolución. Esta escala va desde el valor 0 hasta el 14. Comprender cada segmento de esta escala es fundamental para interpretar los resultados de cualquier medición:
- pH de 0 a < 7: Disoluciones Ácidas. Cuanto más cerca del 0, más ácida es la sustancia. Esto significa una concentración muy alta de iones de hidrógeno. Ejemplos incluyen el ácido de batería (pH 0-1) y el jugo de limón (pH 2-3).
- pH = 7: Disoluciones Neutras. Este valor indica un equilibrio perfecto entre iones de hidrógeno y de hidroxilo. El ejemplo más conocido es el agua pura.
- pH > 7 a 14: Disoluciones Básicas o Alcalinas. Cuanto más cerca del 14, más básica o alcalina es la sustancia. Esto significa una baja concentración de iones de hidrógeno y una alta concentración de iones hidroxilo. Ejemplos incluyen la leche de magnesia (pH 10-11) y la lejía (pH ~13).
Esta escala nos permite clasificar rápidamente cualquier sustancia y comprender su naturaleza química. Es una herramienta indispensable en laboratorios, industrias y en la vida cotidiana para garantizar la seguridad y efectividad de productos y procesos.
Ejemplos de Compuestos Comunes y su pH
Para visualizar mejor la escala de pH, consideremos algunos ejemplos cotidianos:
| Tipo de Sustancia | Ejemplo | Rango de pH Aproximado | Características |
|---|---|---|---|
| Ácido Muy Fuerte | Ácido de Batería (Sulfúrico) | 0 - 1 | Extremadamente corrosivo y perjudicial. |
| Ácido Fuerte | Ácido Estomacal | 1.5 - 3.5 | Necesario para la digestión. |
| Ácido Moderado | Jugo de Limón | 2 - 3 | Cítrico y astringente. |
| Ácido Débil | Lluvia Ácida | 2 - 5 | Fenómeno ambiental con efectos nocivos. |
| Ligeramente Ácido | Café | 5 | Bebida común con ligera acidez. |
| Neutro | Agua Pura | 7 | El estándar de neutralidad. |
| Ligeramente Básico | Leche Materna | 7.1 - 7.7 | Esencial para la nutrición infantil. |
| Básico Moderado | Bicarbonato de Sodio | 8 - 9 | Usado como antiácido y limpiador. |
| Básico Fuerte | Leche de Magnesia | 10 - 11 | Antiácido común. |
| Básico Muy Fuerte | Lejía (Cloro) | 13 | Poderoso desinfectante y blanqueador. |
¿Cómo se Mide el pH? Métodos y Herramientas
La capacidad de medir el pH de una sustancia es crucial para una amplia gama de aplicaciones, desde el control de calidad en la industria alimentaria hasta el monitoreo ambiental. Existen principalmente dos métodos para determinar el pH, cada uno con sus propias ventajas y limitaciones:
1. Uso de Indicadores Ácido-Base
Los indicadores ácido-base son sustancias, generalmente tintes orgánicos, que tienen la particularidad de cambiar de color en función del pH de la disolución en la que se encuentran. Este cambio de color ocurre porque la estructura molecular del indicador se modifica cuando gana o pierde iones de hidrógeno, absorbiendo la luz de manera diferente y, por lo tanto, mostrando un color distinto.
- Papel Tornasol: Es uno de los indicadores más conocidos y sencillos. Se presenta en tiras de papel impregnadas con un tinte. Si se sumerge en una disolución ácida, el papel tornasol se vuelve rojo o anaranjado. Si la disolución es básica, se vuelve azul. Aunque es rápido y económico, el papel tornasol solo proporciona una indicación general del pH (ácido, neutro o básico).
- Papel Indicador de pH Universal: Es una versión más sofisticada del papel tornasol. Estas tiras de papel están impregnadas con una mezcla de varios indicadores, lo que les permite mostrar una gama de colores que corresponden a valores de pH más específicos. Vienen con una tabla de colores de referencia que permite estimar el pH con mayor precisión, a menudo en intervalos de 0.5 o 1 unidad de pH.
- Indicadores Líquidos: Existen numerosos indicadores ácido-base en forma líquida que se añaden directamente a la disolución a medir. Cada indicador tiene un rango de pH específico en el que cambia de color. Algunos ejemplos comunes incluyen:
- Fenolftaleína: Incolora en disoluciones ácidas (pH < 8.2) y de color rosa a fucsia en disoluciones básicas (pH > 10).
- Azul de Timol: Puede mostrar dos cambios de color, de rojo a amarillo (pH 1.2 - 2.8) y de amarillo a azul (pH 8.0 - 9.6).
- Amarillo de Metilo: Rojo en pH bajo (2.9) y amarillo en pH alto (4.0).
- Azul de Bromofenol: Amarillo a pH 3.0 y azul a pH 4.6.
- Verde de Bromocresol: Amarillo a pH 4.0 y azul a pH 5.4.
- Rojo de Metilo: Rojo a pH 4.2 y amarillo a pH 6.2.
- Púrpura de Bromocresol: Amarillo a pH 5.2 y púrpura a pH 6.8.
El uso de indicadores es ideal para estimaciones rápidas o cuando no se requiere una precisión extrema. Son muy utilizados en entornos educativos y para pruebas de campo.
2. Uso de un Potenciómetro o pH-metro
Para mediciones de pH más exactas y precisas, se utiliza un equipo electrónico conocido como pH-metro o potenciómetro. Este instrumento mide la diferencia de potencial eléctrico entre dos electrodos sumergidos en la disolución: un electrodo de referencia (con un potencial conocido y constante) y un electrodo de vidrio (cuyo potencial varía con la concentración de iones H+). La diferencia de potencial generada es directamente proporcional al pH de la disolución.
El pH-metro convierte esta señal eléctrica en un valor de pH que se muestra digitalmente en la pantalla. Para asegurar mediciones precisas, el pH-metro debe ser calibrado regularmente con soluciones tampón (buffers) de pH conocido. Los pH-metros varían en tamaño y sofisticación, desde modelos portátiles de mano hasta unidades de laboratorio de alta precisión que pueden medir con varias cifras decimales.

Enumerados en orden ascendente según el límite inferior del intervalo, los indicadores de pH útiles son: azul de timol, pH 1,2 - 2,8; amarillo de metilo, pH 2,9 - 4,0; azul de bromofenol, pH 3,0 - 4,6; verde de bromocresol, pH 4,0 - 5,4; rojo de metilo, pH 4,2 -6,2; púrpura de bromocresol, pH 5,2 - 6,8; azul de ... Las ventajas del pH-metro incluyen:
- Alta Precisión: Proporciona valores de pH numéricos y exactos.
- Versatilidad: Puede medir el pH de una amplia gama de disoluciones, incluyendo aquellas que son coloreadas o turbias, donde los indicadores visuales no serían efectivos.
- Rapidez: Las mediciones son casi instantáneas una vez que el electrodo se estabiliza.
- Automatización: Algunos modelos avanzados pueden realizar mediciones continuas y registrar datos.
El pH-metro es el método preferido en laboratorios de investigación, control de calidad industrial, agricultura de precisión y cualquier aplicación donde la exactitud en la medición del pH sea crítica.
Soluciones Tampón o Buffers: Guardianes del pH
Un concepto fundamental relacionado con el pH son las soluciones tampón, también conocidas como buffers o amortiguadoras. Estas son disoluciones que tienen la notable propiedad de resistir cambios significativos en el pH, incluso cuando se les añaden pequeñas cantidades de un ácido o una base fuerte. Su capacidad para mantener el pH relativamente constante las hace indispensables en numerosos procesos.
Las soluciones tampón suelen estar compuestas por un ácido débil y su base conjugada, o una base débil y su ácido conjugado. Esta combinación permite que la disolución neutralice los iones H+ o OH- añadidos, minimizando así la variación del pH.
La importancia de las disoluciones tampón es inmensa, especialmente en sistemas biológicos. Por ejemplo, el pH de la sangre humana se mantiene constante gracias a varios sistemas tampón (como el bicarbonato, el fosfato y las proteínas). Esto es vital porque la actividad de las enzimas y la estabilidad de las proteínas son extremadamente sensibles al pH. Si el pH de la sangre varía incluso ligeramente, puede conducir a condiciones médicas graves como la acidosis o la alcalosis.
Además de la biología, los buffers son cruciales en la industria farmacéutica para la formulación de medicamentos, en la biotecnología para el cultivo de microorganismos, en la agricultura para el control del pH del suelo, y en la investigación química para mantener condiciones estables en reacciones experimentales. Son los héroes silenciosos que aseguran la estabilidad y el correcto funcionamiento de innumerables sistemas.
Preguntas Frecuentes sobre el pH
¿Qué significa un pH de 7?
Un pH de 7 indica que una disolución es neutra. Esto significa que la concentración de iones de hidrógeno (H+) es igual a la concentración de iones hidroxilo (OH-). El ejemplo más común es el agua pura a 25 °C.
¿Es peligroso el pH extremo?
Sí, los valores extremos de pH (cercanos a 0 o 14) indican sustancias altamente ácidas o altamente básicas que pueden ser corrosivas y peligrosas. Pueden causar quemaduras graves en la piel, daños en los tejidos y ser perjudiciales para el medio ambiente.
¿El pH de un líquido cambia con la temperatura?
Sí, el pH de una disolución puede variar con la temperatura. Esto se debe a que la autoionización del agua (la forma en que el agua se disocia en iones H+ y OH-) es una reacción dependiente de la temperatura. Por esta razón, los pH-metros a menudo tienen compensación de temperatura para mediciones precisas.
¿Se puede medir el pH de sustancias sólidas?
Directamente no, el pH se refiere a la concentración de iones en una disolución líquida. Sin embargo, se puede medir el pH de una suspensión o pasta formada mezclando la sustancia sólida con agua, o disolviendo la sustancia sólida en un solvente apropiado.
¿Por qué es importante el pH en la agricultura?
El pH del suelo es crucial para la agricultura porque afecta la disponibilidad de nutrientes para las plantas. Cada cultivo tiene un rango de pH óptimo para su crecimiento. Un pH del suelo inadecuado puede bloquear la absorción de nutrientes, incluso si están presentes en abundancia.
Conclusión
El pH es mucho más que un simple número; es un indicador fundamental que nos revela la naturaleza química de las sustancias y su comportamiento. Desde la acidez de un jugo de limón hasta la alcalinidad de un producto de limpieza, el pH nos ayuda a comprender y controlar nuestro entorno. Ya sea a través de la simplicidad de un papel tornasol o la precisión de un pH-metro, la capacidad de medir el potencial de hidrógeno es una herramienta indispensable en la ciencia, la industria y nuestra vida cotidiana. Comprender el pH no solo enriquece nuestro conocimiento, sino que también nos empodera para tomar decisiones más informadas sobre los productos que usamos y los ambientes que habitamos, garantizando la seguridad y la eficiencia en innumerables aplicaciones.
Si quieres conocer otros artículos parecidos a ¿Cómo se Mide el pH? Desentrañando Acidez y Bases puedes visitar la categoría Química.
