27/04/2022
Comprender y calcular el pH es fundamental en química, especialmente cuando se trata de soluciones acuosas. Mientras que el pH de ácidos y bases fuertes puede determinarse de manera directa debido a su disociación completa, el cálculo para las bases débiles presenta un desafío mayor. Esto se debe a que las bases débiles no se disocian completamente en agua, estableciendo un equilibrio entre la forma molecular y sus iones. En este artículo, exploraremos en profundidad los principios y métodos necesarios para calcular el pH de las bases débiles, desde los conceptos fundamentales hasta la aplicación de fórmulas y ejemplos prácticos.
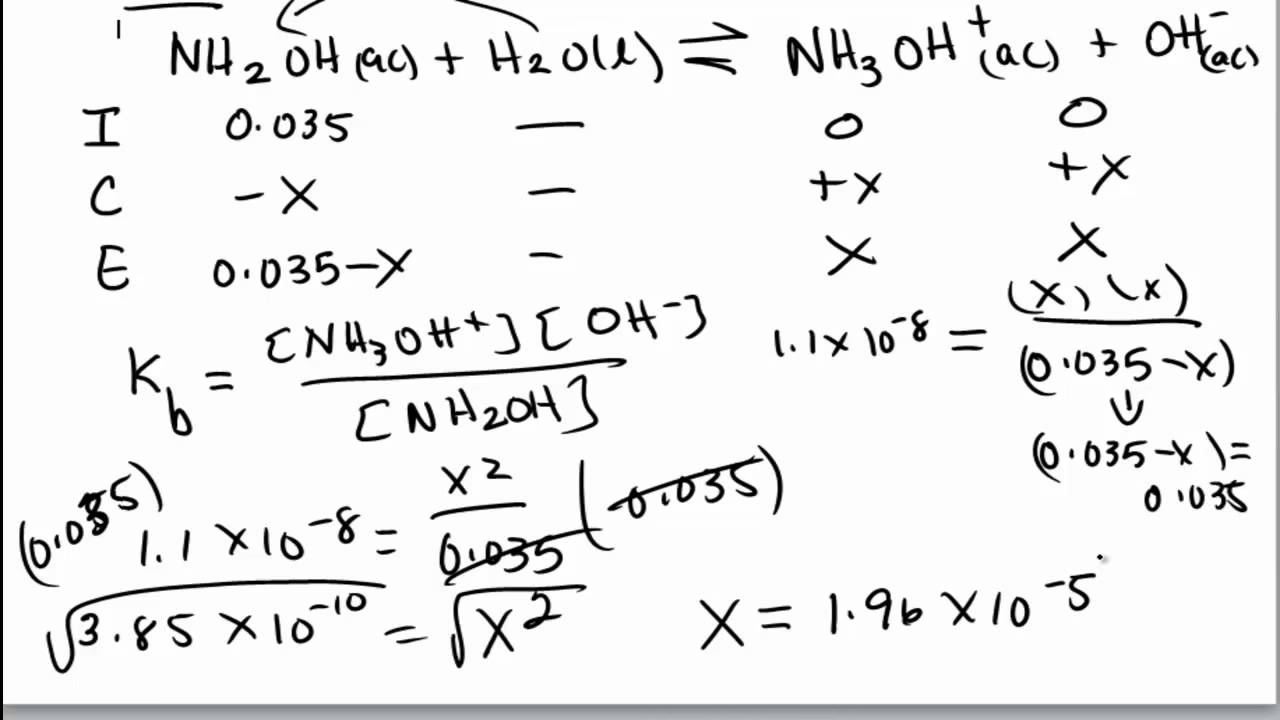
- La Naturaleza de las Bases Débiles y el pH
- La Constante de Ionización de Bases (Kb)
- Método para Calcular el pH de una Base Débil
- Ejemplo Práctico: Cálculo del pH de una Solución de Amoníaco
- Consideraciones Adicionales
- Indicadores de pH para Soluciones Básicas Débiles
- Preguntas Frecuentes (FAQ)
- Conclusión
La Naturaleza de las Bases Débiles y el pH
Para adentrarnos en el cálculo del pH de una base débil, es crucial entender qué las distingue de sus contrapartes fuertes. Una base fuerte, como el hidróxido de sodio (NaOH), se disocia completamente en agua, liberando una cantidad predecible de iones hidroxilo (OH-). Por el contrario, una base débil, como el amoníaco (NH3), solo se ioniza parcialmente en solución. Esto significa que una parte de la base permanece en su forma molecular sin reaccionar, mientras que otra pequeña porción acepta protones del agua, formando iones hidroxilo y su ácido conjugado.
El pH es una medida de la acidez o alcalinidad de una solución, y se define como el logaritmo negativo de la concentración de iones hidrógeno (H+ o H3O+):
pH = -log[H+]
Para las bases, es a menudo más conveniente trabajar primero con el pOH, que es el logaritmo negativo de la concentración de iones hidroxilo:
pOH = -log[OH-]
La relación entre pH y pOH en soluciones acuosas a 25°C está dada por el producto iónico del agua (Kw), que es 1.0 x 10-14:
pH + pOH = 14
Esta relación es fundamental para convertir el pOH, que calcularemos directamente a partir de la concentración de OH- generada por la base débil, en el pH final de la solución.
La Constante de Ionización de Bases (Kb)
La clave para calcular el pH de una base débil reside en su constante de ionización, conocida como Kb. Esta constante es una medida cuantitativa de la fuerza de una base débil, indicando la extensión de su disociación en agua. Cuanto mayor sea el valor de Kb, más fuerte será la base y mayor será su grado de ionización.
Para una base débil genérica (B) que reacciona con agua de la siguiente manera:
B(aq) + H2O(l) ⇌ BH+(aq) + OH-(aq)
La expresión de la constante de equilibrio, Kb, es:
Kb = [BH+][OH-] / [B]
Donde:
[BH+]es la concentración molar del ácido conjugado de la base.[OH-]es la concentración molar de iones hidroxilo en el equilibrio.[B]es la concentración molar de la base no disociada en el equilibrio.
Es importante recordar que el agua (H2O) no se incluye en la expresión de Kb porque es el solvente y su concentración se considera constante.
Método para Calcular el pH de una Base Débil
El cálculo del pH de una base débil generalmente implica el uso de una tabla ICE (Inicial, Cambio, Equilibrio) para determinar las concentraciones de las especies en el equilibrio. A continuación, se detallan los pasos:
Paso 1: Escribir la Ecuación de Ionización de la Base Débil
Primero, escribe la ecuación de equilibrio para la base débil reaccionando con agua. Por ejemplo, para el amoníaco (NH3):
NH3(aq) + H2O(l) ⇌ NH4+(aq) + OH-(aq)
Paso 2: Construir la Tabla ICE
La tabla ICE ayuda a visualizar los cambios en las concentraciones desde el inicio hasta el equilibrio. Supongamos una concentración inicial de la base [B]0 y que 'x' es la cantidad de base que se disocia.
| [B] | [BH+] | [OH-] | |
|---|---|---|---|
| Inicial (I) | [B]0 | 0 | 0 |
| Cambio (C) | -x | +x | +x |
| Equilibrio (E) | [B]0 - x | x | x |
Nota: La concentración inicial de OH- del agua suele despreciarse porque es mucho menor que la que se produce por la disociación de la base, a menos que la base sea extremadamente débil o la solución esté muy diluida.
Paso 3: Sustituir en la Expresión de Kb
Ahora, introduce las concentraciones de equilibrio de la tabla ICE en la expresión de Kb:
Kb = (x)(x) / ([B]0 - x) = x² / ([B]0 - x)
Paso 4: Resolver para 'x' (Concentración de OH-)
Esta es la parte donde pueden surgir dos métodos principales: la aproximación o la ecuación cuadrática.

Método de Aproximación
Si la base es muy débil (Kb es muy pequeña) y la concentración inicial de la base es lo suficientemente alta (generalmente, si [B]0 / Kb > 100 o 400, dependiendo del nivel de precisión requerido), la cantidad 'x' que se disocia es insignificante en comparación con la concentración inicial de la base. En este caso, podemos aproximar ([B]0 - x) ≈ [B]0.
La ecuación se simplifica a:
Kb ≈ x² / [B]0
Despejando 'x':
x² = Kb * [B]0
x = √ (Kb * [B]0)
Donde 'x' es la concentración de [OH-] en el equilibrio.
Este método es rápido y, para la mayoría de las bases débiles comunes, proporciona una buena aproximación. Sin embargo, siempre es recomendable verificar la validez de la aproximación calculando el porcentaje de ionización: (x / [B]0) * 100%. Si este porcentaje es menor al 5%, la aproximación es válida.
Método de la Ecuación Cuadrática
Si la aproximación no es válida (es decir, 'x' no es despreciable en comparación con [B]0), o si se requiere una mayor precisión, se debe resolver la ecuación cuadrática completa:
Kb = x² / ([B]0 - x)
Reorganizando la ecuación obtenemos una forma cuadrática:
x² = Kb([B]0 - x)
x² = Kb[B]0 - Kbx
x² + Kbx - Kb[B]0 = 0
Esta es una ecuación de la forma ax² + bx + c = 0, donde a=1, b=Kb y c=-Kb[B]0. Se resuelve usando la fórmula general para ecuaciones cuadráticas:
x = [-b ± √(b² - 4ac)] / 2a
Dado que 'x' representa una concentración, debe ser un valor positivo. De las dos soluciones que arroja la fórmula cuadrática, se elige la que tenga sentido físico (la positiva).
Paso 5: Calcular el pOH
Una vez que se ha determinado 'x' (que es [OH-] en el equilibrio), se calcula el pOH:
pOH = -log[OH-] = -log(x)
Paso 6: Calcular el pH
Finalmente, se utiliza la relación pH + pOH = 14 para obtener el pH de la solución:
pH = 14 - pOH
Ejemplo Práctico: Cálculo del pH de una Solución de Amoníaco
Calcule el pH de una solución de amoníaco (NH3) 0.15 M. La Kb del amoníaco es 1.8 x 10-5.
Solución:
1. Ecuación de Ionización:
NH3(aq) + H2O(l) ⇌ NH4+(aq) + OH-(aq)
2. Tabla ICE:
| [NH3] | [NH4+] | [OH-] | |
|---|---|---|---|
| Inicial (I) | 0.15 M | 0 | 0 |
| Cambio (C) | -x | +x | +x |
| Equilibrio (E) | 0.15 - x | x | x |
3. Expresión de Kb:
Kb = [NH4+][OH-] / [NH3]
1.8 x 10-5 = (x)(x) / (0.15 - x) = x² / (0.15 - x)
4. Resolver para 'x':
Verificamos la aproximación: 0.15 / (1.8 x 10-5) ≈ 8333. Como este valor es mucho mayor que 400, la aproximación es válida.
1.8 x 10-5 ≈ x² / 0.15
x² = (1.8 x 10-5) * 0.15
x² = 2.7 x 10-6
x = √(2.7 x 10-6)
x = 0.00164 M
Así, [OH-] = 0.00164 M.

Verificación del porcentaje de ionización: (0.00164 / 0.15) * 100% = 1.09%. Como es menor al 5%, la aproximación es válida y el resultado es fiable.
5. Calcular pOH:
pOH = -log[OH-] = -log(0.00164)
pOH ≈ 2.78
6. Calcular pH:
pH = 14 - pOH = 14 - 2.78
pH = 11.22
Por lo tanto, el pH de una solución 0.15 M de amoníaco es aproximadamente 11.22.
Consideraciones Adicionales
Es fundamental recordar que los cálculos de pH son sensibles a la temperatura, ya que la constante de ionización del agua (Kw) y, por ende, las constantes de ionización de ácidos y bases (Ka y Kb), varían con ella. Los valores de Kb suelen proporcionarse a 25°C, que es la temperatura estándar para la mayoría de los cálculos.
Además, la presencia de iones comunes (efecto del ion común) o la formación de soluciones amortiguadoras (buffers) pueden complicar el cálculo del pH, requiriendo el uso de la ecuación de Henderson-Hasselbalch o métodos más avanzados, pero esto va más allá del cálculo básico de una base débil pura en agua.
Indicadores de pH para Soluciones Básicas Débiles
Los indicadores de pH son sustancias orgánicas que cambian de color en un rango específico de pH, lo que los hace útiles para estimar el pH de una solución o para determinar el punto final en una titulación. Para soluciones de bases débiles, especialmente en titulaciones con ácidos fuertes, el punto de equivalencia se encontrará en el lado ácido de la escala de pH (pH < 7).
Una base débil, al ser titulada con un ácido fuerte, producirá un ácido conjugado que es relativamente fuerte. En el punto de equivalencia, la solución contendrá principalmente este ácido conjugado, lo que resultará en un pH ácido. Por lo tanto, el indicador más adecuado para este tipo de titulación será aquel cuyo rango de cambio de color se encuentre en la región ácida, es decir, con un pKin (constante de ionización del indicador) inferior a 7.0.
Ejemplos de Indicadores Adecuados:
- Rojo de Metilo: Cambia de color en un rango de pH de aproximadamente 4.4 a 6.2 (rojo a amarillo). Su pKin es de 5.0, lo que lo hace ideal para titulaciones donde el punto de equivalencia es ligeramente ácido.
- Azul de Bromocresol: Cambia de amarillo a azul en el rango de pH de 3.8 a 5.4.
Por el contrario, indicadores como la fenolftaleína (que cambia de incoloro a rosa en el rango de pH 8.3-10.0) no serían apropiados para una titulación de una base débil con un ácido fuerte, ya que su cambio de color ocurriría mucho después del punto de equivalencia real, llevando a un error significativo.

Preguntas Frecuentes (FAQ)
P: ¿Cuál es la diferencia principal entre una base fuerte y una base débil en términos de pH?
R: La principal diferencia radica en su disociación en agua. Una base fuerte se disocia completamente, liberando todos sus iones OH-, lo que permite un cálculo directo del pOH y pH. Una base débil solo se disocia parcialmente, estableciendo un equilibrio que requiere el uso de su constante de ionización (Kb) y métodos de equilibrio (como la tabla ICE) para determinar la concentración de OH- y, por ende, el pH.
P: ¿Por qué no se incluye el agua en la expresión de Kb?
R: El agua se considera el solvente y su concentración molar en soluciones diluidas es prácticamente constante. Por convención, las concentraciones de solventes puros no se incluyen en las expresiones de las constantes de equilibrio.
P: ¿Cuándo puedo usar la aproximación en el cálculo del pH de una base débil?
R: Puedes usar la aproximación (despreciar 'x' en el denominador) cuando la concentración inicial de la base ([B]0) es al menos 100 o 400 veces mayor que el valor de Kb (es decir, [B]0 / Kb > 100 o 400). Si el porcentaje de ionización (x/[B]0 * 100%) resulta ser menor al 5%, la aproximación es válida.
P: Si tengo el Ka de un ácido conjugado, ¿cómo obtengo el Kb de su base débil?
R: Existe una relación entre la constante de ionización de un ácido y la de su base conjugada (o viceversa) a través del producto iónico del agua (Kw):
Ka * Kb = Kw = 1.0 x 10-14 (a 25°C)
Así, si tienes Ka, puedes calcular Kb como Kb = Kw / Ka.
P: ¿El pH de una base débil siempre es mayor que 7?
R: Sí, por definición, una base produce iones hidroxilo (OH-) en solución, lo que aumenta la alcalinidad y, por lo tanto, el pH será mayor que 7 (el pH de una solución neutra a 25°C).
Conclusión
El cálculo del pH de una base débil es un proceso fundamental en la química que requiere una comprensión clara de los equilibrios químicos y la aplicación de la constante de ionización de bases (Kb). Aunque puede parecer más complejo que el cálculo para bases fuertes, el uso sistemático de la tabla ICE y la selección adecuada del método (aproximación o ecuación cuadrática) simplifican considerablemente el proceso. Dominar estos cálculos no solo es esencial para estudiantes y profesionales de la química, sino que también proporciona una visión profunda de cómo interactúan las sustancias en el mundo molecular, impactando desde procesos biológicos hasta aplicaciones industriales. La precisión en estos cálculos es vital para muchas áreas científicas y tecnológicas.
Si quieres conocer otros artículos parecidos a Cálculo del pH de Bases Débiles: Guía Completa puedes visitar la categoría Química.
