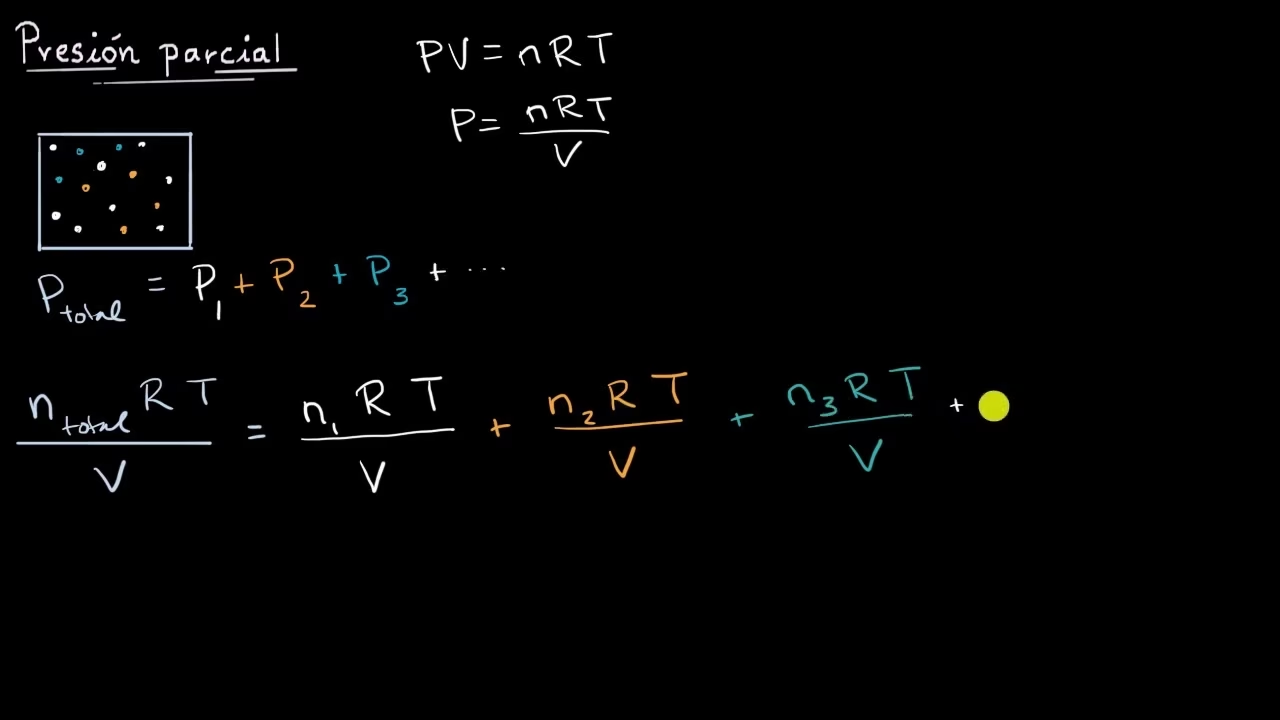20/11/2025
En el vasto universo de la química y la física, comprender el comportamiento de los gases es fundamental para innumerables aplicaciones, desde la ingeniería hasta la meteorología. Cuando trabajamos con una mezcla de gases, una pregunta recurrente es: ¿qué parte del volumen total le corresponde a cada gas individual? Aquí es donde entra en juego el concepto de volumen parcial, una herramienta esencial para analizar el comportamiento de las mezclas gaseosas.

El volumen parcial de un gas en una mezcla se refiere al volumen que ocuparía ese gas si estuviera solo en las mismas condiciones de temperatura y presión total que la mezcla. Este concepto es vital porque los gases, a diferencia de los líquidos o los sólidos, se mezclan completamente y ocupan todo el volumen disponible del recipiente. Sin embargo, para fines de cálculo y comprensión de su comportamiento individual dentro de la mezcla, imaginamos su contribución particular al volumen total.
La clave para entender y calcular el volumen parcial reside en una serie de leyes fundamentales que describen el comportamiento de los gases, especialmente la Ley de Amagat de los Volúmenes Parciales y la omnipresente Ley de los Gases Ideales. A lo largo de este artículo, desglosaremos estas leyes, explicaremos su interconexión y te guiaremos a través de los pasos necesarios para calcular el volumen parcial de un gas en cualquier mezcla.
- La Ley de Amagat de los Volúmenes Parciales: La Suma de las Partes
- La Ley de Dalton de las Presiones Parciales: Una Perspectiva Complementaria
- La Ley de los Gases Ideales: La Herramienta Universal
- Cálculo del Volumen Parcial de un Gas
- Gases Ideales vs. Gases Reales: Una Consideración Importante
- Tabla Comparativa de las Leyes de los Gases
- Preguntas Frecuentes sobre el Volumen Parcial de Gases
- ¿Qué es el volumen parcial de un gas?
- ¿Cuál es la diferencia entre volumen parcial y presión parcial?
- ¿Cuándo se aplica la Ley de Amagat?
- ¿Por qué es importante calcular el volumen parcial?
- ¿Los gases reales siempre obedecen la Ley de Amagat?
- ¿Es posible que el volumen parcial de un gas sea mayor que el volumen total de la mezcla?
- Conclusión
La Ley de Amagat de los Volúmenes Parciales: La Suma de las Partes
La Ley de Amagat, también conocida como la Ley de los Volúmenes Parciales, establece que en una mezcla de gases ideales, el volumen total de la mezcla es igual a la suma de los volúmenes parciales que cada gas ocuparía si estuviera solo a la misma temperatura y presión total de la mezcla. Matemáticamente, se expresa de la siguiente manera:
Vtotal = V1 + V2 + V3 + ... + Vn
Donde Vtotal es el volumen total de la mezcla, y V1, V2, etc., son los volúmenes parciales de cada gas componente. Esta ley es análoga a la Ley de Dalton de las Presiones Parciales, que veremos a continuación, pero se centra en el volumen en lugar de la presión. Es importante recordar que esta ley aplica a condiciones de temperatura y presión constantes para todos los componentes.
Imagina un recipiente que contiene una mezcla de oxígeno y nitrógeno. Según la Ley de Amagat, el volumen total de ese recipiente es la suma del volumen que el oxígeno ocuparía si estuviera solo a esa misma temperatura y presión, más el volumen que el nitrógeno ocuparía bajo las mismas condiciones. Esta ley es particularmente útil cuando se conoce el volumen de cada gas por separado antes de mezclarlos o cuando se desea determinar cuánto espacio 'contribuye' cada gas a la mezcla final.
La Ley de Dalton de las Presiones Parciales: Una Perspectiva Complementaria
Aunque nuestro objetivo principal es el volumen parcial, es imposible hablar de mezclas de gases sin mencionar la Ley de Dalton de las Presiones Parciales. Esta ley, formulada por John Dalton, establece que la presión total ejercida por una mezcla de gases ideales es igual a la suma de las presiones parciales que cada gas ejercería si estuviera solo en el mismo volumen y a la misma temperatura.
Ptotal = P1 + P2 + P3 + ... + Pn
Donde Ptotal es la presión total de la mezcla, y P1, P2, etc., son las presiones parciales de cada gas componente. La presión parcial de un gas es la presión que ese gas ejercería si ocupara solo el volumen total del recipiente a la misma temperatura.
La relación entre la Ley de Amagat y la Ley de Dalton es fundamental. Ambas leyes describen el comportamiento de las mezclas de gases ideales y están intrínsecamente ligadas a la fracción molar de cada componente. La fracción molar (xi) de un gas en una mezcla se define como la relación entre el número de moles de ese gas (ni) y el número total de moles de todos los gases en la mezcla (ntotal):
xi = ni / ntotal
Para gases ideales, la fracción molar de un componente es igual a su fracción de volumen (según Amagat) y también igual a su fracción de presión (según Dalton). Esto significa que:
Vi = xi * Vtotal
Pi = xi * Ptotal
Estas relaciones son increíblemente poderosas, ya que nos permiten calcular el volumen parcial o la presión parcial de un gas si conocemos su fracción molar y el volumen o la presión total de la mezcla.
La Ley de los Gases Ideales: La Herramienta Universal
La Ley de los Gases Ideales es la piedra angular para la mayoría de los cálculos relacionados con gases. Proporciona una relación fundamental entre la presión (P), el volumen (V), el número de moles (n) y la temperatura (T) de un gas. La ecuación es la siguiente:
PV = nRT
Donde:
- P es la presión del gas (en atmósferas, pascales o kilopascales).
- V es el volumen del gas (en litros o metros cúbicos).
- n es el número de moles del gas.
- R es la constante de los gases ideales (un valor que depende de las unidades utilizadas, por ejemplo, 0.08206 L·atm/(mol·K) o 8.3145 J/(mol·K)).
- T es la temperatura absoluta del gas (en Kelvin).
Esta ley es una combinación de varias leyes empíricas de los gases:
- Ley de Boyle: PV = constante (a T y n constantes)
- Ley de Charles: V/T = constante (a P y n constantes)
- Ley de Amontons (o Ley de Gay-Lussac): P/T = constante (a V y n constantes)
- Ley de Avogadro: V/n = constante (a P y T constantes)
La Ley de los Gases Ideales es una herramienta versátil. Nos permite calcular cualquiera de las cinco variables (P, V, n, T, R) si conocemos las otras cuatro. Y lo que es más importante para nuestro tema, nos permite calcular el volumen de un gas (su volumen parcial) si conocemos sus moles, la temperatura y la presión total de la mezcla.
Cálculo del Volumen Parcial de un Gas
Existen principalmente dos métodos para calcular el volumen parcial de un gas en una mezcla, ambos derivados de las leyes que hemos discutido:
Método 1: Usando la Fracción Molar y la Ley de Amagat
Este es el método más directo si ya conoces la fracción molar del gas o puedes calcularla fácilmente.
- Determina el número de moles de cada gas (ni) y el número total de moles (ntotal) en la mezcla. Si te dan las masas, conviértelas a moles usando la masa molar de cada gas.
- Calcula la fracción molar (xi) del gas de interés:
xi = ni / ntotal
- Mide o calcula el volumen total (Vtotal) de la mezcla.
- Calcula el volumen parcial (Vi) usando la siguiente relación:
Vi = xi * Vtotal
Método 2: Usando la Ley de los Gases Ideales
Este método es útil si conoces el número de moles del gas de interés, la temperatura y la presión total de la mezcla, pero no necesariamente el volumen total o la fracción molar.
- Identifica el número de moles (ni) del gas específico cuyo volumen parcial deseas calcular.
- Asegúrate de que la temperatura (T) esté en Kelvin. Si está en grados Celsius, suma 273.15.
- Asegúrate de que la presión total (Ptotal) esté en las unidades consistentes con la constante R que vas a usar.
- Selecciona el valor apropiado de la constante de los gases ideales (R). Por ejemplo, si la presión está en atmósferas y el volumen en litros, usa R = 0.08206 L·atm/(mol·K).
- Aplica la Ley de los Gases Ideales para el gas individual, asumiendo que ocupa el volumen parcial (Vi) a la presión total (Ptotal) de la mezcla:
Vi = (ni * R * T) / Ptotal
Es crucial entender que ambos métodos deberían dar el mismo resultado para gases ideales, ya que están interconectados por las propiedades de las mezclas gaseosas.

Ejemplo Práctico: Calculando el Volumen Parcial de Metano en una Mezcla
Consideremos una mezcla de gases que contiene 40.9 moles de metano (CH4) y 10.0 moles de etano (C2H6). La mezcla se encuentra a 25 °C y una presión total de 0.980 atmósferas. ¿Cuál es el volumen parcial del metano en esta mezcla?
Paso 1: Convertir la temperatura a Kelvin.
T = 25 °C + 273.15 = 298.15 K
Paso 2: Calcular el número total de moles.
ntotal = nCH4 + nC2H6 = 40.9 mol + 10.0 mol = 50.9 mol
Paso 3: Calcular la fracción molar del metano.
xCH4 = nCH4 / ntotal = 40.9 mol / 50.9 mol ≈ 0.8035
Paso 4: Calcular el volumen total de la mezcla usando la Ley de los Gases Ideales.
Utilizaremos la constante R = 0.08206 L·atm/(mol·K).
Vtotal = (ntotal * R * T) / Ptotal
Vtotal = (50.9 mol * 0.08206 L·atm/(mol·K) * 298.15 K) / 0.980 atm
Vtotal ≈ 1269.8 L
Paso 5: Calcular el volumen parcial del metano usando la fracción molar y el volumen total (Método 1).
VCH4 = xCH4 * Vtotal
VCH4 = 0.8035 * 1269.8 L
VCH4 ≈ 1020.2 L
Alternativa (Método 2): Calcular el volumen parcial del metano directamente usando la Ley de los Gases Ideales para el metano.
VCH4 = (nCH4 * R * T) / Ptotal
VCH4 = (40.9 mol * 0.08206 L·atm/(mol·K) * 298.15 K) / 0.980 atm
VCH4 ≈ 1020.2 L
Como puedes observar, ambos métodos arrojan resultados muy similares, con pequeñas diferencias debido al redondeo. Esto demuestra la consistencia de las leyes de los gases cuando se aplican correctamente.
Gases Ideales vs. Gases Reales: Una Consideración Importante
Es crucial recordar que las leyes que hemos discutido (Amagat, Dalton, y la Ley de los Gases Ideales) describen el comportamiento de los gases ideales. Un gas ideal es un modelo teórico en el que se asume que las partículas no tienen volumen y no interactúan entre sí. Aunque ningún gas real es verdaderamente ideal, muchos gases se comportan de manera muy similar a los gases ideales bajo ciertas condiciones.
Las condiciones bajo las cuales un gas real se aproxima mejor al comportamiento ideal son:
- Baja presión: A bajas presiones, las moléculas de gas están muy separadas, lo que minimiza las interacciones intermoleculares.
- Alta temperatura: A altas temperaturas, las moléculas tienen alta energía cinética, lo que hace que las fuerzas de atracción intermoleculares sean insignificantes en comparación con la energía de movimiento.
Cuando las presiones son muy altas o las temperaturas son muy bajas, los gases reales se desvían significativamente del comportamiento ideal. En estas condiciones, las interacciones moleculares y el volumen propio de las moléculas se vuelven importantes, y se requieren ecuaciones de estado más complejas (como la ecuación de Van der Waals) para describir su comportamiento con precisión. Sin embargo, para la mayoría de las aplicaciones prácticas en condiciones ambientales o moderadas, el modelo de gas ideal es una aproximación excelente y simplifica enormemente los cálculos.
Tabla Comparativa de las Leyes de los Gases
Para consolidar la información, aquí tienes una tabla que resume las leyes de los gases más importantes y sus relaciones:
| Ley | Descripción | Fórmula | Condiciones Constantes | Aplicación Principal |
|---|---|---|---|---|
| Ley de Boyle | El volumen de un gas es inversamente proporcional a su presión. | PV = k | Temperatura (T), Moles (n) | Relación P-V a T constante. |
| Ley de Charles | El volumen de un gas es directamente proporcional a su temperatura absoluta. | V/T = k | Presión (P), Moles (n) | Relación V-T a P constante. |
| Ley de Amontons | La presión de un gas es directamente proporcional a su temperatura absoluta. | P/T = k | Volumen (V), Moles (n) | Relación P-T a V constante. |
| Ley de Avogadro | El volumen de un gas es directamente proporcional al número de moles. | V/n = k | Presión (P), Temperatura (T) | Relación V-n a P y T constantes. |
| Ley de los Gases Ideales | Combina las leyes anteriores en una sola ecuación. | PV = nRT | Constante R | Cálculo de P, V, n o T para gases ideales. |
| Ley de Dalton | La presión total de una mezcla es la suma de las presiones parciales. | Ptotal = ∑Pi | Temperatura (T), Volumen (V) | Cálculo de presiones parciales en mezclas. |
| Ley de Amagat | El volumen total de una mezcla es la suma de los volúmenes parciales. | Vtotal = ∑Vi | Temperatura (T), Presión (P) | Cálculo de volúmenes parciales en mezclas. |
Preguntas Frecuentes sobre el Volumen Parcial de Gases
¿Qué es el volumen parcial de un gas?
El volumen parcial de un gas en una mezcla es el volumen que ese gas ocuparía si estuviera solo a la misma temperatura y la misma presión total que la mezcla. Es una forma de conceptualizar la contribución individual de cada componente gaseoso al volumen total del recipiente.
¿Cuál es la diferencia entre volumen parcial y presión parcial?
La diferencia radica en lo que se mide: el volumen parcial se refiere al volumen que un gas individual ocuparía si estuviera solo a la presión total de la mezcla, mientras que la presión parcial se refiere a la presión que un gas individual ejercería si ocupara solo el volumen total de la mezcla.
¿Cuándo se aplica la Ley de Amagat?
La Ley de Amagat se aplica a mezclas de gases ideales. Es más útil cuando se necesita determinar la contribución de volumen de cada gas individual a la mezcla total, especialmente si se conocen las fracciones molares de los componentes o los volúmenes iniciales de los gases antes de mezclarse a la misma P y T.
¿Por qué es importante calcular el volumen parcial?
Calcular el volumen parcial es importante en diversas aplicaciones, como el diseño de procesos químicos donde las proporciones de los gases son críticas, en la ingeniería de gases para determinar el tamaño de los tanques de almacenamiento, o en estudios ambientales para analizar la composición de la atmósfera. Permite comprender mejor la estequiometría y el comportamiento de las mezclas gaseosas.
¿Los gases reales siempre obedecen la Ley de Amagat?
No, la Ley de Amagat (al igual que la Ley de los Gases Ideales y la Ley de Dalton) es una aproximación para gases ideales. Los gases reales se desvían de este comportamiento ideal, especialmente a altas presiones y bajas temperaturas, donde las interacciones intermoleculares y el volumen de las propias moléculas de gas no pueden ignorarse.
¿Es posible que el volumen parcial de un gas sea mayor que el volumen total de la mezcla?
No, esto no es posible para un gas ideal que obedece la Ley de Amagat. Según esta ley, el volumen total de la mezcla es la suma de los volúmenes parciales, lo que significa que el volumen parcial de cualquier componente siempre será menor o igual al volumen total de la mezcla (si es el único componente).
Conclusión
Comprender y calcular el volumen parcial de un gas en una mezcla es una habilidad fundamental en química y campos relacionados. A través de la Ley de Amagat y la Ley de los Gases Ideales, podemos desentrañar cómo cada componente contribuye al volumen total de una mezcla gaseosa. Si bien estas leyes se basan en el modelo de gases ideales, proporcionan aproximaciones excepcionalmente precisas para la mayoría de las condiciones prácticas.
Dominar estos conceptos no solo te permitirá resolver problemas de cálculo, sino que también te brindará una comprensión más profunda del fascinante y complejo comportamiento de los gases, abriendo puertas a un sinfín de aplicaciones en la ciencia y la ingeniería. La próxima vez que pienses en una mezcla de gases, podrás visualizar no solo su presión total, sino también el espacio que cada uno de sus componentes estaría 'ocupando' si estuviera solo.
Si quieres conocer otros artículos parecidos a Descifrando el Volumen Parcial de los Gases puedes visitar la categoría Cálculos.