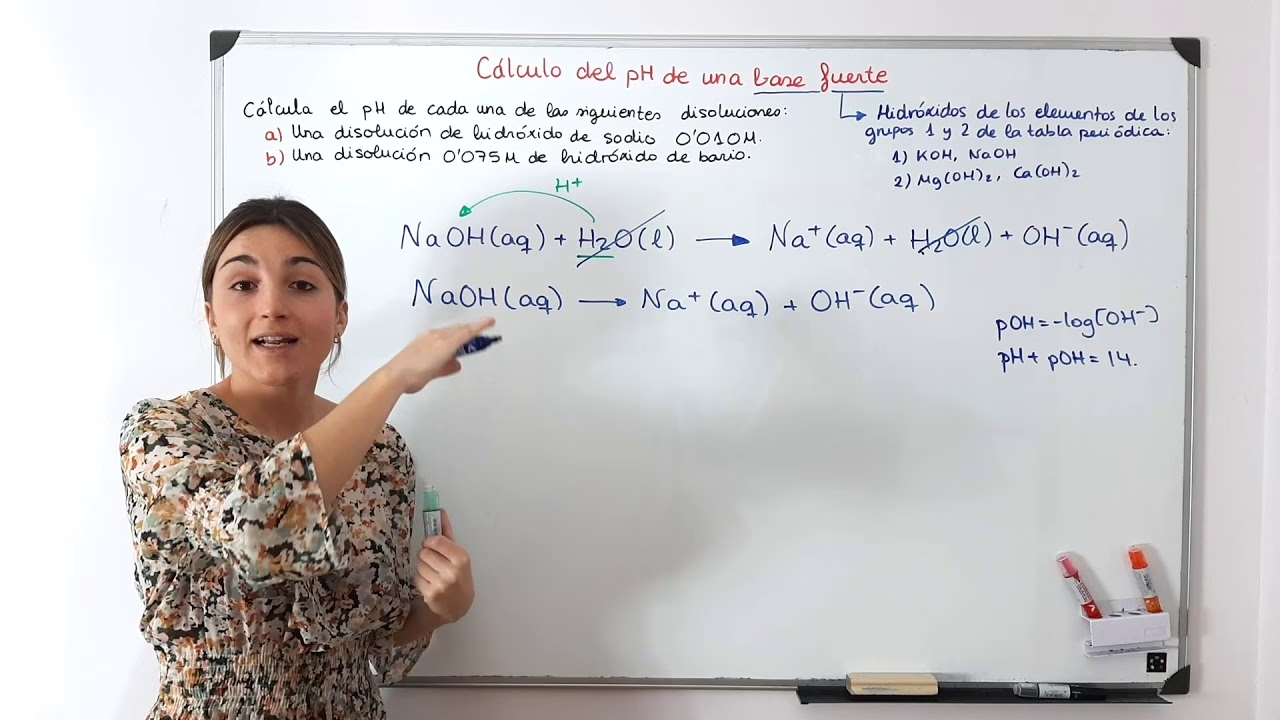25/04/2022
El pH es una medida fundamental en química que nos indica la acidez o alcalinidad de una solución. Comprender cómo se comporta el pH cuando mezclamos diferentes sustancias es crucial, no solo para estudiantes y profesionales de la química, sino también para diversas aplicaciones industriales, ambientales y biológicas. En este artículo, nos sumergiremos en el fascinante mundo de las mezclas de ácidos y bases, enfocándonos específicamente en aquellas compuestas por componentes fuertes. Exploraremos cómo determinar el pH resultante y qué factores influyen en este valor en escenarios comunes como la neutralización y la mezcla de sustancias del mismo tipo.

La simplicidad de los ácidos y bases fuertes radica en su capacidad de disociarse completamente en solución acuosa. Esto significa que, a diferencia de sus contrapartes débiles, podemos predecir con alta precisión la concentración de iones hidronio (H+) o hidróxido (OH-) que liberan, lo que facilita enormemente el cálculo del pH final de la mezcla. Acompáñanos en este recorrido para desvelar los misterios del pH en estas importantes reacciones.
- Entendiendo el Concepto de pH
- Mezclas de Ácido Fuerte y Base Fuerte: La Neutralización Perfecta
- Mezclas de Dos Ácidos Fuertes
- Mezclas de Dos Bases Fuertes
- Consideraciones Importantes al Realizar Mezclas
- Tabla Comparativa de Mezclas de Ácidos y Bases Fuertes
- Preguntas Frecuentes (FAQ)
- ¿Siempre es 7 el pH en el punto de equivalencia de un ácido fuerte con una base fuerte?
- ¿Qué sucede si mezclo un ácido fuerte con un ácido débil?
- ¿La temperatura afecta el pH de las mezclas?
- ¿Cómo se mide el pH en la práctica?
- ¿Por qué se usa la normalidad en algunos cálculos y la molaridad en otros?
- Conclusión
Entendiendo el Concepto de pH
Antes de sumergirnos en las mezclas, es vital recordar qué es el pH. El pH es una escala logarítmica que mide la concentración de iones hidronio (H+) en una solución. Un pH de 7 se considera neutro, valores menores a 7 indican acidez, y valores mayores a 7 indican alcalinidad o basicidad. Matemáticamente, el pH se define como el logaritmo negativo de la concentración molar de iones hidronio: pH = -log[H+]. De manera similar, el pOH mide la concentración de iones hidróxido (OH-), y la relación entre ambos es pH + pOH = 14 a 25°C. Esta escala nos permite cuantificar la fuerza de un ácido o una base en una solución.
Mezclas de Ácido Fuerte y Base Fuerte: La Neutralización Perfecta
Cuando un ácido fuerte se mezcla con una base fuerte, ocurre una reacción de neutralización. Tanto el ácido como la base se disocian completamente en sus iones constituyentes. Por ejemplo, el ácido clorhídrico (HCl) se disocia en H+ y Cl-, y el hidróxido de sodio (NaOH) en Na+ y OH-. La esencia de la neutralización es la reacción entre los iones H+ y OH- para formar moléculas de agua (H2O): H+(aq) + OH-(aq) → H2O(l).
El Punto de Equivalencia: Un pH de 7
El concepto más conocido en una titulación ácido fuerte-base fuerte es el punto de equivalencia. En este punto, la cantidad de moles de iones hidronio (H+) provenientes del ácido es exactamente igual a la cantidad de moles de iones hidróxido (OH-) provenientes de la base. Como se menciona en la información proporcionada, en el punto de equivalencia, todos los iones H+ y OH- reaccionan para formar agua. Esto significa que la solución resultante no contiene un exceso de iones H+ ni de iones OH- que provengan de los reactivos originales. La única fuente significativa de H+ y OH- en la solución es la autoionización del agua (H2O ⇌ H+ + OH-), que produce concentraciones iguales de ambos iones, resultando en un pH de 7 a 25°C. Este es un resultado distintivo y una de las características clave de las titulaciones entre ácidos y bases fuertes.
Antes del Punto de Equivalencia: Exceso de Ácido o Base
El pH de la mezcla no siempre es 7. Depende de las cantidades relativas de ácido y base mezcladas. Si se añade una cantidad de base fuerte insuficiente para neutralizar completamente el ácido fuerte presente, la solución seguirá siendo ácida. El pH estará determinado por el exceso de iones H+ que no han reaccionado. Para calcularlo, primero determinamos los moles iniciales de H+ y OH-. Luego, restamos los moles de OH- a los moles de H+ para encontrar los moles de H+ en exceso. Finalmente, dividimos los moles de H+ en exceso por el volumen total de la mezcla para obtener la concentración molar de H+ y, a partir de ahí, el pH.
De manera análoga, si se añade una cantidad de ácido fuerte insuficiente para neutralizar completamente la base fuerte, la solución será básica. El pH estará determinado por el exceso de iones OH-. El procedimiento de cálculo es similar: determinar moles iniciales de H+ y OH-, restar los moles de H+ a los moles de OH- para encontrar los moles de OH- en exceso, dividir por el volumen total para obtener la concentración de OH-, calcular el pOH y luego el pH.
Después del Punto de Equivalencia: Exceso de Base o Ácido
Una vez que se ha superado el punto de equivalencia, es decir, se ha añadido un exceso de base fuerte a un ácido fuerte (o viceversa), el pH de la solución reflejará este exceso. Si hay un exceso de base fuerte, la solución se volverá marcadamente básica, y el pH aumentará por encima de 7. Si se añadió un exceso de ácido fuerte a una base fuerte, la solución se volverá marcadamente ácida, y el pH disminuirá por debajo de 7. Los cálculos se realizan de la misma manera que antes del punto de equivalencia, identificando el ion en exceso y su concentración final en el volumen total.
Mezclas de Dos Ácidos Fuertes
Cuando se mezclan dos ácidos fuertes, la situación es más sencilla que la neutralización. Ambos ácidos se disocian completamente en solución acuosa, liberando iones H+. Dado que ambos son fuertes, no se perturba el equilibrio de disociación de ninguno de ellos. La concentración total de iones H+ en la mezcla será simplemente la suma de los iones H+ aportados por cada ácido, ajustada por el volumen final.
La información proporcionada establece una fórmula útil para este escenario utilizando la normalidad (N) y el volumen (V):
Si se mezcla un volumen V1 de una solución de ácido fuerte de normalidad N1 con un volumen V2 de otra solución de ácido fuerte de normalidad N2, entonces:
- Número de moles equivalentes de H+ de la primera solución = N1V1
- Número de moles equivalentes de H+ de la segunda solución = N2V2
Si la normalidad final de la mezcla es N y el volumen final es V (donde V = V1 + V2), entonces el número total de moles equivalentes de H+ en la mezcla será:
NV = N1V1 + N2V2
A partir de esta ecuación, podemos despejar la normalidad final N:
N = (N1V1 + N2V2) / (V1 + V2)
Para ácidos monopróticos (aquellos que liberan un solo ion H+ por molécula, como HCl o HNO3), la normalidad es igual a la molaridad (N=M). Por lo tanto, la concentración final de iones H+ en la mezcla será igual a la normalidad final N. Una vez obtenida la concentración de H+, el pH se calcula como pH = -log[H+].
Ejemplo de Cálculo: Mezcla de Ácidos Fuertes
Supongamos que mezclamos 100 mL de HCl 0.1 N con 150 mL de HNO3 0.05 N.
- N1 = 0.1 N, V1 = 0.1 L
- N2 = 0.05 N, V2 = 0.15 L
Volumen total (V) = V1 + V2 = 0.1 L + 0.15 L = 0.25 L
Moles equivalentes de H+ del HCl = N1V1 = 0.1 N * 0.1 L = 0.01 moles eq.
Moles equivalentes de H+ del HNO3 = N2V2 = 0.05 N * 0.15 L = 0.0075 moles eq.
Normalidad final (N) = (0.01 + 0.0075) / 0.25 = 0.0175 / 0.25 = 0.07 N
Dado que ambos son ácidos monopróticos, [H+] = 0.07 M.
pH = -log(0.07) ≈ 1.15
Este cálculo demuestra cómo la concentración final de H+ es una ponderación de las concentraciones iniciales, lo que resulta en un pH más bajo (más ácido) al mezclar dos soluciones ácidas.

Mezclas de Dos Bases Fuertes
De manera completamente análoga a la mezcla de dos ácidos fuertes, cuando se combinan dos bases fuertes, ambas se disocian completamente, liberando iones OH-. La concentración total de iones OH- en la mezcla será la suma de los iones OH- aportados por cada base, ajustada por el volumen final.
Utilizando el mismo principio de normalidad y volumen:
Si se mezcla un volumen V1 de una solución de base fuerte de normalidad N1 con un volumen V2 de otra solución de base fuerte de normalidad N2:
- Número de moles equivalentes de OH- de la primera solución = N1V1
- Número de moles equivalentes de OH- de la segunda solución = N2V2
Si la normalidad final de la mezcla es N y el volumen final es V (donde V = V1 + V2), entonces el número total de moles equivalentes de OH- en la mezcla será:
NV = N1V1 + N2V2
Y la normalidad final N será:
N = (N1V1 + N2V2) / (V1 + V2)
Para bases monohidroxílicas (aquellas que liberan un solo ion OH- por molécula, como NaOH o KOH), la normalidad es igual a la molaridad (N=M). Por lo tanto, la concentración final de iones OH- en la mezcla será igual a la normalidad final N. Una vez obtenida la concentración de OH-, se puede calcular el pOH como pOH = -log[OH-], y luego el pH usando la relación pH = 14 - pOH.
Ejemplo de Cálculo: Mezcla de Bases Fuertes
Consideremos la mezcla de 50 mL de NaOH 0.2 N con 75 mL de KOH 0.1 N.
- N1 = 0.2 N, V1 = 0.05 L
- N2 = 0.1 N, V2 = 0.075 L
Volumen total (V) = V1 + V2 = 0.05 L + 0.075 L = 0.125 L
Moles equivalentes de OH- del NaOH = N1V1 = 0.2 N * 0.05 L = 0.01 moles eq.
Moles equivalentes de OH- del KOH = N2V2 = 0.1 N * 0.075 L = 0.0075 moles eq.
Normalidad final (N) = (0.01 + 0.0075) / 0.125 = 0.0175 / 0.125 = 0.14 N
Dado que ambas son bases monohidroxílicas, [OH-] = 0.14 M.
pOH = -log(0.14) ≈ 0.85
pH = 14 - pOH = 14 - 0.85 = 13.15
Este resultado, un pH alto, es consistente con la mezcla de dos soluciones básicas.
Consideraciones Importantes al Realizar Mezclas
Si bien los cálculos para ácidos y bases fuertes son directos, hay algunas consideraciones prácticas importantes:
- Temperatura: La constante del producto iónico del agua (Kw) es dependiente de la temperatura. Aunque el pH de 7 es neutro a 25°C, a otras temperaturas el punto de neutralidad puede variar ligeramente. Nuestros cálculos asumen una temperatura estándar, generalmente 25°C.
- Volumen Final: Es crucial considerar que el volumen final de la mezcla es la suma de los volúmenes individuales, asumiendo que no hay cambios significativos de volumen al mezclar (lo cual es una buena aproximación para soluciones diluidas).
- Precisión: La precisión de los cálculos del pH depende directamente de la precisión de las mediciones de concentración y volumen de las soluciones iniciales.
- Definición de Normalidad: Es importante recordar que la normalidad (N) se refiere a la concentración de equivalentes por litro. Para ácidos o bases que pueden liberar más de un H+ o OH- por molécula (polipróticos o polihidroxílicos), la normalidad será un múltiplo de la molaridad. Por ejemplo, para H2SO4 (ácido sulfúrico), que es diprótico, 1 M de H2SO4 es 2 N. En los ejemplos anteriores, asumimos que los ácidos y bases son monopróticos/monohidroxílicos para que N=M, simplificando la interpretación directa de [H+] o [OH-] desde la normalidad.
Tabla Comparativa de Mezclas de Ácidos y Bases Fuertes
Para resumir los escenarios discutidos, la siguiente tabla ofrece una visión rápida de los resultados esperados del pH:
| Tipo de Mezcla | Reacción Química Principal | pH Esperado en el Punto de Equivalencia / Concentración Final | Consideraciones Clave |
|---|---|---|---|
| Ácido Fuerte + Base Fuerte | Neutralización (H+ + OH- → H2O) | pH = 7 (solo en el punto de equivalencia) | Depende del exceso de reactivo si no es el punto de equivalencia. |
| Ácido Fuerte + Ácido Fuerte | Adición de H+ | pH < 7 (más ácido) | Suma de moles de H+, luego concentración en volumen total. |
| Base Fuerte + Base Fuerte | Adición de OH- | pH > 7 (más básico) | Suma de moles de OH-, luego concentración en volumen total (calcular pOH y luego pH). |
Preguntas Frecuentes (FAQ)
¿Siempre es 7 el pH en el punto de equivalencia de un ácido fuerte con una base fuerte?
Sí, a 25°C, el pH de 7 es la característica distintiva del punto de equivalencia en la titulación de un ácido fuerte con una base fuerte. Esto se debe a que los productos de la reacción son una sal neutra (si el catión de la base y el anión del ácido no hidrolizan) y agua, y la autoionización del agua es la única fuente significativa de iones H+ y OH-.
¿Qué sucede si mezclo un ácido fuerte con un ácido débil?
La mezcla de un ácido fuerte con un ácido débil es más compleja. El ácido fuerte se disocia completamente y suprime la disociación del ácido débil (efecto del ion común). El pH de la solución resultante estará predominantemente determinado por la concentración del ácido fuerte, aunque la contribución del ácido débil, aunque menor, podría tener un impacto si la concentración del ácido débil es muy alta o si el ácido fuerte es muy diluido. Los cálculos requieren considerar el equilibrio del ácido débil.
¿La temperatura afecta el pH de las mezclas?
Sí, la temperatura afecta el pH. La constante de autoionización del agua (Kw) es sensible a la temperatura. A temperaturas más altas, Kw aumenta, lo que significa que el agua se autoioniza más, y el pH de una solución neutra se desplaza ligeramente de 7. Sin embargo, para la mayoría de los cálculos y aplicaciones a temperatura ambiente, el valor de 7 para la neutralidad es una excelente aproximación.
¿Cómo se mide el pH en la práctica?
En la práctica, el pH se mide comúnmente utilizando un pH-metro, que es un instrumento electrónico con un electrodo sensible a los iones H+. También se pueden usar indicadores de pH, que son colorantes orgánicos que cambian de color en un rango específico de pH, o papel de pH, que contiene una mezcla de indicadores para dar una estimación rápida del pH.
¿Por qué se usa la normalidad en algunos cálculos y la molaridad en otros?
La normalidad es útil en cálculos de reacciones ácido-base porque se refiere a la concentración de equivalentes reactivos (moles de H+ o OH-). Esto simplifica el hecho de que 1 equivalente de ácido reacciona con 1 equivalente de base. La molaridad se refiere a moles de soluto por litro de solución. Para ácidos y bases monopróticos/monohidroxílicos, la normalidad y la molaridad son numéricamente iguales. Sin embargo, para ácidos polipróticos (ej., H2SO4) o bases polihidroxílicas (ej., Ca(OH)2), la normalidad es un múltiplo entero de la molaridad (N = n * M, donde n es el número de H+ o OH- liberados por molécula). En el contexto de este artículo, donde se discuten ácidos y bases fuertes, el uso de la normalidad facilita la suma directa de los equivalentes de H+ u OH-.
Conclusión
Comprender el comportamiento del pH en mezclas de ácidos y bases fuertes es un pilar fundamental en química. La capacidad de predecir si una solución será ácida, básica o neutra después de una mezcla es esencial para el diseño de experimentos, la formulación de productos y la resolución de problemas en diversos campos. Ya sea la perfecta neutralización que produce un pH de 7 en el punto de equivalencia de un ácido fuerte y una base fuerte, o la simple adición de concentraciones de H+ o OH- al mezclar dos sustancias del mismo tipo, los principios subyacentes son claros y predecibles. Con los conocimientos y las fórmulas presentadas, ahora tienes las herramientas para abordar estos cálculos con confianza y precisión, desvelando el pH de cualquier combinación de ácidos y bases fuertes.
Si quieres conocer otros artículos parecidos a El pH en Mezclas de Ácidos y Bases Fuertes puedes visitar la categoría Química.