21/05/2022
El vinagre, un ingrediente humilde pero indispensable en nuestras cocinas, es mucho más que un simple condimento. Desde la antigüedad, ha sido valorado por sus propiedades conservantes y medicinales, y su papel en la gastronomía es innegable. Pero, ¿alguna vez te has preguntado qué lo hace tan especial o cómo se mide su característica principal: la acidez? La clave reside en su componente principal, el ácido acético, y su concentración es un factor determinante de su calidad, sabor y eficacia. Entender cómo se determina esta concentración no solo es fascinante desde una perspectiva científica, sino también crucial para productores, chefs y consumidores curiosos. Acompáñanos en este recorrido para desvelar los métodos y cálculos que nos permiten descifrar la verdadera potencia de este líquido sorprendente.
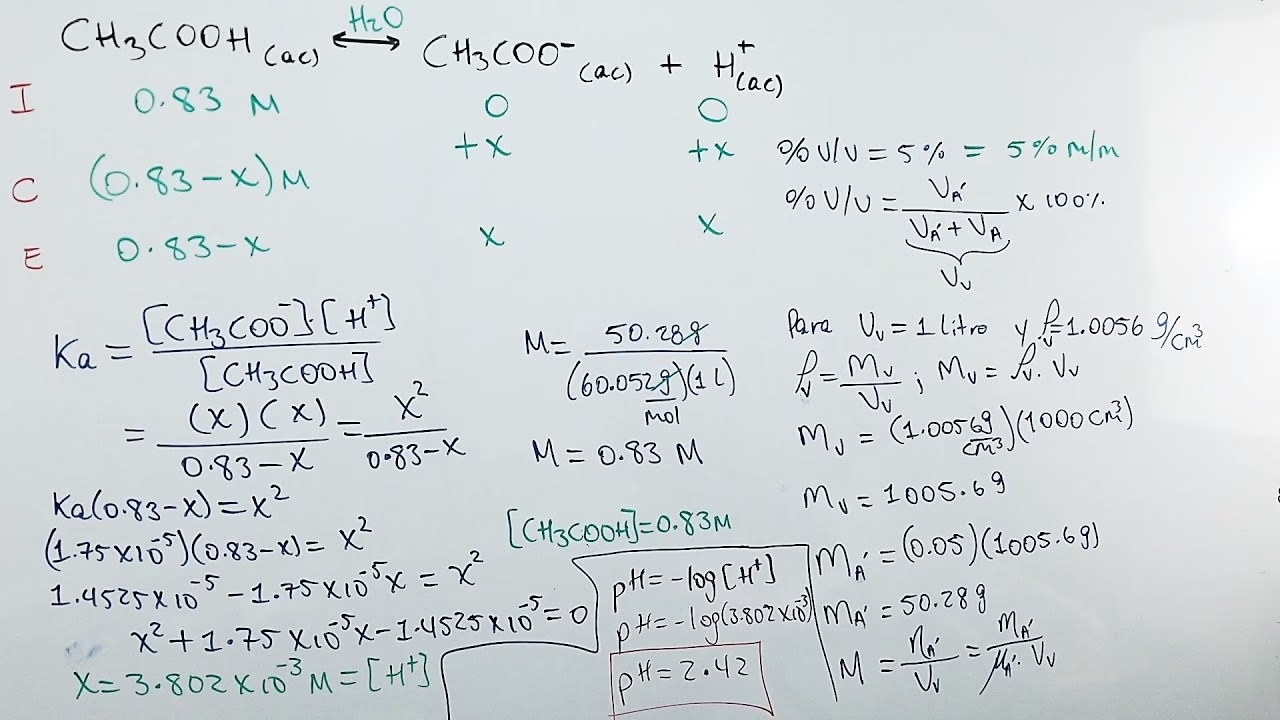
- El Ácido Acético y el Vinagre: Una Alianza Fundamental
- La Importancia de Conocer la Concentración de Ácido Acético
- Métodos Clave para Determinar la Concentración de Ácido Acético
- Factores que Influyen en la Concentración del Vinagre
- Tabla Comparativa: Concentraciones Típicas de Vinagre
- Preguntas Frecuentes (FAQ)
El Ácido Acético y el Vinagre: Una Alianza Fundamental
El vinagre es, en esencia, un líquido ácido obtenido a través de un proceso de doble fermentación. Inicialmente, los azúcares presentes en una fuente como el vino, la sidra o la malta son convertidos en alcohol por levaduras. Posteriormente, en presencia de oxígeno, una familia de bacterias conocidas como Acetobacter transforma ese alcohol en ácido acético, que es el componente que le confiere al vinagre su sabor agrio y sus propiedades conservantes. Esta transformación es un ejemplo clásico de bioconversión que ha sido aprovechado por la humanidad durante milenios.
La concentración de ácido acético es lo que define el “grado” o la “fuerza” de un vinagre. Los vinagres comerciales suelen contener entre un 5% y un 8% de ácido acético, aunque existen variedades especiales con concentraciones más altas o más bajas. Esta variabilidad subraya la importancia de poder medir con precisión su contenido para garantizar la consistencia del producto y su idoneidad para diferentes usos.
La Importancia de Conocer la Concentración de Ácido Acético
Determinar la concentración de ácido acético en el vinagre es fundamental por varias razones:
- Calidad y Consistencia: Para los productores, asegurar que cada lote de vinagre tenga la concentración deseada es vital para mantener la calidad del producto y la satisfacción del consumidor. Un vinagre con una concentración inconsistente puede afectar el sabor de los alimentos o su capacidad de conservación.
- Usos Culinarios: La acidez influye directamente en el perfil de sabor de un plato. Un chef podría necesitar un vinagre con una acidez específica para lograr el equilibrio perfecto en una vinagreta o una marinada.
- Preservación de Alimentos: El ácido acético es un agente conservador natural. Su concentración adecuada es crítica para inhibir el crecimiento de microorganismos y prolongar la vida útil de encurtidos, salsas y otros alimentos.
- Aplicaciones Industriales y Domésticas: Más allá de la cocina, el vinagre se utiliza como limpiador, desinfectante y hasta en horticultura. La efectividad en estas aplicaciones a menudo depende directamente de la concentración de ácido acético.
Métodos Clave para Determinar la Concentración de Ácido Acético
Existen principalmente dos enfoques interconectados para determinar la concentración de ácido acético en el vinagre: la volumetría ácido-base y el cálculo porcentual basado en los resultados de esta. Ambos métodos son pilares en la química analítica y se complementan para ofrecer una medida precisa.
Método 1: La Volumetría Ácido-Base (Titulación)
La volumetría ácido-base, comúnmente conocida como titulación, es una técnica analítica que permite determinar la concentración de una sustancia (en este caso, el ácido acético) reaccionándola con una solución de concentración conocida (un reactivo valorado o titulante). En el caso del vinagre, se utiliza una base fuerte, como el hidróxido de sodio (NaOH), de concentración conocida, para neutralizar el ácido acético.
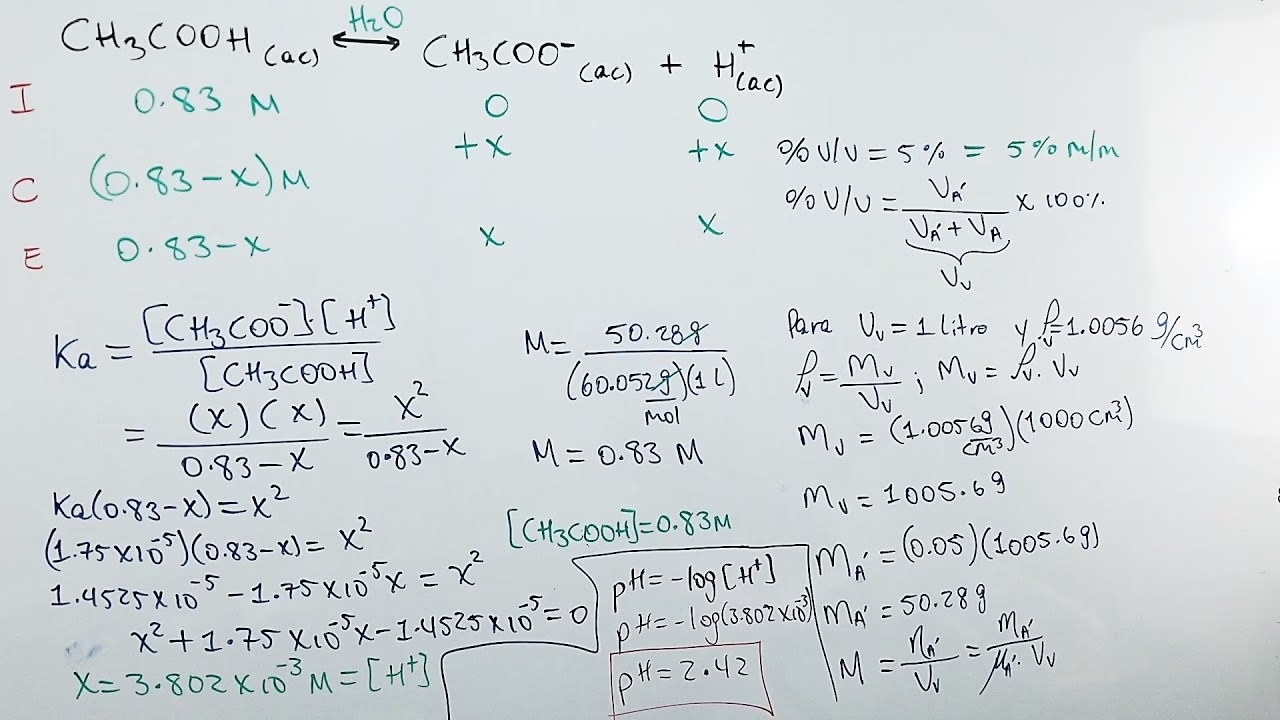
Materiales Necesarios para la Titulación:
- Matraz Erlenmeyer: Recipiente donde se realiza la reacción.
- Bureta: Instrumento de vidrio graduado para dispensar el titulante con precisión.
- Pipeta volumétrica: Para medir con exactitud el volumen de la muestra de vinagre.
- Probeta o vaso de precipitados: Para medir el agua destilada.
- Solución de Hidróxido de Sodio (NaOH) estandarizada: El titulante, cuya concentración es conocida con alta precisión (por ejemplo, 0.1 M).
- Fenolftaleína: Un indicador ácido-base.
- Agua destilada: Para diluir la muestra.
Procedimiento Detallado de Titulación:
- Preparación de la Muestra: Introduzca exactamente 3 ml de la muestra de vinagre comercial en un matraz Erlenmeyer. Es crucial usar una pipeta volumétrica para esta medición, ya que la precisión es clave.
- Dilución: Diluya el vinagre añadiendo aproximadamente 50 ml de agua destilada al matraz. La dilución ayuda a que el cambio de color del indicador sea más notorio y a que la titulación sea más manejable, sin afectar la cantidad total de ácido acético presente.
- Adición del Indicador: Añada 3 gotas de fenolftaleína a la solución en el matraz. La fenolftaleína es incolora en soluciones ácidas y se vuelve rosa brillante en soluciones básicas.
- Titulación: Llene la bureta con la solución estandarizada de NaOH. Anote el volumen inicial en la bureta. Gotee lentamente la solución de NaOH en el matraz Erlenmeyer, agitando constantemente la mezcla. A medida que la base se añade, neutralizará el ácido acético.
- Punto Final: Continúe añadiendo el NaOH gota a gota hasta que la solución en el matraz cambie de incolora a un rosa pálido que persista durante al menos 30 segundos. Este es el punto final de la titulación, que indica que todo el ácido acético ha sido neutralizado. Anote el volumen final de NaOH en la bureta.
- Registro de Datos: Calcule el volumen de NaOH utilizado restando el volumen inicial del volumen final en la bureta.
El Rol de la Fenolftaleína:
La fenolftaleína es un indicador muy utilizado en este tipo de volumetría. Su funcionamiento se basa en un cambio de color abrupto cerca del punto de equivalencia de la reacción, que es el punto en el que la cantidad de base añadida es estequiométricamente equivalente a la cantidad de ácido presente en la muestra. Para el ácido acético (un ácido débil) y el hidróxido de sodio (una base fuerte), el punto de equivalencia ocurre en un pH ligeramente superior a 7, donde la fenolftaleína cambia de incoloro a rosa, haciendo que sea un indicador ideal para esta reacción.
Método 2: Cálculo del Porcentaje de Ácido Acético
Una vez que se ha realizado la titulación y se ha determinado el volumen de base necesario para neutralizar el ácido acético, se puede proceder a calcular el porcentaje de ácido acético en el vinagre. La fórmula general es:
Porcentaje de ácido acético = (masa de ácido acético / masa de vinagre) x 100
Paso a Paso para el Cálculo a Partir de la Titulación:
Para aplicar esta fórmula, necesitamos transformar los datos de la titulación en la masa de ácido acético y la masa de la muestra de vinagre. Aquí te explicamos cómo:
- Calcular los Moles de Base Utilizados:
Utilice la molaridad (concentración) conocida de la solución de NaOH y el volumen que se gastó durante la titulación.
Moles de NaOH = Molaridad de NaOH (mol/L) x Volumen de NaOH gastado (L)
Ejemplo: Si usó 0.025 L (25 ml) de NaOH 0.1 M:
Moles de NaOH = 0.1 mol/L x 0.025 L = 0.0025 moles
- Calcular los Moles de Ácido Acético:
La reacción entre el ácido acético (CH3COOH) y el hidróxido de sodio (NaOH) es una reacción 1:1. Esto significa que un mol de NaOH neutraliza un mol de CH3COOH.
CH3COOH (aq) + NaOH (aq) → CH3COONa (aq) + H2O (l)
Por lo tanto, los moles de ácido acético en la muestra son iguales a los moles de NaOH utilizados.
Moles de CH3COOH = Moles de NaOH = 0.0025 moles
- Calcular la Masa de Ácido Acético:
Para convertir los moles de ácido acético a masa, necesitamos su masa molar. La masa molar del ácido acético (CH3COOH) es aproximadamente 60.05 g/mol (C=12.01, H=1.01, O=16.00).

¿Qué sucede durante la reacción de NaOH + Vinagre? \u2013 el vinagre dona un protón al ion hidróxido y actúa como ácido. El ion hidróxido acepta un protón y actúa como base. Conclusiones: La fenolftaleína es un indicador que comienza a tornarse rosa en presencia de un básico. Masa de CH3COOH = Moles de CH3COOH x Masa Molar de CH3COOH
Ejemplo:
Masa de CH3COOH = 0.0025 mol x 60.05 g/mol = 0.150125 g
- Determinar la Masa de la Muestra de Vinagre:
Para obtener la masa de la muestra de vinagre, necesitamos su volumen inicial y su densidad. Si no se mide la densidad de su vinagre específico, se puede usar una densidad aproximada para el vinagre, que es ligeramente superior a la del agua (aproximadamente 1.01 g/mL).
Masa de vinagre = Volumen de vinagre (mL) x Densidad del vinagre (g/mL)
Ejemplo: Si se usaron 3 ml de vinagre con una densidad de 1.01 g/mL:
Masa de vinagre = 3 mL x 1.01 g/mL = 3.03 g
- Aplicar la Fórmula del Porcentaje:
Finalmente, sustituya los valores calculados en la fórmula del porcentaje.
Porcentaje de ácido acético = (Masa de CH3COOH / Masa de vinagre) x 100
Ejemplo:
Porcentaje de ácido acético = (0.150125 g / 3.03 g) x 100 = 4.95%
Este resultado hipotético indicaría que el vinagre tiene aproximadamente un 4.95% de ácido acético.
Factores que Influyen en la Concentración del Vinagre
La concentración de ácido acético en el vinagre puede variar debido a varios factores:
- La Materia Prima: El tipo de alcohol fermentado (vino, sidra, cereales) influye en la cantidad de alcohol disponible para la conversión y, por ende, en la concentración final de ácido acético.
- La "Madre del Vinagre": Esta es una masa gelatinosa compuesta por bacterias Acetobacter y celulosa. Su presencia es un signo de un proceso de fermentación acética saludable y activa. Si bien no afecta directamente la concentración una vez que el vinagre está embotellado, es crucial para la formación del ácido acético durante la producción. La ausencia de la "madre" puede ralentizar o impedir el inicio de la acetificación.
- Condiciones de Fermentación: Factores como la temperatura, la aireación y el tiempo de fermentación son críticos. Un ambiente óptimo para las bacterias Acetobacter resultará en una conversión más eficiente del alcohol a ácido acético.
- Almacenamiento: Aunque el vinagre es un producto estable, la exposición prolongada al aire puede permitir que las bacterias continúen su actividad, potencialmente alterando la concentración o la calidad si el sellado no es hermético.
Tabla Comparativa: Concentraciones Típicas de Vinagre
Aunque la mayoría de los vinagres comerciales se sitúan en el rango del 5-8% de ácido acético, existen variaciones dependiendo del tipo y del uso.
| Tipo de Vinagre | Rango Típico de Ácido Acético | Notas |
|---|---|---|
| Vinagre Blanco Destilado | 5% - 8% | Comúnmente usado para limpieza y encurtidos debido a su sabor neutro y alta acidez. |
| Vinagre de Manzana | 5% - 6% | Popular por sus supuestos beneficios para la salud y su sabor afrutado. |
| Vinagre de Vino (Tinto/Blanco) | 5% - 7% | Derivado de vinos, ideal para vinagretas y aderezos. |
| Vinagre Balsámico | 4% - 6% | Más complejo en sabor, a menudo envejecido, con una acidez percibida más suave. |
| Vinagre de Arroz | 4% - 4.5% | Más suave, común en la cocina asiática. |
| Vinagres de Limpieza Concentrados | 10% - 20% | No aptos para consumo, formulados específicamente para tareas de limpieza pesadas. |
Preguntas Frecuentes (FAQ)
¿Qué es la "madre del vinagre" y afecta la concentración?
La "madre del vinagre" es una biopelícula de bacterias Acetobacter y celulosa que se forma en la superficie de líquidos alcohólicos durante la producción de vinagre. Es un signo de una fermentación acética activa y saludable. Directamente, la presencia de la madre no altera la concentración de un vinagre ya producido y embotellado, pero es esencial para el proceso de conversión del alcohol en ácido acético. Su ausencia puede indicar que el proceso de fabricación se ha ralentizado o no ha comenzado adecuadamente.

¿Por qué es importante la dilución de la muestra antes de la titulación?
La dilución de la muestra de vinagre antes de la titulación con agua destilada no altera la cantidad total de ácido acético presente en la muestra original, solo reduce su concentración. Esto es importante por varias razones: primero, hace que el cambio de color del indicador, como la fenolftaleína, sea más nítido y fácil de observar, ya que la solución se vuelve menos coloreada y el punto final es más claro. Segundo, permite un uso más controlable del titulante y reduce la posibilidad de "pasarse" del punto final con una sola gota, lo que mejora la precisión de la titulación.
¿Puedo realizar esta prueba en casa sin equipo de laboratorio?
Si bien los principios básicos de la volumetría pueden entenderse, realizar una titulación precisa requiere equipo de laboratorio calibrado (buretas, pipetas volumétricas) y reactivos estandarizados. Los resultados obtenidos con materiales caseros serían aproximados y no tan fiables como los de un laboratorio. Sin embargo, se pueden encontrar kits de prueba de acidez simplificados en el mercado para uso doméstico que ofrecen una estimación razonable.
¿El porcentaje de ácido acético es el único indicador de calidad del vinagre?
No, si bien la concentración de ácido acético es un indicador clave de la fuerza y funcionalidad del vinagre, la calidad general de un vinagre, especialmente en el contexto culinario, también depende de otros factores. Estos incluyen la calidad de la materia prima (el tipo de vino o fruta utilizada), la presencia de otros compuestos aromáticos y de sabor que se desarrollan durante la fermentación y el envejecimiento, y la ausencia de impurezas o defectos. Un vinagre de alta calidad tiene un equilibrio entre acidez, aroma y sabor que va más allá de un simple porcentaje de ácido acético.
La capacidad de determinar la concentración de ácido acético en el vinagre es una demostración clara de cómo los principios de la química analítica se aplican a productos cotidianos. Ya sea para garantizar la calidad en la industria alimentaria o para satisfacer la curiosidad en el hogar, la volumetría ácido-base y el cálculo porcentual ofrecen un camino preciso para descifrar la potencia de este líquido esencial. Comprender estos métodos no solo nos dota de un conocimiento valioso, sino que también nos permite apreciar más profundamente la ciencia detrás de los alimentos que consumimos.
Si quieres conocer otros artículos parecidos a Descifrando el Vinagre: Cómo Medir su Acidez puedes visitar la categoría Cálculos.
