14/06/2025
En el vasto y fascinante mundo de la química, las soluciones son omnipresentes. Desde el café que bebes por la mañana hasta los medicamentos que salvan vidas, o los procesos industriales más complejos, todos implican la disolución de una sustancia en otra. Pero, ¿qué ocurre si necesitas saber con precisión cuánto de esa sustancia principal, el soluto, está presente en tu mezcla? Este es un desafío común que, afortunadamente, tiene soluciones claras y metódicas.

Comprender cómo calcular la cantidad de soluto es una habilidad fundamental no solo para estudiantes y profesionales de la química, sino también para cualquiera que trabaje con formulaciones, preparaciones o análisis de sustancias. Te permitirá controlar la calidad de tus productos, asegurar la eficacia de tus reacciones o simplemente entender mejor lo que estás consumiendo. En este artículo, desglosaremos las definiciones clave y te guiaremos a través de los métodos más comunes y efectivos para encontrar esa escurridiza cantidad de soluto, sin importar la concentración o el tipo de solución.
- ¿Qué son el Soluto, el Solvente y la Solución? Conceptos Fundamentales
- ¿Por Qué es Crucial Calcular la Cantidad de Soluto?
- Métodos para Calcular la Cantidad de Soluto
- Consideraciones Importantes al Calcular Soluto
- Tabla Comparativa de Fórmulas para Calcular Soluto
- Preguntas Frecuentes (FAQ)
- Conclusión
¿Qué son el Soluto, el Solvente y la Solución? Conceptos Fundamentales
Antes de sumergirnos en los cálculos, es crucial tener una base sólida de los términos que utilizaremos:
- Solución: Es una mezcla homogénea de dos o más sustancias. Esto significa que sus componentes están distribuidos uniformemente, de modo que no se pueden distinguir a simple vista. Piensa en el agua con azúcar disuelta: no puedes ver el azúcar una vez que se ha disuelto completamente.
- Solvente: Es el componente de la solución que se encuentra en mayor proporción y que disuelve al otro u otros componentes. Es el medio en el que se dispersa el soluto. El solvente más común y versátil es el agua, conocida como el 'solvente universal'.
- Soluto: Es el componente de la solución que se encuentra en menor proporción y que se disuelve en el solvente. Es la sustancia que se dispersa en el medio. En la solución de agua con azúcar, el azúcar es el soluto.
La concentración de una solución es una medida de la cantidad de soluto disuelto en una cantidad dada de solvente o de solución. Expresar la concentración nos permite cuantificar la composición de una mezcla y es el punto de partida para determinar la cantidad de soluto.
¿Por Qué es Crucial Calcular la Cantidad de Soluto?
Conocer la cantidad de soluto es vital en innumerable campos:
- Laboratorios de Química y Biología: Para preparar soluciones con concentraciones exactas para experimentos, análisis o síntesis.
- Industria Farmacéutica: Asegurar la dosis correcta de un principio activo en un medicamento.
- Producción de Alimentos y Bebidas: Controlar el dulzor, la acidez o la cantidad de conservantes.
- Tratamiento de Aguas: Monitorear la presencia de contaminantes o la efectividad de los tratamientos.
- Agricultura: Preparar soluciones nutritivas o pesticidas con la concentración adecuada.
- Medicina: Administrar soluciones intravenosas o determinar niveles de sustancias en fluidos corporales.
Un cálculo erróneo puede llevar a resultados inexactos, productos defectuosos, o incluso, en casos extremos, consecuencias perjudiciales para la salud. La precisión es, por tanto, una prioridad.
Métodos para Calcular la Cantidad de Soluto
La forma en que calculamos la cantidad de soluto depende de cómo se exprese la concentración de la solución. A continuación, exploraremos los métodos más comunes.
1. A partir de Porcentajes de Concentración
Los porcentajes son una forma muy común y sencilla de expresar la concentración. Existen tres tipos principales:
a) Porcentaje Masa/Masa (% m/m o % p/p)
Indica los gramos de soluto por cada 100 gramos de solución.
Fórmula:% m/m = (masa de soluto / masa de solución) * 100
Para calcular la masa de soluto, se despeja la fórmula:
Masa de soluto = (% m/m / 100) * Masa de solución
Ejemplo: Tienes 500 g de una solución de NaCl al 15% m/m. ¿Cuántos gramos de NaCl hay?
- Masa de soluto = (15 / 100) * 500 g
- Masa de soluto = 0.15 * 500 g
- Masa de soluto = 75 g de NaCl
b) Porcentaje Volumen/Volumen (% v/v)
Indica los mililitros de soluto por cada 100 mililitros de solución. Usado comúnmente para soluciones líquido-líquido.
Fórmula:% v/v = (volumen de soluto / volumen de solución) * 100
Para calcular el volumen de soluto:
Volumen de soluto = (% v/v / 100) * Volumen de solución
Ejemplo: Se tienen 2 litros (2000 mL) de una solución de alcohol etílico al 70% v/v. ¿Cuántos mL de alcohol hay?
- Volumen de soluto = (70 / 100) * 2000 mL
- Volumen de soluto = 0.70 * 2000 mL
- Volumen de soluto = 1400 mL de alcohol etílico
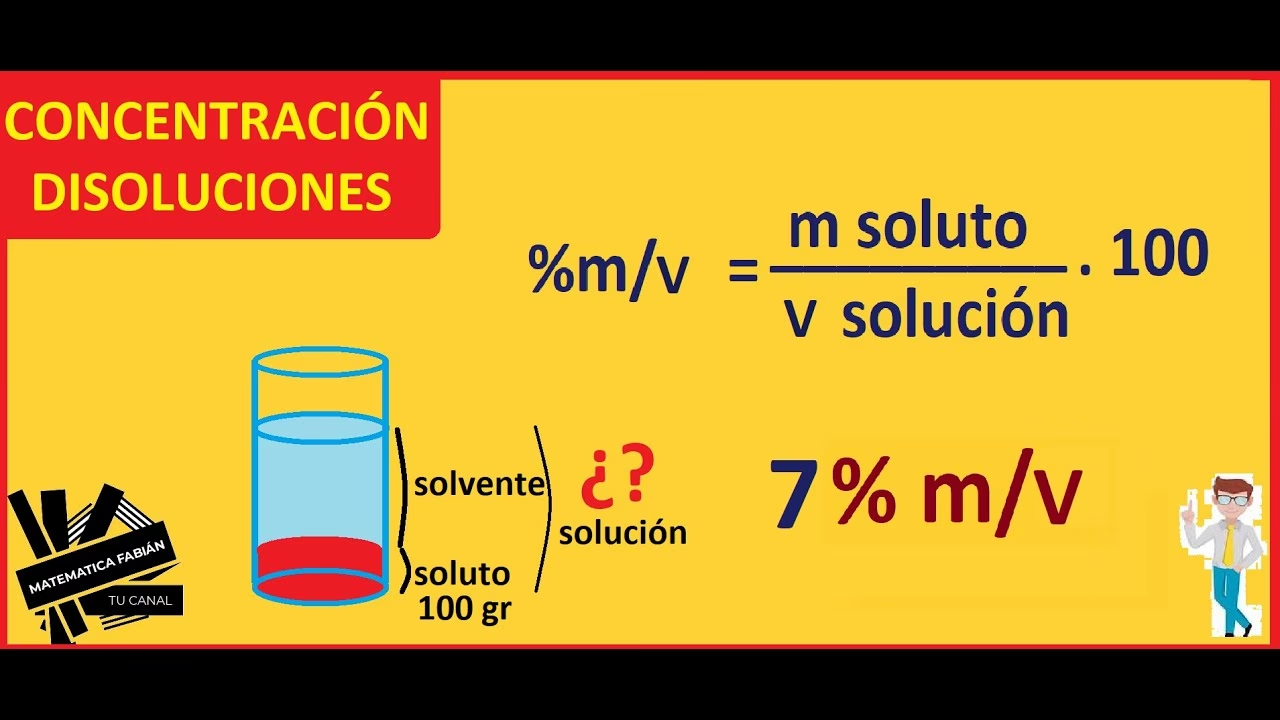
c) Porcentaje Masa/Volumen (% m/v o % p/v)
Indica los gramos de soluto por cada 100 mililitros de solución.
Fórmula:% m/v = (masa de soluto (g) / volumen de solución (mL)) * 100
Para calcular la masa de soluto:
Masa de soluto (g) = (% m/v / 100) * Volumen de solución (mL)
Ejemplo: Se preparó una solución de glucosa de 250 mL al 5% m/v. ¿Cuántos gramos de glucosa se usaron?
- Masa de soluto = (5 / 100) * 250 mL
- Masa de soluto = 0.05 * 250 mL
- Masa de soluto = 12.5 g de glucosa
2. A partir de la Molaridad (M)
La Molaridad (M) es una de las unidades de concentración más importantes y utilizadas en química. Se define como el número de moles de soluto por litro de solución.
Fórmula:M = moles de soluto / litros de solución
Para calcular los moles de soluto:
Moles de soluto = Molaridad (M) * Litros de solución
Una vez que tienes los moles de soluto, puedes convertirlos a masa (gramos) utilizando la masa molar (MM) del soluto (la masa en gramos de un mol de esa sustancia, que se calcula sumando las masas atómicas de todos los átomos en su fórmula química).
Masa de soluto (g) = Moles de soluto * Masa Molar (g/mol)
Pasos para calcular la masa de soluto a partir de la Molaridad:
- Asegúrate de que el volumen de la solución esté en litros. Si está en mL, divide por 1000.
- Calcula los moles de soluto multiplicando la Molaridad por el volumen en litros.
- Calcula la masa molar del soluto (si no la tienes).
- Multiplica los moles de soluto por la masa molar para obtener la masa en gramos.
Ejemplo: ¿Cuántos gramos de hidróxido de sodio (NaOH) hay en 300 mL de una solución 0.5 M de NaOH?
- Paso 1: Convertir volumen a litros: 300 mL = 0.3 L
- Paso 2: Calcular moles de NaOH: Moles = 0.5 mol/L * 0.3 L = 0.15 moles de NaOH
- Paso 3: Calcular la masa molar de NaOH: Na (22.99 g/mol) + O (16.00 g/mol) + H (1.01 g/mol) = 40.00 g/mol
- Paso 4: Calcular la masa de NaOH: Masa = 0.15 moles * 40.00 g/mol = 6.0 g de NaOH
3. A partir de la Molalidad (m)
La Molalidad (m) es otra unidad de concentración, definida como el número de moles de soluto por kilogramo de solvente. A diferencia de la Molaridad, la Molalidad no varía con la temperatura porque se basa en masas, no en volúmenes.

Fórmula:m = moles de soluto / kilogramos de solvente
Para calcular los moles de soluto:
Moles de soluto = Molalidad (m) * Kilogramos de solvente
Similar a la Molaridad, una vez que tienes los moles, los conviertes a masa usando la masa molar:
Masa de soluto (g) = Moles de soluto * Masa Molar (g/mol)
Pasos para calcular la masa de soluto a partir de la Molalidad:
- Asegúrate de que la masa del solvente esté en kilogramos. Si está en gramos, divide por 1000.
- Calcula los moles de soluto multiplicando la Molalidad por la masa del solvente en kilogramos.
- Calcula la masa molar del soluto (si no la tienes).
- Multiplica los moles de soluto por la masa molar para obtener la masa en gramos.
Ejemplo: ¿Cuántos gramos de urea (CH4N2O) se disolvieron en 500 g de agua para obtener una solución 0.2 molal?
- Paso 1: Convertir masa de solvente a kg: 500 g = 0.5 kg de agua
- Paso 2: Calcular moles de urea: Moles = 0.2 mol/kg * 0.5 kg = 0.1 moles de urea
- Paso 3: Calcular la masa molar de urea: C (12.01) + 4H (4*1.01) + 2N (2*14.01) + O (16.00) = 60.06 g/mol
- Paso 4: Calcular la masa de urea: Masa = 0.1 moles * 60.06 g/mol = 6.006 g de urea
4. A partir de Partes por Millón (ppm) y Partes por Billón (ppb)
Las Partes por millón (ppm) y partes por billón (ppb) son unidades de concentración utilizadas para soluciones extremadamente diluidas, donde la cantidad de soluto es muy pequeña en comparación con la cantidad total de solución. Son particularmente comunes en análisis ambientales, de agua y de contaminantes.
Fórmula general para ppm:ppm = (masa de soluto / masa de solución) * 10^6
Para calcular la masa de soluto a partir de ppm:
Masa de soluto = (ppm / 10^6) * Masa de solución
Si la solución es acuosa y diluida, la densidad de la solución es aproximadamente 1 g/mL, por lo que a menudo se asume que 1 kg de solución es aproximadamente 1 L de solución. En este caso, 1 ppm también puede interpretarse como 1 mg de soluto por litro de solución.
Fórmula general para ppb:ppb = (masa de soluto / masa de solución) * 10^9
Para calcular la masa de soluto a partir de ppb:
Masa de soluto = (ppb / 10^9) * Masa de solución
Ejemplo (ppm): Se detecta una concentración de 15 ppm de plomo en 2 kg de una muestra de agua. ¿Cuántos gramos de plomo hay?
- Paso 1: Convertir masa de solución a gramos: 2 kg = 2000 g
- Paso 2: Calcular la masa de soluto: Masa de soluto = (15 / 1,000,000) * 2000 g
- Masa de soluto = 0.000015 * 2000 g
- Masa de soluto = 0.03 g de plomo
Ejemplo (ppb): Una muestra de aire de 5000 kg contiene 20 ppb de dióxido de azufre (SO2). ¿Cuántos gramos de SO2 hay?
- Paso 1: Convertir masa de solución a gramos: 5000 kg = 5,000,000 g
- Paso 2: Calcular la masa de soluto: Masa de soluto = (20 / 1,000,000,000) * 5,000,000 g
- Masa de soluto = 0.000000020 * 5,000,000 g
- Masa de soluto = 0.1 g de SO2
Consideraciones Importantes al Calcular Soluto
- Unidades Consistentes: Siempre asegúrate de que todas las unidades en tu cálculo sean consistentes. Si la masa está en gramos, mantén los gramos; si el volumen está en litros, mantén los litros. Las conversiones son cruciales (por ejemplo, mL a L, g a kg).
- Masa Molar Correcta: Para cálculos que involucran moles (Molaridad, Molalidad), la masa molar del soluto debe ser calculada con precisión a partir de las masas atómicas de sus elementos. Un error aquí propagará un error en el resultado final.
- Temperatura: Las concentraciones basadas en volumen (como el % v/v y la Molaridad) son sensibles a los cambios de temperatura, ya que el volumen de una solución puede expandirse o contraerse. Las concentraciones basadas en masa (% m/m, Molalidad, ppm/ppb en masa) no se ven afectadas por la temperatura.
- Precisión y Exactitud: Utiliza instrumentos de medición precisos para el volumen y la masa de la solución y el solvente. Los errores en las mediciones iniciales afectarán la exactitud del cálculo del soluto.
- Naturaleza del Soluto: Algunos solutos pueden disociarse en iones en solución (electrolitos), mientras que otros no (no electrolitos). Para los cálculos de cantidad de soluto en masa o moles, esto no afecta directamente la cantidad total de la sustancia disuelta, pero sí es relevante para propiedades coligativas.
Tabla Comparativa de Fórmulas para Calcular Soluto
| Tipo de Concentración | Fórmula para Concentración | Fórmula para Calcular Soluto | Unidades Comunes |
|---|---|---|---|
| Porcentaje Masa/Masa (% m/m) | (masa soluto / masa solución) * 100 | (% m/m / 100) * masa solución | g soluto / g solución |
| Porcentaje Volumen/Volumen (% v/v) | (volumen soluto / volumen solución) * 100 | (% v/v / 100) * volumen solución | mL soluto / mL solución |
| Porcentaje Masa/Volumen (% m/v) | (masa soluto (g) / volumen solución (mL)) * 100 | (% m/v / 100) * volumen solución (mL) | g soluto / mL solución |
| Molaridad (M) | moles soluto / litros solución | M * litros solución (para moles) Moles * Masa Molar (para masa) | mol/L |
| Molalidad (m) | moles soluto / kg solvente | m * kg solvente (para moles) Moles * Masa Molar (para masa) | mol/kg |
| Partes por Millón (ppm) | (masa soluto / masa solución) * 10^6 | (ppm / 10^6) * masa solución | mg/kg o mg/L (en agua) |
| Partes por Billón (ppb) | (masa soluto / masa solución) * 10^9 | (ppb / 10^9) * masa solución | μg/kg o μg/L (en agua) |
Preguntas Frecuentes (FAQ)
¿Cuál es la diferencia principal entre soluto y solvente?
La diferencia principal radica en la proporción. El soluto es la sustancia que se disuelve y generalmente está en menor cantidad, mientras que el solvente es la sustancia que disuelve al soluto y está en mayor cantidad, formando el medio de la solución.
¿Por qué es tan importante la masa molar en estos cálculos?
La masa molar es crucial porque nos permite convertir entre la masa de una sustancia (que podemos medir con una balanza) y la cantidad de sustancia en moles. Dado que muchas unidades de concentración (como la Molaridad y la Molalidad) se definen en términos de moles de soluto, la masa molar es el puente indispensable para obtener la masa real del soluto.
¿Siempre se puede calcular el soluto de la misma manera?
No, la forma de calcular el soluto depende directamente de la unidad de concentración en la que se te proporciona la información de la solución. Por ejemplo, si tienes una concentración en % m/m, usarás una fórmula diferente a si la tienes en Molaridad. Es fundamental identificar la unidad de concentración dada para aplicar la fórmula correcta.
¿Qué pasa si la solución es muy diluida?
Para soluciones muy diluidas, donde la cantidad de soluto es extremadamente pequeña, se suelen utilizar unidades de concentración como Partes por millón (ppm) o Partes por billón (ppb). Estas unidades hacen que los números sean más manejables y comprensibles que usar porcentajes o Molaridad que resultarían en valores muy bajos y con muchos decimales.
¿Cómo sé qué fórmula de concentración usar para calcular el soluto?
La elección de la fórmula depende de la información que ya tienes sobre la solución. Si conoces el porcentaje en masa, usa la fórmula de % m/m. Si conoces la Molaridad y el volumen, usa la fórmula de Molaridad. Siempre busca la unidad de concentración que te ha sido proporcionada para determinar el camino a seguir.
Conclusión
Calcular la cantidad de soluto es una habilidad esencial en el ámbito de la química y en numerosas disciplinas prácticas. Como hemos visto, no hay un único método, sino varias aproximaciones que dependen de cómo se exprese la concentración de la solución. Ya sea mediante porcentajes, Molaridad, Molalidad o Partes por millón, cada método tiene su lógica y sus pasos específicos.
Dominar estos cálculos te permitirá no solo resolver problemas teóricos, sino también aplicar tus conocimientos en situaciones reales, garantizando precisión y control en tus preparaciones. Recuerda siempre prestar atención a las unidades, comprender el significado de cada término y, sobre todo, practicar. Con esta guía, tienes las herramientas necesarias para desentrañar la composición de cualquier solución y determinar con confianza la cantidad de soluto que contiene.
Si quieres conocer otros artículos parecidos a Cálculo de Soluto: La Guía Esencial puedes visitar la categoría Química.