21/11/2022
El calcio es un mineral fundamental para la vida, conocido principalmente por su papel en la salud ósea y dental. Sin embargo, su influencia se extiende a innumerables procesos fisiológicos, desde la contracción muscular y la transmisión nerviosa hasta la coagulación sanguínea. Pero, ¿alguna vez te has preguntado cómo el nivel de acidez o alcalinidad, es decir, el pH, interactúa con este vital elemento? La relación entre el calcio y el pH es un campo de estudio crucial, especialmente en contextos biológicos y químicos, donde pequeñas variaciones pueden tener grandes consecuencias. Este artículo explorará no solo la complejidad del calcio en nuestro organismo y cómo el pH lo afecta, sino también las propiedades y usos de un compuesto clave: el hidróxido de calcio, una sustancia con un pH notablemente alcalino y aplicaciones sorprendentes en nuestra vida diaria.
Acompáñanos en este recorrido para entender cómo el calcio se comporta bajo diferentes condiciones de pH, la importancia de medir sus distintas formas en el cuerpo y cómo una sustancia tan básica como el hidróxido de calcio juega un papel tan versátil en diversos campos, desde la medicina hasta la alimentación y el arte.
- El Calcio en el Cuerpo Humano y su Relación con el pH
- Calcio Total vs. Calcio Iónico: Métodos de Detección y su Relevancia Clínica
- El pH del Hidróxido de Calcio, Ca(OH)₂: Una Base Fuerte para Múltiples Usos
- ¿Cómo Calcular el pH de Soluciones de Hidróxido de Calcio?
- Preguntas Frecuentes (FAQ)
- Conclusión
El Calcio en el Cuerpo Humano y su Relación con el pH
El calcio es el mineral más abundante en el cuerpo humano, con más del 99% almacenado en los huesos y dientes. La pequeña fracción restante, menos del 1%, circula en la sangre, donde se presenta en tres formas principales. Aproximadamente el 40% del calcio sanguíneo está unido a proteínas plasmáticas, principalmente la albúmina; cerca del 10% está unido a aniones como el citrato o el fosfato; y la mitad restante existe como calcio libre, conocido como calcio iónico (CaI).
El calcio iónico es, con diferencia, la forma biológicamente activa del mineral. Es el calcio que participa directamente en todas las funciones celulares críticas, lo que lo convierte en la medida más relevante del estado del calcio en el organismo. Sin embargo, la concentración de calcio iónico es altamente dependiente del pH de la sangre. En la práctica clínica, cuando se mide el calcio iónico en suero venoso, los valores se corrigen a un pH estándar de 7.4. Esto se debe a que las variaciones en el pH sanguíneo alteran la unión del calcio a la albúmina: en condiciones de acidosis (pH bajo), hay menos sitios disponibles en la albúmina para que el calcio se una, lo que aumenta la concentración de calcio iónico libre. Por el contrario, en alcalosis (pH alto), más calcio se une a la albúmina, reduciendo la cantidad de calcio iónico disponible. Esta sensibilidad al pH es crucial para la interpretación de los resultados de laboratorio y para entender el verdadero estado del calcio en un paciente.
Dada esta dependencia, una medición precisa del calcio iónico es fundamental en ciertas situaciones clínicas, especialmente cuando hay desequilibrios ácido-base. Por ejemplo, en pacientes con acidosis metabólica, el calcio iónico puede estar elevado incluso si el calcio total está dentro del rango normal. Comprender esta interacción es vital para diagnosticar y tratar afecciones relacionadas con el metabolismo del calcio.
Calcio Total vs. Calcio Iónico: Métodos de Detección y su Relevancia Clínica
La medición del calcio en sangre se realiza principalmente de dos maneras: como calcio total (CaT) o como calcio iónico (CaI). El calcio total mide la suma de todas las fracciones de calcio en la sangre (unido a proteínas, unido a aniones e ionizado), mientras que el calcio iónico mide únicamente la porción libre y biológicamente activa. Aunque el CaI es considerado el indicador más preciso del estado del calcio, su medición es más laboriosa y difícil de automatizar en comparación con el CaT. Esto ha llevado a un debate sobre cuál de las dos pruebas es más adecuada para el cribado rutinario de condiciones como la hipercalcemia (niveles elevados de calcio en sangre), especialmente en entornos de urgencias.

Un estudio reciente, realizado en un departamento de emergencias, comparó la eficacia del CaI y el CaT para identificar la hipercalcemia clínicamente relevante en pacientes ingresados. Los hallazgos sugirieron que el CaT es una prueba aceptable para el cribado de hipercalcemia en este contexto. El estudio encontró que, al usar CaT como método de cribado, muy pocos pacientes con hipercalcemia no reconocida previamente habrían sido pasados por alto, y no se produjo un número significativo de falsos positivos. Esto es particularmente relevante porque la medición del CaT es más accesible y menos costosa en muchos entornos clínicos.
Sin embargo, a pesar de la utilidad del CaT para el cribado general, el CaI sigue siendo preferido en situaciones clínicas específicas donde la precisión es primordial. Estas incluyen:
- Enfermedades del metabolismo del calcio, como el hiperparatiroidismo primario.
- Enfermedad renal crónica (ERC), donde las alteraciones en el pH y la albúmina son comunes.
- Pacientes con niveles bajos de albúmina (hipoalbuminemia), ya que el CaT podría subestimar el calcio activo.
- Ciertos tipos de cáncer, como el mieloma múltiple, donde las alteraciones del calcio son frecuentes y pueden ser complejas.
En resumen, mientras que el CaT puede servir como una herramienta de cribado eficaz y práctica, el CaI ofrece una visión más precisa del estado fisiológico del calcio, siendo indispensable en el manejo de casos complejos y en la confirmación de diagnósticos. La elección entre CaT y CaI a menudo depende del contexto clínico y de la disponibilidad de recursos.
Tabla Comparativa: Calcio Total (CaT) vs. Calcio Iónico (CaI)
| Característica | Calcio Total (CaT) | Calcio Iónico (CaI) |
|---|---|---|
| Definición | Medida de todas las formas de calcio en la sangre (unido a proteínas, aniones y libre). | Medida solo del calcio libre y biológicamente activo en la sangre. |
| Dependencia del pH | Menor influencia directa; la influencia es indirecta a través de la unión a proteínas. | Alta influencia; los valores se corrigen a un pH estándar (7.4) para una interpretación consistente. |
| Facilidad de Medición | Más fácil de realizar, se puede automatizar en laboratorios de rutina. | Más laborioso, requiere equipos específicos y es menos común en el cribado masivo. |
| Relevancia Clínica | Útil para el cribado general de hipercalcemia en situaciones agudas (ej. urgencias). | Considerado el indicador más preciso del estado del calcio; esencial en casos complejos. |
| Factores que Afectan | Principalmente la concentración de proteínas plasmáticas, especialmente la albúmina. | El pH sanguíneo, la concentración de proteínas y aniones. |
| Cuándo Preferirlo | Cribado rutinario, cuando no hay sospecha de alteraciones importantes del pH o proteínas. | Sospecha de enfermedades metabólicas del calcio, enfermedad renal crónica, niveles de albúmina anormales, o en pacientes críticos. |
El pH del Hidróxido de Calcio, Ca(OH)₂: Una Base Fuerte para Múltiples Usos
Más allá del calcio en el cuerpo, existe un compuesto inorgánico de calcio con un pH muy particular y de gran relevancia: el hidróxido de calcio, Ca(OH)₂. Este compuesto es conocido comúnmente como cal apagada o cal hidratada. Cuando se disuelve en agua, forma una solución alcalina que es ampliamente utilizada en diversas industrias y aplicaciones domésticas. El agua de cal, que es el nombre común de una solución acuosa saturada de hidróxido de calcio, es transparente e incolora, con un ligero olor a tierra y un sabor astringente/amargo. Su pH es notablemente alto, alcanzando un valor de 12.4. Esto lo clasifica como una base fuerte.
La preparación del agua de cal es sencilla: se mezcla hidróxido de calcio con agua y se retira el exceso de soluto no disuelto, por ejemplo, mediante filtración. Si se añade un exceso de hidróxido de calcio o si las condiciones ambientales cambian (como un aumento de temperatura), la solución puede volverse lechosa debido a la suspensión homogénea del exceso de hidróxido de calcio, lo que se conoce tradicionalmente como lechada de cal.
La naturaleza altamente básica del hidróxido de calcio le confiere una amplia gama de aplicaciones:
- Prueba de Dióxido de Carbono: Una de sus aplicaciones más conocidas en el ámbito escolar y de laboratorio es la prueba de dióxido de carbono. Cuando el CO₂ gaseoso burbujea a través del agua de cal, reacciona para formar carbonato de calcio insoluble (CaCO₃), lo que produce una solución lechosa. Esta reacción es fundamental para demostrar la presencia de CO₂.
- Industria: En la industria, el agua de cal se utiliza para limpiar gases residuales que contienen dióxido de azufre (SO₂), un contaminante tóxico. Este proceso, llamado sulfatación, atrapa el SO₂ como sulfito de calcio (CaSO₃), un precipitado sólido, ayudando a reducir la contaminación atmosférica.
- Tratamiento de Aguas: El hidróxido de calcio es un agente crucial en el tratamiento de aguas. Se emplea en el proceso de ablandamiento con cal para reducir la dureza del agua, eliminando iones de calcio y magnesio. También se utiliza como agente neutralizante en el tratamiento de aguas residuales no industriales debido a su alcalinidad.
- Arte: En la pintura al fresco (buon fresco), el agua de cal se usa como disolvente de color. Los pigmentos se mezclan con agua de cal y se aplican sobre yeso fresco, permitiendo que los colores se unan químicamente a la superficie a medida que el yeso se seca.
- Cuidado Personal y Aseo: Históricamente, el agua de cal se ha utilizado para tratar el cabello, endureciéndolo y decolorándolo. También se ha empleado como agente depilatorio debido a sus propiedades alcalinas que disuelven el pelo.
- Preparación de Alimentos: Una aplicación muy importante es en la preparación de maíz para tortillas y otros productos culinarios, mediante un proceso llamado nixtamalización. Este proceso, que implica cocer el maíz en una solución de agua de cal, hace que la niacina (Vitamina B3) esté nutricionalmente disponible y previene la pelagra, una enfermedad por deficiencia nutricional. En algunas culturas asiáticas, también se ha usado para conservar frutas como el caqui y eliminar su astringencia.
- Otros Usos: Los acuaristas marinos utilizan el hidróxido de calcio (conocido como Kalkwasser) como suplemento principal de calcio y alcalinidad para los acuarios de arrecife, ya que los corales necesitan carbonato de calcio para construir sus esqueletos. También se emplea en el curtido de cuero y en la fabricación de pergaminos.
La versatilidad del hidróxido de calcio, derivada de su fuerte naturaleza básica, lo convierte en un compuesto invaluable en una multitud de campos, destacando la importancia del pH en la química y sus aplicaciones prácticas.

¿Cómo Calcular el pH de Soluciones de Hidróxido de Calcio?
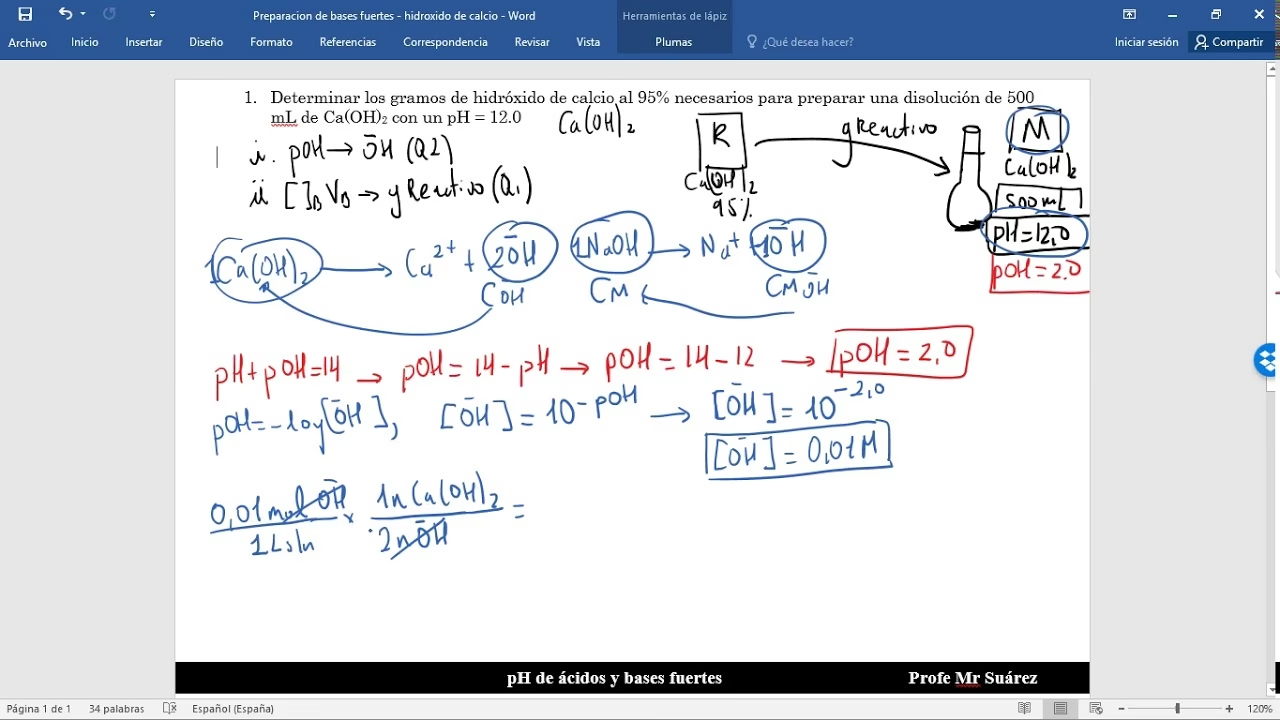
El cálculo del pH para una solución de hidróxido de calcio, Ca(OH)₂, es un proceso relativamente sencillo si se comprende su comportamiento en el agua. El hidróxido de calcio es una base fuerte, lo que significa que se disocia casi por completo en iones en una solución acuosa. La ecuación de disociación es la siguiente:
Ca(OH)₂(s) → Ca²⁺(aq) + 2OH⁻(aq)
Como puedes observar, por cada mol de hidróxido de calcio que se disuelve, se liberan dos moles de iones hidróxido (OH⁻). Esta característica es crucial para el cálculo del pH.
Los pasos para calcular el pH son los siguientes:
- Determinar la concentración molar de Ca(OH)₂: Primero, necesitas conocer la concentración de la solución de hidróxido de calcio en moles por litro (M).
- Calcular la concentración de iones OH⁻: Debido a que cada molécula de Ca(OH)₂ produce dos iones OH⁻, la concentración molar de OH⁻ será el doble de la concentración molar de Ca(OH)₂.
- Calcular el pOH: El pOH es una medida de la basicidad de una solución y se calcula utilizando la fórmula:
pOH = -log[OH⁻]
Donde [OH⁻] es la concentración molar de iones hidróxido. - Calcular el pH: Finalmente, el pH se obtiene a partir del pOH utilizando la relación fundamental entre pH y pOH en soluciones acuosas a 25°C:
pH = 14 - pOH
Por ejemplo, si tuvieras una solución de Ca(OH)₂ con una concentración de 0.01 M:
- La concentración de OH⁻ sería 2 * 0.01 M = 0.02 M.
- El pOH sería -log(0.02) ≈ 1.7.
- El pH sería 14 - 1.7 = 12.3.
Este ejemplo ilustra cómo la estequiometría de la disociación del hidróxido de calcio es fundamental para determinar su pH, confirmando su naturaleza altamente alcalina.
Preguntas Frecuentes (FAQ)
- ¿Cuál es el pH normal del calcio en la sangre?
- No existe un "pH del calcio" como tal. El calcio en la sangre, específicamente el calcio iónico, es sensible al pH de la sangre. Las mediciones de calcio iónico en suero se corrigen a un pH estándar de 7.4 para reflejar la concentración biológicamente activa en condiciones fisiológicas normales. El pH normal de la sangre humana es de 7.35 a 7.45.
- ¿Qué significa un pH de 12.4 para el hidróxido de calcio?
- Un pH de 12.4 indica que el hidróxido de calcio es una base muy fuerte. Esto significa que cuando se disuelve en agua, libera una alta concentración de iones hidróxido (OH⁻), lo que le confiere propiedades alcalinas pronunciadas y lo hace útil en una variedad de aplicaciones industriales y domésticas.
- ¿Por qué el pH afecta la medición del calcio ionizado en la sangre?
- El pH afecta la medición del calcio ionizado porque influye en la unión del calcio a las proteínas plasmáticas, principalmente la albúmina. Un pH más bajo (acidosis) reduce la unión del calcio a la albúmina, aumentando la cantidad de calcio iónico libre. Un pH más alto (alcalosis) aumenta esta unión, reduciendo el calcio iónico libre. Por esta razón, el calcio iónico se corrige a un pH estándar de 7.4 para una evaluación precisa.
- ¿Es el calcio total suficiente para detectar problemas de calcio en el cuerpo?
- Para el cribado general de hipercalcemia en situaciones de urgencia o de rutina, el calcio total (CaT) ha demostrado ser una herramienta aceptable y práctica. Sin embargo, en casos específicos como enfermedades metabólicas del calcio, enfermedad renal crónica, o alteraciones en los niveles de albúmina, el calcio iónico (CaI) es la medida preferida y más precisa, ya que refleja mejor la porción biológicamente activa del calcio.
- ¿Qué es la nixtamalización y cómo se relaciona con el hidróxido de calcio?
- La nixtamalización es un proceso tradicional de cocción y remojo de granos de maíz en una solución alcalina, comúnmente agua de cal (hidróxido de calcio). Este proceso mejora el valor nutricional del maíz, liberando niacina (vitamina B3) y mejorando la digestibilidad, además de prevenir la pelagra. También mejora la textura y el sabor para la elaboración de tortillas y otros productos.
Conclusión
La interacción entre el calcio y el pH es un concepto fundamental tanto en la bioquímica del cuerpo humano como en la química inorgánica aplicada. Hemos visto cómo el pH sanguíneo ejerce una influencia directa y crucial sobre la forma biológicamente activa del calcio, el calcio iónico, haciendo que su medición y corrección a un pH estándar sean indispensables en el ámbito clínico. Aunque el calcio total puede ser un método de cribado eficaz, el calcio iónico permanece como el patrón de oro para una evaluación precisa en situaciones complejas.
Por otro lado, el hidróxido de calcio, con su distintivo pH altamente alcalino de 12.4, demuestra la versatilidad de este mineral en el mundo exterior al cuerpo humano. Desde su uso en la detección de dióxido de carbono y el tratamiento de aguas residuales, hasta su papel en la nixtamalización de alimentos y las técnicas artísticas, el hidróxido de calcio es un testimonio de cómo las propiedades químicas de un compuesto pueden ser aprovechadas para una amplia gama de propósitos prácticos. Comprender el pH del calcio y sus compuestos no solo enriquece nuestro conocimiento de la química, sino que también subraya su importancia en la salud, la industria y nuestra vida cotidiana.
Si quieres conocer otros artículos parecidos a El pH del Calcio y su Impacto Vital puedes visitar la categoría Química.

