15/04/2026
En el vasto universo de la química, el concepto de pH es una de las herramientas más fundamentales para comprender la naturaleza de las soluciones acuosas. Desde la acidez de un jugo de limón hasta la alcalinidad de un limpiador doméstico, el pH nos indica cuán ácida o básica es una sustancia. Sin embargo, cuando hablamos de sales, especialmente aquellas formadas a partir de la reacción entre un ácido débil y una base débil, el cálculo de su pH puede parecer un desafío. A diferencia de las sales de ácidos o bases fuertes, cuyo comportamiento en solución es más predecible, las sales de componentes débiles introducen un fascinante equilibrio que rige su pH final. Este artículo desentrañará los misterios detrás de cómo calcular el pH de estas soluciones, explorando la fórmula clave y demostrando con un ejemplo práctico cómo la naturaleza intrínseca de los ácidos y bases influye en el resultado.
- Comprendiendo las Sales y la Hidrólisis
- El Concepto de pH
- Factores que Influyen en el pH: Ka, Kb y Kw
- Derivación y Fórmula para el pH de Sal de Ácido Débil/Base Débil
- Caso de Estudio: Cuando Ka = Kb
- ¿Qué Sucede Cuando Ka ≠ Kb?
- Aplicaciones Prácticas e Importancia
- Conceptos Erróneos Comunes
- Tabla Comparativa de Escenarios de pH (Hipótetica)
- Preguntas Frecuentes (FAQs)
- Conclusión
Comprendiendo las Sales y la Hidrólisis
Para comprender el pH de una sal, primero debemos entender qué es una sal y el proceso de hidrólisis. Una sal es un compuesto iónico que se forma a partir de la reacción de neutralización entre un ácido y una base. Cuando una sal se disuelve en agua, se disocia en sus iones constituyentes. Estos iones pueden interactuar con las moléculas de agua en un proceso llamado hidrólisis, alterando el equilibrio de iones H⁺ y OH⁻ en la solución y, por lo tanto, su pH.
Existen cuatro tipos principales de sales, clasificadas según la fuerza de sus ácidos y bases progenitores:
- Sal de ácido fuerte y base fuerte: Por ejemplo, NaCl. Sus iones no hidrolizan significativamente el agua, por lo que el pH de la solución es neutro (pH ≈ 7).
- Sal de ácido débil y base fuerte: Por ejemplo, CH₃COONa (acetato de sodio). El anión del ácido débil (CH₃COO⁻) hidroliza el agua para producir OH⁻, haciendo que la solución sea básica (pH > 7).
- Sal de ácido fuerte y base débil: Por ejemplo, NH₄Cl (cloruro de amonio). El catión de la base débil (NH₄⁺) hidroliza el agua para producir H⁺, haciendo que la solución sea ácida (pH < 7).
- Sal de ácido débil y base débil: Por ejemplo, CH₃COONH₄ (acetato de amonio). Este es el caso que nos ocupa. Tanto el anión del ácido débil como el catión de la base débil hidrolizan el agua. El pH final dependerá del equilibrio relativo entre las constantes de disociación del ácido (Ka) y la base (Kb).
Es esta última categoría la que presenta el escenario más interesante y a menudo el más complejo para el cálculo del pH, ya que ambos iones contribuyen a la acidez o basicidad de la solución.
El Concepto de pH
El pH es una medida de la acidez o basicidad de una solución. Se define como el logaritmo negativo de la concentración de iones de hidrógeno [H⁺] (o más precisamente, iones hidronio [H₃O⁺]).
pH = -log[H⁺]
Una escala de pH varía típicamente de 0 a 14. Un pH de 7 indica neutralidad, un pH menor de 7 indica acidez, y un pH mayor de 7 indica basicidad (o alcalinidad). La concentración de iones de hidrógeno y de iones hidroxilo (OH⁻) en agua pura a 25°C está en equilibrio, donde [H⁺] = [OH⁻] = 1.0 x 10⁻⁷ M, lo que resulta en un pH de 7. Este equilibrio se rige por la constante del producto iónico del agua, Kw.
Factores que Influyen en el pH: Ka, Kb y Kw
Para las sales de ácidos y bases débiles, las constantes de disociación de sus componentes son cruciales.
- Ka (Constante de Disociación Ácida): Mide la fuerza de un ácido débil. Cuanto mayor sea Ka, más fuerte será el ácido. Se define para una reacción genérica de disociación de un ácido HA:
HA(aq) ⇌ H⁺(aq) + A⁻(aq)Ka = ([H⁺][A⁻]) / [HA] - pKa: Es el logaritmo negativo de Ka (pKa = -logKa). Un pKa más bajo indica un ácido más fuerte.
- Kb (Constante de Disociación Básica): Mide la fuerza de una base débil. Cuanto mayor sea Kb, más fuerte será la base. Se define para una reacción genérica de disociación de una base B:
B(aq) + H₂O(l) ⇌ BH⁺(aq) + OH⁻(aq)Kb = ([BH⁺][OH⁻]) / [B] - pKb: Es el logaritmo negativo de Kb (pKb = -logKb). Un pKb más bajo indica una base más fuerte.
- Kw (Constante del Producto Iónico del Agua): Representa el producto de las concentraciones de iones H⁺ y OH⁻ en el agua. A 25°C, Kw es aproximadamente 1.0 x 10⁻¹⁴.
Kw = [H⁺][OH⁻] - pKw: Es el logaritmo negativo de Kw (pKw = -logKw). A 25°C, pKw es aproximadamente 14.
pKw = pKa + pKb(para pares ácido-base conjugados)
La interrelación entre estas constantes es lo que nos permitirá determinar el pH de la solución de una sal de ácido débil y base débil.
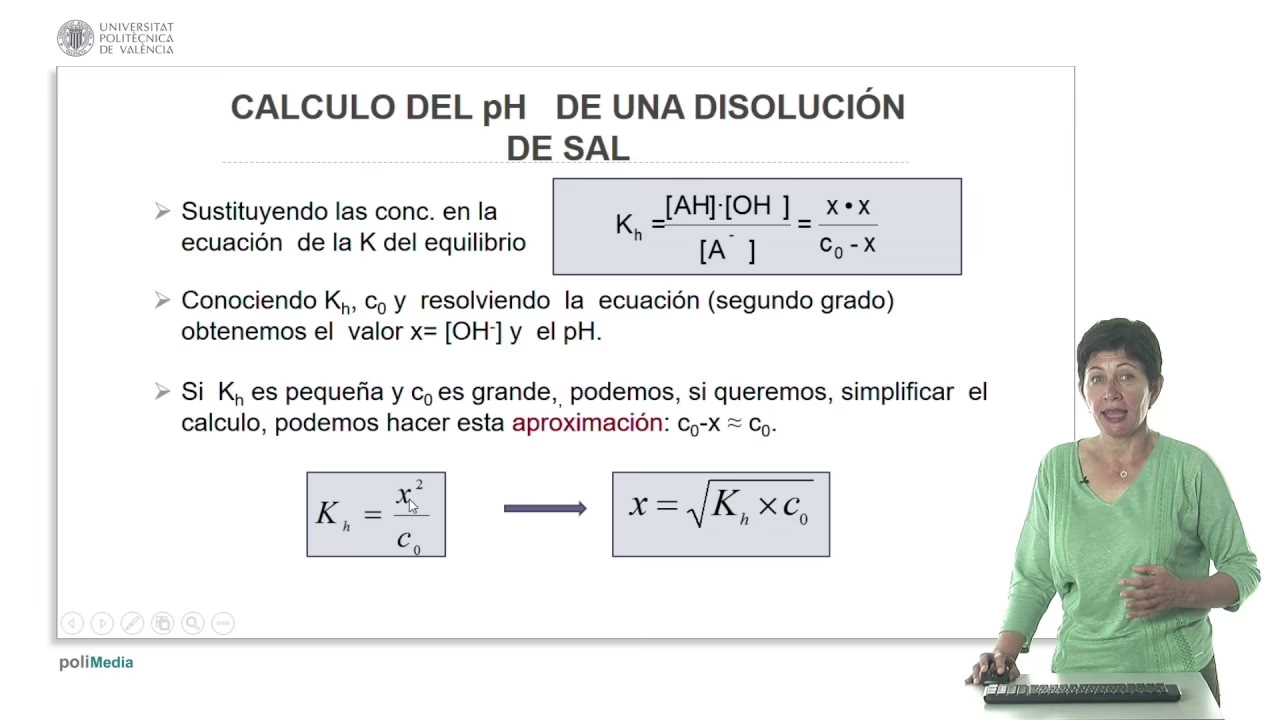
Derivación y Fórmula para el pH de Sal de Ácido Débil/Base Débil
Cuando una sal formada por un ácido débil (HA) y una base débil (BOH) se disuelve en agua, los iones resultantes (A⁻ y B⁺) pueden hidrolizar el agua. El anión A⁻ reacciona con el agua para producir OH⁻ (hidrólisis básica), y el catión B⁺ reacciona con el agua para producir H⁺ (hidrólisis ácida). El pH final de la solución dependerá de la magnitud relativa de estas dos hidrólisis.
La fórmula general para calcular el pH de una solución de una sal formada a partir de un ácido débil y una base débil es:
pH = 1/2 pKw + 1/2 pKa - 1/2 pKb
Analicemos cada término de la fórmula:
- 1/2 pKw: Este término representa la contribución de la autoionización del agua al pH. Dado que pKw es 14 a 25°C, este término base es 7, lo que indica el punto de neutralidad.
- 1/2 pKa: Este término refleja la fuerza del ácido débil del cual proviene el anión. Un pKa más bajo (ácido más fuerte) tiende a hacer la solución más ácida.
- -1/2 pKb: Este término refleja la fuerza de la base débil de la cual proviene el catión. Un pKb más bajo (base más fuerte) tiende a hacer la solución más básica. El signo negativo indica que una base más fuerte (menor pKb) compensará la acidez o impulsará la basicidad.
Es crucial recordar que esta fórmula es una aproximación y es más precisa para sales donde la concentración es moderada y las constantes Ka y Kb no son extremadamente pequeñas o grandes. Sin embargo, es una herramienta poderosa para entender el comportamiento general.
Caso de Estudio: Cuando Ka = Kb
Ahora, apliquemos la fórmula a un caso particular y muy ilustrativo: ¿Qué sucede con el pH de una solución de una sal formada a partir de un ácido débil y una base débil cuando sus constantes de disociación son iguales (Ka = Kb)? Este escenario es común en problemas de química y nos permite simplificar significativamente la fórmula general.
Vamos a seguir los pasos detallados:
Paso 1: Identificar la relación entre Ka y Kb
Se nos ha dado la condición de que Ka = Kb. Podemos denotar ambas constantes simplemente como 'K'.
Por lo tanto, si Ka = K, entonces pKa = -logK.
Y si Kb = K, entonces pKb = -logK.
Esto significa que pKa = pKb en este caso particular.
Paso 2: Sustituir pKa y pKb en la fórmula del pH
La fórmula general es:
pH = 1/2 pKw + 1/2 pKa - 1/2 pKbSustituyendo pKa y pKb por sus equivalentes en términos de 'K':
pH = 1/2 pKw + 1/2 (-logK) - 1/2 (-logK)O, más directamente, como pKa = pKb:
pH = 1/2 pKw + 1/2 pKa - 1/2 pKaPaso 3: Simplificar la ecuación
Observemos los términos relacionados con pKa y pKb:
+ 1/2 pKa - 1/2 pKaEstos dos términos son idénticos pero con signos opuestos, por lo que se cancelan entre sí.
Esto nos deja con una ecuación mucho más simple:
pH = 1/2 pKw + 0pH = 1/2 pKwPaso 4: Calcular pKw a 25°C
A una temperatura estándar de 25°C, el valor de pKw es universalmente aceptado como 14.
Sustituyendo este valor en la ecuación simplificada:
pH = 1/2 * 14pH = 7
Resultado Final
Por lo tanto, el pH de la solución de una sal de un ácido débil y una base débil, donde Ka = Kb a 25°C, es 7. Esto significa que la solución es neutra. Este resultado tiene sentido intuitivo: si la fuerza del componente ácido para hidrolizar el agua es exactamente igual a la fuerza del componente básico para hidrolizar el agua, sus efectos sobre el pH se anulan mutuamente, resultando en una solución neutra.
¿Qué Sucede Cuando Ka ≠ Kb?
Aunque el caso de Ka = Kb simplifica el cálculo a un pH de 7, es importante entender qué sucede cuando estas constantes no son iguales. La fórmula general pH = 1/2 pKw + 1/2 pKa - 1/2 pKb sigue siendo válida y nos da la clave.
- Si Ka > Kb (o pKa < pKb): Esto significa que el ácido débil es relativamente más fuerte que la base débil. En este caso, el componente ácido de la sal tendrá una mayor tendencia a hidrolizar el agua y producir iones H⁺, superando la capacidad del componente básico para producir OH⁻. El resultado será un pH < 7, es decir, la solución será ácida.
- Si Kb > Ka (o pKb < pKa): Esto significa que la base débil es relativamente más fuerte que el ácido débil. En esta situación, el componente básico de la sal tendrá una mayor tendencia a hidrolizar el agua y producir iones OH⁻, superando la capacidad del componente ácido para producir H⁺. El resultado será un pH > 7, es decir, la solución será básica.
Comprender esta relación es fundamental para predecir la naturaleza de la solución sin necesidad de realizar un cálculo exacto, solo comparando las magnitudes relativas de Ka y Kb.
Aplicaciones Prácticas e Importancia
El cálculo del pH de sales de ácidos y bases débiles no es solo un ejercicio académico; tiene profundas implicaciones en diversas áreas:
- Bioquímica y Biología: Muchos sistemas biológicos, como la sangre humana, utilizan sistemas amortiguadores (buffers) compuestos precisamente por ácidos débiles y sus bases conjugadas (sales) para mantener un pH constante, vital para el funcionamiento de enzimas y proteínas. La comprensión de cómo estas sales influyen en el pH es crucial.
- Farmacología: La solubilidad y la estabilidad de muchos medicamentos dependen críticamente del pH. Las formulaciones farmacéuticas a menudo contienen sales de ácidos o bases débiles para asegurar que el fármaco esté en su forma más efectiva y estable en el cuerpo.
- Industria Alimentaria: El pH es un factor determinante en la conservación, el sabor y la textura de los alimentos. Se utilizan aditivos que son sales de ácidos y bases débiles para controlar el pH y prolongar la vida útil de los productos.
- Química Analítica: En titulaciones y preparaciones de soluciones estándar, el conocimiento del pH de estas sales es esencial para obtener resultados precisos.
- Tratamiento de Aguas: El control del pH es vital en el tratamiento de aguas residuales y potables para optimizar procesos como la coagulación, la floculación y la desinfección.
En esencia, la capacidad de predecir y controlar el pH de estas soluciones es una habilidad indispensable para ingenieros químicos, farmacéuticos, bioquímicos y cualquier profesional que trabaje con sistemas acuosos complejos.
Conceptos Erróneos Comunes
Al abordar el pH de estas sales, surgen algunas ideas erróneas comunes:
- "Todas las sales son neutras": Esta es la más grande. Como hemos visto, solo las sales de ácido fuerte y base fuerte son neutras en solución. Las sales de componentes débiles pueden ser ácidas, básicas o neutras.
- "La concentración de la sal no importa": Si bien la fórmula simplificada
pH = 1/2 pKw + 1/2 pKa - 1/2 pKbno incluye explícitamente la concentración de la sal, es una aproximación válida bajo ciertas condiciones (concentraciones moderadas). Para soluciones muy diluidas o muy concentradas, o para constantes de disociación extremadamente pequeñas, se requieren cálculos más complejos que sí consideran la concentración inicial. - "Ka y Kb son siempre iguales": El caso Ka=Kb es una simplificación conveniente para la enseñanza, pero en la realidad, es raro que sean exactamente iguales. Lo más común es que una sea mayor que la otra, lo que lleva a soluciones ácidas o básicas.
Estar consciente de estas sutilezas ayuda a aplicar correctamente los principios de la química ácido-base.
Tabla Comparativa de Escenarios de pH (Hipótetica)
Para consolidar la comprensión de cómo Ka y Kb influyen en el pH, presentamos una tabla comparativa con escenarios hipotéticos, asumiendo una temperatura de 25°C (pKw = 14):
| Escenario | Relación Ka vs. Kb | pKa vs. pKb | pH Esperado | Naturaleza de la Solución |
|---|---|---|---|---|
| Ácido Acético (Ka=1.8x10⁻⁵) y Amoníaco (Kb=1.8x10⁻⁵) | Ka = Kb | pKa ≈ pKb (4.74 ≈ 4.74) | 1/2(14) + 1/2(4.74) - 1/2(4.74) = 7 | Neutra |
| Ácido Fluorhídrico (Ka=6.8x10⁻⁴) y Amoníaco (Kb=1.8x10⁻⁵) | Ka > Kb | pKa < pKb (3.17 < 4.74) | 1/2(14) + 1/2(3.17) - 1/2(4.74) ≈ 6.22 | Ácida |
| Ácido Cianhídrico (Ka=4.9x10⁻¹⁰) y Metilamina (Kb=4.4x10⁻⁴) | Kb > Ka | pKb < pKa (3.36 < 9.31) | 1/2(14) + 1/2(9.31) - 1/2(3.36) ≈ 9.98 | Básica |
Esta tabla demuestra claramente cómo la balanza entre las fuerzas del ácido y la base débiles determina el pH final de la solución de la sal.
Preguntas Frecuentes (FAQs)
Aquí respondemos algunas de las preguntas más comunes sobre el cálculo del pH de sales de ácidos y bases débiles:
P: ¿Por qué la concentración de la sal no aparece en la fórmula principal?
R: La fórmula simplificada pH = 1/2 pKw + 1/2 pKa - 1/2 pKb es una aproximación que asume que la extensión de la hidrólisis es pequeña en comparación con la concentración inicial de la sal. Para concentraciones muy diluidas o cuando Ka y Kb son muy pequeñas (lo que implica una hidrólisis significativa), se requeriría un cálculo más riguroso que sí considere la concentración inicial de la sal.
P: ¿Esta fórmula es válida para cualquier temperatura?
R: La fórmula es conceptualmente válida para cualquier temperatura, pero el valor de pKw es dependiente de la temperatura. A 25°C, pKw es 14. Si la temperatura es diferente, el valor de pKw cambiará, y esto afectará el resultado del pH. Por ejemplo, a 0°C, pKw es 14.94, y a 100°C, pKw es 12.25.
P: ¿Qué tan precisos son estos cálculos?
R: Los cálculos utilizando esta fórmula son bastante precisos para fines educativos y para la mayoría de las aplicaciones prácticas donde las concentraciones son moderadas y las constantes de disociación no son extremadamente pequeñas. Para una precisión muy alta en investigación o aplicaciones industriales, a menudo se necesitan modelos más complejos que consideren la fuerza iónica de la solución y la actividad de los iones.
P: ¿Qué es un par conjugado ácido-base?
R: Un par conjugado ácido-base consiste en un ácido y una base que difieren solo en un protón (H⁺). Por ejemplo, el ácido acético (CH₃COOH) y el ion acetato (CH₃COO⁻) forman un par conjugado. De manera similar, el amonio (NH₄⁺) y el amoníaco (NH₃) son un par conjugado. La relación entre Ka y Kb para un par conjugado es Kw = Ka * Kb (o pKw = pKa + pKb).
Conclusión
El cálculo del pH de las sales formadas por ácidos débiles y bases débiles es un tema central en la química ácido-base, que revela la delicada danza de equilibrios en soluciones acuosas. Hemos explorado cómo la fórmula pH = 1/2 pKw + 1/2 pKa - 1/2 pKb nos permite predecir la acidez, basicidad o neutralidad de estas soluciones, destacando el caso particular donde Ka = Kb y el pH resultante es 7. Más allá de los números, comprender la interacción entre las fuerzas relativas del ácido y la base progenitores es la clave para desentrañar el comportamiento de estos compuestos tan importantes. Desde la biología hasta la industria, la capacidad de manipular y predecir el pH de estas soluciones es una habilidad invaluable, que subraya la importancia de dominar los principios fundamentales de la química.
Si quieres conocer otros artículos parecidos a Cálculo del pH de Sales de Ácido y Base Débil puedes visitar la categoría Química.

