10/09/2022
En el fascinante mundo de la química, la capacidad de separar y purificar sustancias es tan crucial como sintetizarlas. Imagina una mezcla compleja donde deseas aislar un componente específico, eliminando impurezas o subproductos. Aquí es donde entra en juego una técnica poderosa y ampliamente utilizada: la extracción. La extracción es un proceso de separación que permite transferir uno o más componentes de una mezcla de sustancias, llamada material de extracción, a un agente de extracción. Este agente es generalmente un disolvente, y la sustancia extraída se denomina extracto, incluso si permanece en forma disuelta. Si el proceso no altera químicamente la sustancia, es un proceso físico, como la disolución. Sin embargo, si hay una reacción química, se considera un proceso químico. Cuando hablamos de la extracción líquido-líquido, nos adentramos en un método donde dos fases líquidas inmiscibles se utilizan para lograr esta separación selectiva, aprovechando las diferencias de solubilidad de los compuestos.
La extracción líquido-líquido (ELL) es una técnica vital en química orgánica y analítica, así como en procesos industriales a gran escala. Su propósito principal es aislar un compuesto objetivo de una fase líquida a otra, separándolo de materiales de partida no reaccionados o impurezas. Esta técnica es particularmente útil cuando el disolvente original es difícil de eliminar por evaporación, como aquellos con puntos de ebullición elevados. A diferencia de otras formas de extracción, como la sólido-líquido (por ejemplo, la preparación de café o té, donde la cafeína se extrae de sólidos a agua caliente), la ELL se centra exclusivamente en la transferencia entre dos líquidos inmiscibles.
- ¿Qué es la Extracción Líquido-Líquido (ELL)?
- El Proceso de Extracción Líquido-Líquido Paso a Paso
- Coeficiente de Partición: La Clave de la Eficacia
- Selección del Par de Disolventes Ideal
- Tipos Especializados de Extracción Líquido-Líquido: Extracción Ácido-Base
- El Método de Hunter-Nash: Un Enfoque Cuantitativo
- Importancia y Aplicaciones de la Extracción Líquido-Líquido
- Preguntas Frecuentes sobre la Extracción Líquido-Líquido
¿Qué es la Extracción Líquido-Líquido (ELL)?
La extracción líquido-líquido implica la transferencia de un soluto de una fase líquida a otra. Para que esto sea posible, se requiere la presencia de dos fases líquidas que no se mezclen entre sí, es decir, que sean inmiscibles. Las dos fases líquidas en una extracción suelen ser:
- Fase Acuosa: Compuesta por agua o una disolución acuosa. Esta fase es polar y tiende a disolver compuestos iónicos o muy polares.
- Fase Orgánica: Compuesta por una disolución o un disolvente orgánico que es inmiscible con el agua. Esta fase es típicamente no polar o de baja polaridad y disuelve mejor los compuestos orgánicos neutros.
Es importante distinguir entre los términos 'extracción' y 'lavado'. Aunque ambos implican el uso de un disolvente para separar componentes, su objetivo difiere. En la extracción, el objetivo es transferir el compuesto de interés de una fase a otra. En el lavado, el objetivo es eliminar impurezas no deseadas de una fase, dejando el compuesto de interés en la fase original. Por ejemplo, si tienes un compuesto orgánico disuelto en una fase orgánica y quieres eliminar sales inorgánicas, usarías un lavado con agua. Si quieres mover tu compuesto orgánico de una fase acuosa a una orgánica, harías una extracción.
El Proceso de Extracción Líquido-Líquido Paso a Paso
La extracción líquido-líquido se lleva a cabo comúnmente utilizando un embudo de separación, una pieza de vidrio con forma de pera que permite la separación de líquidos inmiscibles. El proceso típico es el siguiente:
- Preparación: La disolución que contiene el soluto a extraer (generalmente la fase acuosa) se añade al embudo de separación.
- Adición del Disolvente de Extracción: Se añade un disolvente orgánico no miscible con el agua al embudo. Es fundamental que este disolvente tenga una mayor afinidad por el soluto que la fase original.
- Mezclado: Los contenidos del embudo se agitan vigorosamente para asegurar un contacto íntimo entre las dos fases y permitir que el soluto se transfiera. Es importante liberar periódicamente la presión acumulada abriendo la llave del embudo.
- Asentamiento de Fases: Una vez mezcladas, las dos fases se dejan reposar. Debido a sus diferentes densidades, los líquidos inmiscibles se separarán en capas discretas. La fase más densa se asentará en la parte inferior, y la menos densa en la parte superior. La mayoría de los disolventes orgánicos son menos densos que el agua y flotarán, con la excepción de los disolventes orgánicos clorados, como el diclorometano, que son más densos y se irán al fondo.
- Separación: Una vez que las capas están completamente separadas, se abre la llave del embudo de separación para drenar cuidadosamente la capa inferior en un recipiente. Luego, la capa superior se vierte por la boca del embudo en otro recipiente.
La fase líquida de la que se ha removido el soluto se conoce como refinado, mientras que la fase líquida que ha ganado el soluto se denomina extracto. Es común realizar múltiples extracciones con volúmenes más pequeños de disolvente en lugar de una sola extracción con un gran volumen, ya que esto suele ser más eficiente para la recuperación del soluto.

Coeficiente de Partición: La Clave de la Eficacia
La eficacia de una extracción líquido-líquido depende fundamentalmente de cómo se distribuye el compuesto de interés entre las dos fases inmiscibles. Esta distribución se describe mediante el coeficiente de partición (K), también conocido como coeficiente de distribución. El coeficiente de partición para un soluto es la relación de la concentración del soluto en la capa orgánica dividida por su concentración en la fase acuosa, una vez que se ha alcanzado el equilibrio:
K = [Concentración del Soluto en la Fase Orgánica] / [Concentración del Soluto en la Fase Acuosa]
El coeficiente de partición es una constante para un soluto dado y un par específico de disolventes a una temperatura determinada. Es una expresión de la preferencia del soluto por cada uno de los dos disolventes. Los solutos con un valor de K grande tienen una mayor tendencia a ser extraídos hacia la fase orgánica, lo que indica que son mucho más solubles en el disolvente orgánico que en el agua. Por el contrario, los solutos con valores de K pequeños prefieren permanecer en la fase acuosa. Para una extracción eficiente, buscamos un sistema donde el coeficiente de partición del compuesto de interés sea lo más alto posible en el disolvente de extracción.
Selección del Par de Disolventes Ideal
Elegir el par de disolventes adecuado es un paso crítico para el éxito de una extracción líquido-líquido. Se deben considerar varios factores clave:
- Solubilidad del Soluto: El soluto debe ser significativamente más soluble en el disolvente de extracción que en la fase original (generalmente agua). Conocer el coeficiente de partición del soluto en un par de disolventes potencial es esencial.
- Inmiscibilidad: Los dos disolventes deben ser inmiscibles entre sí y no deben formar una disolución homogénea cuando se mezclan. Si se mezclan, no habrá separación de fases y la extracción no será posible.
- Inertidad: Los disolventes deben ser inertes, es decir, no deben reaccionar con el soluto ni con ningún otro componente de la mezcla. Una reacción indeseada podría alterar el compuesto de interés o generar nuevos productos.
- Volatilidad: El disolvente de extracción debe ser lo suficientemente volátil como para poder ser eliminado fácilmente del soluto una vez que la extracción ha concluido. Esto se logra generalmente por evaporación, destilación o rotavaporación. Un disolvente con un punto de ebullición bajo es preferible.
- Densidad: Es crucial conocer las densidades relativas de los disolventes para identificar correctamente las capas superior e inferior en el embudo de separación. Como se mencionó, la mayoría de los líquidos orgánicos son menos densos que el agua, pero los disolventes clorados (como el cloroformo o el diclorometano) son más densos y formarán la capa inferior.
- Seguridad y Costo: También se deben considerar factores prácticos como la toxicidad, inflamabilidad y el costo del disolvente.
Los disolventes orgánicos inmiscibles con el agua suelen ser de naturaleza no polar o de baja polaridad, lo que les permite disolver compuestos orgánicos con propiedades similares (recordemos el principio de 'lo semejante disuelve lo semejante').
Tipos Especializados de Extracción Líquido-Líquido: Extracción Ácido-Base
La extracción ácido-base es una variación poderosa de la extracción líquido-líquido que se utiliza para separar compuestos orgánicos basándose en sus propiedades ácido-base. La clave de esta técnica reside en la capacidad de transformar un compuesto orgánico neutro en una especie iónica (o viceversa) cambiando el pH del medio. Los compuestos iónicos son generalmente mucho más solubles en agua que en disolventes orgánicos.

El principio es el siguiente: la mayoría de los compuestos orgánicos neutros son más solubles en disolventes orgánicos que en agua. Sin embargo, si un compuesto orgánico posee grupos funcionales ácidos (como ácidos carboxílicos o fenoles) o básicos (como aminas), su estado de carga puede modificarse por un cambio de pH. Al reaccionar un ácido orgánico con una base, se forma su sal conjugada, que es una especie iónica y, por lo tanto, mucho más soluble en la fase acuosa. De manera similar, al reaccionar una base orgánica con un ácido, se forma su sal conjugada, también iónica y soluble en agua.
Consideremos un ejemplo de una mezcla que contiene un ácido carboxílico, una amina y un compuesto neutro. Si el ácido carboxílico tiene seis o más carbonos, será insoluble en agua y soluble en disolventes orgánicos. Sus bases conjugadas (sales carboxilato), sin embargo, son solubles en agua e insolubles en disolventes orgánicos. De manera similar, una amina con siete o más carbonos es insoluble en agua pero soluble en disolventes orgánicos, mientras que sus ácidos conjugados (sales de amonio) son solubles en agua.
El proceso para separar esta mezcla sería:
- Disolver la mezcla en un disolvente orgánico.
- Lavar la disolución orgánica con una base acuosa (por ejemplo, hidróxido de sodio). Esto neutralizará el ácido carboxílico, transformándolo en su sal carboxilato iónica. Esta sal se transferirá a la fase acuosa, mientras que la amina y el compuesto neutro permanecerán en la fase orgánica. Las dos fases se separan.
- La fase acuosa que contiene la sal del ácido carboxílico se acidifica (por ejemplo, con ácido clorhídrico) para regenerar el ácido carboxílico neutro, que precipitará o podrá ser extraído de nuevo en un disolvente orgánico fresco.
- La fase orgánica original, que ahora contiene la amina y el compuesto neutro, se lava con un ácido acuoso (por ejemplo, ácido clorhídrico). Esto neutralizará la amina, transformándola en su sal de amonio iónica, que se transferirá a la fase acuosa. El compuesto neutro permanecerá en la fase orgánica. Las dos fases se separan.
- La fase acuosa que contiene la sal de amonio se alcaliniza (por ejemplo, con hidróxido de sodio) para regenerar la amina neutra, que podrá ser extraída de nuevo en un disolvente orgánico.
- El compuesto neutro permanece en la fase orgánica original y puede ser recuperado por evaporación del disolvente.
Esta técnica es increíblemente versátil y también se utiliza para separar dos ácidos débiles o dos bases débiles con una diferencia significativa en sus valores de pKa. El ácido o la base más fuerte se neutraliza selectivamente con una base o ácido débil, respectivamente, lo que permite su extracción selectiva en la fase acuosa.

El Método de Hunter-Nash: Un Enfoque Cuantitativo
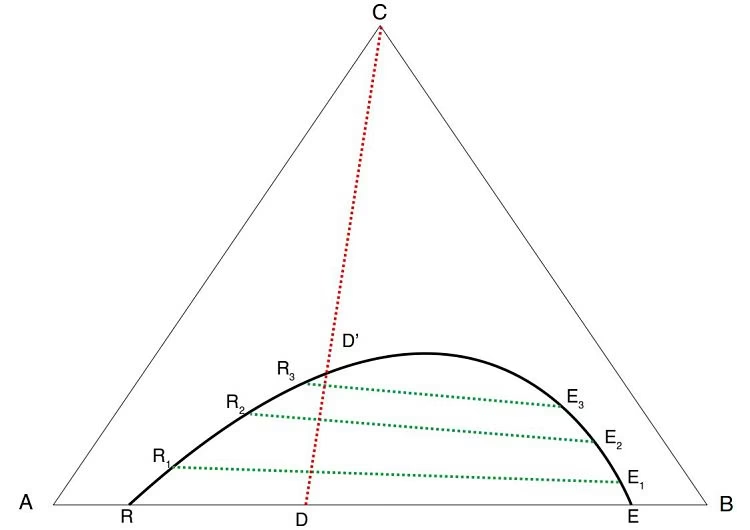
Cuando se trata de procesos de extracción líquido-líquido a escala industrial o para diseños de ingeniería, es fundamental determinar el número óptimo de etapas de equilibrio necesarias para lograr una separación deseada. Aquí es donde entra en juego el método de Hunter-Nash. Este método es una herramienta gráfica que utiliza balances de materia y un diagrama de fases ternario (un diagrama triangular que representa las composiciones de tres componentes) con separación de fases para determinar el número de etapas de equilibrio necesarias para la extracción. El sistema generalmente involucra un disolvente, un portador (la fase original que contiene el soluto) y un soluto. Al trazar las líneas de operación y las líneas de unión en el diagrama ternario, los ingenieros pueden visualizar y calcular cuántas veces se debe contactar la mezcla con el disolvente fresco para extraer eficientemente el soluto hasta una concentración deseada. Este método es esencial para el diseño y optimización de extractores en contracorriente, donde múltiples etapas de extracción se realizan de manera continua para maximizar la eficiencia.
Importancia y Aplicaciones de la Extracción Líquido-Líquido
La extracción líquido-líquido es una técnica de separación de inmenso valor, con aplicaciones que abarcan desde el laboratorio de investigación hasta la producción a gran escala en diversas industrias. Su versatilidad la convierte en una herramienta indispensable para la purificación y el aislamiento de compuestos. Algunas de sus aplicaciones clave incluyen:
- Industria Farmacéutica: Es fundamental para la extracción de principios activos de materiales naturales o de mezclas de reacción complejas durante la síntesis de fármacos. Permite purificar antibióticos, vitaminas y otros compuestos bioactivos.
- Industria Alimentaria: Se utiliza para descafeinar café, extraer aceites esenciales, sabores y aromas de plantas, o para eliminar impurezas en la producción de aceites vegetales.
- Química Analítica: En el análisis de muestras, la ELL se emplea para preconcentrar analitos, eliminar interferencias o para la preparación de muestras antes de técnicas como la cromatografía o la espectroscopia.
- Industria Petroquímica: Se usa para la separación de hidrocarburos, la eliminación de impurezas de combustibles y lubricantes, y la recuperación de componentes valiosos del petróleo.
- Tratamiento de Aguas y Medio Ambiente: Permite la eliminación de contaminantes orgánicos de aguas residuales o la recuperación de metales pesados de soluciones acuosas.
- Minería: En la hidrometalurgia, la extracción líquido-líquido es crucial para la recuperación y purificación de metales como el cobre, el uranio o el oro de lixiviados minerales.
En resumen, la extracción líquido-líquido es una piedra angular en los procesos de separación, aprovechando las propiedades de solubilidad de los compuestos en fases inmiscibles. Desde la simple purificación en el laboratorio hasta los complejos diseños industriales que utilizan métodos como el de Hunter-Nash, esta técnica permite la obtención de sustancias con la pureza requerida para una vasta gama de aplicaciones. Su comprensión es esencial para cualquier químico o ingeniero que trabaje con mezclas complejas.
Preguntas Frecuentes sobre la Extracción Líquido-Líquido
| Pregunta | Respuesta |
|---|---|
| ¿Por qué es mejor realizar varias extracciones pequeñas que una sola extracción grande? | Realizar varias extracciones con volúmenes pequeños de disolvente de extracción es más eficiente que una sola extracción con un gran volumen. Esto se debe a que el coeficiente de partición rige la distribución del soluto en cada equilibrio. Al realizar extracciones repetidas, se desplaza continuamente el equilibrio, permitiendo que una mayor proporción del soluto se transfiera a la fase de extracción con cada paso. |
| ¿Cómo sé qué capa es la fase acuosa y cuál es la orgánica en el embudo de separación? | La identificación de las capas depende de las densidades relativas de los disolventes. La capa más densa siempre estará en la parte inferior y la menos densa en la parte superior. El agua tiene una densidad de aproximadamente 1 g/mL. La mayoría de los disolventes orgánicos comunes son menos densos que el agua (por ejemplo, éter dietílico: 0.71 g/mL), por lo que flotarán. Sin embargo, los disolventes halogenados como el diclorometano (1.33 g/mL) o el cloroformo (1.49 g/mL) son más densos que el agua y formarán la capa inferior. Si tienes dudas, puedes añadir una pequeña gota de agua a la mezcla; si la gota se mezcla con la capa inferior, esa es la fase acuosa. |
| ¿Qué precauciones de seguridad debo tomar al realizar una extracción líquido-líquido? | Siempre se debe trabajar en una campana de extracción bien ventilada debido a la volatilidad y posible toxicidad de los disolventes orgánicos. Use equipo de protección personal adecuado, como gafas de seguridad y guantes resistentes a productos químicos. Al agitar el embudo de separación, asegúrese de liberar la presión regularmente ("ventilar") para evitar la acumulación de gases y la expulsión del tapón. Nunca dirija la boca del embudo hacia usted o hacia otra persona al ventilar. |
Si quieres conocer otros artículos parecidos a Extracción Líquido-Líquido: Guía Completa puedes visitar la categoría Química.
