15/07/2023
En el vasto y fascinante universo de la química, comprender las cantidades es tan crucial como entender las reacciones. Saber cómo calcular los gramos de una molécula o la proporción de un elemento dentro de un compuesto no es solo un ejercicio académico, sino una habilidad fundamental que abre las puertas a la estequiometría, la síntesis de nuevos materiales, el diseño de fármacos y un sinfín de aplicaciones prácticas. Si alguna vez te has preguntado cómo los químicos determinan las cantidades exactas de sustancias necesarias para una reacción, o cómo analizan la pureza de un material, la respuesta reside en dominar estos cálculos esenciales.

Este artículo te guiará paso a paso a través de los conceptos y métodos necesarios para calcular con precisión los gramos en el mundo microscópico de las moléculas y los elementos. Desde la base de la masa atómica hasta la determinación de la composición porcentual, desglosaremos cada concepto para que puedas aplicarlo con confianza y precisión.
La Masa Molar: El Peso de una Molécula en Gramos
Antes de sumergirnos en los cálculos, es vital entender el concepto de Masa Molar. Piensa en ella como el peso de una molécula, pero expresado en una unidad que podemos medir y utilizar en el laboratorio: gramos por mol (g/mol). Para comprender la masa molar, primero debemos entender dos conceptos relacionados: la masa atómica y la masa molecular.
Masa Atómica: El Fundamento
Cada elemento en la tabla periódica tiene una masa atómica. Esta masa se expresa en Unidades de Masa Atómica (uma). Una uma es aproximadamente la masa de un protón o un neutrón. Por ejemplo, el carbono tiene una masa atómica de aproximadamente 12.01 uma, el hidrógeno de 1.008 uma y el oxígeno de 15.999 uma. Estas masas son promedios ponderados de los isótopos de cada elemento, lo que explica por qué no son números enteros exactos.
Masa Molecular: El Peso de un Compuesto
La masa molecular, a veces también llamada peso molecular, es simplemente la suma de las masas atómicas de todos los átomos presentes en una molécula. Se calcula sumando las masas atómicas de cada elemento, multiplicadas por el número de veces que aparece ese elemento en la fórmula química del compuesto. Al igual que la masa atómica, la masa molecular se expresa en uma.
Calculando la Masa Molecular: Ejemplos Prácticos
Para ilustrar, calculemos la masa molecular de algunas moléculas comunes:
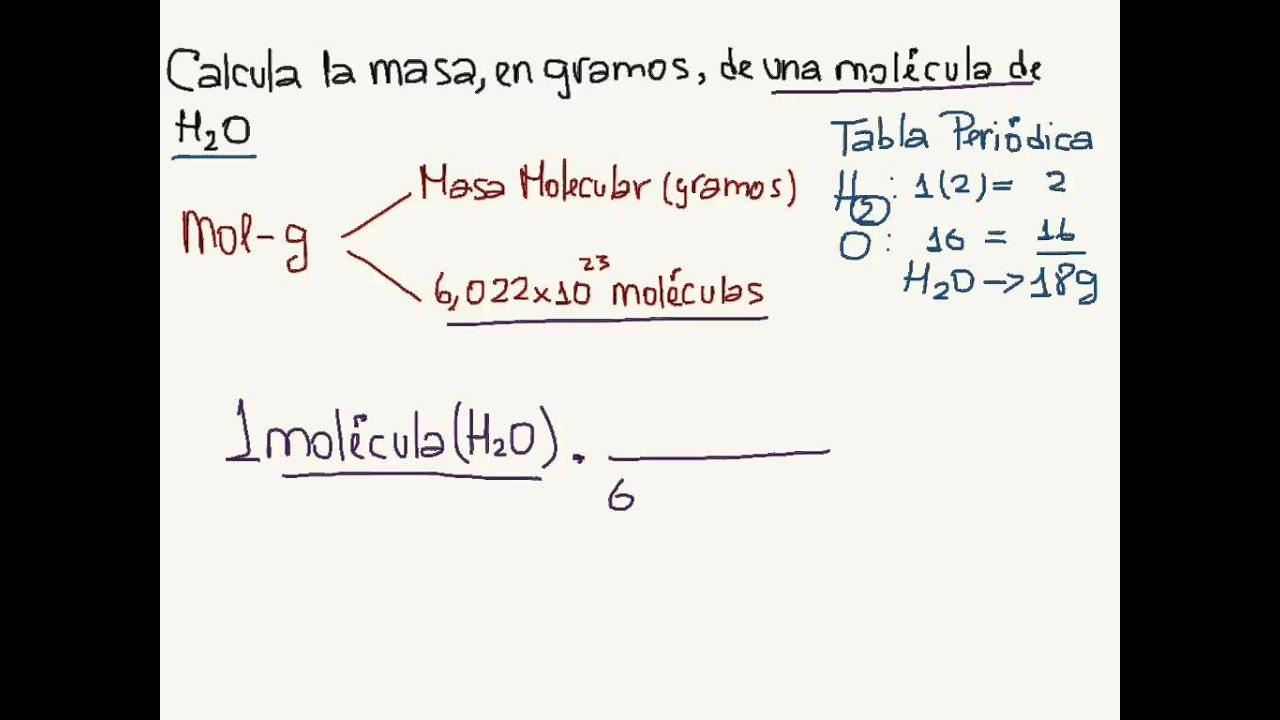
- Agua (H₂O):
- Hidrógeno (H): 2 átomos * 1.008 uma/átomo = 2.016 uma
- Oxígeno (O): 1 átomo * 15.999 uma/átomo = 15.999 uma
- Masa Molecular de H₂O = 2.016 + 15.999 = 18.015 uma - Dióxido de Carbono (CO₂):
- Carbono (C): 1 átomo * 12.011 uma/átomo = 12.011 uma
- Oxígeno (O): 2 átomos * 15.999 uma/átomo = 31.998 uma
- Masa Molecular de CO₂ = 12.011 + 31.998 = 44.009 uma - Glucosa (C₆H₁₂O₆):
- Carbono (C): 6 átomos * 12.011 uma/átomo = 72.066 uma
- Hidrógeno (H): 12 átomos * 1.008 uma/átomo = 12.096 uma
- Oxígeno (O): 6 átomos * 15.999 uma/átomo = 95.994 uma
- Masa Molecular de C₆H₁₂O₆ = 72.066 + 12.096 + 95.994 = 180.156 uma
De uma a Gramos: El Concepto de Mol
Aquí es donde entra el concepto de mol. Un mol es una cantidad de sustancia que contiene un número específico de partículas (átomos, moléculas, iones, etc.), conocido como el número de Avogadro (aproximadamente 6.022 x 10²³ partículas). Lo realmente útil es que la masa molar de una sustancia, expresada en gramos por mol (g/mol), es numéricamente igual a su masa atómica o molecular expresada en uma.
Es decir, si la masa molecular del agua es 18.015 uma, entonces la masa molar del agua es 18.015 g/mol. Esto significa que un mol de moléculas de agua tiene una masa de 18.015 gramos. Esta equivalencia es la piedra angular para convertir entre la escala atómica (uma) y la escala macroscópica (gramos) que usamos en el laboratorio.
Aplicando la Masa Molar en Cálculos de Gramos
Para calcular los gramos de una molécula dada una cantidad de moles, simplemente multiplicamos el número de moles por la masa molar del compuesto. De manera inversa, si tenemos una cantidad en gramos y queremos saber cuántos moles representa, dividimos los gramos por la masa molar.
Fórmulas Clave:
- Gramos = Moles × Masa Molar (g/mol)
- Moles = Gramos / Masa Molar (g/mol)
Ejemplo: ¿Cuántos gramos hay en 0.5 moles de CO₂?
- Primero, calculamos la masa molar de CO₂: 44.009 g/mol (como vimos anteriormente).
- Gramos = 0.5 moles × 44.009 g/mol = 22.0045 gramos de CO₂.
Ejemplo: ¿Cuántos moles son 90 gramos de H₂O?
- Primero, calculamos la masa molar de H₂O: 18.015 g/mol.
- Moles = 90 g / 18.015 g/mol = 4.996 moles de H₂O.
Composición Porcentual: Gramos de un Elemento en un Compuesto
Ahora que sabemos cómo manejar los gramos de una molécula completa, ¿qué pasa si queremos saber cuántos gramos de un elemento específico hay dentro de una cantidad dada de un compuesto? Aquí es donde entra en juego la Composición Porcentual.

La composición porcentual nos indica el porcentaje en masa de cada elemento en un compuesto. Es una herramienta invaluable en química analítica, para verificar la pureza de una sustancia, para determinar la fórmula empírica de un compuesto desconocido, o simplemente para entender la proporción de cada componente.
Cálculo de la Composición Porcentual
Para calcular el porcentaje en masa de un elemento en un compuesto, utilizamos la siguiente fórmula:
% de Elemento = ( (Número de átomos del elemento × Masa atómica del elemento) / Masa molar del compuesto ) × 100%
Ejemplos Detallados de Composición Porcentual
Usemos los ejemplos anteriores para calcular la composición porcentual de sus elementos:
- Agua (H₂O):
- Masa Molar de H₂O = 18.015 g/mol
- Porcentaje de Hidrógeno (H):
- (2 átomos de H × 1.008 g/mol de H) / 18.015 g/mol de H₂O × 100%
- (2.016 g/mol) / 18.015 g/mol × 100% = 11.19% H
- Porcentaje de Oxígeno (O):
- (1 átomo de O × 15.999 g/mol de O) / 18.015 g/mol de H₂O × 100%
- (15.999 g/mol) / 18.015 g/mol × 100% = 88.81% O
(Nota: La suma de los porcentajes debe ser aproximadamente 100%. 11.19% + 88.81% = 100%) - Glucosa (C₆H₁₂O₆):
- Masa Molar de C₆H₁₂O₆ = 180.156 g/mol
- Porcentaje de Carbono (C):
- (6 átomos de C × 12.011 g/mol de C) / 180.156 g/mol de C₆H₁₂O₆ × 100%
- (72.066 g/mol) / 180.156 g/mol × 100% = 40.00% C
- Porcentaje de Hidrógeno (H):
- (12 átomos de H × 1.008 g/mol de H) / 180.156 g/mol de C₆H₁₂O₆ × 100%
- (12.096 g/mol) / 180.156 g/mol × 100% = 6.71% H
- Porcentaje de Oxígeno (O):
- (6 átomos de O × 15.999 g/mol de O) / 180.156 g/mol de C₆H₁₂O₆ × 100%
- (95.994 g/mol) / 180.156 g/mol × 100% = 53.28% O
(Nota: 40.00% + 6.71% + 53.28% = 99.99%, la pequeña diferencia es por el redondeo.)
Calculando Gramos de un Elemento a Partir de una Cantidad Dada del Compuesto
Una vez que conocemos la composición porcentual, podemos determinar fácilmente cuántos gramos de un elemento hay en una cantidad específica de un compuesto. Solo necesitamos multiplicar la cantidad total de gramos del compuesto por el porcentaje del elemento (expresado como decimal).
Gramos del Elemento = Gramos del Compuesto × (% del Elemento / 100)
Ejemplo: ¿Cuántos gramos de oxígeno hay en 50 gramos de agua (H₂O)?
- Sabemos que el agua contiene 88.81% de oxígeno.
- Gramos de O = 50 g de H₂O × (88.81 / 100) = 50 g × 0.8881 = 44.405 gramos de O.
Este tipo de cálculo es fundamental en la Estequiometría, que es la rama de la química que estudia las relaciones cuantitativas entre los reactivos y productos en una reacción química. Permite a los químicos predecir la cantidad de producto que se formará o la cantidad de reactivo necesaria para una reacción.
Aplicaciones Prácticas de Estos Cálculos
La capacidad de calcular los gramos de moléculas y elementos es más que un simple ejercicio teórico; tiene aplicaciones críticas en una multitud de campos:
- Farmacología y Medicina: Los farmacéuticos utilizan estos cálculos para formular medicamentos con dosis precisas de ingredientes activos. Los médicos pueden entender la composición de compuestos en el cuerpo humano.
- Industria Química: Para optimizar procesos de producción, los ingenieros químicos necesitan saber las cantidades exactas de reactivos y subproductos. Es crucial para el control de calidad y la eficiencia.
- Ciencias Ambientales: Para analizar la composición de contaminantes en el aire o el agua, o para determinar la cantidad de ciertos elementos en muestras de suelo.
- Análisis de Materiales: En metalurgia o ciencia de materiales, se utilizan para determinar la pureza de las aleaciones o la composición de nuevos materiales.
- Nutrición y Alimentos: Para calcular la cantidad de nutrientes específicos (como el hierro o el calcio) en los alimentos, lo cual es esencial para el etiquetado nutricional.
Tabla de Masas Atómicas Comunes
Para facilitar tus cálculos, aquí tienes una tabla con las masas atómicas aproximadas de algunos elementos comunes:
| Elemento | Símbolo | Masa Atómica (uma o g/mol) |
|---|---|---|
| Hidrógeno | H | 1.008 |
| Carbono | C | 12.011 |
| Nitrógeno | N | 14.007 |
| Oxígeno | O | 15.999 |
| Sodio | Na | 22.990 |
| Magnesio | Mg | 24.305 |
| Aluminio | Al | 26.982 |
| Silicio | Si | 28.085 |
| Fósforo | P | 30.974 |
| Azufre | S | 32.06 |
| Cloro | Cl | 35.453 |
| Potasio | K | 39.098 |
| Calcio | Ca | 40.078 |
| Hierro | Fe | 55.845 |
| Cobre | Cu | 63.546 |
| Zinc | Zn | 65.38 |
Preguntas Frecuentes (FAQ)
¿Qué diferencia hay entre masa atómica y masa molar?
La masa atómica es la masa de un átomo de un elemento, generalmente expresada en unidades de masa atómica (uma). Por ejemplo, la masa atómica del carbono es 12.011 uma. La masa molar, en cambio, es la masa de un mol de átomos o moléculas de una sustancia, expresada en gramos por mol (g/mol). Numéricamente, la masa molar es igual a la masa atómica (o molecular), pero la unidad es diferente. Así, la masa molar del carbono es 12.011 g/mol, lo que significa que 6.022 x 10²³ átomos de carbono pesan 12.011 gramos.
¿Por qué es importante calcular la composición porcentual de un compuesto?
La composición porcentual es crucial por varias razones. Permite verificar la pureza de una sustancia en el laboratorio, ya que un porcentaje diferente al esperado podría indicar impurezas. También es fundamental para determinar la Fórmula Empírica y molecular de un compuesto desconocido a partir de datos experimentales. En la industria, ayuda a los químicos a asegurar que los productos tienen la proporción correcta de cada elemento, lo cual es vital para su función y calidad.
¿Dónde encuentro las masas atómicas de los elementos?
Las masas atómicas de todos los elementos se encuentran en la tabla periódica. La mayoría de las tablas periódicas listan la masa atómica de cada elemento debajo de su símbolo. Es importante usar la masa atómica promedio (que es la que se lista en la tabla periódica estándar) para la mayoría de los cálculos, ya que considera la abundancia natural de los isótopos del elemento.
¿Qué es una Unidad de Masa Atómica (uma)?
La Unidad de Masa Atómica (uma) es una unidad de masa estándar utilizada para expresar las masas de átomos y moléculas. Se define como 1/12 de la masa de un átomo de carbono-12. Es una unidad muy pequeña, diseñada para ser conveniente en la escala atómica, donde los gramos serían un número extremadamente pequeño. Una uma es aproximadamente 1.6605 x 10⁻²⁴ gramos.
Conclusión
El cálculo de los gramos de una molécula a través de su masa molar, y la determinación de los gramos de un elemento dentro de un compuesto mediante la composición porcentual, son habilidades fundamentales en el estudio y la aplicación de la química. Estos conceptos no solo te permiten cuantificar y comprender las sustancias a un nivel profundo, sino que también son la base para cálculos más avanzados en estequiometría y análisis químico. Al dominar estas técnicas, te equipas con una herramienta poderosa para explorar el mundo molecular y sus infinitas posibilidades. La práctica constante y la comprensión de los principios subyacentes son clave para convertir estos cálculos en una segunda naturaleza.
Si quieres conocer otros artículos parecidos a Calculando Gramos: De Moléculas a Elementos puedes visitar la categoría Química.