07/09/2024
En el vasto universo de la química, las sustancias se clasifican de diversas maneras para comprender mejor sus propiedades y reacciones. Una de las clasificaciones fundamentales es la de ácidos y bases, pilares esenciales en innumerables procesos, desde la digestión en nuestro cuerpo hasta la fabricación de productos industriales. Si bien a menudo escuchamos hablar de pH para medir la acidez o basicidad de una solución, la verdadera fuerza de una base va mucho más allá de un simple número. Comprender qué define una base fuerte es crucial para predecir su comportamiento y aplicaciones. Acompáñanos en este viaje para desentrañar los misterios de las bases y cómo podemos cuantificar su poder.
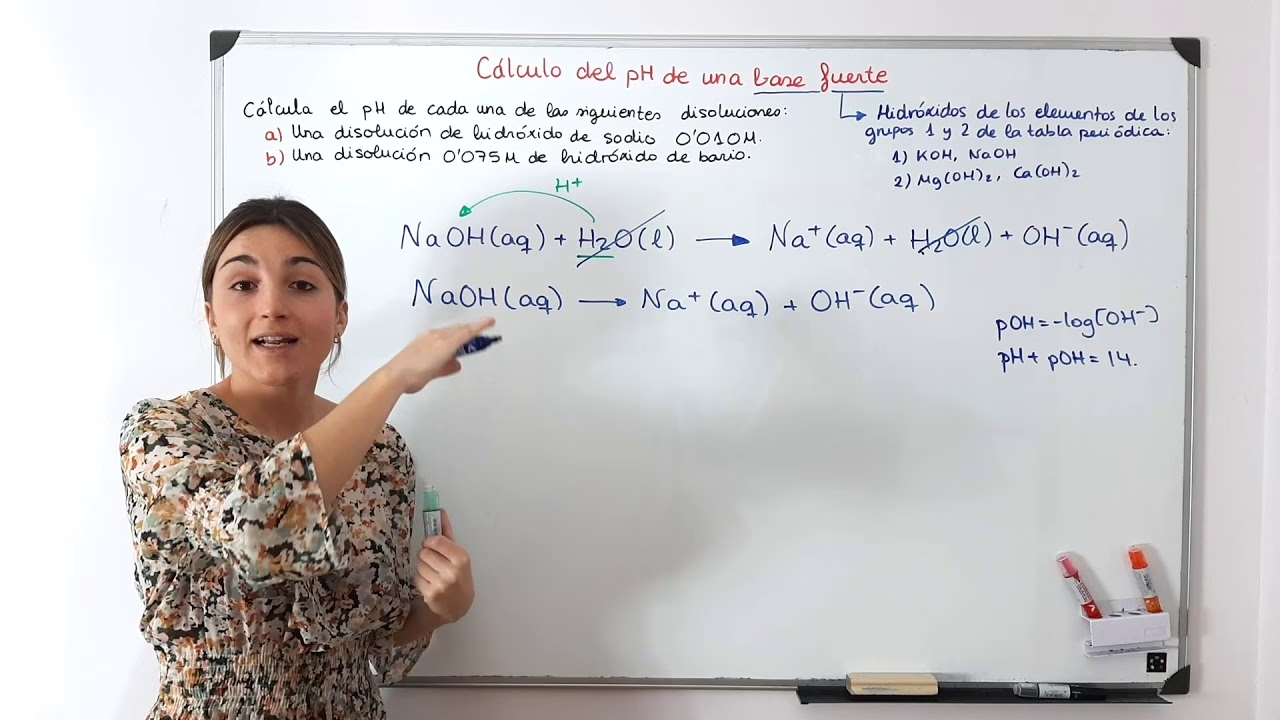
- ¿Qué es una Base en Química?
- La Diferencia Clave: Bases Fuertes vs. Bases Débiles
- Cuantificando la Fortaleza: La Constante de Disociación de Bases (Kb) y pKb
- Entendiendo el pH en Soluciones de Bases Fuertes
- Tabla Comparativa: Bases Fuertes vs. Bases Débiles
- Preguntas Frecuentes sobre la Fuerza de las Bases
¿Qué es una Base en Química?
Antes de sumergirnos en la fortaleza de las bases, es fundamental recordar qué son. En términos generales, una base es una sustancia capaz de aceptar protones (iones H+) o de ceder iones hidroxilo (OH-) en una solución acuosa. Existen varias teorías para definir bases, pero las más comunes son la teoría de Arrhenius (sustancias que producen OH- en agua) y la teoría de Brønsted-Lowry (sustancias aceptoras de protones). Para los fines de este artículo, nos centraremos principalmente en su comportamiento en soluciones acuosas y su capacidad para generar iones hidroxilo, los cuales son los responsables directos de su carácter básico.
La Diferencia Clave: Bases Fuertes vs. Bases Débiles
La distinción entre una base fuerte y una base débil es análoga a la de ácidos fuertes y débiles, y reside en su grado de disociación o ionización en solución acuosa. Una base fuerte es aquella que se disocia completamente o se ioniza al 100% en iones en solución. Esto significa que, si disuelves un mol de una base fuerte en agua, obtendrás prácticamente un mol de iones hidroxilo (OH-) en la solución, además de los iones metálicos correspondientes. No queda prácticamente ninguna molécula de la base sin disociar en la solución.
Por otro lado, una base débil es aquella que solo se disocia parcialmente en solución acuosa, estableciendo un equilibrio entre la forma molecular de la base y sus iones. Esto significa que una porción significativa de la base permanece en su forma molecular sin ionizar, liberando una menor cantidad de iones hidroxilo en comparación con una base fuerte de la misma concentración.
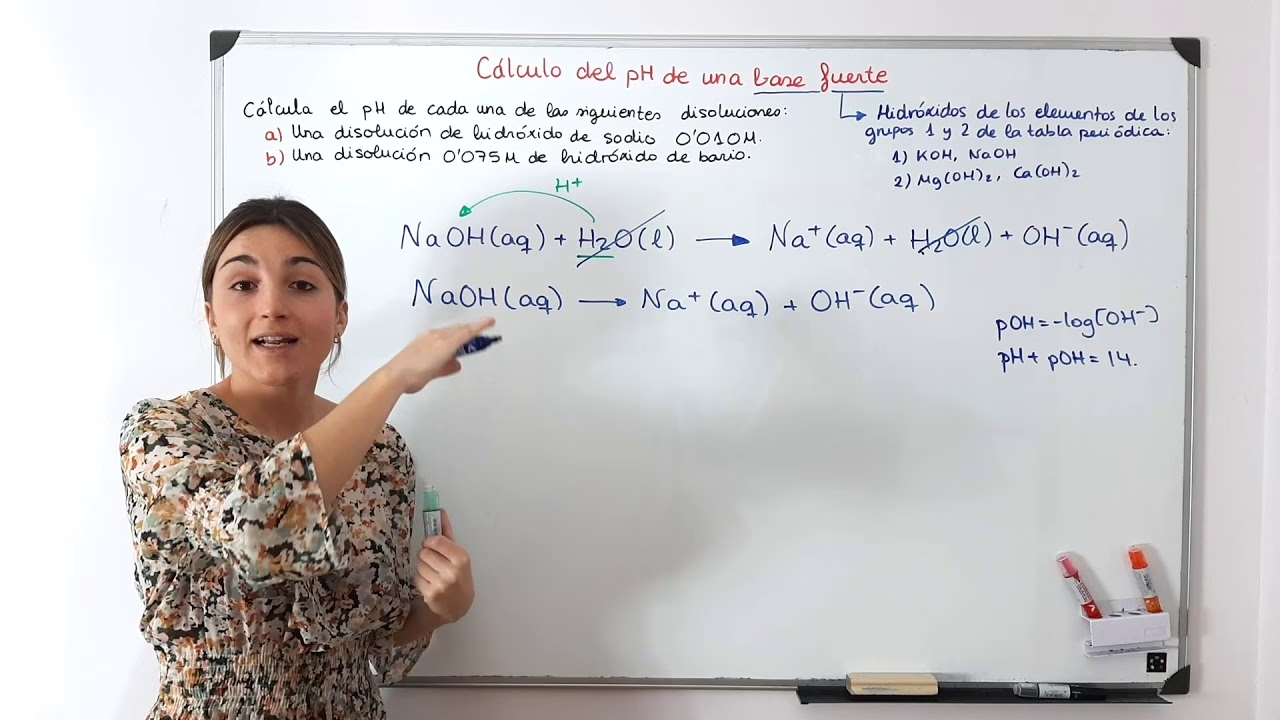
Ejemplos de Bases Fuertes
Las bases fuertes más comunes suelen ser los hidróxidos de los metales alcalinos (Grupo 1 de la tabla periódica) y algunos hidróxidos de los metales alcalinotérreos (Grupo 2). Algunos ejemplos prominentes incluyen:
- Hidróxido de Sodio (NaOH): Conocido como soda cáustica, es una de las bases fuertes más utilizadas en la industria y en el hogar.
- Hidróxido de Potasio (KOH): Similar al NaOH, pero a menudo se prefiere en ciertas aplicaciones por sus propiedades específicas.
- Hidróxido de Calcio (Ca(OH)2): Aunque su solubilidad en agua es relativamente baja, la porción que sí se disuelve lo hace completamente, liberando iones calcio y dos iones hidroxilo por cada unidad de Ca(OH)2. Es importante destacar que la baja solubilidad de una base no la convierte en débil; lo que importa es el grado de ionización de la porción que se disuelve.
- Hidróxido de Bario (Ba(OH)2): Otro hidróxido de metal alcalinotérreo que exhibe un comportamiento de base fuerte.
La clave para estas sustancias es que, una vez disueltas, se comportan como si fueran 100% iones metálicos y iones hidroxilo. La concentración de iones hidroxilo en la solución es directamente proporcional a la concentración inicial de la base fuerte.
Cuantificando la Fortaleza: La Constante de Disociación de Bases (Kb) y pKb
Para comparar de manera cuantitativa la fuerza de las bases, los químicos utilizan una constante de equilibrio conocida como la constante de disociación de bases, o Kb. Esta constante es una medida de la extensión en que una base se ioniza en una solución acuosa. Para una base genérica, B, que reacciona con agua:
B(aq) + H2O(l) ⇌ BH+(aq) + OH-(aq)
La expresión para Kb es:
Kb = [BH+][OH-] / [B]
Donde los corchetes [ ] denotan las concentraciones en equilibrio de las especies. Cuanto mayor sea el valor de Kb, mayor será la concentración de iones OH- producidos en el equilibrio, lo que indica que la base es más fuerte. Para bases muy fuertes, como el NaOH, la disociación es tan completa que el valor de Kb es extremadamente grande (a menudo se considera que tiende a infinito), lo que dificulta su medición precisa y rara vez se tabula para ellas, ya que se asume una disociación total.
De manera similar a cómo se usa el pH para expresar la acidez, se utiliza el pKb para expresar la fuerza de una base de una manera más manejable. El pKb se define como el logaritmo negativo de base 10 de Kb:
pKb = -log10(Kb)
La relación es inversa: una base más fuerte tendrá un valor de Kb más grande y, por lo tanto, un valor de pKb más pequeño. De hecho, para las bases fuertes, sus pKb son muy pequeños o incluso negativos, lo que refuerza la idea de su disociación completa.
Entendiendo el pH en Soluciones de Bases Fuertes
El pH es una medida de la concentración de iones hidrógeno (H+) en una solución, y una solución básica se caracteriza por tener una baja concentración de H+ y una alta concentración de OH-. Aunque las bases fuertes producen principalmente iones OH-, los iones H+ siguen estando presentes debido al equilibrio de autoionización del agua:
H2O(l) ⇌ H+(aq) + OH-(aq)
Este equilibrio se describe por la constante del producto iónico del agua, Kw, que a 25°C tiene un valor de 1.0 x 10-14:
Kw = [H+][OH-] = 1.0 x 10-14
Cuando se añade una base fuerte al agua, la concentración de OH- aumenta drásticamente. Según el Principio de Le Chatelier, el equilibrio de autoionización del agua se desplaza hacia la izquierda, consumiendo iones H+ y reduciendo su concentración. Es por esta razón que las soluciones básicas tienen valores de pH superiores a 7 (lo que indica una baja concentración de H+).
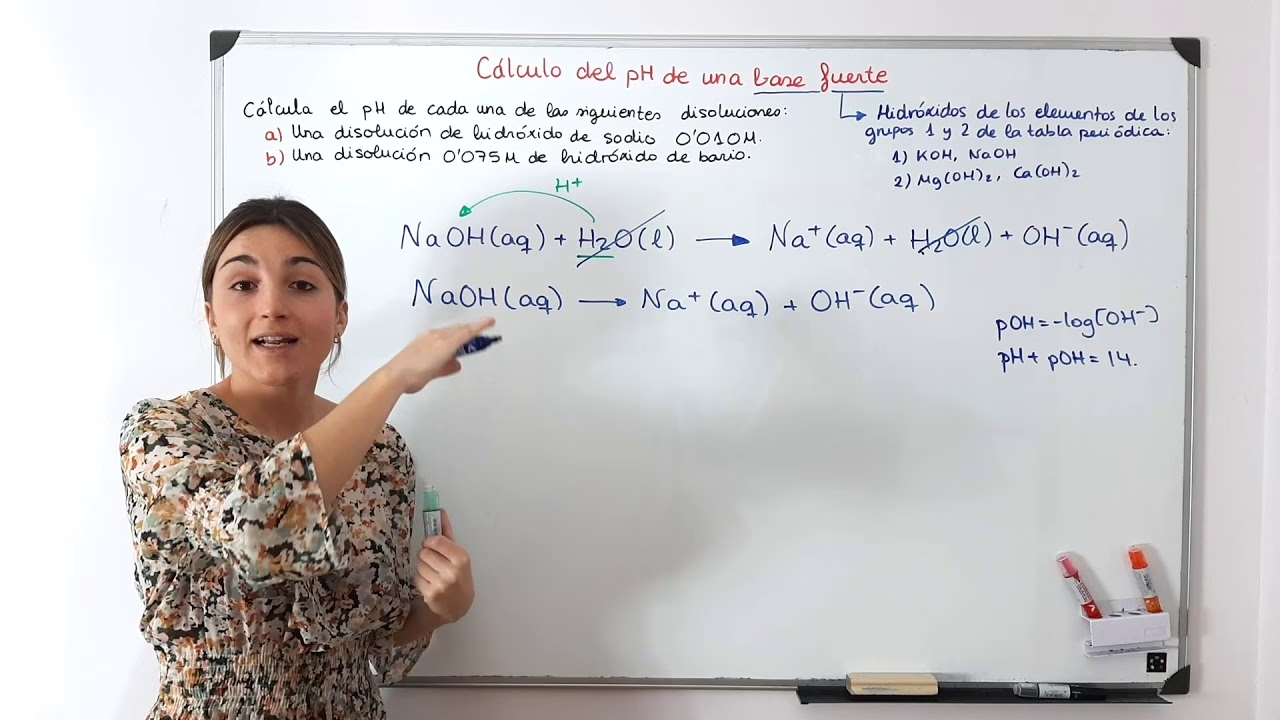
Cálculo del pH de una Solución de Base Fuerte
Calcular el pH de una solución de base fuerte es relativamente sencillo, dado que se asume una disociación completa. Aquí te explicamos los pasos:
- Determinar la concentración de iones hidroxilo ([OH-]): Para una base fuerte, la concentración de iones OH- en la solución es igual a la concentración inicial de la base, multiplicada por el número de iones OH- que libera por molécula. Por ejemplo, si tienes una solución 0.1 M de NaOH, [OH-] = 0.1 M. Si tienes una solución 0.05 M de Ca(OH)2, que libera dos iones OH- por molécula, entonces [OH-] = 2 * 0.05 M = 0.1 M.
- Calcular el pOH: El pOH es una medida de la concentración de iones OH- y se calcula de manera similar al pH:
pOH = -log10[OH-]
- Calcular el pH: Una vez que tienes el pOH, puedes encontrar el pH utilizando la relación fundamental a 25°C:
pH + pOH = 14
pH = 14 - pOH
Este proceso de cálculo es una herramienta fundamental para químicos y estudiantes, permitiendo predecir la acidez o basicidad de una solución con alta precisión cuando se trabaja con bases fuertes.
Tabla Comparativa: Bases Fuertes vs. Bases Débiles
Para consolidar la comprensión, la siguiente tabla resume las principales diferencias entre bases fuertes y bases débiles:
| Característica | Bases Fuertes | Bases Débiles |
|---|---|---|
| Grado de Disociación/Ionización | Completa (100%) en solución acuosa. | Parcial (menos del 100%) en solución acuosa. |
| Producción de OH- | Alta concentración de OH-. | Baja concentración de OH-. |
| Valor de Kb | Muy grande (tiende a infinito), no se tabula comúnmente. | Pequeño, se tabula y es un valor específico. |
| Valor de pKb | Muy pequeño o negativo. | Mayor que 0, positivo. |
| pH de Soluciones (a igual concentración) | Muy alto (generalmente 13-14 para concentraciones típicas). | Moderadamente alto (generalmente 8-12 para concentraciones típicas). |
| Ejemplos Comunes | NaOH, KOH, Ca(OH)2, Ba(OH)2. | NH3 (amoníaco), CH3NH2 (metilamina), piridina. |
| Reversibilidad de Reacción | Irreversible (reacción unidireccional). | Reversible (equilibrio químico). |
Preguntas Frecuentes sobre la Fuerza de las Bases
¿Cómo sé si una base es fuerte sin tener que buscar su Kb?
Generalmente, las bases fuertes son los hidróxidos de los metales alcalinos (LiOH, NaOH, KOH, RbOH, CsOH) y los hidróxidos de los metales alcalinotérreos más pesados (Ca(OH)2, Sr(OH)2, Ba(OH)2). Si una base no cae en estas categorías, es muy probable que sea una base débil.
¿La solubilidad de una base afecta su fuerza?
No directamente. La fuerza de una base se refiere a qué tan completamente se disocia la porción que se disuelve. Una base como el Ca(OH)2 es "poco soluble" en el sentido de que no se disuelve mucha cantidad en el agua, pero la pequeña cantidad que sí se disuelve se ioniza por completo. Por lo tanto, sigue siendo una base fuerte. La solubilidad afecta la concentración máxima que se puede alcanzar de la base en solución, pero no la naturaleza intrínseca de su fortaleza.

¿Por qué es importante saber si una base es fuerte o débil?
Es crucial por varias razones:
- Seguridad: Las bases fuertes son corrosivas y pueden causar quemaduras graves en la piel y los ojos.
- Aplicaciones Industriales: Su uso en la fabricación de jabones, limpiadores, productos farmacéuticos y en procesos de neutralización requiere conocer su fuerza para controlar las reacciones.
- Química Analítica: En titulaciones y análisis cuantitativos, la distinción entre bases fuertes y débiles es fundamental para seleccionar los indicadores adecuados y realizar cálculos precisos.
- Biología: El equilibrio ácido-base en los sistemas biológicos es vital, y comprender la fuerza de las bases ayuda a entender cómo interactúan con las biomoléculas.
¿Pueden las bases fuertes ser neutralizadas por ácidos débiles?
Sí, una base fuerte puede ser neutralizada por un ácido débil. La neutralización es una reacción entre un ácido y una base que produce una sal y agua. Sin embargo, el pH del punto de equivalencia (donde la cantidad de ácido y base es estequiométricamente igual) no será neutro (pH 7), sino que será ligeramente básico debido a la hidrólisis de la sal formada.
¿Cuál es la base más fuerte conocida?
En el contexto de soluciones acuosas, los hidróxidos de los metales alcalinos (como NaOH y KOH) son considerados las bases fuertes más comunes y potentes. Sin embargo, en química orgánica y en ausencia de agua, existen "superbases" que son mucho más fuertes, como el hidruro de sodio (NaH) o el butil-litio (BuLi), capaces de desprotonar incluso compuestos que normalmente no se consideran ácidos. Pero para el alcance de este artículo, centrado en soluciones acuosas, los hidróxidos de metales alcalinos son los referentes.
En resumen, la fuerza de una base se define por su capacidad de disociarse completamente en iones hidroxilo en una solución acuosa. Esta disociación total es lo que las distingue de las bases débiles y lo que les confiere sus propiedades corrosivas y su alta reactividad. La constante Kb y su logaritmo negativo pKb son las herramientas cuantitativas que nos permiten comparar y clasificar estas sustancias. Comprender estos conceptos no solo es fundamental para los estudios de química, sino también para apreciar la importancia de estas sustancias en nuestra vida cotidiana y en la industria. La próxima vez que uses un limpiador o te encuentres con un producto que contenga soda cáustica, recordarás la ciencia detrás de su poderosa acción básica.
Si quieres conocer otros artículos parecidos a La Fuerza de las Bases: Más Allá del pH puedes visitar la categoría Química.
